石杉碱甲口服固体制剂质量分析
2015-01-05孙春艳刘新宇柳艳云姜红
孙春艳,刘新宇,柳艳云,姜红
(湖北省食品药品监督检验研究院,武汉 430064)
石杉碱甲口服固体制剂质量分析
孙春艳,刘新宇,柳艳云,姜红
(湖北省食品药品监督检验研究院,武汉 430064)
目的 评价石杉碱甲口服固体制剂的质量现状及存在问题。方法 按照国家评价性抽验的总体要求,在按照法定检验方法检验的基础上,开展探索性研究,统计分析石杉碱甲口服固体制剂的质量现状并进行评价;对不同分析方法所得的结果进行分析。结果 按照法定标准检验,结果显示86批样品合格率为96.5%。其中有3批不合格,不合格的项目涉及有关物质、含量均匀度、含量。部分企业样品溶出较低、批内和批间差异较大;有的样品有关物质较高、含量处于低限。探索性研究结果显示,不同企业样品溶出行为存在差异;不同企业生产的产品所使用的原料药质量不同;现行标准含量测定方法能准确体现样品含量的真实值,但有关物质检测方法有待完善;建立的近红外一致性检验模型可以对相应厂家生产的样品进行有效识别。结论 按现行标准检验,石杉碱甲口服固体制剂总体合格率较好,但部分企业需改进生产工艺及处方,提高产品质量。
石杉碱甲口服固体制剂;质量分析;法定检验
石杉碱甲(huperzine A,Hup A)是来源于蕨类植物蛇足石杉的一种倍半萜生物碱,为高效、高选择性、可逆性的乙酰胆碱酯酶(acetylcholine esterase,AChE)抑制药,1986年其结构得到确认[1]。有神经保护以及对抗氧化应激、改善脑缺血损伤、修复记忆损伤等作用。目前,Hup A治疗阿尔茨海默病(Alzheimer's disease,AD)疗效显著,此外还用于治疗重症肌无力和小儿麻痹症、提高青春期学生的记忆力、缓解有机磷中毒等。现国内有片剂、胶囊剂、注射剂3种剂型,国外仅美国有石杉碱甲片保健品上市。片剂有9个批准文号、胶囊剂有3个批准文号,注射剂有2个批准文号。石杉碱甲片/胶囊是国家基本药物,规格均为50 μg。收载于《中华人民共和国药典》2010年版二部,国外药典均无收载。
石杉碱甲片/胶囊是2013年国家评价性抽验品种,根据国家食品药品监督管理局统一安排对86批抽验产品实施了法定检验,并对出现的问题及质量现状进行了探索性研究。
1 仪器与试药
1.1 仪器 高效液相色谱仪(岛津LC-20AT、Ulimate 3000、Agilent 1260);RCZ-8B 药物溶出仪(天大天发科技有限公司),日本理学Rigaku D/max2500型粉末X-射线衍射仪,MATRIX-F近红外光谱仪。
1.2 试药 石杉碱甲对照品(中国食品药品检定研究院,批号:100243-201202,含量:98.4%);石杉碱甲原料5批:A厂提供(本企业生产,批号:y130102)、B厂提供(Z厂生产,批号:Q0413091)、C厂提供(Z厂生产,批号:Q04130305)、D厂提供(Z厂生产,批号:Q04130412;N厂生产,批号:20130412)。
2 实验方法
按照《中华人民共和国药典》二部标准对样品进行法定检验,针对企业对该产品研发、生产、检验的情况,对企业进行调研;参照文献[2-4]报道,结合按法定标准检验的结果,开展了一系列的探索性研究。
2.1 抽样简介 共抽取样品86批,其中石杉碱甲片82批,石杉碱甲胶囊4批。石杉碱甲片涉及生产企业6个,占全国该品种生产企业总数66.7%;石杉碱甲胶囊涉及生产企业2个,占全国该品种总的生产企业数的66.7%。样品涉及全国24个省、市、自治区,其中批次最多的区域为上海。在医疗机构抽取34批,占样品总数的39.5%;生产企业抽取7批,占样品总数的8.1%;药品经营企业抽取45批,占样品总数的52.3%。
2.2 依据现行质量标准检验结果及分析 本次抽取样品86批,均按《中华人民共和国药典》2010年版二部检验,合格样品83批,合格率为96.5%。有3批样品不符合规定,均为石杉碱甲片,涉及2个企业,3批不合格的样品中有2批样品有关物质不合格,1批样品含量及含量均匀度不合格。
2.3 探索性研究结果及分析 结合调研及检验情况,针对影响产品质量的溶出度、有关物质、含量等关键因素进行如下研究。
2.3.1 石杉碱甲片溶出曲线考察 石杉碱甲片为低规格药物,为了客观评价该产品内在质量,采用4种溶出介质(0.1 mol·L-1盐酸溶液、水、pH4.5缓冲液和pH6.8缓冲液),利用高效液相色谱法考察石衫碱甲片在不同介质中的溶出曲线。分析各厂家产品在4种不同溶出介质中得到的溶出曲线,从而了解国内石杉碱甲片的溶出情况以及各厂家间的差异。根据按法定标准检验的结果,考虑到D厂生产的石衫碱甲片为本次评价性抽验中样品量最大、取得批准文号的时间较早,且实验中该厂家药品在不同介质中的溶出率较高,因此采用该公司的石衫碱甲片作为参比。对其他厂家的石衫碱甲片进行相似因子计算,比较溶出行为的差异[5]。
结果显示:①以0.1 mol·L-1盐酸溶液为溶出介质,所有厂家在15 min内均达到规定限度的80%,前10 min的溶出量显示各厂家由于工艺和原料不同,溶出行为有一定差异,其中D、A和C三家企业产品在5 min时溶出率高于50%,E、B与F三家企业产品在5 min时溶出率低于50%,在规定的30 min溶出时间内,各企业产品溶出行为差异不明显。②以水为溶出介质,在各时间点上,各厂家产品的溶出率差异较大。D厂的产品在水中的溶出情况较好。与在0.1 mol·L-1盐酸溶液中的溶出率比较,其余厂家产品的溶出率均有不同程度的降低。其中,A企业的产品在实验进行到30 min时溶出率未达到规定限度的80%。在该介质中,不同企业产品溶出行为差异明显。③以pH4.5缓冲液为溶出介质和以pH6.8缓冲液为溶出介质,各厂家药品的溶出行为与在0.1 mol·L-1盐酸溶液中的较为一致。D、A与C 3个厂家的药品在5 min时溶出率已达到60%左右或以上,其余3个厂家样品溶出率均低于40%,在5 min以后溶出率才开始有显著上升。④A企业的药品与参比制剂相似程度最高,在3个介质中的相似因子均>50,说明其溶出过程与参比制剂较为相似。C企业的药品仅在pH4.5的介质中相似因子较高,与参比制剂较为一致。其余厂家在4种介质中的溶出行为与参比制剂有较大的差异。因此可初步判断A企业的药品与参比制剂的工艺与辅料质量更为接近,C企业的药品与参比制剂在处方工艺上也有一定的相似度。其余3个厂家的药品的处方工艺与参比制剂差异较大。
2.3.2 有关物质检测方法的考察 在按照法定标准对样品进行检测的过程中发现:标准规定有关物质检查记录色谱图至主峰保留时间的2倍,但实验发现部分样品在主峰保留时间2倍之后仍有杂质峰及较大辅料峰出现,给下一个样品的检测带来干扰。故对有关物质检测方法进行了探讨,考察辅料对有关物质检查的影响,同时对不同企业生产的原料的有关物质进行考察,比较不同来源原料药质量差异。
色谱条件:色谱柱为Acclaim 120 C18(250 mm×4.6 mm,5 μm),流动相A为磷酸盐缓冲液(取磷酸二氢钾2.72 g,加水1 000 mL溶解,用磷酸调节pH至2.5),流动相B为乙腈;分别采用等度(A:B=92:8)和梯度的方式(表1)进行洗脱;检测波长310 nm,流速1.0 mL·min-1,柱温35 ℃,进样量50 μL。

表1 梯度洗脱表 %
首先采用等度加延长记录时间(记录至主峰保留时间的5倍)的方法,对本次抽验的86批样品有关物质进行检测。结果显示,部分样品有关物质测定结果增加,该项目合格率由原来的97.7%变为96.5%。典型样品溶液色谱图及空白辅料溶液色谱图见图1A、B。采用等度的方法(记录至主峰保留时间的2.5倍)对不同企业生产的原料的有关物质进行考察。发现不同企业生产的原料杂质个数及总量差异较大,杂质个数较多的是A企业生产的原料,杂质个数较少的是N药业有限公司生产的原料。按法定标准检测的结果显示,A企业的制剂中有关物质含量普遍高于其他企业样品中有关物质含量,提示原料药质量是A企业制剂中有关物质的重要影响因素。
为提高效率,缩短分析时间,采用梯度洗脱的方式检测有关物质,空白溶剂色谱图见图1C、空白辅料溶液色谱图见图1D、典型样品溶液色谱图见图1E。结果显示:①采用梯度洗脱的方式与采用等度加延长记录时间的方法所测得结果一致。②采用梯度洗脱的色谱条件既能保证杂质与主峰、杂质与辅料的有效分离,又能让保留时间过长的辅料峰的出峰时间大大提前,从而节省了分析时间。③梯度洗脱测得有关物质的结果与等度基础上延长保留时间的方法测得的杂质个数及杂质含量一致,但辅料峰个数增加,说明采用梯度洗脱的方式更有利于辅料的洗脱,减小了对色谱柱损伤及对其他样品检测的干扰,提高了工作效率。
2.3.3 原料药晶型和粒度考察 按照现行标准检验发现不同原料来源的企业生产的样品有关物质、溶出度检测结果有差异,笔者采用X-粉末衍射和电镜扫描的方式对不同企业生产的原料进行分析,探讨原料药晶型和粒度的差异对产品质量的影响[6]。
X-粉末衍射结果显示,不同企业生产的石杉碱甲原料X-射线粉末衍射图衍射峰的强度和个数略有差异。电镜扫描结果显示:在500倍的放大倍数下,N企业生产的原料药的粒径最小,呈无定型状;A企业生产的原料稍大,呈片状和无定型状;而Z企业生产的原料药粒径最大,呈较规则的立体结晶状,粒径是N企业有限公司生产的原料药粒径的数10倍。不同企业生产产品的电镜扫描图见图2。X-射线粉末衍射和电镜扫描结果提示:不同生产企业石杉碱甲原料药的结晶工艺存在差异,这些差异与有关物质及溶出度等内在质量的相关性还需进一步研究。
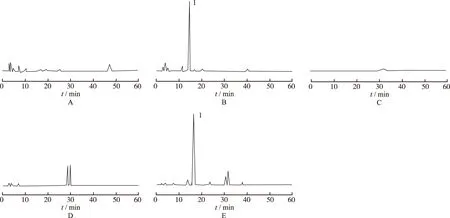
A.空白辅料(等度条件);B.样品溶液(等度条件);C.空白溶剂(梯度条件);D.空白辅料(梯度条件);E.样品溶液(梯度条件);1.石杉碱甲
图1 5种溶液不同检测方法所得色谱图
2.3.4 含量测定方法的考察 在对样品含量及含量均匀度检测中发现,很多样品的含量接近于低限,有1批样品含量均匀度及含量不符合规定,该批样品各片之间的差异较小,含量均匀度不合格的主要原因为含量较低,导致A+1.80s中的A值(A=|100-含量|)较大。不合格的样品由C企业生产,该企业样品的平均片质量约为0.13 g,而主药石杉碱甲只有50 μg。在含量测定中,辅料可能会影响石杉碱甲的溶解。因此,主药石杉碱甲的溶出及回收情况是含量测定的关键。故从三个方面对含量测定结果的影响因素进行探讨:①采用该企业提供的原料及空白辅料,进行了回收率实验;②取石杉碱甲原料药配成与含量测定一致的浓度的溶液,分别考察超声不同时间、自然光照1 d、98 ℃水浴2 h、铁离子(Fe3+)对含量测定结果的影响;③考察滤膜对含量测定的影响,为石杉碱甲片/胶囊含量测定方法提供参考。
结果显示:现行标准石杉碱甲片的含量测定方法回收好,能体现样品含量的真实值。滤膜对石杉碱甲无吸附,样品溶液滤过后不会造成含量测定结果偏低。超声、光照、高温、Fe3+均能造成石杉碱甲含量下降。超声5 min下降约0.5%,建议在石杉碱甲片/胶囊含量测定过程中避免长时间超声及光照,在溶出度测定过程中应注意避免Fe3+的影响,选择材质较好的搅拌桨。

图2 A、Z、N企业生产的原料的电镜扫描图(×500)
2.3.5 快检方法研究 石杉碱甲片2013年国家评价性抽样共涉及6个厂家,其中4个厂家的抽样符合近红外一致性检验模型建模条件,针对该4个厂家分别建立近红外一致性检验模型,可以为各厂家样品快速筛查、快速质量分析提供有效技术支持。按中国食品药品检定研究院建议的一致性模型建模参数条件,选择本厂家的部分光谱作为建模光谱,建立各厂家的一致性检验模型,其余部分光谱作为验证,并用不同厂家的光谱作验证。采用OPUS软件,针对不同厂家生产的样本分别建立模型,光谱预处理方法为二阶导数+向量归一化,13点平滑,阈值为7,在谱段9 000~7 500 cm-1,6 900~5 600 cm-1,5 000~4 250 cm-1区间范围可以建立较好的一致性模型。
用未参与建模的本厂家光谱与各不同厂家的光谱对建立的一致性模型进行验证,验证结果显示建立的各厂家产品的一致性检验模型均能准确识别本厂家的样品光谱,并区分不同厂家的样品光谱,经验证建立的模型准确可靠,一致性指数(conformity index,CI)分布见图3。
3 讨论
溶出度是指药物从片剂或胶囊剂等固体制剂在规定介质中溶出的速度和程度,它是评价一种药物不同剂型之间、不同厂家的同一样品、同一厂家同一样品不同批次间的重要质量指标。生物药剂学分类系统(biopharmaceutics classification system ,BCS)根据药物制剂中活性成分(active pharmaceutical ingredient ,IPA)的水溶性和渗透性对药品进行分类。石杉碱甲在水中不溶,脂溶性较强,属于低溶解性高渗透性的药物,为第Ⅱ类。通过按照法定标准检验和探索性研究,反映不同企业样品溶出行为存在差异,主要与原料药的质量、生产工艺的优劣有关,如原料药的粒度、晶型、制粒的均一性、压片的硬度、生产投料等。也反映原料药生产到制剂生产过程中的一系列问题:①不同企业原料药含量和晶型有所不同,需改善结晶工艺,提高含量。②调研结果显示,质量控制的关键工艺参数有粘合剂浓度、混合时间、筛网数目、颗粒率、含量、水分、温度、烘干时间、总混时间等。混合时间与颗粒含量相关,颗粒水分、颗粒率与崩解时限、脆碎度有关,颗粒度与片重差异有关,干燥的时间和温度与有关物质、水分含量有关。探索性研究结果显示,Fe3+和光照均能造成石杉碱甲的降解,故应在生产及储存过程中注意Fe3+和光照的影响。③调研结果还显示D企业生产按103%~105%投料,该企业产品含量测定结果在95.0%~100.0%之间,而A企业生产的样品含量普遍较低,C企业样品有一批含量不符合规定,提示可能存在低限投料。
采用DAD检测器对有关物质检测的色谱图进行分析,提取主峰及各杂质峰、辅料峰的紫外吸收色谱图发现:主峰在230及307 nm波长处有最大吸收,而样品溶液色谱图中tR=47.7 min处的辅料峰也在232及307 nm波长处有最大吸收,故在此条件下辅料峰比较明显。探索性研究结果显示,石杉碱甲片/胶囊采用梯度洗脱的方式优于现行标准的方法,表现为:①梯度洗脱色谱图上辅料峰更多,说明采用梯度洗脱的方式可以尽可能地将辅料洗脱下来;②梯度洗脱可以使辅料出峰时间提前,避免辅料峰对其他样品的干扰,并可通过采用辅料进行定位,扣除空白辅料,避免样品有关物质检测结果偏高;③现行标准规定有关物质检测记录的时间为主峰保留时间的2倍,而实验发现部分样品主峰保留时间2倍之外仍有杂质峰出现,采用梯度洗脱保证了有关物质的检出,避免样品有关物质检测结果偏低的情况。

●为验证样本;◆为建模样本;CI限度线以下的●均为本厂家光谱,CI限度线以上的●均为其他厂家光谱
现行标准能基本反映产品的质量状况,但有关物质检测方法有待完善。现行标准溶出度的方法为溶出度测定法第三法,溶出介质为0.1 mol·L-1盐酸,介质体积为100 mL,转速为50 r·min-1,经30 min取样,限度为标示量的80%。鉴于以水为溶出介质时,溶出曲线在15 min时已达平台,水的区分能力较强,建议在原标准方法的基础上,将溶出时间修订为20 min,溶出介质修订为水,并进一步考察。采用此方法对6个企业的6批样品进行检测,结果有1批样品的溶出度低于限度值。质量评价结果亦显示部分合格产品也存在溶出行为差异大、有关物质偏高、含量处于低限的现象,提示工艺和生产过程管理有待提升。
[1] 许明,宋新波,张丽娟.石杉碱甲的研究进展[J].药物评价研究,2010,33(6):442-446.
[2] 胡昌勤.对抗生素药品评价性抽验基本思路与方法的思考[J].中国抗生素杂志,2013,38(1):1-11.
[3] 张斗胜,王晨,刘文,等.2009年国产注射用阿奇霉素评价性抽验结果与质量评价[J].药物分析杂志,2010,30(9):1804-1808.
[4] 王敏.药品评价性抽验工作的作用和意义[J].海峡药学,2007,19(6):133-134.
[5] 张启明,谢沐风,宁保明,等.采用多条溶出曲线评价口服固体制剂的内在质量[J].中国医药工业杂志,2009,40(12):946-950.
[6] 曾凡彬.影响难溶性药物口服固体制剂溶出特性的理化因素——晶型和粒度[J].中国新药杂志,2002,11(7):507-509.
数字对象唯一标识符(digital object unique identifier,DOI)由美国出版协会(Association of American Publishers,AAP)于1994年提出,为互联网上的数字对象提供了独一无二的标识,他具有可靠性和永久性的特性,方便了计算机的互操作,并可逐步实现各种数字产品的流通和交易,因而被形象地称为“互联网上的条形码”。读者可根据每篇文章DOI编码,在htttp://dx.doi.org查找到本刊的原始电子文献,并实现在各文献检索平台中由引文到全文的链接,有利于本刊论文数字资源的长久保存和唯一识别。DOI编码的另一个重要功能是:只需点击本刊每篇论文后参考文献表中的某条文献,即能看到该文献的题名、作者、摘要和出处。详细资料和DOI查询请参考中文DOI主页,网址为http://www.chinadoi.cn。
《医药导报》自2009年第1期起全面启用DOI编码。这意味着自2009年第1期起在《医药导报》发表的论文已经获得国际通用的唯一永久标识。
按照万方数据公司2015年7月公布的《DOI编码与印刷指南》(版本1.4),《医药导报》论文的DOI编码为doi:10.3870/j.issn.1004-0781.yyyy.nn.zzz,其中10.3870为中文DOI注册中心分配给华中科技大学期刊的前缀,后缀j.issn.1004-0781.yyyy.nn.zzz,其中j表示期刊,issn.1004-0781表示《医药导报》的issn号,yyyy为出版的年份,nn为期号,zzz为同一期中论文的流水号。如《医药导报》2015年第9期第9篇论文的DOI编码如下,doi:10.3870/j.issn.1004-0781.2015.09.009。
《医药导报》编辑部
2014-05-13
2014-10-27
孙春艳(1975-),女,湖北随州人,副主任药师,硕士,研究方向:药物分析。电话:027-87895875,E-mail:suncy25@126.com。
R971;R927.1
B
1004-0781(2015)09-1215-05
10.3870/j.issn.1004-0781.2015.09.027
导报》论文
功能介绍
