异常黑胆质成熟剂对银屑病模型小鼠的治疗作用*
2015-01-05热比姑丽伊斯拉木尤力都孜买买提买合素提卡德尔斯拉甫艾白
热比姑丽·伊斯拉木,尤力都孜·买买提,买合素提·卡德尔,斯拉甫·艾白
(1.新疆医科大学基础医学院药理教研室,乌鲁木齐 830054;2.新疆维吾尔医方剂学实验室,乌鲁木齐 830049;3.新疆维吾尔自治区维吾尔医药研究所,乌鲁木齐 830049)
异常黑胆质成熟剂对银屑病模型小鼠的治疗作用*
热比姑丽·伊斯拉木1,2,3,尤力都孜·买买提2,3,买合素提·卡德尔2,3,斯拉甫·艾白1,2,3
(1.新疆医科大学基础医学院药理教研室,乌鲁木齐 830054;2.新疆维吾尔医方剂学实验室,乌鲁木齐 830049;3.新疆维吾尔自治区维吾尔医药研究所,乌鲁木齐 830049)
目的 探讨异常黑胆质成熟剂对银屑病模型小鼠的作用。方法 建立小鼠鼠尾鳞片表皮模型,观察异常黑胆质成熟剂对该模型病理状态影响;建立盐酸普萘洛尔致小鼠耳部皮肤银屑病样模型,观察异常黑胆质成熟剂对小鼠体质量、脾脏指数、胸腺指数及病理状态的影响。采用酶联免疫吸附(ELISA)法检查各组小鼠血清白细胞介素(IL)-10、IL-17、IL-23水平。结果 2,4,8 g·kg-1异常黑胆质成熟剂组小鼠一般状况、体质量均无明显异常变化(P>0.05);2 g·kg-1异常黑胆质成熟剂组小鼠胸腺指数(1.903±0.885)mg·g-1,比模型对照组(2.841±1.211)mg·g-1明显降低(P<0.05);2,4,8 g·kg-1异常黑胆质成熟剂组小鼠血清IL-10、IL-17、IL-23水平无明显变化(P>0.05);2,4,8 g·kg-1异常黑胆质成熟剂能促进小鼠鼠尾表皮颗粒层细胞的形成,改善小鼠耳部皮肤银屑病样组织病理学变化。结论 异常黑胆质成熟剂对实验性银屑病有较好的治疗作用。
异常黑胆质成熟剂;银屑病,实验性;指数,胸腺
银屑病维吾尔医学名为节热比[1],是指以发生于全身皮肤,无传染性红斑鳞屑为主要特征的病症。病因多由在体内外不良因素的影响下,体液失衡,气质失调,碱性黏液质偏盛变成为异常黑胆质,并凝结沉着于皮肤,损伤局部所致。异常黑胆质型(汉文直译为非自然黑胆质)银屑病在新疆维吾尔自治区银屑病患者中比较常见[2-3]。异常黑胆质成熟剂(木尼孜其·赛危大依)是维吾尔医学临床治疗异常黑胆质型银屑病的首选药物(经典方剂),疗效确切,无明显毒副作用[3-4]。甲氨蝶呤是叶酸拮抗药,具有很强的免疫抑制作用,是一种传统的抗银屑病药物,临床疗效好、安全性高,且价格低廉[5]。因小鼠尾部表皮天然缺少颗粒层细胞,类似银屑病表皮角化不全病理改变,因而可作为银屑病角化异常的传统天然模型[5-7]。笔者通过实验性银屑病小鼠模型,探讨其药效作用。
1 材料与方法
1.1 动物 健康昆明种小鼠,130只,雌雄各半,无特定病原体(specific pathogen free,SPF)级,体质量18~22 g,由新疆实验动物研究中心提供。实验动物生产许可证号:SCXK(新)2011-0001,使用许可证号:SYXK(新)2011-0006,饲养于新疆维吾尔自治区维吾尔医药研究所药物安全性评价中心SPF级动物房,室温20~26 ℃,相对湿度40%~70%,光照、黑暗12 h交替,给予SPF鼠繁殖饲料及纯化水。
1.2 药品与试剂 异常黑胆质成熟剂(木尼孜其·赛危大依,维吾尔语命名为Munziq Sawda,批准文号:新药制字M20052635)由新疆维吾尔自治区维吾尔医医院制剂室提供。甲氨蝶呤片由上海信谊药厂有限公司生产,批准文号:国药准字H31020644,批号:20130403。盐酸普萘洛尔片(心得安)由常州康普药业有限公司生产,批准文号:国药准字H32021276,批号:1203004。小鼠白细胞介素(interleukin,IL)-10试剂盒[国食药监械(准)字2009第3400951号]、小鼠IL-17试剂盒[国食药监械(准)字 2012第3401164号]、小鼠IL-23试剂盒[国食药监械(准)字2012第3401163,批号均为:201310]由乌鲁木齐西域医鸣商贸有限公司提供。
1.3 仪器 TGL-5-A低速大容量离心机(上海安亭科学仪器厂);Anthos 2010酶标仪、Anthos iWO洗板机(郑州安图实验仪器有限公司);DM2500生物显微镜、RM2235切片机(德国莱卡公司);KD-BM生物组织自动包埋机、KD-TS3D生物组织自动脱水机(浙江金华科迪仪器设备有限公司);KZPG-1A摊片烤片机(天津天利航空机电有限公司)。
1.4 异常黑胆质成熟剂对银屑病模型小鼠的作用
1.4.1 对小鼠鼠尾鳞片表皮模型的作用 取小鼠60只,适应性饲养2 d,检疫合格后,取50只小鼠按体质量随机分为5组,即正常对照组,甲氨蝶呤组(剂量1.5 mg·kg-1),2,4,8 g·kg-1异常黑胆质成熟剂组(根据急性毒性实验、临床应用量、药效预实验确定剂量),每组10只,雌雄各半。每10 g体质量0.2 mL,每天1次,灌胃给予相应药物连续20 d。给药第21天处死小鼠,取鼠尾距离根部3 cm皮肤标本,用10%甲醛固定、脱水、石蜡包埋并用苏木精-伊红(hematoxylin eosin,HE)染色后在光镜下观察。
1.4.2 对盐酸普萘洛尔致小鼠耳部皮肤银屑病样模型作用 取小鼠70只,适应性饲养2 d,检疫合格后,取60只小鼠按体质量随机分为6组,即正常对照组,模型对照组,甲氨蝶呤组(1.5 mg·kg-1)及2,4,8 g·kg-1异常黑胆质成熟剂组,每组10只,雌雄各半。除正常对照组外,其余各组用5%盐酸普萘洛尔乳剂(取盐酸普萘洛尔5 g用50%乙醇溶解,加入月桂氮酮作为透皮吸收促进剂,加入聚乙烯吡咯烷酮5 g为成膜材料,再加50%乙醇至100 mL,即得),均匀涂抹于小鼠双耳背部皮肤,每耳涂抹0.1 mL,早晚各一次,连续涂抹20 d(在本实验室条件下,此模型已成熟,根据皮肤肉眼观察可以准确判断模型是否成立,建模型动物数为50只,正常对照组10只)。造模第21天开始,除模型对照组小鼠涂抹造模剂外,其余各给药组小鼠上午涂抹造模剂,下午灌胃给予相应药物,每10 g 体质量0.2 mL,每天1次,连续20 d。给药第21天,末次给药2 h后,取血,随后取脾脏、胸腺及双侧耳廓。先称脾脏、胸腺,后与右侧耳廓一起迅速放入低温冰箱(-86 ℃),待测相关指标。左侧耳廓皮肤标本,用10%甲醛固定、脱水、石蜡包埋并用HE染色后在光镜下观察。分离血清,酶联免疫吸附测定(enzyme linked immunosorbent assay,ELISA)法检测小鼠血清IL-10、IL-17、IL-23水平,操作步骤均严格按照试剂盒说明书进行[8-9]。

2 结果
2.1 一般情况 与正常对照组比较,模型对照组,甲氨蝶呤组,2,4,8 g·kg-1异常黑胆质成熟剂组小鼠在实验期间,行为活动、皮毛、粪便、饮食等未见异常。
2.2 体质量 与正常对照组比较,模型对照组,甲氨蝶呤组,2,4,8 g·kg-1异常黑胆质成熟剂组小鼠在实验期间,体质量变化差异无统计学意义(P>0.05)。见表1,2。
2.3 胸腺、脾脏指数 与正常对照组比较,模型对照组小鼠胸腺指数升高(F=1.992,P<0.05);与模型对照组比较,甲氨蝶呤组、2 g·kg-1异常黑胆质成熟剂组小鼠胸腺指数降低(F=2.190,P<0.05);对脾脏指数的影响差异无统计学意义(P>0.05)。 见表3。
2.4 小鼠血清IL-17、IL-23、IL-10水平 与正常对照组比较,模型对照组小鼠血清IL-10、IL-17、IL-23水平无明显变化(P>0.05)。与模型对照组比较,甲氨蝶呤组、异常黑胆质成熟剂组(2,4,8 g·kg-1)小鼠血清IL-10、IL-17、 IL-23水平无明显变化(P>0.05),见表4。
2.5 小鼠皮肤组织病理学变化
2.5.1 耳朵皮肤组织病理学变化 正常对照组角质层为不全角化,上皮变薄。有颗粒细胞层,但颗粒不明显。真皮内无炎细胞浸润。皮脂腺、毛囊结构清晰。
与正常对照组比较,模型对照组角质层增厚,角质层内有角栓和微小脓肿形成。有颗粒细胞层,且颗粒明显,棘层增厚。真皮内血管扩张充血,大量炎细胞浸润。说明模型成立[10]。与模型对照组比较,甲氨蝶呤组角质层变薄、均匀,角质层内角栓和微小脓肿明显减少。有1或2层颗粒细胞层,且颗粒明显。棘层变薄3或4层。真皮内炎症明显减轻。2,4,8 g·kg-1异常黑胆质成熟剂组角质层渐变薄,角质层内微小脓肿逐渐减少;有1或2层颗粒细胞层,且细胞内颗粒明显;棘细胞层变薄;真皮层内炎细胞逐渐减少。无明显剂量规律性。见图1。
表1 6组小鼠造模期间体质量变化
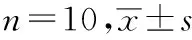
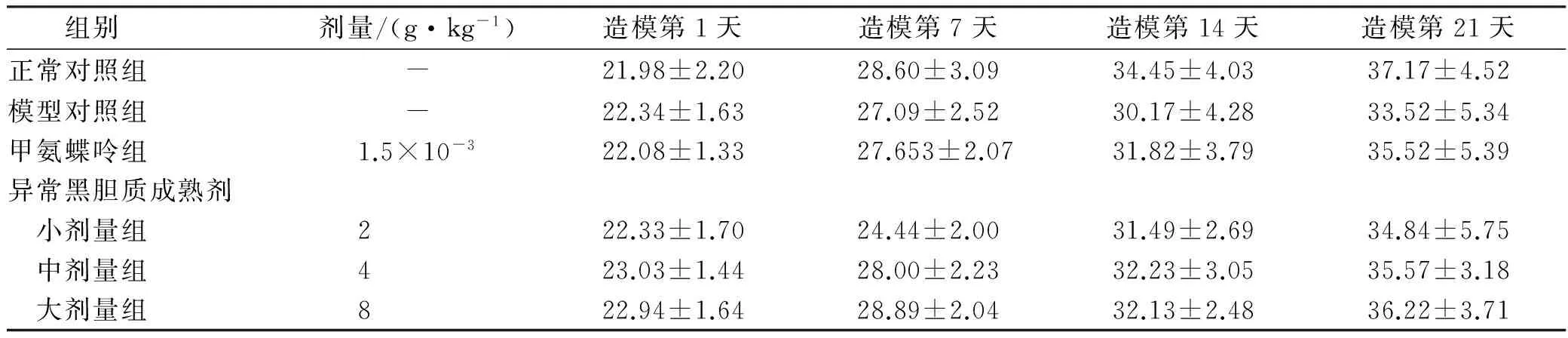
组别剂量/(g·kg-1)造模第1天造模第7天造模第14天造模第21天正常对照组-21.98±2.2028.60±3.0934.45±4.0337.17±4.52模型对照组-22.34±1.6327.09±2.5230.17±4.2833.52±5.34甲氨蝶呤组1.5×10-322.08±1.3327.653±2.0731.82±3.7935.52±5.39异常黑胆质成熟剂 小剂量组222.33±1.7024.44±2.0031.49±2.6934.84±5.75 中剂量组423.03±1.4428.00±2.2332.23±3.0535.57±3.18 大剂量组822.94±1.6428.89±2.0432.13±2.4836.22±3.71
表2 6组小鼠给药期间体质量变化情况
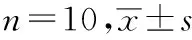
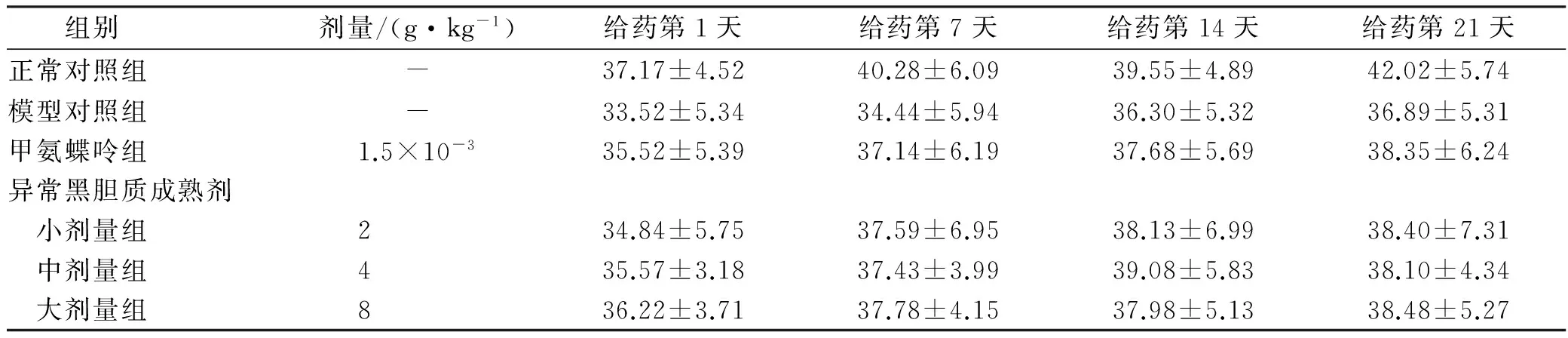
组别剂量/(g·kg-1)给药第1天给药第7天给药第14天给药第21天正常对照组-37.17±4.5240.28±6.0939.55±4.8942.02±5.74模型对照组-33.52±5.3434.44±5.9436.30±5.3236.89±5.31甲氨蝶呤组1.5×10-335.52±5.3937.14±6.1937.68±5.6938.35±6.24异常黑胆质成熟剂 小剂量组234.84±5.7537.59±6.9538.13±6.9938.40±7.31 中剂量组435.57±3.1837.43±3.9939.08±5.8338.10±4.34 大剂量组836.22±3.7137.78±4.1537.98±5.1338.48±5.27
表3 6组小鼠胸腺、脾脏指数比较
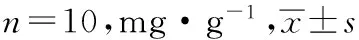
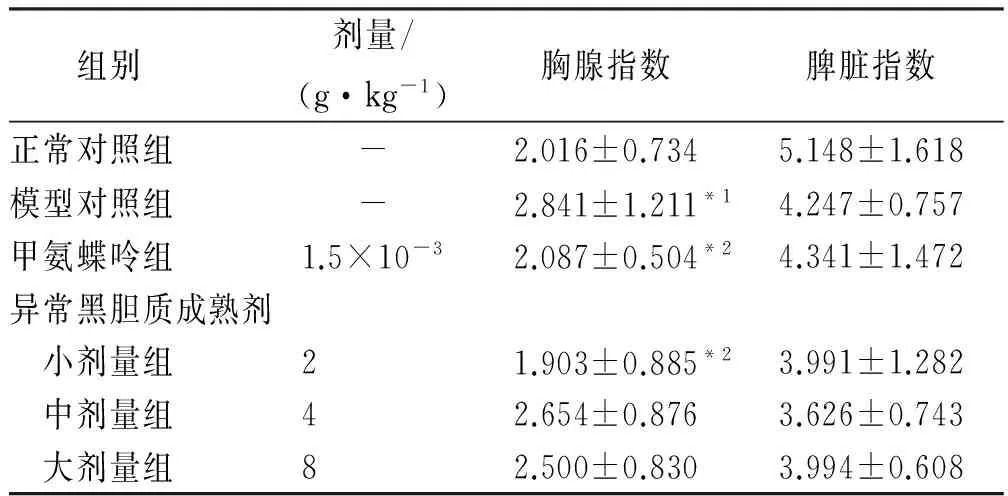
与正常对照组比较,*1P<0.05;与模型对照组比较,*2P<0.05Compared with normol control group,*1P<0.05;compared with model control group,*2P<0.05
2.5.2 尾部皮肤组织病理学变化 小鼠尾部表皮天然缺少颗粒层细胞,类似银屑病表皮角化不全病理改变,因而可作为银屑病角化异常的传统天然模型。正常对照组无颗粒细胞层,实际上相当于模型对照组。与正常对照组比较,甲氨蝶呤组个别区域内出现1或2层颗粒细胞层,但细胞内颗粒不明显。2,4,8 g·kg-1异常黑胆质成熟剂组大部分区域出现1~2层颗粒细胞层,细胞内颗粒较明显。无明显剂量规律性。见图2。
表4 6组小鼠血清IL-10、IL-17、IL-23水平比较
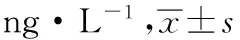

组别小鼠数剂量/(g·kg-1)IL-10IL-17IL-23正常对照组10-61.21±7.704.98±0.674.17±0.34模型对照组10-49.55±4.335.27±0.484.38±0.27甲氨蝶呤组101.5×10-357.65±11.595.02±0.314.41±0.25异常黑胆质成熟剂 小剂量组10257.26±6.424.74±0.505.08±0.68 中剂量组10454.25±3.764.85±0.444.97±0.37 大剂量组10854.44±3.465.04±0.525.15±0.64
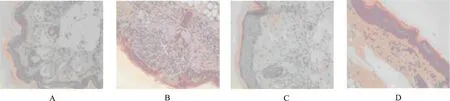
A.正常对照组;B.模型对照组;C.甲氨蝶呤组;D.异常黑胆质成熟剂组(8 g·kg-1剂量)

A.正常对照组;B.甲氨蝶呤组;C.异常黑胆质成熟剂组(2 g·kg-1剂量);D.异常黑胆质成熟剂组(4 g·kg-1剂量)
3 讨论
维吾尔医学将正常体液(合立体·台比依)分为胆液质、血液质、黏液质和黑胆质等4种体液,其中正常黑胆质体液(赛危大依·台比依)是一种色略黑、味酸涩的液体[3],相对其他体液较浓,属性干寒。它具有形成沉淀、保持器官形状与特质的功能。黑胆质体液产生于肝脏,贮于脾脏,由于它对脾胃活动有一定的影响,因而被认为具有增强胃吸收力的功能。维吾尔医学认为,许多疾病都是因为处于平衡状态下的4种正常体液的质和(或)量发生异常变化引起。异常体液性疾病首先是指体液自身发生的变化,其次是指发生变化后的体液对全身或局部产生的作用,并由此导致的疾病[1-2,11]。
维吾尔医学临床实践中,对异常体液(合立体·海日·台比依)性疾病的治疗经常采用维吾尔医独具特色的成熟和清除疗法,首先给予该体液的成熟剂,待物质成熟的特征出现后,再给予清除异常体液的该类体液的清除剂,待全身被清理后,再根据失调气质引起的疾病症状给予专门的治疗药物或补益药[1-2,11]。新疆维吾尔自治区维吾尔医医院制剂异常黑胆质成熟剂由破布木果实、铁线蕨、地锦草等单味药组成,笔者通过现代银屑病动物实验模型探讨其作用。近年来,Th17细胞和Treg细胞失衡与银屑病的关系日益受到重视[12-13],其中IL-17是Th17细胞分泌的重要细胞因子具有促进炎症反应功能,并受IL-23细胞因子调控;IL-10是Treg细胞分泌的重要的抑制性细胞因子,有临床研究应用于银屑病的治疗。
本研究结果表明,异常黑胆质成熟剂能促进小鼠鼠尾表皮颗粒层细胞的形成,改善盐酸普萘洛尔致小鼠耳部皮肤银屑病样组织病理学变化,血液细胞因子IL-17、IL-23、IL-10变化不明显;但仍提示单独使用异常黑胆质成熟剂对实验性银屑病小鼠模型有一定的改善作用,证实维吾尔医临床用药的合理性。
[1] 伊沙克江·马合穆德.中国医学百科全书——维吾尔医学[M].上海:上海科学技术出版社,2005:26-28,141.
[2] 哈木拉提·吾甫尔,阿不都热依木·玉素甫.维吾尔医气质、体液论及其现代研究[M].乌鲁木齐:新疆科学技术出版社,2003:85-86.
[3] 哈木拉提·吾甫尔,阿不都热依木·玉素甫,努尔买买提·艾买提.维吾尔医异常黑胆质新理论[M].乌鲁木齐:新疆人民出版社,2009:3-6.
[4] 伊合帕尔·木拉提,艾合买提·买买提,玛依努尔·阿不拉.维吾尔医治疗银屑病108例临床观察[J].中国民族医药杂志,2005,11(3):3.
[5] 龙亭.甲氨蝶呤治疗银屑病临床观察[J].中国实用医药,2014,9(4):161-162
[6] 孙健,李东宁,阎铁夫,等.丹参注射液对小鼠鼠尾表皮细胞分化及Th1/ Th2细胞因子的影响[J].中国皮肤性病学杂志,2013,27(8):775-777.
[7] BHATIA A,SINGH B,WADHWA S,et al.Novel phosph-olipid-based topical formulations of tamoxifen:evaluation for antipsoriatic activity using mouse-tail model[J].Pharm Devel Tech,2014,19(2):160-163.
[8] 艾克拜尔·安扎尔,夏木西努尔·肖盖提,热比姑丽·伊斯拉木,等.土大黄对实验性银屑病的作用[J].中药药理与临床,2012,28(1):109-111.
[9] 余清宏,赵瑞芝,卢传坚.银屑灵优化方对银屑病豚鼠及炎性刺激角质形成细胞增殖的影响[J].中华中医药杂志,2013,25(5):1531-1533.
[10] 孙建方,高天文.皮肤组织病理学[M].北京:人民卫生出版社,2013:53-55.
[11] 阿不都热依木·卡德尔·阿塔哥.中国新疆维吾尔医药学[M].乌鲁木齐:新疆人民卫生出版社,2013:100-104.
[12] 张立文.寻常型银屑病皮损组织中Th17/Treg失衡的研究[D].武汉:华中科技大学,2012 :6-19.
[13] 贺勤,李慎秋,帅俊,等.白芍总苷对寻常型银屑病患者皮损IL-17表达的影响[J].医药导报,2012,31(7):898-900.
Therapeutic Effect of Munziq Sawda on Mouse Psoriasis Model
RABIGUL Islam1,2,3,YULTUZ Mamat2,3,MAHSUTJAN Kadirt2,3,SIRAPIL Abay1,2,3
(1.DepartmentofPharmacology,BasicMedicalCollegeofXinjiangMedicalUniversity,Urumqi830054,China; 2.LaboratoryofTraditionalUyghurMedicinePrescriptionofXinjiang,Urumqi830049,China; 3.InstituteofXinjiangTraditionalUyghurMedicine,Urumqi830049,China)
Objective To study anti-psoriasis effect of Munziq Sawda on mouse model. Methods We established the mouse tail scale epidermis and psoriasis-like skin inflammation model by applying 5%propranol hydrochloride emulsion on mouse ears,and then observed body weight,thymus and spleen index,measured IL-10 ,IL-17,IL-23 secretion in serum with ELISA method,and also detected istopathological changes of the skin of tail and ears in mouse. Results No obvious abnormalities were found of general condition and body weight (P>0.05)during the experiment period in the Munziq Sawda treated groups(2,4,8 g·kg-1) ; Compared with the model control group,2 g·kg-1Munziq Sawda decreased thymus index(2.841±1.211)vs(1.903±0.885) mg·g-1(P<0.05); Munziq Sawda at 2,4,8 g·kg-1did not obviously impact on the serum level of IL-10,IL-17 and IL-23 (P>0.05); Munziq Sawda 2,4,8 g·kg-1promoted the formation of epidermis granular layer in mouse tail and improved histopathological changes of the mouse ear skin. Conclusion Munziq Sawda has therapeutic action on experimental psoriasis model.
Munziq Sawda; Psoriasis ,experimental; Index,thymus
2014-06-16
2014-08-29
*新疆维吾尔自治区公益性科研院所项目(KY201302)
热比姑丽·伊斯拉木(1970-),女,维吾尔族,新疆阿图什人,副研究员,博士,研究方向:维药药理学。电话:(0)13394919907,E-mail:rabiya@126.com。
斯拉甫·艾白(1960-),男,维吾尔族,新疆伊犁人,教授,博士生导师,研究方向:维药药理学。电话:(0)13999193503,E-mail:aibai@263.net。
R285;R291.5
A
1004-0781(2015)09-1135-05
10.3870/j.issn.1004-0781.2015.09.003
