溶剂法脱除天然气中有机硫的原理及发展趋势
2015-01-03王亚军李春虎迟明浩
王亚军 李春虎 薛 真 迟明浩
中国海洋大学化学化工学院, 山东 青岛 266100
0 前言
天然气的主要成分是烷烃,此外还有H2S、CO2、H2O、有机硫等杂质。在天然气中的有机硫化合物主要有二硫化碳(CS2)、羰基硫(COS)、硫醇(RSH)、硫醚(RSR)及二硫醚(RSSR)等。含硫化物组分在天然气开采、处理、储运过程中会造成设备和管线腐蚀;用作燃料时会带来环境污染,危害用户健康;用作化工原料时会导致下游催化剂中毒。所以近年来,国际社会对商品天然气中有机硫含量的要求愈来愈严格,部分欧洲国家要求民用天然气有机硫含量低于16 mg /m3[1],因而天然气中有机硫脱除工艺技术的研发受到了普遍关注。国内外专家学者对天然气中有机硫脱除的机理、工艺研究做了大量的研究工作,本文将重点阐述溶剂法脱除天然气中有机硫的工艺现状及发展趋势。
1 溶剂法脱除天然气中有机硫的原理
1.1 物理溶剂法
物理溶剂法是依靠有机硫在不同压力、温度下在溶剂中有不同的溶解度来取得脱除效果的方法。其工艺过程一般是通过加压、降温等手段使有机硫、H2S、CO2等酸性气体溶解在物理溶剂中,再通过减压、升温、汽提的方法将酸气从溶剂富液中解吸,使溶剂再生。有机硫气体在溶剂中的溶解度遵循亨利定律。常用的物理溶剂有环丁砜(SUL)、二甲基甲酰胺(DMF)、二甲基亚砜(DMSO)、磷酸三丁酯(TBP)、碳酸丙稀酯(PC)等。工业上Selexol 物理溶剂法应用最广泛,其溶剂的主要成分是碳链长度为3 ~8 的聚乙二醇二甲醚。
物理溶剂对气体组分的吸收取决于其挥发度,气体组分的挥发度可以用常压下的沸点来衡量[2],常压沸点愈高的组分愈容易被物理溶剂吸收,而挥发度(常压沸点)相近的组分则同时被吸收。从表1 可以看出,脱除COS 时将有大量丙烷组分被共吸收;脱除甲硫醇时则有大量丁烷组分被共吸收。

表1 天然气中常见组分的常压沸点
物理溶剂法的优点是溶剂稳定性好,对设备腐蚀小,溶剂循环量少,能耗低;但物理溶剂通常有重烃共吸收性高、选择性差的缺点,并且需要在高压条件下操作,设备成本相对较高。
1.2 化学溶剂法
化学溶剂法是通过有机硫和溶剂中的碱性物质发生酸碱中和反应,使有机硫转化成盐溶解在溶剂中,从而脱除天然气中的有机硫气体。工业上常用的化学溶剂最具有代表性的是醇胺法。
醇胺类化合物的分子结构中至少包含有1 个羟基和1 个胺基。羟基的作用是降低化合物的蒸汽压,并增加其水溶性;而胺基则为水溶液提供必要的碱度,促进对酸性气体组分的吸收。按连接在胺基的氮原子上的“活泼”氢原子数,醇胺可分为伯醇胺(如MEA)、仲醇胺(如DEA、DIPA)和叔醇胺(如MDEA)三大类。
根据Lewis 酸碱理论,醇胺首先与天然气中酸性较强的H2S 和CO2反应,再与酸性较弱的有机硫反应。醇胺法脱除天然气中的有机硫化合物存在以下二种机理:
1)有机硫在醇胺溶液中的物理溶解。
2)部分有机硫与醇胺直接反应生成可再生或难以再生的含硫化合物,也有部分有机硫化合物与水发生水解反应而生成H2S 和CO2,进一步被醇胺吸收,统称为化学溶解。
1.2.1 COS 的脱除机理
根据脱除过程本质的不同可将砜胺溶液对COS 的溶解脱除作用区分为物理溶解、化学吸收、催化水解反应后再吸收。
1.2.1.1 物理溶解
COS 的沸点与丙烷相近,在水中的溶解度较低,仅为1.254 g /L。
1.2.1.2 水解反应
COS 的分子结构为线性分子,可以水解。
反应式:

当COS 水解为H2S 及CO2时,易脱除。然而,低温下COS 水解的反应速率颇慢,25 ℃下的拟一级反应速率常数仅有0.001 1 s-1[3]。
1.2.1.3 化学吸收
COS 分子的结构和性质与CO2类似,与碱性的胺类化合物的反应遵从类似CO2的反应机理[4],碱性较强的伯胺和仲胺能够与COS 反应生成相应的硫代氨基甲酸盐,基于生成两性离子的反应式如下:
伯胺:

仲胺:

对于叔胺而言,基于碱催化方式的反应式为:
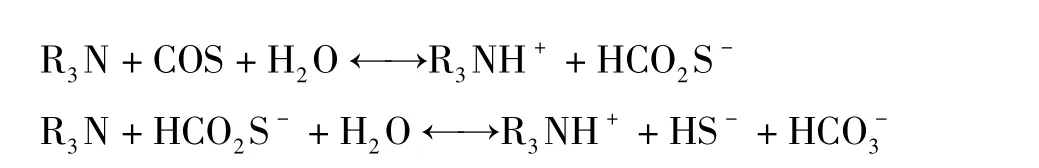
Littel RJ 等人[5]在研究COS 在MEA、DEA、DGA、DIPA、MMEA 和AMP 等醇胺水溶液中反应动力学时发现,COS 与醇胺分子反应形成的两性离子在相应醇胺分子催化作用下的脱质子反应速率均比该两性离子在水分子催化作用下的脱质子反应速率快100 倍以上。因此,两性离子脱质子反应中起主要作用的是胺类分子。对于MDEA 这类叔醇胺而言,通过化学反应脱除天然气中COS 的方式仅限于碱催化过程。根据Amararene FBC 等人[6]关于COS 在DEA 和MDEA 溶液中吸收动力学的研究结果,通过碱催化方式脱除COS 的过程比基于生成两性离子的过程具有更低的反应速率。
MEA 会与COS 发生不可逆的降解反应,所以当天然气中含有COS 时应避免使用MEA;DEA 是仲醇胺,与MEA 相比,它与COS 的反应速率较低,故与有机硫化合物发生副反应而造成的溶剂损失量相对较少,主要通过催化水解反应脱除COS 适用于原料气中有机硫化合物含量较高的原料气;DIPA 溶剂比热容较高,CO2共吸收率甚高,再生时能耗较高,在天然气脱有机硫领域应用较少,由于DIPA 具有良好的脱除COS 的能力,多用于处理炼厂气;MDEA 溶液脱除COS 的脱除率仅20左右。
1.2.2 硫醇的脱除
Bedell SA 等人[7]认为硫醇在混合溶剂中的溶解过程可以用图1 表示。

图1 硫醇在混合溶剂中溶解示意图
从图1 可知,硫醇的溶解是由物理溶解和化学溶解两部分组成的。物理溶解量与温度、压力有关;化学溶解量等于硫醇在胺液中形成的硫醇盐(RS-)的溶解量。
1.2.2.1 物理溶解
硫醇在物理溶剂中的溶解度取决于体系的亨利常数,其值愈小则溶解度愈大。甲硫醇气体在常见醇胺水溶液中的亨利常数,见表2。例如,40 ℃下甲硫醇溶解于MDEA 水溶液的亨利常数颇大,在吸收了H2S 和CO2后亨利常数进一步升高,溶解度更低[8]。
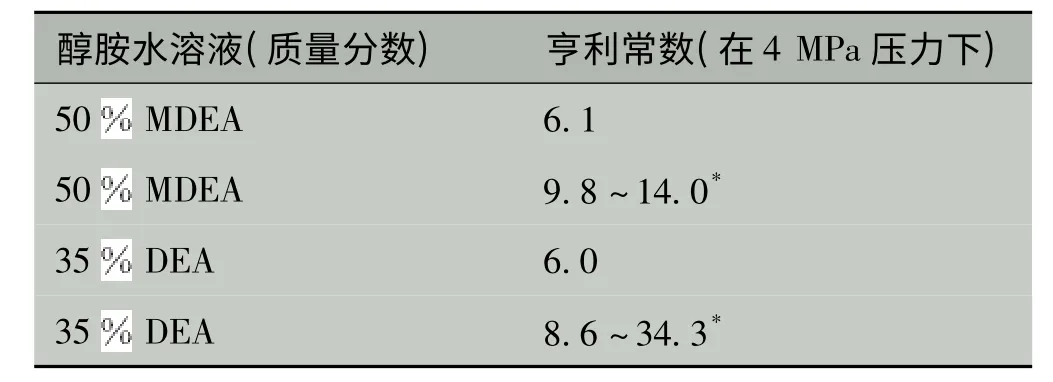
表2 甲硫醇溶解于醇胺水溶液的亨利常数(40 ℃)
1.2.2.2
Mahmud A 等人[9]探讨了硫醇与醇胺可能的反应方式,结果表明,醇胺分子很难与硫醇分子发生离子反应,两种分子之间可能形成一种Lewis 酸碱加合物。以MEA为例,加合方式可能为:
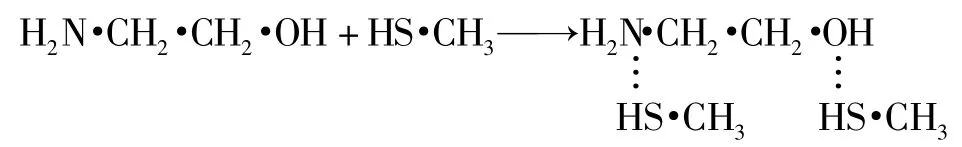
Bede S A 等人[7]认为,硫醇化合物也能够与醇胺发生化学反应形成相应的硫醇盐而溶解于溶液中,反应式如下:

但是由于硫醇化合物的酸性比COS 还弱,反应速率更低,且醇胺化合物对硫醇分子的化学溶解性随溶剂中酸性组分负荷的增加而迅速下降,当醇胺的酸性组分负荷大于0.1 mol(酸气)/mol(醇胺)时,醇胺水溶液对硫醇的化学溶解度迅速下降到占物理溶解度的10左右。对于CO2、有机硫石油天然气的净化工艺,溶剂中酸性组分负荷将明显大于0.1 mol(酸气)/mol(醇胺),因此原料气中的硫醇化合物将主要依靠物理溶解而脱除,但醇胺化合物对硫醇的物理溶解性同样较低。由于一般的醇胺化合物对硫醇分子的化学溶解性和物理溶解性均不理想,因此总体脱除率不高,且随着硫醇分子碳数的增加,硫醇化合物的酸性降低,脱除率显著下降。
1.2.3 CS2的脱除
砜胺溶液对CS2的溶解脱除作用主要为化学反应、物理溶解和催化水解反应后再吸收三种。
1)以伯胺为例,主要发生以下化学反应:
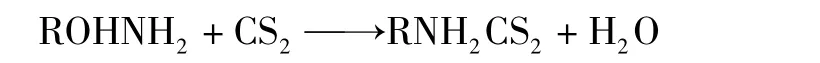
2)砜胺溶液中的碱性有利于CS2的水解,CS2催化水解反应的反应式如下:

CS2水解后生成的H2S 和CO2非常容易脱除。
在用于天然气脱除有机硫的各种烷醇胺中,MEA 是最强的有机碱,在一定工况条件下,MEA 会与CS2发生不可逆的降解反应,所以当天然气中含CS2时应避免使用MEA 类伯胺;与MEA 等伯胺相比,仲胺、叔醇胺与CS2的反应速率较低,主要通过催化水解反应脱除CS2。
1.2.4 硫醚(RSR)及二硫醚(RSSR)的脱除
硫醚在天然气中的含量极少,属中性物质,化学反应性差,只能通过物理溶解脱除。
1.3 混合溶剂法
混合溶剂是用物理溶剂和化学溶剂按一定比例复配得到的,该法兼具物理溶剂法和化学溶剂法的特点。工业上最常用的混合溶剂是砜胺法溶液。砜胺法溶液由环丁砜、醇胺和水组成。
砜胺法溶液中的环丁砜和水对有机硫酸性组分的吸收属于物理吸收,有机硫化合物易溶于环丁砜,它们基本上服从享利定律;砜胺法溶液中醇胺对有机硫酸性组分的吸收属于化学吸收;砜胺溶液吸收有机硫酸性组分是物理溶解与化学吸收作用的总和。
砜胺类溶剂脱除有机硫工艺中,国外比较有代表性的有Sulfinol 法、Flexsorb 混合SE 法、Optisol 法。国内近些年也对混合溶剂法做了大量研究,中国石油西南油气田公司天然气研究院开发的CT8 -20 配方溶剂适用于天然气中高浓度有机硫的脱除。华东理工大学章建华[4]开发的XDS、UDS 溶剂,也有较好的脱除有机硫能力,并且腐蚀性、发泡倾向比MDEA 水溶液低。
混合溶剂法兼具物理溶剂法和化学溶剂法的优点。与化学溶剂法相比,污染小,再生能耗低,可将有机硫、H2S 和CO2在同一单元一起脱除;与物理溶剂法相比,重烃吸收少,选择性高;混合溶剂法可调范围大,该法已成为国内外重点开发对象。
2 溶剂法净化工艺的发展趋势
2.1 脱有机硫溶剂配方优化、系列化
由于醇胺类脱有机硫溶剂技术的操作数据和经验的日益丰富,具有针对性的各种溶剂不断涌现,复合型已成为砜胺类脱有机硫溶剂技术的主流,把吸收量大、腐蚀性低、能耗小、空间位阻系数较大的醇胺(如MDEA、AMP)与反应速率较高但吸收量相对较低的胺(如伯胺、仲胺)相混合,再加入部分有机溶剂,可大大改善有机硫的处理过程。另一方面是溶剂的系列化,国外各种牌号的商业溶剂均是系列化溶剂。系列化溶剂已成为国外公司的专有技术,在世界范围内形成优势和堡垒。值得注意的是,优化和系列化都是建立在基础研究上的,由于有基础理论的支持,则可以预见和开发一种全新的溶剂。
2.2 新型脱有机硫溶剂的开发
物理化学混合溶剂法成为脱除有机硫最好的选择,如果找到一种物质,兼具物理溶剂和化学溶剂的特点,理论上这种新型物质肯定能提高天然气中有机硫的脱除率。新型脱有机硫溶剂可以通过质子化平衡常数、Taft空间位阻常数、沸点[10]加以衡量:
1)质子化平衡常数(pKa):醇胺的碱性源自其分子中氮原子上未配对电子对质子的亲合能力,而氮原子上烷基取代基团的存在则不同程度地削弱了亲合能力,导致其碱性减弱,且气液界面上与酸性气体反应的平衡常数也发生变化。pKa称为醇胺的质子化平衡常数,是醇胺溶液氢离子浓度的负对数,用以衡量醇胺吸收酸性气体的反应活性,其值愈大则醇胺的化学反应活性愈高。适合工业化有机胺pKa应>8.6,最佳适宜范围为9.5 ~10.6,如果<8.6,吸收的硫化氢容易解吸;>10.6,会增加再生时的能量消耗。
2)Taft 空间位阻常数(—Es):醇胺分子中的胺基(—NH2)上引入不同有机基团对选吸效果的影响,可以用Taft 空间位阻常数—Es来加以衡量。研究表明,胺基上的H 原子被空间位阻常数>1.74 的叔丁基取代后,就能得到选吸效果比MDEA 好得多的空间位阻胺。
3)沸点:选择醇胺的沸点最好>180 ℃(1 标准大气压下),>225 ℃就更佳,可以大大减少再生时溶剂的损失。
两种新型脱有机硫溶剂:叔丁胺基乙氧基乙醇,结构式如下。简称TBEE,一种透明液体,有氨味、易溶于水,常压沸点242 ℃,空间位阻系数2.1,pKa为10.3,对H2S的相对选择性是MDEA 的3 倍。

两种化合物比MDEA 具有更强的空间位阻系数,胺基、醚基数量增多,代表在同样摩尔含量情况下,会有更强的酸性气体吸收能力。两种物质既有胺基,又有Selexol 法物理溶剂中具有的羟基、醚基,兼具物理溶剂和化学溶剂的优点,将是未来天然气脱有机硫工艺新型溶剂的首选。
2.3 有机硫转化的催化剂研制
通过结构设计和修饰官能团,合成具有促进有机硫转化的新型催化剂。将新型催化剂与醇胺溶液复配,可以开发全新的配方型脱有机硫溶剂。专利US 6531103[12]介绍,磺化酞菁铁盐和卟吩铁盐中金属离子和有机硫中硫醇形成配位键,数据表明,加入1质量分数磺化酞菁铁盐的MDEA 溶液中硫醇的脱除率达99以上。这种对环境友好、低挥发,对酸气组分有较高溶解能力和选择性等独特功能的催化剂的应用有可能成为天然气净化领域中一个全新的技术开发方向。
2.4 现有的装置改进
近年来为提高天然气中有机硫的脱除效率,很多装置的工艺流程有了大量改进,设置混合器、吸收塔多点进料、半贫液分流等[13]改进措施常能获得很好的效果。
3 结论
近年来为提高天然气中有机硫的脱除效率,开发出了多种不同天然气脱有机硫的工艺,其中应用最为广泛则是混合溶剂吸收法。
溶剂法工艺的未来发展趋势是开发兼具物理溶剂和化学溶剂特点的新型脱有机硫溶剂。新型脱有机硫溶剂可以通过质子化平衡常数、Taft 空间位阻常数、沸点加以衡量。同时,有机硫转化催化剂与醇胺溶液复配也是天然气净化领域中一个全新的技术开发方向。
[1]王开岳.天然气净化工艺脱硫脱碳、脱水、硫磺回收及尾气处理[M].北京:石油工业出版社,2005:4 -5.Wang Kaiyue.Purification Process such as Natural Gas Desulfurization Decarbonization,Dehydration,Sulfur Recovery and Tail Gas Treatment[M]. Beijing:Petroleum Industry Press,2005:4 -5.
[2]Hugo R W. Deep COS Removal[J]. Hydrocarbon Engineering,2000,5(6):73 -77.
[3]王开岳. 天然气中COS 的脱除[J]. 石油与天然气化工,2007,36(1):28 -36.Wang Kaiyue.Removal of COS in Natural Gas[J]. Chemical Engineering of Oil & Gas,2007,36(1):28 -36.
[4]章建华.新型溶剂高效吸收净化高酸性石油天然气技术开发研究[D].上海:华东理工大学,2011.Zhang Jianhua. Research and Development of the Novel Solvent with Excellent Desulfurization Performance for Purifying High Sour Petroleum Natural Gas[D]. Shanghai:East China University of Science & Technology,2011.
[5]Littel R J,Versteeg G F,Swaajj W P M.Kinetics of COS with Primary and Secondary Amines in Aqueous Solutions[J].AIChE Journal,1992,38(2):244 -250.
[6]Amararene F B C.Kinetics of Carbonyl Sulfide Absorption with Aqueous Solutions of Diethanolamine and Methyldiethanolamine[J]. Industrial & Engineering Chemistry Research,2004,43(19):6136 -6141.
[7]Bedell S A,Miller M. Aqueous Amines as Reactive Solvents for Mercaptan Removal[J].Industrial & Engineering Chemistry Research,2007,46(11):3729 -3733.
[8]陈赓良,常宏岗.配方型溶剂的应用与气体净化工艺的发展动向[M].2 版.北京:石油工业出版社,2009:70.Chen Gengliang,Chang Hongang. Application of Formulated Solvent and Development of Gas Purification Technology[M].2nd ed.Beijing:Petroleum Industry Press,2009:70.
[9]Rahman M A,Maddox R N,Mains G J.Reactions of Carbonyl Sulfide and Methyl Mercaptan with Ethanolamines[J].Industrial & Engineering Chemistry Research,1989,28(4):470 -475.
[10]Ho WWS,Sartori G,Stogryn EL.Absorbent Composition Containing a Severely-hindered Amine Mixture with Amine Salts and/or Aminoacid Additives for the Absorption of H2S:US,7442840[P].2007 -05 -04.
[11]Stogryn E L,Savage D W,Sartori G.Process for Selective Removal of H2S from Mixtures Containing H2S and CO2Using Di-severely Sterically Hindered Secondary Aminoether:US,4405583[P].1983 -09 -30.
[12]Hakka L E,Forte P.Process for Removing Sulfur Compounds from Gas and Liquid Hydrocarbon Streams:US,6531103[P].2003 -03 -11.
[13]陈赓良,缪明富,马 卫. 天然气中有机硫化合物脱除工艺评述[J].天然气工业,2007,27(10):120 -122.Chen Gengliang,Miao Mingfu,Ma Wei.A Review on Natural Gas Desulfurization Technology[J]. Natural Gas Industry,2007,27(10):120 -122.
