长柄扁桃仁多酚提取工艺及抗氧化活性研究
2015-01-02樊金拴赵韵美高智辉
苏 锐,樊金拴,郑 涛,赵韵美,马 菁,高智辉
(西北农林科技大学 林学院,陕西 杨陵712100)
长柄扁桃(Amygdalus pedunculata),又叫野樱桃、柄扁桃、苦豆子、山樱桃、布衣勒斯,属多年生木本植物,落叶灌木。长柄扁桃主要分布于内蒙古阴山浅山区和陕北神木、定边、横山、榆林等地,在榆林有集中分布[1]。长柄扁桃具有抗旱、固沙、抗风蚀、适应范围广等优良特性,是我国西部干旱、半干旱地区山地和沙地良好的水土保持树种、观赏灌木,是育种的原始材料及嫁接繁殖普通扁桃的砧木[1-2]。长柄扁桃的果仁出油率高,用压榨法提取,最高出油率可达46%。其中的棕榈油酸有益于皮肤保健、预防治疗高血压、心血管系统疾病,微量元素对人的身体健康也大有裨益。以长柄扁桃油为原料,可成功制备生物柴油,转化率可达98%以上,产油率在9%以上[3]。长柄扁桃仁中苦杏仁甙含量约为0.2%。苦杏仁甙是重要的医药原材料,具有降气、止咳、平喘、润肠和通便的功效[4]。
植物多酚(plant polyphenol)是一类广泛存在于植物体内的多酚类物质,在植物中的含量仅次于纤维素、半纤维素和木质素,储量丰富[5]。酚类物质对人体有着重要的生理功能,具有很强的抗氧化效果[6]。目前,国内外对于多酚类物质的研究主要集中在苹果、核桃、板栗、茶树等方面[7-11],对长柄扁桃的研究主要集中在叶片结构、生理生化特性、种仁油料提取、仁中矿质元素分析等方面[12-16],而对长柄扁桃仁中多酚物质的含量及其抗氧化活性等报道较少。本研究以多酚提取量为指标,通过单因素及正交试验对长柄扁桃仁中多酚的提取工艺进行研究,并且利用DPPH法、ABTS法及FRAP法测定了陕西神木、榆阳、内蒙古乌审旗、固阳、河北丰宁5个不同种源地样品清除自由基的能力及总还原力,旨在开发高附加值的长柄扁桃仁多酚,为长柄扁桃的综合利用和产业化开发提供理论依据。
1 材料与方法
长柄扁桃种子→脱壳→粉碎→超声处理→抽滤→测定多酚提取量→测定抗氧化活性
1.1 材料与试剂
长柄扁桃种子由西北农林科技大学园艺学院郭春会教授提供(分别采自陕西榆阳、陕西神木、内蒙古乌审旗、内蒙古固阳、河北丰宁)。
二苯基苦味酰基苯肼基自由基(1,1-diphenyl-2-picrylhydrazyl,DPPH)、2,2'-联 氮-双-(3-乙 基 苯噻唑啉-6-磺酸)[(2,2'-azino-bis(3-ethylbenzthiazoline-6-sulfpnic acid),ABTS]、三 吡 啶 三 吖 嗪(tripyridyl-triazine,TPTZ)美国sigma公司;福林酚 北京索莱宝科技有限公司;没食子酸 上海晶纯生化科技股份有限公司;无水碳酸钠 广东光华化学厂有限公司;石油醚、磷酸氢二钠、磷酸二氢钾、浓盐酸、过硫酸钾、醋酸钠、三氯化铁 天津博迪化工股份有限公司;无水乙醇、氯化钠、氯化钾、冰乙酸 成都市科龙化工试剂厂。
1.2 仪器与设备
UV-3100紫外-可见分光光度计 上海美谱达仪器有限公司;XMTD电热恒温水浴锅 北京科伟试验仪器设备厂;FA2004分析天平 上海精科天平;KQ-500DE超声清洗器昆山市超声仪器有限公司;SHB-Ⅲ循环式多用真空泵 郑州长城科工贸有限公司;H1650台式高速离心机 长沙湘仪离心机仪器有限公司;FW-200高速万能粉碎机 北京中兴伟业仪器有限公司。
1.3 材料处理
将5个种源地的长柄扁桃种子进行破壳,把种仁粉碎成粉末按照料液比1g∶21mL加入石油醚(沸程60~90℃),在50℃350W 下进行超声处理30min。抽滤得去油脂后的样品粉末(提取率约为66.0%),置于-4℃冰箱保存[17-19]。
1.4 长柄扁桃仁多酚的提取
1.4.1 单因素试验 以陕西省榆林市榆阳区采得种子为材料,采用超声辅助提取法[20-22],研究料液比、乙醇体积分数、超声时间、提取温度对长柄扁桃仁中多酚提取量的影响,试验重复5次,取平均值。
1.4.1.1 料液比 准确称取0.5g脱脂后的仁粉,按照1∶10、1∶20、1∶30、1∶40、1∶50、1∶60、1∶70、1∶80(g∶mL)的料液比加入体积分数为50%的乙醇,在30℃350W功率下超声提取30min,抽滤得提取液,定容至50mL,得10mg·mL-1提取液。以多酚提取量为考察指标确定最佳料液比。
1.4.1.2 乙醇体积分数 准确称取0.5g脱脂后的仁粉,加入15mL体积分数分别为0、10%、20%、30%、40%、50%、60%、70%、80%的乙醇,在30℃350W功率下超声提取30min,抽滤得提取液,定容至50mL,得10mg·mL-1提取液。以多酚提取量为考察指标确定最佳乙醇体积分数。
1.4.1.3 时间 准确称取0.5g脱脂后的仁粉,加入15mL体积分数为20%乙醇,在30℃350W功率下分别超声提取15、30、45、60、75min和90min,抽滤得提取液,定容至50mL,得10mg·mL-1提取液。以多酚提取量为考察指标确定最佳提取时间。
1.4.1.4 温度 准确称取0.5g脱脂后的仁粉,加入15mL体积分数为20%的乙醇,分别在30、40、50、60℃和70℃350W功率下超声提取60min,抽滤得提取液,定容至50mL,得10mg·mL-1提取液。以多酚提取量为考察指标确定最佳提取温度。
1.4.2 正交试验 在单因素试验结果的基础上,对长柄扁桃仁多酚提取工艺的料液比、乙醇体积分数、提取温度和时间进行4因素3水平的L9(34)正交试验(表1),确定最佳提取条件组合,试验重复3次。
1.5 长柄扁桃仁多酚提取量的测定
采用福林酚法[23-24]进行多酚提取量测定。将没食子酸作为标准品,准确称取25mg没食子酸,加蒸馏水定容至1 000mL,制得0.025mg·mL-1的标准液。分别准确称取0.0、0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0、4.5mL和5.0mL没食子酸标准液加入0.5mL Folin-Ciocalteau显色剂,反应20 min后加入2.5mL 1mol·L-1Na2CO3溶液定容至25mL。在30℃下避光水浴1h后离心,测定765nm处的吸光值。以没食子酸质量浓度(μg·mL-1)为横坐标,测得吸光值为纵坐标绘制标准曲线,得线性回归方程y=0.104 9x+0.020 2,R2=0.996 5。

表1 正交试验设计Table 1 Orthogonal experiment
取1mL提取液按照上述方法显色,测定765 nm处的吸光值。依据线性回归方程,计算可得提取液中多酚提取量m(没食子酸当量)。
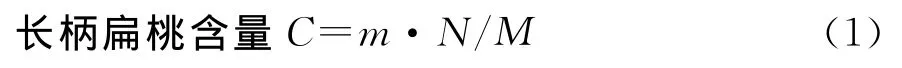
式中:m为1mL提取液中所含多酚质量(mg),M为长柄扁桃仁脱脂后质量(g),N为提取液的稀释倍数。
1.6 抗氧化活性测定
1.6.1 DPPH自由基清除能力测定 参照Yen[25,27-28]等方法,有改动。分别取最佳工艺下神木、榆阳、乌审旗、固阳、丰宁5个种源地的长柄扁桃仁多酚提取液5mL定容至25mL,依次稀释得2 000、1 500、1 200、1 000、900、800、600、400、200、100、50μg·mL-1和25μg·mL-1样品。分别吸取2mL样液、2mL 0.1mmol·L-1DPPH 溶液混匀,避光静置30min后,在517nm测得试样吸光值(Ai),取2mL 20%乙醇代替样液测得空白吸光值(Ac),以2mL样液中加入2mL 20%乙醇测得样液吸光值(Aj),按下列公式计算清除率K(%)。

以稀释后的质量浓度(μg·mL-1)为横坐标,清除率K(%)为纵坐标绘制对数曲线,计算清除率50%时样品的浓度(IC50),试验重复3次。
1.6.2 ABTS自由基清除能力测定 参照Re R[26-30]等方法,有改动。
ABTS·+反应液配制:将7mmol·L-1ABTS溶液与2.45mmol·L-1K2S2O8溶液按1∶1混合,室温反应过夜(12~16h)制成ABTS·+储备液。使用前用10mmol·L-1的PBS缓冲液稀释,调节其在30℃,734nm下的吸光值为0.70±0.02,制得成ABTS·+反应液。
以Vc为标准品计算抗氧化活性(VCEAC值,单位μmol·g-1)。称取0.017 6g抗坏血酸,蒸馏水溶解定容至100mL,得到1mmol·L-1的Vc标准液。依次取0.0、1.0、2.0、3.0、4.0mL 和5.0 mL Vc标准液于10mL容量瓶中,蒸馏水定容,得到0.0、0.1、0.2、0.3、0.4mmol·L-1和0.5mmol·L-1浓度梯度的Vc标准液。
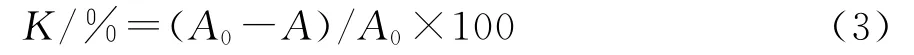
式中:A0为Vc浓度为0.0mmol·L-1时测得的吸光值。
取0.1mL不同浓度梯度的Vc标准液于试管中,加入3.9mL ABTS·+工作液混匀,37℃水浴10min,测定734nm处的吸光值A734,计算清除率K(%)。以Vc浓度(μmol·L-1)为横坐标,清除率K(%)为纵坐标绘制标准曲线,得回归方程y=92.104x+0.200 7,R2=0.999 7。将最佳工艺下5个不同种源地的长柄扁桃仁多酚提取液稀释至6 mg·mL-1,进行以上操作,测得清除率计算VCEAC 值(μmol·g-1),试验重复3次。
1.6.3 FRAP法测定总还原力 参照Benzie和Strain[31-32]等方法,有改动。
FRAP工作液配制:300mmol·L-1醋酸盐缓冲液、10mmol·L-1TPTZ溶液、20mmol·L-1三氯化铁溶液按10∶1∶1配制,现用现配。
准确称取0.030 4g硫酸亚铁溶于适量的水中,加入18mo1·L-1的硫酸2.5mL,加蒸馏水定容至100mL。取上述溶液5mL于50mL容量瓶中,蒸馏水定容,即为2 000μmol·L-1FeSO4溶液。稀释依次配得0、25、50、75、100、125、150、175 μmol·L-1和200μmol·L-1标准溶液。
取0.4mL不同浓度梯度的FeSO4标准溶液,加入3mL FRAP工作液,37℃下反应10min,测定593nm处的吸光值A593。以FeSO4标准溶液浓度(μmol·L-1)为横坐标,测得吸光值A593为纵坐标,绘制标准曲线,得回归方程y=0.002 6x+0.161 2,R2=0.993 6。将最佳提取工艺下5个不同种源地的长柄扁桃仁多酚提取液稀释至1mg·mL-1,进行以上操作,计算FRAP值,试验重复3次。
1.7 统计学处理
2 结果与分析
2.1 料液比对多酚提取的影响
由图1可知,随着乙醇使用量的增加,多酚提取量呈先上升后下降的趋势。当料液比1g∶10mL时,多酚提取量为(1.279±0.043)mg·g-1,料液比1g∶20mL时多酚提取量为(1.378±0.046)mg·g-1,显著高于其他各料液比(p<0.05),之后呈下降趋势。这可能是因为料液比为1∶20时,溶剂对多酚的溶解已基本达到饱和,继续增加溶剂用量,并不能显著提高多酚提取量。
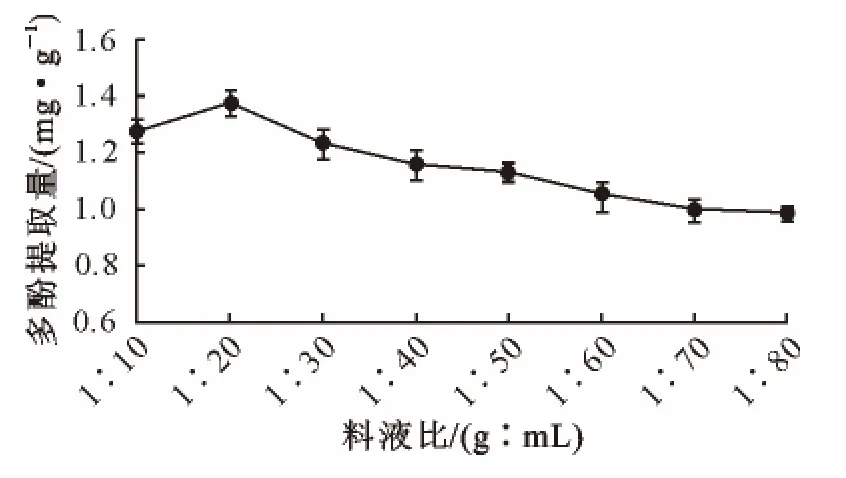
图1 不同料液比对多酚提取量的影响Fig.1 Effect of ratio of material to solvent on the polyphenols extraction
2.2 乙醇体积分数对多酚提取的影响
由图2可知,随着乙醇体积分数升高,多酚提取量呈先下降后上升再下降的趋势。当乙醇体积分数为0%,即使用水提取时,多酚提取量为(1.927±0.163)mg·g-1,当使用10%乙醇提取时,多酚提取量下降至(1.771±0.095)mg·g-1,当使用20%乙醇提取时,多酚提取量最高为(1.980±0.119)mg·g-1,显著高于使用30%乙醇时的多酚提取量(p<0.05),之后多酚提取量呈下降趋势。这可能是因为当乙醇体积分数过高时,其他物质如醇溶性杂质等成分溶出量增加,这些物质与多酚竞争乙醇-水分子,使得多酚溶出量降低,进而导致多酚得率下降。因此,乙醇体积分数以20%为最佳[33]。

图2 不同乙醇体积分数对多酚提取的影响Fig.2 Effect of concentration on the polyphenols extraction
2.3 超声时间对多酚提取的影响
由图3可知,当提取时间介于15~60min时,长柄扁桃仁多酚提取量随着提取时间的增加而增加,60min时含量达到最高,为(2.032±0.065)mg·g-1,显著高于15~45min时的提取量(p<0.05)。而当提取时间超过60min时,多酚提取量随着提取时间的增加而略有降低。这可能是由于浸提时间太短,与蛋白质、纤维素结合的酚类物质来不及溶出;提取时间过长,由于多酚类物质稳定性不好,容易发生分解[34],所以提取时间过长,其含量降低。因此,提取时间以60min为最佳。
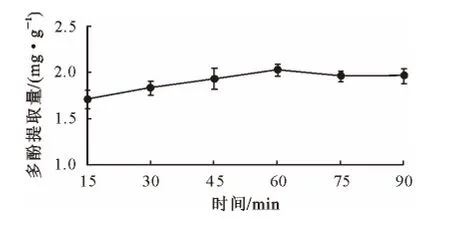
图3 不同超声时间对多酚提取的影响Fig.3 Effect of time on the polyphenols extraction
2.4 提取温度对多酚提取的影响
由图4可知,随着提取温度的升高,多酚提取量呈下降趋势。当在30℃下提取时,多酚提取量为(2.067±0.131)mg·g-1,显著高于其他各温度梯度(p<0.05),在50℃下提取时,多酚提取量为(1.720±0.024)mg·g-1,当提取温度为70℃时,多酚提取量仅为(0.503±0.110)mg·g-1。
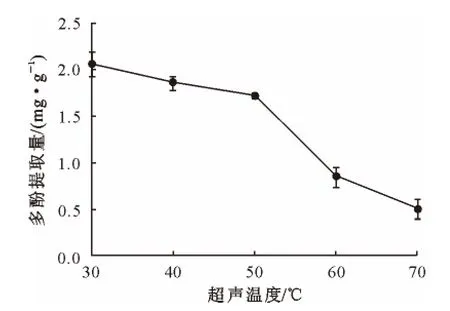
图4 不同提取温度对多酚提取的影响Fig.4 Effect of temperature on the polyphenols extraction
一般来说,温度越高,扩散速度越快。因为温度升高,使得植物组织软化快,易膨胀,从而增加可溶性物质的溶解度和扩散速度,促进有效成分浸出。但温度过高,酚类物质结构易受到破坏,导致多酚提取量降低。因此,提取温度以30℃为佳。
2.5 长柄扁桃仁多酚提取的正交试验结果
在单因素试验结果的基础上,对长柄扁桃仁多酚提取工艺中的料液比、乙醇体积分数、提取温度和时间4个因素按照L9(34)正交表进行试验,结果如表2、表3所示。
由表2可以看出,长柄扁桃仁中多酚的最佳提取工艺为处理二,即乙醇体积分数20%,料液比1∶20,提取温度40℃,提取60min。通过方差分析(表3)可以看出,超声时间和乙醇体积分数有极显著差异(p<0.01),温度和料液比有显著差异(p<0.05)。各因素对多酚提取量影响大小依次为:乙醇体积分数>料液比>温度>时间,说明在选取的各因素梯度范围内,超声辅助提取多酚对乙醇体积分数、料液比非常敏感,对温度、时间较敏感。

表2 正交试验结果Table 2 Results of orthogonal experiment
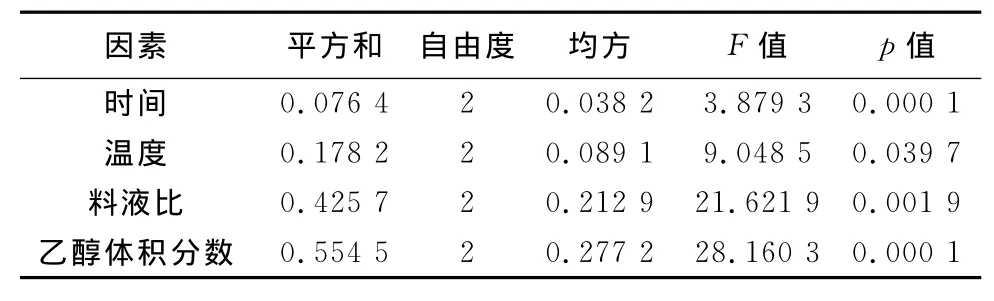
表3 方差分析结果Table 3 Results of variance analysis
2.6 最佳工艺验证试验
准确称取0.5g脱脂后的仁粉,按照上述最佳工艺条件提取,计算多酚提取量。表4表明,最佳条件下多酚的平均提取量是2.102mg·g-1,重复性好,按此条件提取的多酚提取量均高于表2中的任何一组。因此在本试验范围内处理2为最佳提取工艺参数。
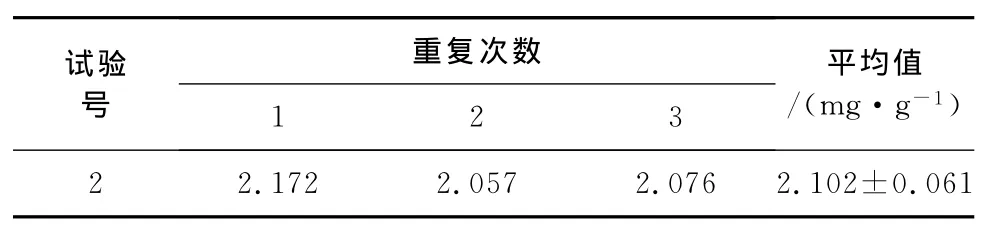
表4 验证试验结果Table 4 Results of validation experiment
2.7 不同种源地种仁的抗氧化活性比较
由图5、表5可知,不同种源地的长柄扁桃仁多酚提取液均有不同的清除自由基能力。其中神木样品的IC50值和VCEAC值分别为(199.90±14.07)μg·mL-1和(139.65±1.43)μmol·g-1,清除自由基能力显著强于另外4个种源地样品(p<0.05),榆阳、乌审旗样品次之,IC50值和VCEAC值分别为(388.66±9.36)μg·mL-1、(127.78±3.30)μmol·g-1和(394.31±8.96)μg·mL-1、(132.43±1.78)μmol·g-1,丰宁样品IC50值和VCEAC 值仅分别为(640.87±24.45)μg·mL-1和(55.68±3.52)μmol·g-1。
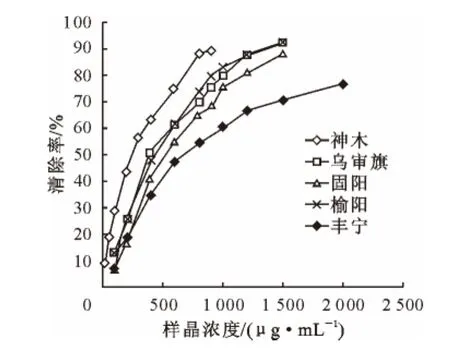
图5 不同种源地样品DPPH清除率比较Fig.5 DPPH scavenging effect of the samples of five provenances
不同种源地的长柄扁桃仁多酚提取液也表现出了不同的总还原力。采自乌审旗的样品FRAP值为(117.36±2.56)μmol·g-1,总还原力显著强于另外4个种源地样品(p<0.05),神木次之,FRAP值为(112.49±1.55)μmol·g-1,丰宁样品FRAP值为(45.56±1.82)μmol·g-1。
综上可知,采自陕北神木、榆阳、乌审旗地区的长柄扁桃仁的自由基清除能力以及总还原力相对高于其他2个种源地区,初步说明在适宜的环境中生长的长柄扁桃中的仁表现出了较强的抗氧化活性。
3 结论与讨论
目前,国内外对于多酚类物质的研究主要集中在核桃、茶树[9,11]等方面,而对长柄扁桃仁中多酚物质的含量及其抗氧化活性等报道较少。本试验以陕西榆阳地区长柄扁桃仁为材料,通过单因素和正交试验确定了长柄扁桃仁中多酚的最佳提取工艺为∶乙醇体积分数20%,料液比1g∶20mL,提取温度40℃,超声时间60min,提取率为2.076mg·g-1。当乙醇体积分数为0,即用水进行提取时,多酚提取率为(1.927±0.163)mg·g-1,与乙醇体积分数为20%时提取效果无显著差异(p<0.05),故可进一步研究用于生产应用。综上所述,对长柄扁桃仁中多酚提取工艺研究对提高长柄扁桃综合利用率有着重要的理论价值。
正交试验表明,乙醇体积分数和料液比对长柄扁桃仁中多酚的提取影响显著强于时间和温度。高体积分数的乙醇会使得其他醇溶性杂质等溶出,与多酚竞争乙醇-水分子;当乙醇使用量足够时,多酚的溶解基本达到饱和,用量过多时,产生溶解杂质较多的同时,因抽滤阶段无法密封,而经历一定温度提取后抽滤耗时又较长,容易造成多酚的挥发。因此提取过程中乙醇体积分数和料液比比较敏感。由于多酚的结构类型多,分子量跨度范围较大,与蛋白质的连接键牢固程度不一样[35],所以提取过程中各因素对多酚提取量的影响差异也较大。

表5 不同种源地样品抗氧化活性比较Table 5 The antioxidant activity of the samples of five provenances
本试验运用DPPH法、ABTS法及FRAP法对5个不同种源地的长柄扁桃仁中多酚提取液抗氧化活性进行了研究,采自陕北神木、榆阳、乌审旗3个县区的样品表现出了较强的抗氧化活性,固阳、丰宁样品相对较差。长柄扁桃长期生长在西北干旱、半干旱地区,在陕北地区有集中分布,在适宜环境中生长的长柄扁桃中的仁有效成分含量较高,故表现出了较强的抗氧化活性。干旱是限制植物分布和生长的主要非生物因素[14],而丰宁地处中温带半湿润半干旱气候区,不利于长柄扁桃次生代谢产物的累积,导致其抗氧化活性较差。长柄扁桃仁中多酚抗氧化活性与环境因素的关系有待进一步的研究。
长柄扁桃抗旱、抗风蚀、适应范围广的优良特性使得它可在西北干旱、半干旱地区广泛种植,具有巨大的生态、经济利用潜力[4]。但针对其各部位的利用研究尚未完全展开,有待于进一步的综合开发利用,为生产应用提供技术依据。
[1] 罗树伟,郭春会,张国庆,等.沙地植物长柄扁桃光合特性研究[J].西北农林科技大学学报:自然科学版,2010,38(1):125-132.LUO S W,GUO C H,ZHANG G Q,et al.Study on photosynthetic characteristic of sand Amygdalus pedunculat aPall.Journal of Northwest A&F University:Nat.Sci.Edi.,2010,38(1):125-132.(in Chinese)
[2] 郭春会,罗梦,马玉华,等.沙地濒危植物长柄扁桃特性研究进展[J].西北农林科技大学学报:自然科学版,2005,33(12):125-129.GUO C H,LUO M,MA Y H,et al.Advances of charaeteristic research of threatened long carpopodium almond.Journal of Northwest A&F University:Nat.Sci.Edi.,2005,33(12):125-129.(in Chinese)
[3] 许新桥,褚建民.长柄扁桃产业发展潜势分析及问题对策研究[J].林业资源管理,2013(1):22-25.XU X Q,CHU J M.Analysis on development potential and countermeasures of amygdalus pedunculata industry[J].Forest Resources Management,2013(1):22-25.(in Chinese)
[4] 张萍,申烨华,王晓玲,等.高效液相色谱法测定长柄扁桃仁中的苦杏仁甙[J].分析试验室,2007,26(10):80-83.ZHANG P,SHEN Y H,WANG X L,et al.Determination of amygdalus in amygdalus pedunculatus pall by high performance liquid chromatography[J].Chinese Journal of Analysis Laboratory,2007,26(10):80-83.(in Chinese)
[5] 宋立江,狄莹,石碧.植物多酚研究与利用的意义及发展趋势[J].化学进展,2000,12(2):161-170.SONG L J,DI Y,SHI B.The significance and development trend in research of plant polyphenols[J].Progress in Chemistry,2000,12(2):161-170.(in Chinese)
[6] JOHNSTON K L,CLIFFORD M N,MORGAN L M.Possible role for apple juice phenolic compounds in the acute modification of glucose tolerance and gastrointestinal hormone secretion in humans[J].Journal of the Science of Food and Agriculture,2002,82(15):1800-1805.
[7] BURDA S,OLESZEK W,LEE C.Phenolic compounds and their changes in apples during maturation and cold storage[J].Journal of Agricultural and Food Chemistry,1990,38(4):945-948.
[8] BONÍKOVÁD,TÓTH T,TOMÁJ,et al.Effective antioxidant phenolic compounds in selected varieties of apples[J].Potravinarstvo,2012,6(4):11-15.
[9] 陈虹霞,王成章,周昊,等.核桃酚类化合物的研究进展[J].林产化学与工业,2013,33(1):130-135.CHEN H X,WANG C Z,ZHOU H,et al.Research progress of phenolic compounds from Wanlnut(Juglans regia L.)[J].Chemistry and Industry of Forest Products,2013,33(1):130-135.(in Chinese)
[10] 綦菁华,王芳,庞美霞,等.板栗酚类活性成分提取及其抗氧化活性研究[J].中国粮油学报,2009,9(24):141-143.QI J H,WANG F,PANG M X,et al.Active phenolic compound extraction from chestnut and their Antioxidation activities[J].Journal of the Chinese Cereals and Oils Association,2009,9(24):141-143.(in Chinese)
[11] 胡秀芳,沈生荣.茶多酚抗氧化机理研究现状[J].茶叶科学,1999,19(2):93-103.HU X F,SHEN S R.Review on antioxidative mechanism of tea polyphenols[J].Journal of Tea Science,1999,19(2):93-103.(in Chinese)
[12] 王燕,申烨华,李国平.长柄扁桃仁的氨基酸和矿质元素分析[J].陕西师范大学学报:自然科学版,2008,36:78-81.WANG Y,SHEN Y H,LI G P.Analysis of amino acids and elements in Amygdalus[J].Journal of Shaanxi Normal University:Nat.Sci.Edi.,2008,36:78-81.(in Chinese)
[13] 李冰.沙生植物长柄扁桃种子油及副产品开发研究[D].西安:西北大学,2010.
[14] 郭改改,封斌,麻保林,等.不同区域长柄扁桃抗旱性的研究[J].植物科学学报,2013,31(4):360-369.GUO G G,FENG B,MA B L,et al.Studies on drought resistance of different regional Amygdalus pedunculata Pall.[J].Plant Science Journal,2013,31(4):360-369.(in Chinese)
[15] 张檀,郑瑞杰,梅立新,等.长柄扁桃种子萌发特性的研究[J].西北林学院学报,2006,21(4):73-76.ZHANG T,ZHENG R J,MEI L X,et al.Germination characters of the seeds of the Amygdalus pedunculata Pall.[J].Journal of Northwest Forestry University,2006,21(4):73-76.(in Chinese)
[16] 徐金娟,苏印泉,张强,等.溶剂法提取长柄扁桃油的工艺研究[J].西北林学院学报,2011,26(4):184-187.XU J J,SU Y Q,ZHANG Q,et al.Process of the extraction of Amygdalus pedunculata Pall.oil[J].Journal of Northwest Forestry University,2011,26(4):184-187.(in Chinese)
[17] 刘志明,王树文,唐彦君,等.大庆地产板蓝根总多糖含量及摩尔质量分布测定[J].食品科学,2012,33(2):169-172.LIU Z M,WANG S W,TANG Y J,et al.Determination of polysaccharide content and molar mass distribution of isatis indigotica fortune roots planted in Daqing[J].Food Science,2012,33(2):169-172.(in Chinese)
[18] 刘国聪,曾楚杰,刘力恒,等.沙田柚皮水溶性多糖的提取和测定[J].食品科学,2007,28(11):223-226.LIU G C,ZENG C J,LIU L H,et al.Extraction and determination of water-soluble polysaccharides from peels of grapefruit planted in sand-soil[J].Food Science,2007,28(11):223-226.(in Chinese)
[19] 李银保,彭金年,彭湘君,等.不同提取方法对菟丝子总黄酮和金属元素锌的含量比较研究[J].光谱实验室,2009,26(5):1299-1302.LI Y B,PENG J N,PENG X J,et al.Studies on the extraction of total flavonoids and metical element zinc from semen cuscutae[J].Chinese Journal of Spectroscopy Laboratory,2009,26(5):1299-1302.(in Chinese)
[20] 马亚琴,叶兴乾,吴厚玖,等.温州蜜柑皮多酚物质的超声提取及抗氧化特性[J].食品科学,2011,32(22):100-104.MA Y Q,YE X Q,WU H J.et al.Ultrasound-assisted extraction of polyphenols from satsuma mandarin (Citrus unshiu Marc)peel and its antioxidant capacity[J].Food Science,2011,32(22):100-104.(in Chinese)
[21] 郭树琴,吴胜举,李岱.响应面法优化超声提取绿茶茶多酚工艺[J].生物加工工程,2009,7(1):39-43.GUO S Q,WU S J,LI D.Optimization of ultrasonic extraction of tea polyphenols from green tea by response surface methodology[J].Chinese Journal of Bioprocess Engineering,2009,7(1):39-43.(in Chinese)
[22] KHAN M K,ABERT-VIAN M,FABIANO-TIXIER A S,et al.Ultrasound-assisted extraction of polyphenols (flavanone glycosides)from orange (Citrus sinensis L.)peel[J].Food Chemistry ,2010,119(2):851-858.
[23] JAGOTA S,DANI H.A new colorimetric technique for the estimation of vitamin C using Folin phenol reagent[J].Ana-lytical biochemistry 1982,127(1):178-182.
[24] LEE K R,SVORONOS S S,IRIGOYEN P,et al.Spectrophotometric determination of the total phenol content in commercial beverages via the Folin-Ciocalteau micromethod[J].Abstracts of papers of the American chemical society,2010,240:851-858
[25] YEN G C,CHEN H Y.Antioxidant activity of various tea extracts in relation to their antimutagenicity[J].Journal of Agricultural and Food Chemistry 1995,43(1):27-32.
[26] RE R,PELLEGRINI N,PROTEGGENTE A,et al.Antioxidant activity applying an improved ABTS radical cation decolorization assay[J].Free Radical Biology and Medicine,1999,26(9):1231-1237.
[27] WANG S S,WANG D M,PU W J,et al.Phytochemical profiles,antioxidant and antimicrobial activities of three Potentillaspecies[J].BMC complementary and alternative medicine,2013,13(1):321.
[28] 苑子夜,苏印泉,张强,等.DPPH法评价杜仲叶提取物的抗氧化活性[J].西北林学院学报,2011,26(6):119-123.YUAN Z Y,SU Y Q,ZHANG Q,et al.Ecaluation of antioxidant activity of Eucommia ulmoides leaf extracts by DPPH·assay[J].Journal of Northwest Forestry University,2011,26(6):119-123.(in Chinese)
[29] RU Q M,WANG L J,LI W M,et al.In vitro antioxidant properties of flavonoids and polysaccharides extract from tobacco(Nicotiana tabacumL.)leaves[J].Molecules,2012,17(9):11281-11291.
[30] 芦艳,鲁周民,樊美丽.枇杷花不同花期醇提物抗氧化活性的比较[J].现代食品科技,2013,29(9):2141-2146.LU Y,LU Z M,FAN M L.Antioxidant activity of ethanol extracts of loquat flowers at different flowering phases[J].Modern Food Science &Technology,2013,29(9):2141-2146.(in Chinese)
[31] BENZIE I F,STRAIN J.The ferric reducing ability of plasma(FRAP)as a measure of“antioxidant power”:the FRAP assay[J].Analytical Biochemistry,1996,239(1):70-76.
[32] 方敏,王耀峰,宫智勇.15种水果和33种蔬菜的抗氧化活性研究[J].食品科学,2008,29(10):97-100.FANG M,WANG Y F,GONG Z Y.Study on antioxidant activities of fifty kinds of fruits and thirty-three kinds of vegetables[J].Food Science,2008,29(10):97-100.(in Chinese)
[33] 汪洪涛,陈成,余芳,等.紫叶李果实总多酚的提取工艺及其抗氧化活性研究[J].河南农业科学,2013,42(10):153-156.WANG H T,CHEN C,YU F,et al.Study on extraction process and antioxidative activity of total polyphenol from pranus cerasifera fruit[J].Journal of Henan Agricultural Sciences,2013,42(10):153-156.(in Chinese)
[34] 石碧,狄莹.植物多酚[M].北京:科学出版社,2000.
[35] 李西柳,庞明,王俊儒,等.柿子渣中多酚的提取工艺及其抗氧化性研究[J].西北植物学报,2010(7):1475-1480.LI X L,PANG M,WANG J R,et al.Polyphenols extraction methods from persimmon pomace and its antioxidant activity[J].Acta Botanica Boreali-Occidentalia Sinica,2010(7):1475-1480.(in Chinese)
