铀在离子液体中的物种及电化学行为研究进展
2014-12-25邱凌云袁立永谭绪凤石伟群刘良军
邱凌云,袁立永,谭绪凤,石伟群,刘良军,*
1.南华大学 核科学技术学院,湖南 衡阳 421001;
2.中国科学院 高能物理研究所 核辐射与核能技术重点实验室,北京 100049
离子液体又称室温熔融盐,也称液态有机盐,是完全由特定的阳离子和阴离子构成在室温或近室温下呈液态的熔盐体系。离子液体具有很多传统有机溶剂无法比拟的突出优点,如极低的蒸气压、高的热稳定和化学稳定性、优良的溶解性能、宽的电化学窗口、高导电性、优异的电化学性能以及易回收、可设计等[1]。离子液体已经广泛应用于分离、有机合成及超级电容器、电化学等各个领域[2-5]。离子液体在放射化学尤其是乏燃料后处理领域也具有很好的应用前景,如将其应用于目前已商业化的水法Purex流程。使用低挥发性、高稳定性的离子液体取代挥发性的传统溶剂应用于水法后处理流程将更加绿色环保。此外,乏燃料干法后处理近年来也越来越受到全世界各国的高度重视。强腐蚀性高温熔盐的使用对设备的耐腐性提出了苛刻的要求,同时乏燃料在高温熔盐中的溶解也是一个难题。这些问题在一定程度上限制了干法后处理的规模化应用。离子液体作为可设计的室温熔盐,将其用于干法后处理将有望提供更温和的后处理条件同时为乏燃料的溶解提供更广阔的空间。目前离子液体用于乏燃料后处理研究尚处于初级阶段,与实际应用相关的众多科学问题亟待研究,这些科学问题包括离子液体的低成本宏量制备;离子液体本身的性质和行为;锕系元素在离子液体中的溶解及存在形态;离子液体体系对锕系离子的萃取行为及机理,锕系离子在离子液体中的电化学行为及机理等。
锕系离子在离子液体中的物理化学性质、利用离子液体体系萃取分离锕系离子、离子液体自身的物理化学性质及辐照稳定性[6-11]等已被广泛研究和报道,关于这类研究已有很多综述文章发表[12-15],这里不再赘述。本文重点关注铀在离子液体中的存在物种及电化学相关的研究内容,以下分述。
1 铀在离子液体中的存在物种
1.1 直接溶解后铀的存在物种
铀在离子液体中的存在物种与铀的配体密切相关。在众多对离子中,氯离子和硝酸根离子是目前研究和报道最多的两类。这是因为,含氯离子液体在乏燃料干法后处理中具有更好的应用潜力,而硝酸溶液在当前水法后处理过程中必不可少。下面将根据不同对离子分别阐述铀在离子液体中的存在物种。

图1 在[Bmim][NTf2]离子液体中[UO2(NO3)n]2-n(n=0~3)配合物物种分布[32]Fig.1 Species distribution diagram of[UO2(NO3)n]2-n(n=0-3)complexes[32]
1.1.3 其它对离子 铀氧化物在离子液体中的溶解一直是个难题,因此很多学者转而研究含不同阴离子的铀盐在离子液体中的性质和行为。如Nockemann等[28]使用紫外-可见吸收光谱研究了乙酸根/[Bmim][NTf2]中的配合物种态,发现存在的物种为[UO2(CH3COO)3]-。同时,Sornein和Takao等[33-34]还发现铀酰与Br-、三苯基氧化膦(OPPh3)在1-丁基-3-甲基咪唑双三氟磺酰盐([Bmim][NfO])离子液体中形成物种分别为[UO2Br4]2-和[UO2(OPPh3)4]2+。Yao等[35]首次报道了含铁的咪唑离子液体对二氧化铀不添加氧化剂的直接溶解过程。Liu等[36]利用紫外-可见吸收光谱、荧光发射光谱和电喷雾离子化-离子阱质谱法,研究离子液体中铀酰离子与中性二齿配体亚甲基二膦酸四乙酯(TEMBP)的配位作用,确认了双电荷配离子[UO2(TEMBP)2]2+的存在。
1.2 萃取后铀的存在物种
由于离子液体特殊的结构和性质,其与传统有机溶剂萃取体系相比,萃取机理有所不同,萃取后形成的萃合物物种也不尽相同。
咪唑型离子液体/TBP体系对铀的萃取研究较为广泛。Giridhar[37]较早研究了[Rmim][PF6](R=n-CmH2m+1,m=4和8)离子液体在浓度为0.01~8mol/L的硝酸下萃取铀,两种离子液体对铀的萃取分配比均随硝酸浓度升高而增加,以lgc(TBP)和lg D作图,其斜率分析得出体系中铀以中性萃合物UO2(NO3)2(TBP)2形式存在,与在正十二烷中形成的物种类似。Wang等[38]使用超临界CO2在[Bmim][NTf2]离 子 液 体 中 使 用 超 过0.1mol/L硝酸萃取铀时也发现了此UO2(NO3)2(TBP)2中性萃合物的存在。但随后有人提出不同观点。Giridhar等[39-40]在 系 统 研 究 了[Bmim][NTf2]/TBP体系从硝酸介质中萃取铀后指出,当硝酸浓度为0.01~1mol/L时,其对铀萃取分配比随硝酸浓度增加而降低,当硝酸浓度大于1mol/L时分配比开始增大。对于这一萃取现象,作者并未给出合理的解释,也未给出铀在离子液体中的存在物种。Billard等[41]和Murali等[42]对于上述萃取现象进行了更深入的研究。Billard等[41]的研究发现,在低浓度硝酸下铀萃取符合阳离子交换机理,而高浓度下则为阴离子交换机理。使用化学计量法计算出阳离子和阴离子交换机理所形成的物种分别为[UO2(TBP)2]2+和[UO2(NO3)3(TBP)2]-。Murali等[42]则通过基质辅助激光解析电离质谱(MALDI-MS)和电喷雾质谱(ESIMS)表征发现,[Bmim][PF6]/TBP体系 中对萃取机理为阳离子交换,主要萃合物物种为[UO2(NO3)(TBP)2]+。
除了TBP,其他萃取剂如对正辛基苯基-N,N’-二异丁基胺甲酰甲基氧化膦(CMPO),N,N,N’,N’-四辛基-3-氧戊二酰胺(TODGA)等酰胺类化合物[43-47]也被广泛用于离子液体体系萃取铀。Visser等[43]利用EXAFS和紫外-可见吸收光谱等手段研究了CMPO在[Bmim][PF6]和[Omim][NTf2]离子液体中从水相萃取铀,发现存在[UO2(NO3)CMPO]+,而传统有机溶剂正十二烷体系中则为UO2(NO3)2CMPO物种。当加入其他萃取剂时,硝酸根离子和铀的配位发生改变,例如在含有1mol/L HNO3水溶液中使用0.1mol/L CMPO、1mol/L TBP萃 取 剂 在[Bmim][PF6]离子液体中萃取铀酰离子,形成[UO2(NO3)(CMPO)]+物 种[47],Chaumont等[48]则通过分子动力学模拟发现,硝酸根离子、CMPO、3个水分子在赤道平面五配位形成了[UO2(NO3)(CMPO)(H2O)3]+。
将普通离子液体的阳离子或阴离子进行有机功能基团的共价键修饰即得到功能化离子液体。由于存在有机功能基团,功能化离子液体同时具有溶剂和萃取剂的功能。目前国内外很多学者致力于这方面的研究并合成了一系列咪唑、哌啶、吡咯、季铵盐等含各种官能团的功能化离子液体[49-52],但遗憾的是,铀在这些功能性离子液体中的存在物种鲜见报道。虽然功能化离子液体还存在一些不足,但是相信在不久的将来其会为高效提取铀提供一种安全简单的方法。表1列出了文献报道的铀在不同离子液体体系中的存在物种。
2 铀在离子液体中的电化学行为
2.1 铀盐或氧化物溶解在离子液体中的电化学行为
不同含铀物种在氯化铝型离子液体中的电化学研究已非常详细。Anderson等[55]研究了UO2Cl2在酸性AlCl3-C2MimCl离子液体中的氧化还原行为,发现UO2Cl2在此溶液中不稳定,铀酰离子易脱氧分解形成UO4+,最终被还原成,溶液中的阴离子被氧化成Cl2。其过程如下:
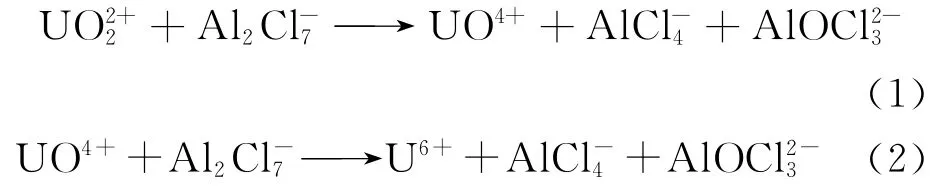
张秋月等[56]研究了硝酸铀酰在BmimCl中电化学过程,一步还原为UO2,扫描速率为10~100mV/s时为可逆,增大扫描速率不可逆。
Waele等[53]发现UCl4在酸性AlCl3/BuPyCl(2∶1)离子液体中主要含铀物种为,随着离子液体酸性的降低部分转变为,使得成为主要的含铀物种,并且当酸性继续降低时UCl4便以沉淀的形式出现。U(Ⅵ)在溶液中被还原成U(Ⅲ),在溶液中它不是以氯铀离子形式而是以U(Ⅲ)存在;U(Ⅳ)也可以被氧化成U(Ⅴ)、U(Ⅵ),但氧化成U(Ⅵ)时,其氧化电位在溶液的电位窗口之外,Cl-被氧化成为氯气。在碱性的AlCl3-BuPyCl型离子液体中,能够稳定存在于离子液体中,U(Ⅵ)被还原成。但U3+不能稳定存在,易被BuPy+氧化,少量的U(Ⅲ)能迅速发生歧化反应生成U(Ⅳ)和铀单质。
此外Deetlefs等[57-58]将[Emim]2[UCl6]和[Emim]2[UO2Cl4]溶于碱性AlCl3-EmimCl中。发现[UO2Cl4]2-经历一个快速的单步两电子还原和一个慢速的单步一电子还原最终生成。具体反应如下:

[Emim]2[UCl6]盐溶液仅发生后面单电子的还原步 骤,而 将[Emim]2[UBr6]和[Emim]2[UO2Br4]溶于碱性AlCl3-EmimBr中U(Ⅵ)的氧化还原行为与氯盐一致。
Giridhar等[59]研究了硝酸铀酰在BmimCl中的电化学行为,6~25mmol/L的铀酰离子在70~100℃下离子液体中-0.7V处发生单步两电子还原过程。在扫描速率较小时其分别出现-0.5V和0.3V两个氧化峰,但扫描速率大于0.5V/s时,在0.3V处的肩峰消失,铀酰离子最终在铂电极上还原得到无定形致密的黑色氧化物薄膜,经TG-DTG、EDX和XRD手段测定得知其还原产物主要成分为UO2,但其中会夹杂一些BmimCl离子液体。
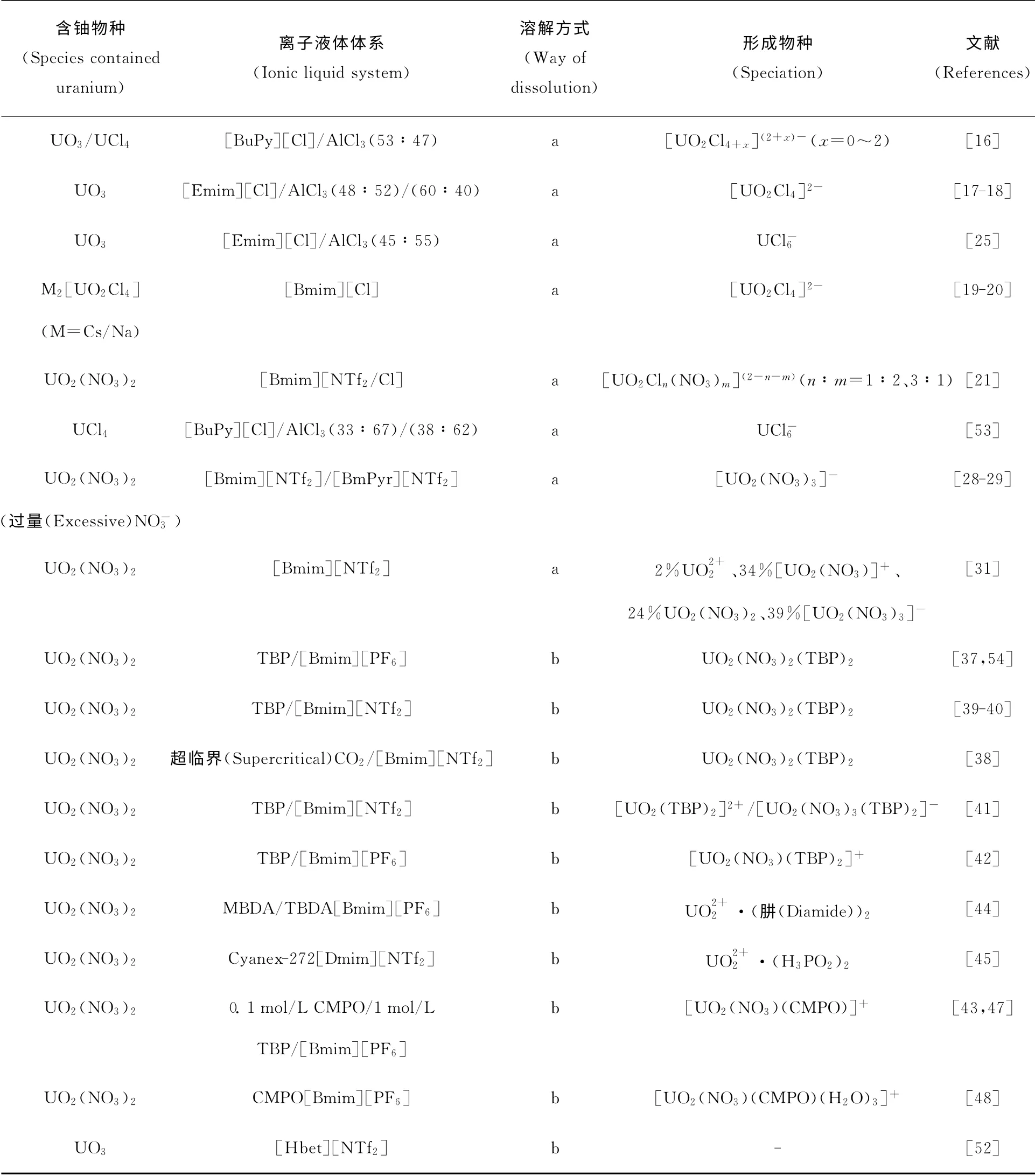
表1 U(Ⅵ)在不同离子液体体系中的存在物种Table 1 Species of U(Ⅵ)in different ionic liquids
Asanuma等[60]尝试将U3O8分别加入BmimCl、[Bmim][BF4]、[Bmim][NfO]离子液体中,再以氯气作为氧化剂,得到含有的溶液,以玻碳电极为工作电极、Pt为对电极、Ag/AgCl为参比电极研究了在上述3种离子液体中的电化学行为。他们发现BmimCl离子液体中在-0.758V处经单电子转移的准可逆过程还原成稳定存在的。在电极表面的传递受扩散控制,扩散系数约为4.8×10-8cm2/s,其扩散系数远小于在有机溶剂介质或者水溶液介质电极表面的扩散系数,其原因是离子液体较高的粘度不利于在电极表面的扩散。利用相同的电极体系,在[Bmim][BF4]、[Bmim][NfO]呈现不同的氧化还原现象。在[Bmim][BF4]中,在-0.7V处还原为一种可能是UO2的黑色物质;在[Bmim][NfO]中,在-0.6V和-0.2V处被还原为U(Ⅴ),在0.85V处U(Ⅴ)被还原得到黑色的UO2产物。从以上3种离子液体中的还原电位不同可知,一方面是与含铀的不同离子种态在离子液体中的稳定性有关,另一方面,在离子液体中的还原还与离子液体的粘度有关,随着粘度的减少,还原电位也相应减小。Ikeda[61]改变溶质研究了Cs2UO2Cl4和UO2Cl2·nH2O在BmimCl离子液体中以及[Emim]2UO2Cl4在BmimCl和[Bmim][BF4](1∶1)混合离子液体中的氧化还原性质,其相似处在于电化学窗口之内只经历了一步单电子的可逆反应,即

Rao等[62]直接将UO2溶于HNTf2,经搅拌回流干燥处理后得到产物U(NTf2)4,将U(NTf2)4溶解在电化学窗口较大的[MPPi][NTf2]离子液体中,以玻碳电极为工作电极、玻碳棒为对电极、钯丝为参比电极发现U(Ⅳ)在[MPPi][NTf2]离子液体中-0.76、-1.14V处发生单电子还原得到U(Ⅲ),继而在-2.8V处被还原为单质铀,利用SEM、EDS方法表征电极表面沉积物,发现形成了均匀的立方小晶粒,且为单质铀,且沉积过程电流效率约为80%。表2总结了不同铀盐在不同离子液体体系中的电化学行为。

表2 铀在离子液体体系中的电化学行为Table 2 Electrochemical behavior research of uranium in ionic liquids
2.2 铀萃合物在离子液体中的电化学行为
Giridhar等[40]首次提出萃取-电沉积(EXEL)流程并应用于锕系元素乏燃料后处理。他们使用1.1mol/L TBP为萃取剂将U(Ⅵ)萃入BmimNTf2离子液体相,然后直接在离子液体相中电沉积得到铀氧化物。1 000℃热处理沉积物后变成黑色粉末,其XRD图谱显示为U3O8。循环伏安图显示U(Ⅵ)在-1.3V(vs Pt)处发生还原,在1.56V处发生氧化。U(Ⅵ)经过一步两电子还原为U(Ⅳ),但是法拉第电流效率仅为20%左右。作者并未给出U(Ⅵ)被萃入离子液体相后详细的电化学行为过程。此流程有望解决铀氧化物在离子液体中的溶解问题,但萃取后形成的络合物电还原过程及如何解决萃取时加入的硝酸对电还原过程的影响[63]等问题,有待学者们进一步深入研究。
吴京珂等[64]发现,使用含CMPO的[Bmim][NTf2]萃取硝酸铀酰水溶液后,将萃取液在(-0.885±0.008)V(vs Fc/Fc+)恒电位电解,电沉积产物中包含U(Ⅵ)、U(Ⅳ)和氧。虽然电流效率很低,也表明用电沉积的方法实现铀的反萃是可行的。
综上所述,离子液体、萃取剂和电解质已被用于乏燃料中铀的净化分离研究(如表1、2所示),这些研究展现出离子液体在乏燃料后处理中的巨大应用潜力。
3 结束语
离子液体因其优良的物理化学性质在后处理研究中受到高度的重视。目前离子液体用于乏燃料后处理的研究尚处于初级阶段,铀及其他锕系元素和裂变产物在离子液体的存在物种和电化学行为等方面的研究空间还很大。未来铀在离子液体中的物种及电化学行为研究可从以下几方面着手:
(1)深入研究离子液体的电化学稳定性、粘度、对铀的溶解性能等基础性质,从而设计出令人满意且可实际应用的离子液体;使用各种光谱、EXAFS等先进的化学表征手段深入研究铀在离子液体中的物种分布,同时可利用分子动力学等方法辅助验证实验数据的准确性;
(2)研究电化学还原铀时,需首先确定不同温度下不同离子液体中铀的电化学还原电位,并设法提高电流效率;然后使用各种电化学测试技术研究铀在不同离子液体中的氧化还原过程,利用原子力显微镜、电化学石英晶体微天平(EQCM)等先进的原位测量技术展示电极表面铀的还原过程;目前离子液体中还原铀为金属单质的报道极少,可选取电化学窗口较大的离子液体,重点研究此过程的电化学行为。
总之,离子液体在乏燃料水法及干法后处理中展现出了巨大的应用潜力,但与之相关的基础研究还任重而道远。相信在全世界各国研究学者的共同努力下,离子液体必将在未来先进核能系统中发挥重要作用。
[1]Earle M J,Seddon K R.Ionic liquids:green solvents for the future[J].Pure Appl Chem,2000:1391-1398.
[2]Shobukawa H,Tokuda H,Tabata S-I,et al.Preparation and transport properties of novel lithium ionic liquids[J].Electrochim Acta,2004,50(2-3):305-309.
[3]Tadesse H,Luque R.Advances on biomass pretreatment using ionic liquids:an overview[J].Energy Environ Sci,2011,4(10):3913-3929.
[4]Hallett J P,Welton T.Room-temperature ionic liquids:solvents for synthesis and catalysis[J].Chem Rev,2011,111(5):3508-3576.
[5]Han X,Armstrong D W.Ionic liquids in separations[J].Acc Chem Res,2007,40(11):1079-1086.
[6]Yuan L Y,Peng J,Xu L,et al.Influence ofγ-radiation on the ionic liquid[C4mim][PF6]during extraction of strontium ions[J].Dalton Trans,2008(45):6358-6360.
[7]Yuan L Y,Peng J,Xu L,et al.Radiation effects on hydrophobic ionic liquid[C4mim][NTf2]during extraction of strontium ions[J].J Phys Chem B,2009,113(26):8948-8952.
[8]Yuan L Y,Peng J,Xu L,et al.Radiation-induced darkening of ionic liquid[C4mim][NTf2]and its decoloration[J].Radiat Phys Chem,2009,78(12):1133-1136.
[9]Yuan L Y,Peng J,Zhai M,et al.Influence ofγradiation on room-temperature ionic liquid[Bmim][PF6]in the presence of nitric acid[J].Radiat Phys Chem,2009,78(7):737-739.
[10]Yuan L Y,Xu C,Peng J,et al.Identification of the radiolytic product of hydrophobic ionic liquid[C4mim][NTf2]during removal of Sr2+from aqueous solution[J].Dalton Trans,2009(38):7873-7875.
[11]褚泰伟,秦丽,刘新起,等.离子液体用于溶剂萃取铀酰离子的初步研究[J].核化学与放射化学,2007,29(3):146-150.
[12]Cocalia V A,Gutowski K E,Rogers R D.The coordination chemistry of actinides in ionic liquids:a review of experiment and simulation[J].Coord Chem Rev,2006,250(7):755-764.
[13]Binnemans K.Lanthanides and actinides in ionic liquids[J].Chem Rev,2007,107(6):2592-2614.
[14]Mudring A V,Tang S.Ionic liquids for lanthanide and actinide chemistry[J].Eur J Inorg Chem,2010(18):2569-2581.
[15]Sun X,Luo H,Dai S.Ionic liquids-based extraction:apromising strategy for the advanced nuclear fuel cycle[J].Chem Rev,2012,112(4):2100-2128.
[16]Heerman L,De Waele R,D′olieslager W J.Electrochemistry and spectroscopy of uranium in basic AlCl3+N-(n-butyl)pyridinium chloride room temperature molten salts[J].J Electroanal Chem Interfacial Electrochem,1985,193(1-2):289-294.
[17]Dai S,Shin Y,Toth L,et al.Comparative UV-vis studies of uranyl chloride complex in two basic ambient-temperature melt systems:the observation of spectral and thermodynamic variations induced via hydrogen bonding[J].Inorg Chem,1997,36(21):4900-4902.
[18]Hopkins T A,Berg J M,Costa D A,et al.Spectroscopy of UO2Cl42-in basic aluminum chloride-1-ethyl-3-methylimidazolium chloride[J].Inorg Chem,2001,40(8):1820-1825.
[19]Giridhar P,Venkatesan K,Subramaniam S,et al.Electrochemical behavior of uranium(Ⅵ)in 1-butyl-3-methylimidazolium chloride and in 0.05M aliquat-336/chloroform[J].Radiochim Acta,2006,94(8/2006):415-420.
[20]Gaillard C,Chaumont A,Billard I,et al.Uranyl coordination in ionic liquids:the competition between ionic liquid anions,uranyl counterions,and Cl-anions investigated by extended X-ray absorption fine structure and UV-visible spectroscopies and molecular dynamics simulations[J].Inorg Chem,2007,46(12):4815-4826.
[21]Gaillard C,Chaumont A,Billard I,et al.Competitive complexation of nitrates and chlorides to uranyl in a room temperature ionic liquid[J].Inorg Chem,2010,49(14):6484-6494.
[22]Chaumont A,Engler E,Wipff G.Uranyl and strontium salt solvation in room-temperature ionic liquids:a molecular dynamics investigation[J].Inorg Chem,2003,42(17):5348-5356.
[23]Chaumont A,Wipff G.Solvation of uranyl(Ⅱ)and europium(Ⅲ)cations and their chloro complexes in a room-temperature ionic liquid:a theoretical study of the effect of solvent“humidity”[J].Inorg Chem,2004,43(19):5891-5901.
[24]Chaumont A,Wipff G.Chloride complexation by uranyl in a room temperature ionic liquid:a computational study[J].J Phys Chem B,2008,112(38):12014-12023.
[25]Anderson C J,Choppin G,Pruett D,et al.Electrochemistry and spectroscopy ofin acidic AlCl3-EMIC[J].Radiochim Acta,1999,84(1):31-36.
[26]Ogura T,Takao K,Sasaki K,et al.Spectroelectrochemical identification of a pentavalent uranyl tetrachloro complex in room-temperature ionic liquid[J].Inorg Chem,2011,50(21):10525-10527.
[27]Wenz D A,Adams M D,Steunenberg R K.Formation and spectra of uranyl(Ⅴ)chloride in molten chloride solvents[J].Inorg Chem,1964,3(7):989-992.
[28]Nockemann P,Servaes K,Van Deun R,et al.Speciation of uranyl complexes in ionic liquids by optical spectroscopy[J].Inorg Chem,2007,46(26):11335-11344.
[29]Servaes K,Hennig C,Billard I,et al.Speciation of uranyl nitrato complexes in acetonitrile and in the ionic liquid 1-buty-3-methylimidazolium bis(trifluoromethylsulfonyl)imide[J].Eur J Inorg Chem,2007(32):5120-5126.
[30]Quach D L,Wai C M,Pasilis S P.Characterization of uranyl(Ⅵ)nitrate complexes in a room temperature ionic liquid using attenuated total reflectionfourier transform infrared spectrometry[J].Inorg Chem,2010,49(18):8568-8572.
[31]Georg S,Billard I,Ouadi A,et al.Determination of successive complexation constants in an ionic liquid:complexation ofwith NO-3in C4-mimTf2Nstudied by UV-vis spectroscopy[J].J Phys Chem B,2010,114(12):4276-4282.
[32]Takao K,Bell T J,Ikeda Y.Actinide chemistry in ionic liquids[J].Inorg Chem,2012,52(7):3459-3472.
[33]Sornein M-O,Mendes M,Cannes C,et al.Coordination environment of[UO2Br4]2-in ionic liquids and crystal structure of[Bmim]2[UO2Br4][J].Polyhedron,2009,28(7):1281-1286.
[34]Takao K,Takahashi T,Ikeda Y.Complex formation of uranyl ion with triphenylphosphine oxide and its ligand exchange reaction in 1-butyl-3-methylimidazolium nonafluorobutanesulfonate ionic liquid[J].Inorg Chem,2009,48(4):1744-1752.
[35]Yao A,Chu T.Fe-containing ionic liquids as effective and recoverable oxidants for dissolution of UO2in the presence of imidazolium chlorides[J].Dalton Trans,2013,42(23):8413-8419.
[36]Liu Y P,Chu T W,Wang X Y.A 2∶1dicationic complex of tetraethyl methylenebisphosphonate with uranyl ion in acetonitrile and ionic liquids[J].Inorg Chem,2013,52(2):848-854.
[37]Giridhar P,Venkatesan K,Srinivasan T,et al.Effect of alkyl group in 1-alkyl-3-methylimidazolium hexafluorophosphate ionic liquids on the extraction of uranium by tri-n-butylphosphate diluted with ionic liquids[J].J Nucl Radiochem Sci,2004,5(2):21-26.
[38]Wang J S,Sheaff C N,Yoon B,et al.Extraction of uranium from aqueous solutions by using ionic liquid and supercritical carbon dioxide in conjunction[J].Chem—Eur J,2009,15(17):4458-4463.
[39]Giridhar P,Venkatesan K,Srinivasan T,et al.Extraction of uranium(Ⅵ)from nitric acid medium by 1.1Mtri-n-butylphosphate in ionic liquid diluent[J].J Radioanal Nucl Chem,2005,265(1):31-38.
[40]Giridhar P,Venkatesan K A,Subramaniam S,et al.Extraction of uranium(Ⅵ)by 1.1Mtri-nbutylphosphate/ionic liquid and the feasibility of recovery by direct electrodeposition from organic phase[J].J Alloys Compd,2008,448(1-2):104-108.
[41]Billard I,Ouadi A,Jobin E,et al.Understanding the extraction mechanism in ionic liquids:/HNO3/TBP/C4-mimTf2Nas a case study[J].Solvent Extr Ion Exch,2011,29(4):577-601.
[42]Murali M S,Bonville N,Choppin G R.Uranyl ion extraction into room temperature ionic liquids:species determination by ESI and MALDI-MS[J].Solvent Extr Ion Exch,2010,28(4):495-509.
[43]Visser A E,Rogers R D.Room-temperature ionic liquids:new solvents for f-element separations and associated solution chemistry[J].J Solid State Chem,2003,171(1):109-113.
[44]Shen Y,Tan X,Wang L,et al.Extration of the uranyl ion from the aqueous phase into an ionic liquid by diglycolamide[J].Sep Purif Technol,2011,78(3):298-302.
[45]Cocalia V A,Jensen M P,Holbrey J D,et al.Identical extraction behavior and coordination of trivalent or hexavalent f-element cations using ionic liquid and molecular solvents[J].Dalton Trans,2005(11):1966-1971.
[46]Bell T J,Ikeda Y.The application of novel hydrophobic ionic liquids to the extraction of uranium(Ⅵ)from nitric acid medium and a determination of the uranyl complexes formed[J].Dalton Trans,2011,40(39):10125-10130.
[47]Visser A E,Jensen M P,Laszak I,et al.Uranyl coordination environment in hydrophobic ionic liquids:an in situ investigation[J].Inorg Chem,2003,42(7):2197-2199.
[48]Chaumont A,Wipff G.Solvation of uranyl-CMPO complexes in dry vs.humid forms of the[BMI][PF6]ionic liquid:a molecular dynamics study[J].Phys Chem Chem Phys,2006,8(4):494-502.
[49]Rout A,Venkatesan K,Srinivasan T,et al.Unusual extraction of plutonium(Ⅳ)from uranium(Ⅵ)and americium(Ⅲ)using phosphonate based task specific ionic liquid[J].Radiochim Acta,2010,98(8):459-466.
[50]Srncik M,Kogelnig D,Stojanovic A,et al.Uranium extraction from aqueous solutions by ionic liquids[J].Appl Radiat Isot,2009,67(12):2146-2149.
[51]Ouadi A,Klimchuk O,Gaillard C,et al.Solvent extraction of U(Ⅵ)by task specific ionic liquids bearing phosphoryl groups[J].Green Chem,2007,9(11):1160-1162.
[52]Nockemann P,Thijs B,Pittois S,et al.Task-specific ionic liquid for solubilizing metal oxides[J].J Phys Chem B,2006,110(42):20978-20992.
[53]De Waele R,Heerman L,D’olieslager W J.Electrochemistry of uranium(Ⅵ)in acidic AlCl3+N-(nbuyl)pyridinium chiloride room-temperature molten salts[J].Electroanal Chem Interface Electrochem,1982,142(1-2):137-146.
[54]Giridhar P,Venkatesan K,Srinivasan T,et al.Comparison of diluent characteristics of imidazolium hexafluorophosphate ionic liquid with n-dodecane[J].J Nucl Radiochem Sci,2004,5(2):17-20.
[55]Anderson C J,Deakin M R,Choppin G R,et al.Spectroscopy and electrochemistry of uranium(Ⅳ)/uranium(Ⅲ)in basic aluminum chloride-1-ethyl-3-methylimidazolium chloride[J].Inorg Chem,1991,30(21):4013-4016.
[56]张秋月,黄小红,唐洪彬,等.铀(Ⅵ)在氯化1-丁基-3-甲基咪唑中的电化学性质[J].核化学与放射化学,2011,33(2):101-105.
[57]Deetlefs M,Hitchcock P B,Hussey C L,et al.Uranium halide complexes in ionic liquids[M].US:America Chemical Society,2005,901(4):47-67.
[58]Deetlefs M,Hussey C L,Mohammed T J,et al.Uranium halide complexes in ionic liquids:an electrochemical and structural study[J].Dalton Trans,2006(19):2334-2341.
[59]Giridhar P,Venkatesan K,Srinivasan T,et al.Electrochemical behavior of uranium(Ⅵ)in 1-butyl-3-methylimidazolium chloride and thermal characterization of uranium oxide deposit[J].Electrochim Acta,2007,52(9):3006-3012.
[60]Asanuma N,Harada M,Yasuike Y,et al.Electrochemical properties of uranyl ion in ionic liquids as media for pyrochemical reprocessing[J].J Nucl Sci Technol,2007,44(3):368-372.
[61]Ikeda Y,Hiroe K,Asanuma N,et al.Electrochemical studies on uranyl(Ⅵ)chloride complexes in ionic liquid,1-butyl-3-methylimidazolium chloride[J].J Nucl Sci Technol,2009,46(2):158-162.
[62]Rao J,Venkatesan K,Nagarajan K,et al.Electrodeposition of metallic uranium at near ambient conditions from room temperature ionic liquid[J].J Nucl Mater,2011,408(1):25-29.
[63]Chen P-Y.The assessment of removing strontium and cesium cations from aqueous solutions based on the combined methods of ionic liquid extraction and electrodeposition[J].Electrochim Acta,2007,52(17):5484-5492.
[64]吴京珂,沈兴海,陈庆德.CMPO-离子液体萃取分离铀(Ⅵ)体系的电化学性质[J].物理化学学报,2013,29(8):1705-1711.
