抗蛋白粘附表面的制备与表征
2014-12-16曾叶汪维成郑超
曾叶 汪维成 郑超
(浙江省医疗器械研究所 浙江杭州 310009)
1 前言
蛋白质类药物具有活性高、特异性强、低毒性、副作用小、生物功能明确、有利于临床应用等特点而倍受关注。但是其来源稀少、价格昂贵、药效极高,由于容器壁的吸附而造成的浓度减小和波动通常会给药物的有效利用带来麻烦[1,2]。实验和临床都反复证实,胰岛素等蛋白类药物在存储和使用过程中因吸附于器壁的损失率可高达70%,这不仅造成医疗资源的极大浪费,还使得药物疗效大打折扣;再者,因器壁吸附而导致的药物浓度波动致使蛋白类药物的用药安全性受到很大的挑战,蛋白类药物的高效性决定了其较小的有效浓度和较窄的有效浓度范围,当体内血药浓度超出有效浓度范围时会产生诸多副作用,严重时将危及患者的生命[3,4]。因此,减少或者杜绝器壁对药物的吸附是蛋白类药物在使用过程中亟需解决的问题。
日本科学家浅川直树等[5]尝试了在胰岛素溶液中加入不同浓度的卵磷脂等两亲性小分子,实验结果表明在微量卵磷脂存在的情况下,胰岛素在容器壁和输送器壁上的吸附量都大大减少,回收率在90%以上,研究者们还发现这种卵磷脂等两亲性小分子加入法对亲水性容器和疏水性容器有同样的效果。但是加入的两亲性小分子会随着药液进入人体,容易在体内堆积,给患者带来未知的风险,使得这一方法并没有很好地得到推广。
国内外专家通过在固体表面接枝磷酸胆碱(Phosphoryc holine),模拟磷脂双分子层的结构,实现了类似细胞膜的非特异性高阻抗性能。不断有报道证实,磷酸胆碱修饰的固体表面能够实现抗凝血、抗蛋白吸附、抗细胞及细菌粘附等效果。目前,不少带磷酸胆碱基团的化合物已经被FDA批准用于生物医药领域。随着研究的不断深入,表面修饰用磷酸胆碱类化合物的种类不断丰富,合成工艺不断优化,最常用的2-(甲基丙烯酰氧基)乙基-2-(三甲基氨基)乙基磷酸酯(MPC)已经商品化。
本研究通过将细胞膜仿生处理技术用于药液存储和输送器皿的表面修饰上,在不向药物溶液引入其它物质的前提下,实现类似细胞膜表面的非特异性高阻抗效应,从根本上解决蛋白类药物吸附损失的问题,杜绝由于药物吸附而造成的药物浓度波动,节省医药开支,增加用药安全性。
2 实验部分
2.1 材料
胰岛素、2-(甲基丙烯酰氧基)乙基-2-(三甲基氨基)乙基磷酸酯(MPC)、多巴胺盐酸盐(DOPA)、聚乙烯亚胺(PEI)购自sigmaaldrich,γ-氨丙基三乙氧基硅烷(APTS)和FITC购自阿拉丁试剂。
2.2 制备方法
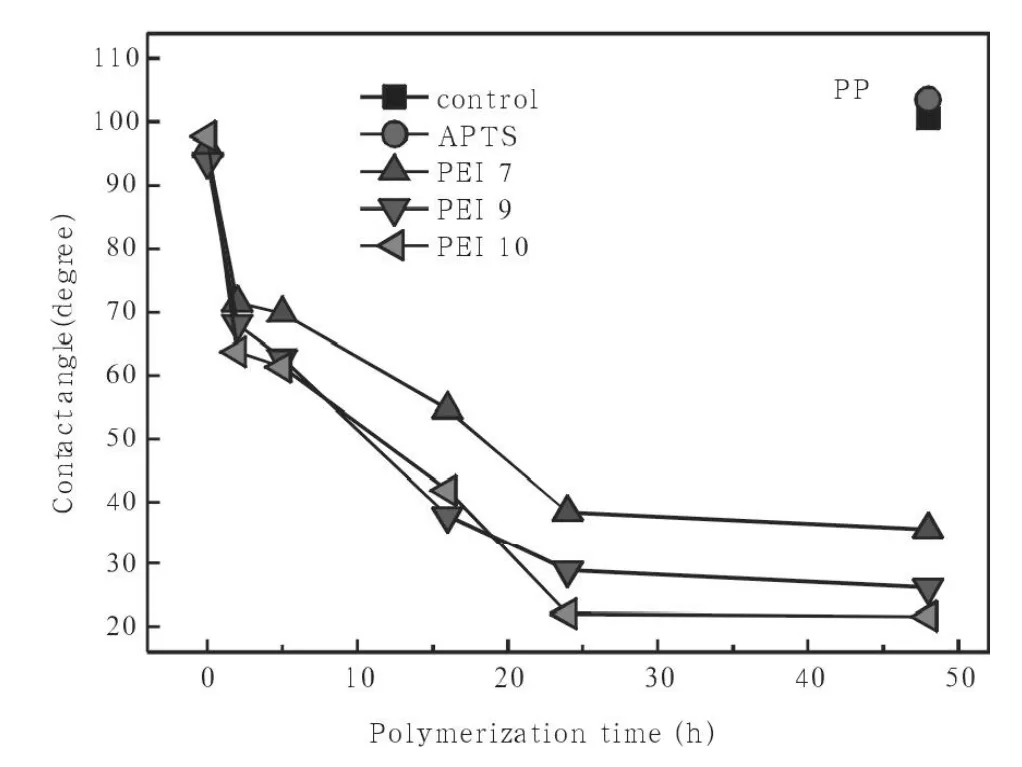
图2 聚丙烯表面氨基化处理后接触角的变化:■空白;●APTS处理;▲ 分别是DOPA聚合不同时间后覆盖pH为7、9、10的PEI。
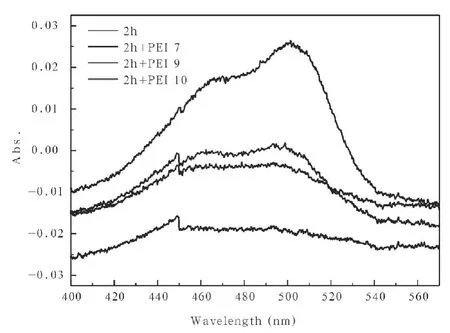
图3 FITC标记后不同pH值PEI处理表面的紫外-可见吸收光谱

图4 FITC标记后不同聚合时间DOPA表面的紫外-可见吸收光谱
为制备细胞膜仿生的抗蛋白粘附表面,我们以聚丙烯板(PP)和玻璃片为基材,充分清洗之后,浸泡到多巴胺盐酸盐(DOPA)溶液中反应一段时间,清洗吹干后浸泡到聚乙烯亚胺(PEI)溶液中一段时间,最后浸泡到2-(甲基丙烯酰氧基)乙基-2-(三甲基氨基)乙基磷酸酯(MPC)溶液中一段时间,洗净吹干即可。

图5 FITC标记后不同处理方法表面的紫外-可见吸收光谱
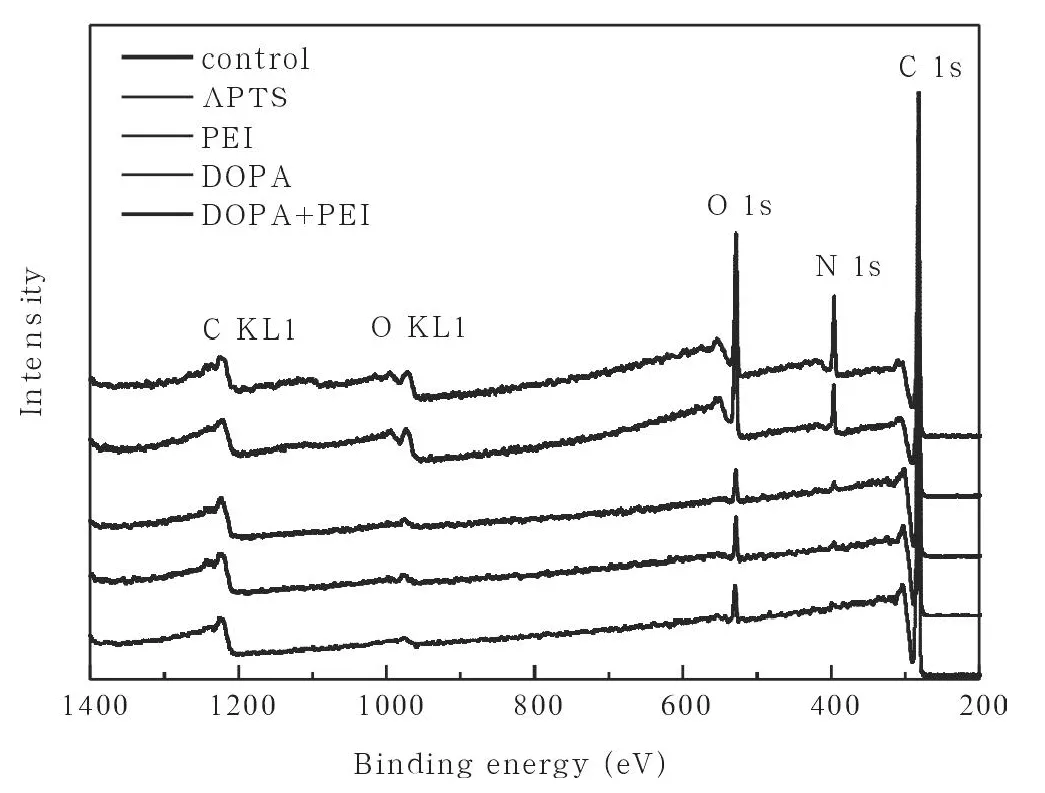
图6 PP基材上不同氨基化表面的xps图谱

图7 PP基材上N原子的百分比随DOPA聚合时间延长的变化曲线
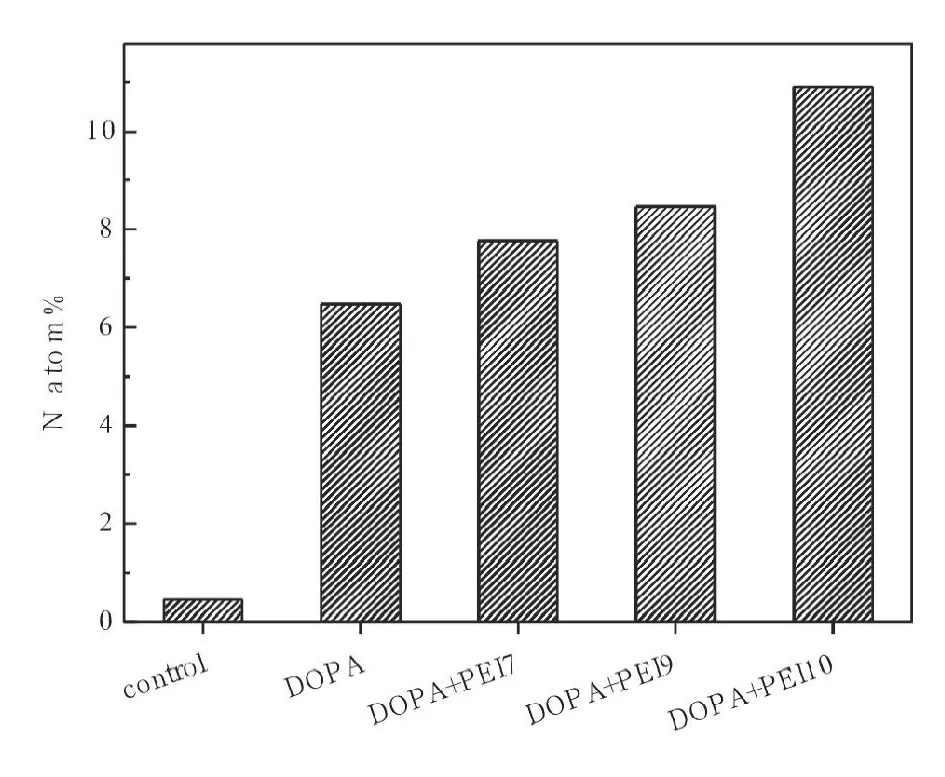
图8 PP基材上不同氨基化处理表面N原子百分比

图9 聚丙烯基材不同表面MPC固定化前后的接触角变化
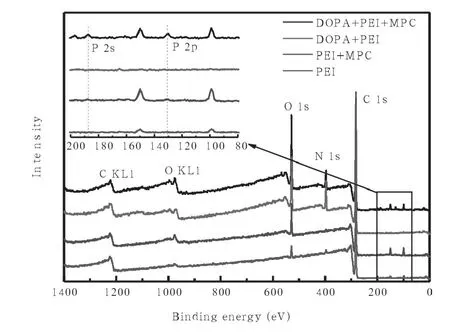
图10 PP基材上氨基化表面固定MPC前后的xps图谱

图11 PP空白片吸附胰岛素前后的xps图谱
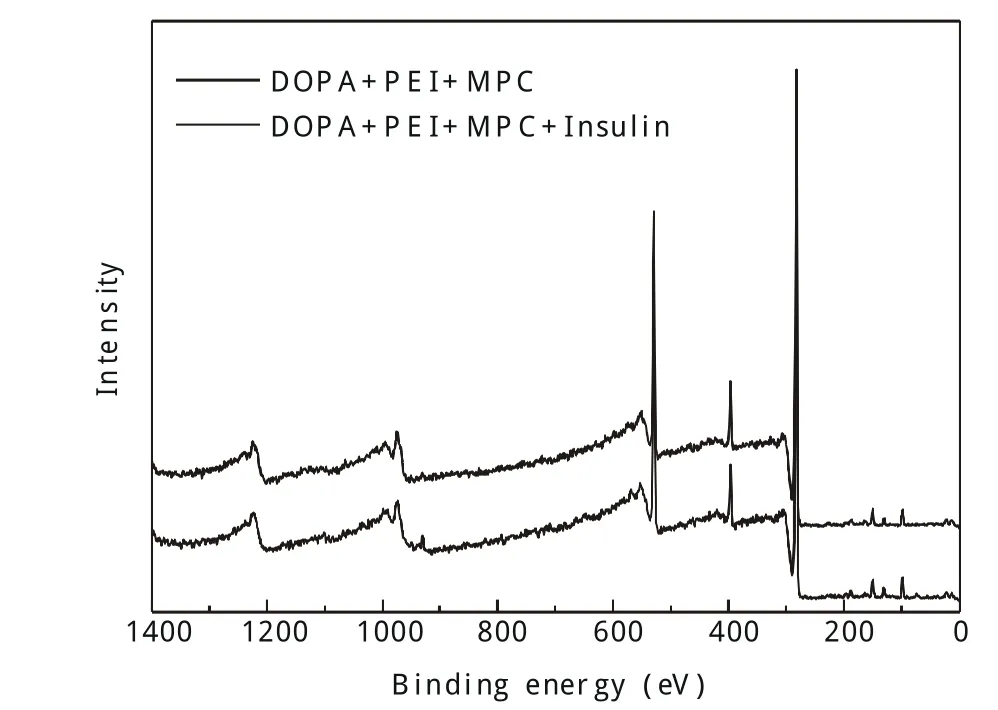
图12 MPC固定化的PP片吸附胰岛素前后的xps图谱
3 结果与讨论
本研究的工作内容主要包括表面预处理、磷酸胆碱的表面固定化、表面蛋白吸附性能检测这几块内容。
3.1 基材的预处理
表面预处理的目的是使材料表面带上氨基功能基团,以方便接枝带有磷酸胆碱基团的分子。高的表面氨基覆盖率是成功制备细胞膜仿生表面的前提条件。这里我们首先使生物粘附分子DOPA在基材表面进行聚合活化表面,随后吸附一层PEI大分子,使得表面具有较高密度的氨基覆盖率。图1和图2分布给出了玻璃和聚丙烯表面氨基化处理前后的接触角数据。从图1中可知,未处理的玻璃表面亲水性很强,接触角接近0°,硅烷偶联剂APTS处理之后,接触角增加到了近30°;亲水玻璃对PEI的吸附能力很强,不同pH的PEI浸泡后接触角也上升到30°左右,DOPA在玻璃表面聚合后再浸泡到PEI溶液中,表面的接触角先增大后减小,最终稳定在20-30°,表明表面氨基化的顺利完成。(图1、图2)
从图2可知,聚丙烯(PP)基材表面呈疏水性,接触角高达100°,在硅烷偶联剂APTS处理之后,接触角并没有改变,这是因为PP表面没有活性基团可与硅烷偶联剂反应,致使APTS的氨基化反应失败;PEI分子在疏水的PP表面的吸附也不明显,PP在不同pH的PEI溶液中浸泡后,接触角并未见下降,而在DOPA聚合并进行PEI浸泡后,表面接触角迅速下降,最终稳定在30°左右,表明在疏水的PP基材上表面氨基化的顺利完成。
为进一步验证表面氨基化的完成并考察氨基覆盖程度,我们使用绿色荧光素(FITC)对氨基进行标记,随后通过紫外-可见光谱对FITC进行了表征。图3-图5给出的是不同氨基化处理表面FITC标记后的紫外-可见光谱图。如图3所示,DOPA聚合2h时,FITC标记后500nm左右没有明显的吸收峰,证明DOPA聚合后表面并没有氨基,继续浸泡到PEI溶液中并经FITC标记后,500nm左右出现明显的吸收峰,且随着PEI溶液pH值的增加吸收峰值越大,表明PEI分子很容易吸附到DOPA聚合膜上,且吸附量随着溶液pH值的增加而增加。
图4跟踪了不同聚合时间的DOPA膜表面吸附PEI后氨基的量,可见随着DOPA聚合时间的延长,紫外-可见吸收光谱的基线升高,体现了DOPA聚合膜厚的增加,同时500nm左右的特征吸收峰值的增加也说明了随着聚合时间的增加,吸附PEI的能力也逐渐增强并趋于饱和而稳定。DOPA聚合膜上吸附PEI的量与PEI直接吸附于玻璃片上的量相当,且此时基材表面氨基的量小于APTS处理后的氨基量(图5)。
结合接触角与紫外-可见光谱数据可知,对玻璃表面进行氨基化处理的最佳方式是硅烷偶联剂APTS,同时通过DOPA聚合然后吸附PEI的方式也可以实现表面氨基化。
对于疏水的PP表面,我们通过xps对不同处理方式的氨基化表面进行了进一步的验证(图6-图8)。由图6可知,PP在经过硅烷偶联剂APTS处理后,基本没有变化,这与接触角的数据一致,再次证实硅烷偶联剂处理的方法不适用于PP这类惰性表面;PEI浸泡后N1s的位置有微弱的小峰,表明有极少量的PEI吸附到PP表面上;DOPA聚合后,N峰明显增强;DOPA聚合膜上吸附PEI后N峰进一步增强,证实DOPA可以成功在惰性的PP表面进行聚合,并介导PEI的吸附。
图7给出了随着DOPA聚合时间的增加,N原子百分数的变化情况,可见随着聚合时间的增加,N原子在表面原子中所占的比例也大大增加,体现了DOPA表面聚合的顺利进行。
图8给出的是PP基材上DOPA聚合24h后浸泡到不同pH值的PEI溶液中吸附PEI分子后表面N原子的百分比。可见,随着浸泡的PEI溶液的pH值的增加,N原子百分含量增加,表面PEI溶液pH的升高有助于表面吸附更大量的PEI分子。这一现象跟玻璃基材上的情况一致。
结合接触角和xps数据证实:虽然APTS处理和直接吸附PEI的方法不能有效作用于PP这类疏水的惰性表面,但是DOPA可以成功在改表面聚合,并能够顺利介导PEI的吸附,从而实现表面氨基化。
3.2 磷酸胆碱的表面固定化
经过预处理的,表面带有氨基功能基团的基底材料,其表面的氨基能与MPC分子反应,从而实现表面MPC的固定化。我们首先用接触角对基材表面的MPC固定化进行了跟踪,如图9所示,直接吸附PEI的表面在浸泡到MPC溶液中之后其接触角仍保持在90-100°之间,这一接触角与PP基材的接触角很接近,表明MPC不能顺利接到该表面上;DOPA聚合2、5h后的表面在MPC固定化前后接触角也没有变化,而在DOPA聚合16、24h的表面上经MPC固定化之后,接触角上升到50-60°之间。
XPS用来进一步验证MPC在材料表面的固定化情况,从图10中可以看出,PEI直接吸附的PP表面在浸泡到MPC溶液中后,无论是N还是P的峰位都没有明显的吸收;而在DOPA介导的PEI吸附表面上,在固定了MPC之后,在P的峰位出现了明显的吸收峰,证实了MPC成功地接枝到了基材表面。且不同DOPA聚合时间介导的PEI吸附表面都能够固定MPC。
3.3 基材表面蛋白吸附性能检测
为考查基材表面细胞膜仿生修饰的有效性,我们以胰岛素为模型蛋白,通过xps检测基材在与胰岛素溶液接触前后表面化学组成的变化。
图11和图12分别展示了空白PP和经DOPA介导PEI吸附并固定MPC后的PP片上胰岛素的吸附情况。从图11上可以明显看到,在浸泡到胰岛素溶液中之后,PP表面出现了N吸收峰,且O的吸收峰形发生变化同时吸收值大大增加,这些现象均证实了胰岛素在PP表面的吸附。
图12显示的是经DOPA介导吸附了PEI并且固定了MPC表面在浸泡到MPC溶液中前后的xps图谱,可见该表面在浸泡到胰岛素溶液前后没有明显的变化,证实了该表面良好的抗蛋白(胰岛素)粘附性能。
4 全文结论
本文通过DOPA表面聚合介导PEI分子在疏水惰性表面的吸附,并进一步固定MPC,成功地在聚丙烯及玻璃基材上制备了细胞膜仿生的磷酸胆碱两性分子表面,接触角、紫外-可见吸收光谱、xps证实了这一过程的顺利进行;xps数据还进一步证实该表面能够有效阻抗胰岛素的粘附。
[1]侯惠如,孟晓敏,吴素芬,等.输液装置对胰岛素吸附作用的研究[J].中华护理杂志,1999,34(11):649.
[2]王忍.药物在输液管中的损失[J].中国药房,1992,3(4):40.
[3]庞英杰,陈晰敏,糖尿病病人静脉用药后低血糖反应的分析与对策[J].护理研究杂志,2007(S0):98.
[4]柴晓媛,庞英杰,陈淑敏,等.振摇法预防临床输注胰岛素突发低血糖反应的研究[J].中国实用护理杂志,2008,24(9):52.
[5]浅川直树.防止容器对胰岛素的吸附作用[J].药学杂志,1984,104(3):311.