HPLC法测定人血浆中拉莫三嗪的浓度及其影响因素研究
2014-12-03宋霞张建隆邱雯兰州大学第二医院药学部兰州730030天水市第一人民医院药剂科甘肃天水741000
宋霞,张建隆,邱雯(1.兰州大学第二医院药学部,兰州730030;.天水市第一人民医院药剂科,甘肃天水 741000)
癫痫是脑部神经元突发性异常放电,导致短暂的大脑功能障碍的一种常见的神经系统慢性发作性疾病。药物治疗是治疗癫痫的首选方法,对大约70%的癫痫患者治疗有效。但传统抗癫痫药(如丙戊酸钠、卡马西平、苯巴比妥、苯妥英钠、扑痫酮、乙琥胺)耐受性问题严重,不良反应较多,因而近十几年来已有不少新型抗癫痫药问世。拉莫三嗪(Lamotrigine,LTG)是一种新型抗癫痫药,是封闭电压应用依从性的钠离子高通道阻滞药,主要通过抑制神经元释放病理性谷氨酸递质而发挥抗癫痫(EP)作用,具有广泛的抗癫痫谱,对多种类型的发作均有效。由于LTG适用人群广、药动学个体差异大,有必要对LTG用药患者进行治疗药物监测,以促进LTG合理应用及个体化用药方案的调整。本文建立了HPLC法测定LTG血药浓度,并收集我院癫痫患者LTG治疗药物监测情况进行相关分析。
1 材料
1.1 仪器
Agilent 1100型HPLC仪,包括G1315 A型二元泵、G1315 B型二极管阵列检测器、G2170 AA型色谱工作站(美国安捷伦公司);GENIUS电子天平(德国赛多利斯集团);TGL-16 GB小型通用离心机(上海安亭科学仪器厂制造)。
1.2 药品与试剂
拉莫三嗪对照品(中国食品药品检定研究院,批号:100775-200401);内标:氯霉素对照品(上海申药股份有限公司,批号:941203);卡马西平对照品(中国食品药品检定研究院,批号:100142-199503);苯妥英钠对照品(中国食品药品检定研究院,批号:100210-200401);苯巴比妥(PB)对照品(国家麻醉品实验室,批号:1222-9602);地西泮对照品(国家麻醉品实验室,批号:1230-9601);氯硝西泮对照品(中国食品药品检定研究院,批号:1227-9701)。对照品均为含量测定用。甲醇、乙腈为色谱纯,其他试剂均为分析纯,水为纯化水。
1.3 资料来源
2012年7月-2013年6月在我院癫痫中心、神经内科、神经外科诊治并进行LTG治疗药物监测的患者320例次,收集患者性别、年龄、体质量、LTG维持剂量、末次服药时间、取血时间、合并用药的药物和剂量等信息。
2 方法与结果
2.1 HPLC含量测定方法的建立
2.1.1 色谱条件:色谱柱为Luna C18(250 mm×4.6 mm,5 μm);流动相为乙腈-磷酸盐缓冲液(0.02 mol/l磷酸二氢钾,1 mol/L氢氧化钠调节pH至6.0,30∶70,V/V);流速为1.0 ml/min;进样量为20 μl;柱温为30℃;检测波长为306 nm。在该色谱条件下,拉莫三嗪与氯霉素的保留时间分别为7.48、11.73 min,色谱见图1。
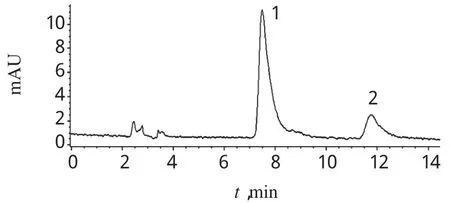
图1 对照品高效液相色谱图1.拉莫三嗪;2.氯霉素Fig 1 HPLC chromatograms of standard control1.lamotrigine;2.chloramphenicol
2.1.2 标准溶液的配制:准确称取LTG对照品10.8 mg,置于10 ml量瓶中,用甲醇溶解并定容,得1.08 mg/ml LTG储备液。将LTG储备液用甲醇稀释,配制质量浓度分别为4.0、8.0、16.0、40.0、64.0、80.0、96.0、128.0、160.0μg/ml的 LTG 标准溶液,将储备液与标准溶液于4℃下保存。
2.1.3 内标溶液的配制:准确称取氯霉素对照品10.0mg,置100 ml量瓶中,用甲醇溶解并定容,得100 μg/ml的内标溶液,于4℃下保存。
2.1.4 血浆样品的处理及测定:精密吸取血浆样品200 μl,置1.5ml离心管中,加入甲醇25μl及内标溶液25μl,涡旋混匀30 s后加入300 μl甲醇沉淀,涡旋混匀1 min,以离心半径为8 cm、10000 r/min离心10 min,取上清液经0.22 μm滤膜过滤,取滤液20 μl进样。
2.1.5 专属性考察:取空白血浆200 μl,按“2.1.4”项下方法操作,取上清液20 μl进样分析,得到空白血浆色谱图2 A。将空白血浆和拉莫三嗪与氯霉素对照品混合,按“2.1.4”项下方法操作,取上清液20 μl进样分析,得到样品溶液色谱图2 B。如图2所示,在该色谱条件下,血浆中的内源性物质对拉莫三嗪的测定无影响。
2.1.6 线性关系考察:精密吸取空白血浆200μl共9份,置于1.5 ml离心管中,分别加入不同质量浓度的LTG标准溶液25 μl及内标溶液25 μl,涡旋混匀30 s,使LTG血药浓度分别相当于0.5、1.0、2.0、5.0、8.0、10.0、12.0、16.0、20.0μg/ml。分别加入甲醇300 μl沉淀,涡旋混匀1 min,以离心半径8 cm、10000 r/min离心10min,取上清液经0.22μm滤膜滤过,取滤液20μl进样测定,记录色谱。以LTG系列溶液的峰面积(As)和内标峰面积(Ai)之比(y)为纵坐标、LTG质量浓度(x)为横坐标进行线性回归,得回归方程:y=0.1736 x+0.0147(r=0.9995,n=9)。结果表明,LTG血药浓度在0.5~20 μg/ml范围内线性关系良好。
2.1.7 回收率与精密度试验:分别于200μl空白血浆中加入低、中、高3种质量浓度的LTG标准溶液20 μl,涡旋混匀30 s,使血药浓度分别相当于1.0、10.0、20.0 μg/ml,按“2.1.4”项下方法处理并测定。以LTG血药浓度测得量与加入量之比计算方法回收率。以同日内测得的LTG浓度计算日内精密度,以1周内6次测定的LTG浓度计算日间精密度,详见表1。
表1 回收率与精密度试验结果(±s,n=5)Tab 1Results of recovery and precision test(s±s ,n=5)
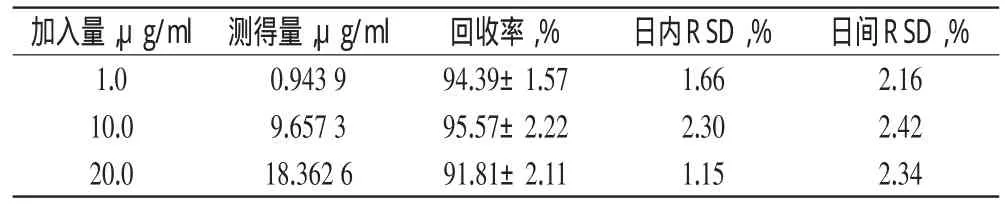
表1 回收率与精密度试验结果(±s,n=5)Tab 1Results of recovery and precision test(s±s ,n=5)
加入量,μg/ml 1.010.020.0测得量,μg/ml 0.94399.657318.3626回收率,%94.39±1.5795.57±2.2291.81±2.11日内R SD,%1.662.301.15日间R SD,%2.162.422.34
2.1.8 重复性试验:按“2.1.4”项样品制备方法制备同浓度样品8份,按并依法测定LTG浓度。结果,样品中LTG平均含量的RSD为1.89%,表明该法重复性良好。
2.1.9 干扰性试验:取临床常用的抗癫痫药卡马西平、PB、苯妥英钠、地西泮、氯硝西泮对照品适量,分别配制10.0 μg/ml的供试溶液,同时将上述所有对照品溶液与拉莫三嗪混合,按“2.1.1”项下色谱条件进样。结果表明,卡马西平、PB、苯妥英钠、地西泮、氯硝西泮对拉莫三嗪的测定均不产生干扰。另外,丙戊酸(VPA)分子结构中缺乏特征的紫外光谱吸收,用高效液相色谱法不能直接测定,因此,在本试验条件下,VPA对拉莫三嗪的测定无影响。
2.2 LTG血药浓度相关结果分析
2.2.1 样品采集:测定稳态时LTG的血药谷浓度。患者于下一次服药前抽取全血2~3 ml,置于普通采血管中,以离心半径为8 cm、4000 r/min于室温离心10 min,于-20℃冰箱保存待测。
2.2.2 分组及统计方法:将搜集的320例病例,按照LTG单用及联用分为3组:单用LTG组、LTG+VPA组、LTG+PB组,依次定义为1、2、3组。结果采用SPSS软件进行统计分析。应用逐步回归分析法评价分析影响LTG血药浓度的各类因素;用相关分析论证LTG与VPA以及PB之间的相互作用。
2.2.3 人群分布特征:2012年7月-2013年6月我院LTG血药浓度监测患者总人数为320例。其中男性158例,女性162例,男女性别比例为0.98∶1;17~45岁患者中女性居多,1~16岁患者中男性所占比例大。从患者年龄看,1~16岁患者占52.5%,儿童为我院LTG血药浓度监测患者中所占比例最大的人群;17~45岁青壮年患者占35.31%,属于第二主体人群;46~75岁中老年患者所占比例最小,见表2。
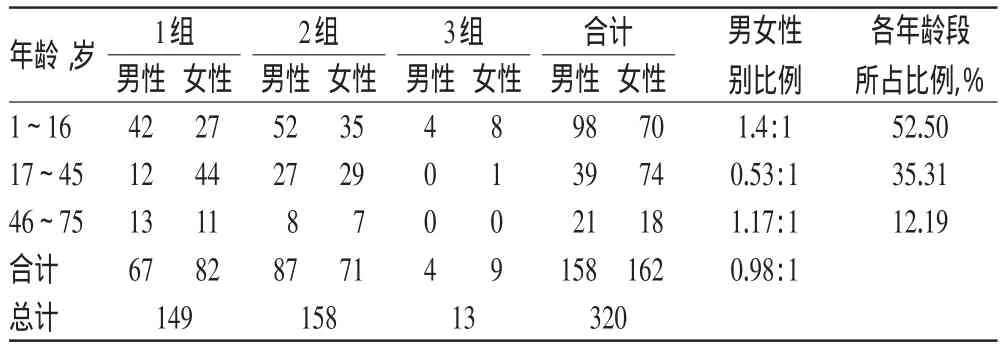
表2 监测患者人群性别与年龄分布(例)Tab 2 Population sex and age distribution of monitored patients(case)
2.2.4 LTG血药浓度的影响因素:整理320例血浆样本中LTG的含量及其可能的相关因素:性别、年龄、体质量、LTG给药剂量(mg/kg)、治疗组类别(1组:LTG单药治疗组;2组:LTG+VPA联合治疗组;3组:LTG+PB联合治疗组)输入统计学软件以通过逐步回归分析法逐步剔除或筛选影响LTG血药浓度的因素(检验水平为0.05)。结果显示,LTG给药剂量、联用VPA、联用PB可显著影响LTG血药浓度(P<0.05),性别、年龄、体质量则与其不存在显著性的相关关系(P>0.05)(见表3)。将影响因素LTG给药剂量、联用VPA、联用PB分别设定为自变量x1、x2、x3,LTG血药浓度设为因变量y,得逐步回归方程为:y=0.6417 x1+2.5698 x2-2.0482 x3-0.2078;经方差分析,P<0.01。由此方程可知,LTG血药浓度与LTG给药剂量、VPA的影响呈正相关,与PB的影响呈负相关。即增大LTG给药剂量或加用VPA可提高LTG的血浆水平,加用PB则能降低其血浆水平。
2.2.5 联合应用其他抗癫痫药对LTG血药浓度的影响:各组一般资料及药物剂量与血药浓度比较见表4。2组VPA剂量范围为1.85~58.33mg/(kg·d);3组PB剂量范围为1.19~5.29mg/(kg·d)。其中PB联合治疗组的拉莫三嗪血药浓度[(0.8±0.92)μg/ml]<LTG单药治疗组[(3.02±2.55)μg/ml]<VPA联合治疗组[(5.37±3.47)μg/ml]。应用方差分析法比较3组血药浓度,得到F值为0.0190,P<0.01,表明各治疗组间拉莫三嗪的血药浓度存在着极显著的差异。
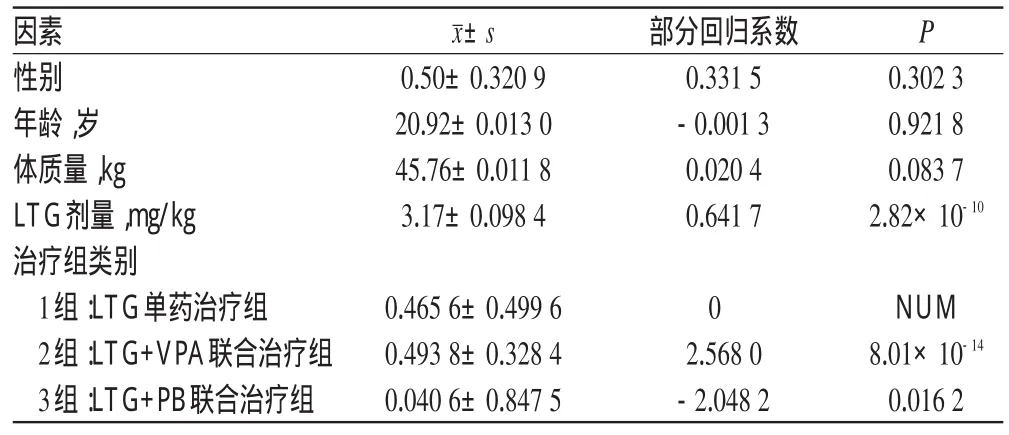
表3 影响LTG血药浓度的因素分析(n=320)Tab 3 Analysis of influential factors of plasma concentration of LTG(n=320)
表4 血浆样本中拉莫三嗪的血药浓度(±s,n=320)Tab 4 Plasma concentrations of LTG in plasma samples(±s ,n=320)
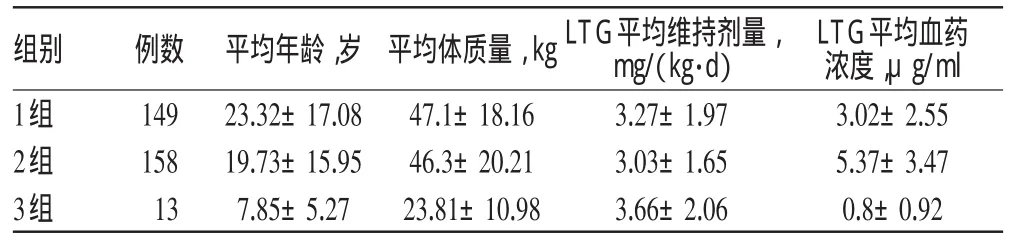
表4 血浆样本中拉莫三嗪的血药浓度(±s,n=320)Tab 4 Plasma concentrations of LTG in plasma samples(±s ,n=320)
组别1组2组3组例数14915813平均年龄,岁23.32±17.0819.73±15.957.85±5.27平均体质量,k g 47.1±18.1646.3±20.2123.81±10.98 LT G平均维持剂量,mg/(k g·d)3.27±1.973.03±1.653.66±2.06 LT G平均血药浓度,μg/ml 3.02±2.555.37±3.470.8±0.92
2.3 不同组别中药物因素与LTG血药浓度的相关性分析
2.3.1 LTG单药治疗组:LTG给药剂量与LTG血药浓度的相关性:采用Pearson相关分析,对LTG给药剂量与LTG血药浓度之间的相互关系进行分析。结果表明,r=0.119,P>0.01。散点图显示,LTG血药浓度随着剂量的增加有上升趋势,但无统计学意义,见图3。
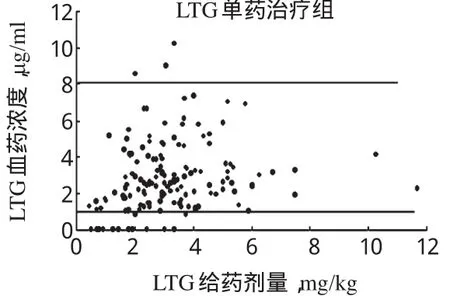
图3 LTG给药剂量与LTG血药浓度的相关性散点图Fig 3 The scatter diagram of LTG dose and LTG plasma concentration
2.3.2 LTG与VPA联合治疗组:(1)LTG给药剂量与LTG血药浓度的相关性。对LTG给药剂量与LTG血药浓度之间的相互关系进行分析,结果r=0.536,P<0.01,表明LTG血药浓度与LTG给药剂量具有显著的正相关关系。散点图显示,LTG血药浓度随着LTG给药剂量的增加而增加,见图4。(2)VPA给药剂量与LTG血药浓度的相关性。对VPA给药剂量与LTG血药浓度之间的相互关系进行分析,结果r=0.112,P>0.01。散点图显示,LTG血药浓度随着VPA剂量的增加有上升趋势,无统计学意义,见图5。(3)VPA血药浓度与LTG血药浓度的相关性。对VPA血药浓度与LTG血药浓度之间的相互关系进行分析,结果r=0.206,P<0.01,表明LTG血药浓度与VPA血药浓度具有显著的正相关关系。散点图显示,LTG血药浓度随着丙戊酸血药浓度的上升而上升,见图6。
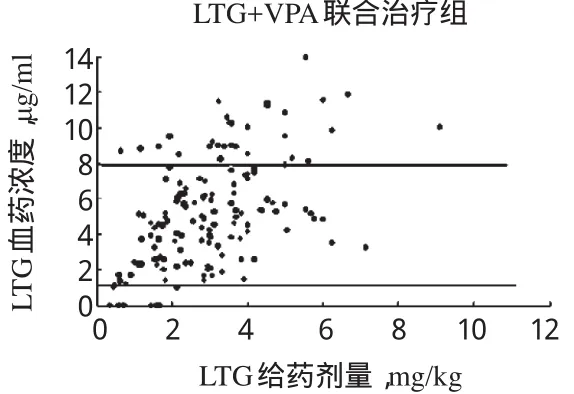
图4 LTG给药剂量与LTG血药浓度的相关性散点图Fig 4 The scatter diagram of LTG dose and LTG plasma concentration

图5 VPA给药剂量与LTG血药浓度的相关性散点图Fig 5 The scatter diagram of VPA dose and LTG plasma concentration
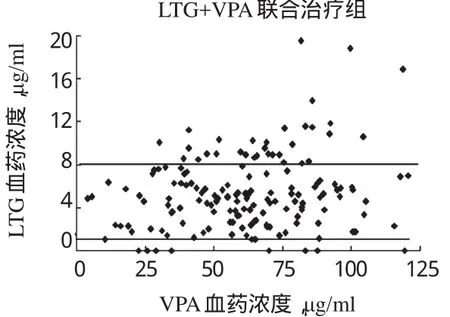
图6 VPA血药浓度与LTG血药浓度的相关性散点图Fig 6 The scatter diagram of VPA plasma concentration and LTG plasma concentration
2.3.3 LTG与PB联合治疗组:对LTG给药剂量与LTG血药浓度之间的相互关系进行分析,结果r=0.320,P>0.01。对PB给药剂量与LTG血药浓度之间的相互关系进行分析,结果r=0.040,P>0.01。两种结果差异均无统计学意义。由于此组别中进行苯巴比妥血药浓度测定的样本较少,故不便进行PB血药浓度与LTG浓度的Parson相关分析。
3 讨论[1-6]
3.1 影响LTG血药浓度的因素
LTG属于苯基三嗪类化合物,是一种新型抗癫痫药,具有弱的抗叶酸活性。鉴于其良好的抗癫痫作用,可用于各种癫痫的治疗,也可单用或联合添加使用。近年来,国外也有资料报道显示LTG单药治疗部分性发作为主的成人及儿童癫患者也有较好的效果[1-2]。
本文特选取320例采用LTG治疗的癫痫患者,通过逐步回归分析法依次剔除或筛选影响LTG血药浓度的因素,结果显示LTG给药剂量、联合应用VPA或PB对LTG血药浓度影响具有统计学意义(P<0.05)。从作用大小来看,联合应用VPA对LTG血药浓度的影响最为明显,其次为LTG给药剂量。从作用性质来看,LTG血药浓度与LTG给药剂量、VPA的影响呈正相关,与PB的影响呈负相关,即增大LTG给药剂量或者联合应用VPA可提高LTG血浆水平,而加用PB则可降低LTG的血浆水平。基于此,LTG的临床治疗不能仅仅通过给药剂量而了解其血药浓度。为了更好地实现个体化给药,为患者制订安全、合理、有效的治疗方案,建立该药的血药浓度监测工作必不可少。此外,体质量对LTG血药浓度的影响在国外文献亦有报道,研究指出由于高体质量患者体内LTG的清除速率较慢因而血浆水平较高[3]。本文研究未出现此结果。
3.2 联合用药对LTG血药浓度的影响
VPA与LTG联合应用是目前临床治疗难治性癫痫的主要方法。在药效学方面,LTG可增强γ-氨基丁酸(GABA)能突触后作用,VPA抑制兴奋性氨基酸释放,共同使膜电位趋于稳定,两药抗癫痫机制互补。在药动学方面,90%的LTG主要通过与葡萄糖醛酸结合代谢,大约30%~50%的VPA也经葡萄糖醛酸结合代谢,VPA可竞争性抑制LTG与葡萄糖醛酸的结合,使LTG清除率下降,从而延长LTG的半衰期,提高LTG的血浆水平。Gidal BE等[4]在一项研究中发现,丙戊酸的血药浓度在治疗水平(50~120μg/ml)便显著抑制LTG的清除率,VPA浓度超过20 μg/ml时对LTG的口服清除率的抑制程度最大。Paraskevas GP等[5]研究表明VPA与LTG合用临床疗效显著,且血浆内谷氨酸含量明显降低,其效果优于LTG单药治疗。
LTG在与具有肝酶诱导作用的药物如PB、卡马西平、苯妥英钠合用时,其药动学可发生改变,半衰期缩短。临床上联合使用时,通常需要增加LTG的剂量[6]。本研究通过逐步回归分析发现联合应用其他抗癫痫药是影响LTG血药浓度的重要因素(P<0.05)。LTG单药治疗组与2个联合用药组做F值检验,显示3组LTG血药浓度有显著差异(P<0.01)。VPA治疗组的LTG平均血药浓度最高,LTG单药治疗组次之,PB治疗组最低,表明加用PB可显著降低LTG血药浓度,加用VPA则能显著升高其血药浓度。
[1]Fakhoury TA,Barry JJ,Mitchell Miller J,et al.Lamotrigine in patients with epilepsy and comorbid depressive symptoms[J].Epilepsy&Behavior,2007,10(2):155.
[2]McKee JR,Sunder TR,FineSmith R,et al.Lamotrigine as adjunctive therapy in patients with refractory epilepsy and mental retardation[J].Epilepsy&Behavior,2003,4(5):386.
[3]Gidal GE,Anderson GD,Rutecki PR,et al.Lack of an effect of valproate concentration on lamotrigine pharmacokinetics in developmentally disabled patients with epilepsy[J].Epilepsy Research,2000,42(1):23.
[4]Gidal BE,Sheth R,Parnell J,et al.Evaluation of VPA dose and concentration effects on lamotrigine pharmacokinetics:implications for conversion to lamotrigine monotherapy[J].Epilepsy Research,2003,57(1):85.
[5]Paraskevas GP,Triantafyllou NI,Kapaki E,et al.Add-on lamotrigine treatment and plasma glutamate levels in epilepsy:relation to treatment response[J].Epilepsy Research,2006,70(2/3):184.
[6]包军,何英,苏渊,等.影响拉莫三嗪稳态血药浓度的相关因素研究[J].中华儿科杂志,2001,39(8):457.
