内皮素受体拮抗剂治疗肺动脉高压疗效和耐受性的网状Meta分析
2014-12-02梁富翔宋兵祁泉李元敏刘瑞生
梁富翔,宋兵,祁泉,李元敏,刘瑞生
肺动脉高压是由多种原因导致的肺血管床受累,进一步使肺循环阻力进行性增加,最终导致右心衰竭和死亡的一类严重疾病[1]。肺动脉高压的病理特点尚未明确,但已确认血管收缩与舒张以及增生与抗增生之间的失衡在肺动脉循环异常中发挥重要作用[2,3]。肺动脉高压发病率较低,但预后极差。研究显示每百万人中有15人患有肺动脉高压[4],平均生存时间为2.8年,其中约15%的患者在治疗期间1年内死亡[5,6]。
内皮素受体拮抗剂是一类强有力的血管舒张和抗增殖物质,可以特异性的扩张和重塑肺动脉系统,是目前治疗肺动脉高压的常规药物之一。内皮素受体主要分为内皮素A受体和内皮素B受体,内皮素A受体常见于血管平滑肌细胞,其通过增加细胞内钙离子浓度而使血管收缩,内皮素B受体主要存在于内皮细胞,主要通过刺激一氧化氮和前列腺素释放而使血管舒张。无论是单独选择性拮抗A受体或是同时拮抗A和B受体,都能使血管扩张。目前经FDA批准上市的内皮素受体拮抗剂主要有安贝生坦(Ambrisentan)、波生坦(Bosentan)、西他生坦(Sitaxsentan)和马西替坦(Macitentan)。已有相关系统评价了内皮素受体拮抗剂与安慰剂比较治疗肺动脉高压的疗效[7,8],并未有内皮素受体拮抗剂4种药物之间进行比较的研究,同时,也没有分析这4种药物在疗效、耐受性以及其他结局指标方面的排名。
网状Meta分析(network Meta-analysis,NMA)是由传统的Meta分析发展而来,即从标准的两组试验Meta分析扩展为同时将一系列多个不同处理因素进行相互分析比较的方法[9]。NMA最大的优越性在于它能将治疗同类疾病的不同干预措施汇总后进行定量化的统计分析比较。本研究采用网状Meta分析的方法对四种内皮素受体拮抗剂治疗肺动脉高压在疗效和耐受性进行评价,并基于当前证据提供排序。
1 资料与方法
1.1 文献纳入标准 ①P:肺动脉高压患者,满足ACCF/AHA 2009年指南中对肺动脉高压的分类及诊断标准1;②I:内皮素受体拮抗剂;③C:安慰剂或与干预措施不同的另一种内皮素受体拮抗剂;④O:主要结局指标包括疗效和耐受性,疗效以6分钟步行距离为标准,耐受性以各种原因导致退出试验患者为标准;次要结局指标包括病死率和临床恶化率,病死率指在治疗周期内死亡患者的比率,不包括随访周期,临床恶化率为复合型结局指标,是指患者在治疗周期内发生包括住院、心血管问题、肺移植等在内的各类事件的比率。⑤S:随机对照试验(Randomized controlled trial,RCT)。
1.2 文献检索策略 计算机检索PubMed、EMBASE、Cochrane Library和中国生物医学文献数据库、中国知网、万方数据库,中文检索词包括肺动脉高压、肺心病、内皮素受体拮抗剂、安贝生坦、波生坦、西他生坦、马西替坦;英文检索词包括Pulmonary hypertension、lung hypertension、endothelin receptor antagonist、ambrisentan、bosentan、sitaxsentan、macitentan。检索时限均为建库至2014年1月31日,所有数据库检索均采用主题词PubMed(MeSH),EMBASE(EMtree)与自由词相结合的方式,根据具体数据库适当调整。检索策略都通过多次预检索后确定,检索文种不限。检索相关专业期刊、会议论文集、临床试验注册平台(ClinicalTrials.gov)和追溯纳入文献和相关Meta分析的参考文献,以获取以上检索未发现的相关信息。
1.3 文献筛选与数据提取 文献筛选过程和数据提取均由2位研究者独立进行,按照纳入标准分别阅读文题和摘要进行初筛,进一步查找并阅读全文进行复筛。数据提取采用Excel数据库独立提取资料,主要提取试验组与对照组的基线情况、治疗方案和结果指标数据。第3名研究者解决文献筛选与资料提取中的不一致。
1.4 纳入文献的质量评价 由2名研究者独立完成,如遇分歧讨论解决或由第3名研究者判定。采用Cochrane handbook for systematic reviews of interventions 5.1.0[10]版本推荐偏倚风险评估工具评价纳入研究的偏倚风险[9],主要包括随机序列号产生、分配隐藏、盲法实施、不完整报道、选择性报道和其他偏倚。
1.5 统计方法 首先,采用Revman5.2软件进行直接Meta分析。对于二分类变量使用比值比(odds ratio, OR)及95%可信区间(confidence interval,CI)为疗效分析统计量。对于连续性变量使用均数差(mean difference,MD)及其95%CI为统计量。使用I2进行异质性检验,小于20%为轻度异质性,20%~50%为中度异质性,大于50%为高度异质性。如各研究结果之间有足够的统计学和临床同质性,则采用固定效应模型进行合并分析;若纳入研究结果间存在异质性,则首先分析产生异质性的原因,进而确定是否采用随机效应模型进行合并分析。
其次,采用GEMTC软件[11]进行网状Meta分析,通过DerSimonian-Laird随机效应模型和蒙特卡罗马尔科夫模型(Monte Carlo Markov Chain,MCMC)进行合并。对于二分类变量,使用OR及95%CI为疗效分析统计量。对于连续性变量,使用MD及其95%CI为统计量。使用等级概率图(rank probability plot)对干预措施疗效排序。
通过绘制网状关系图呈现不同干预措施间存在的直接比较与间接比较关系[12]。直接与间接比较的不一致性通过节点分裂值(node split)衡量[13],当P<0.05时认为不一致性明显。
2 结果
2.1 文献筛选 通过题目及摘要筛选后,共纳入1693篇文献。去重333篇文献,阅读文献摘要,根据研究药物、研究类型、相关结局指标等共排除1363篇文献,下载并阅读剩余文献全文后,根据纳入排除标准,最终共纳入文献12[14-25]篇包含2191例患者。筛选流程见图1。
2.2 基线特征 纳入的12篇文献中,2篇文献[24,25]来自于中国,4篇文献[14,15,17,20]来自于美国,其余均为国际性研究。有1篇文献19纳入了2个RCT,其余都只纳入了1个RCT。1项研究15为3臂研究,比较了西他生坦、波生坦和安慰剂,其余均为2臂研究,219个RCT比较了安贝生坦与安慰剂,7个RCT[14,17,18,20,22,24,25]比较了波生坦与安慰剂,1个RCT21比较了马西替坦与安慰剂,2个RCT[16,23]比较了西他生坦与安慰剂。具体基线情况见表1。网状关系见图2。
2.3 偏倚风险结果 质量评价方面,13个RCT均提及随机,但只有6个RCT[15-20]具体描述了随机方法;4个RCT[18,19,21]提及分配隐藏,其余研究未提及分配隐藏;有2个RCT[24,25]未说明是否采用盲法,其余RCT均为双盲研究,实施对象为研究对象与观察者;有2个RCT[24,25]有不完整的结局报道;有4个RCT[19,24,25]选择性结局报道;有4个RCT[16,18,21,23]有相关药物公司资助,其余研究的其他偏倚不清楚。

图1 文献筛选流程图
2.4 直接比较Meta分析 在疗效方面,4种内皮素受体拮抗剂的6分钟步行距离均优于安慰剂,其中安贝生坦效果最好(MD=41.51米,95%CI: 25.34~57.69),波生坦与西他生坦的比较差异无统计学意义。在耐受性方面,只有安贝生坦的效果优于安慰剂(OR=0.44,95%CI:0.23~0.84),其余药物与安慰剂的比较差异无统计学意义,波生坦与西他生坦的比较差异无统计学意义(表2)。
在病死率方面,4种药物与安慰剂比较差异均无统计学意义。在临床恶化率方面,安贝生坦(OR=0.27,95%CI:0.13-0.57)、波生坦(OR=0.34,95%CI:0.20-0.60)、西他生坦(OR=0.34,95%CI:0.16-0.76)均优于安慰剂,出现较少的临床恶化事件,马西替坦的研究未报道临床恶化率,波生坦与西他生坦的比较差异无统计学意义(表3)。
在异质性方面,波生坦与安慰剂以及安贝生坦和安慰剂在临床恶化率方面的比较I2大于50%,其余研究异质性都为轻度或无异质性(表2和表3)。
2.5 网状Meta分析 在疗效方面,安贝生坦和波生坦的6分钟步行距离高于安慰剂,西他生坦及马西替坦与安慰剂比较以及各种药物的互相比较差异均无统计学意义(表4)。等级排名中,安贝生坦效果最佳,其次为波生坦、西他生坦,马西替坦疗效最差(图3)。
在耐受性方面,安贝生坦与西他生坦的耐受性优于安慰剂,其余药物与安慰剂比较及各类药物之间的比较差异均无统计学意义(表4)。等级概率图显示:耐受性最好的药物为安贝生坦,其余依次为西他生坦、马西替坦,最差为波生坦(图4)。

图2 网状关系图
在病死率方面,4种药物之间以及与安慰剂的比较差异均无统计学意义(表5)。等级概率图方面,安贝生坦效果最好,其次依次为马西替坦、波生坦,最差为西他生坦(图5)。
在临床恶化率方面,西他生坦与波生坦的疗效均优于安慰剂,安贝生坦及马西替坦与安慰剂的比较及4种药物间的比较差异无统计学意义(表5)。等级概率图中可看出:西他生坦效果最佳,其次为波生坦,最差为安贝生坦(图6)。
节点分裂值分析,在所有评价的四项结局指标中,P值均大于0.05,反映直接比较与间接比较的结果无明显不一致性。为客观反映各干预措施的疗效与安全性,以网络Meta分析结果为主。
3 讨论
在肺动脉高压患者中,内皮素被过度表达[26],且血浆中过高的内皮素浓度与患者的不良预后关系密切[27],此外,过量的内皮素还可导致肺血管的重建[28-30],而内皮素受体拮抗剂可有效改善患者的症状并具有较好的安全性[8]。
本研究探讨了包括4种药物在内的内皮素受体拮抗剂治疗肺动脉高压的疗效及耐受性并给出不同药物的治疗等级排名。在疗效上,6分钟步行试验已被证实是有效的终点替代指标[31],是目前RCT和Meta分析中常用的主要结局指标[1]。直接Meta中,四种药物均优于安慰剂,在网状Meta分析中,安贝生坦疗效最佳,其次为波生坦、西他生坦和马西替坦。本结论与2009年指南一致,该指南中将安贝生坦与波生坦都推荐为WHO/NYHA功能分级2/3级患者的ⅠA类证据[1,32]。
各种原因导致的试验终止率(All-cause discontinuation)被广泛使用于衡量药物治疗的耐受性[33,34]。之前的Meta分析中[7,8],尚未对治疗肺动脉高压药物的耐受性进行研究,本研究综合所有内皮素受体拮抗剂治疗肺动脉高压的RCT,在直接Meta分析中,只有安贝生坦优于安慰剂,在网状Meta分析中,安贝生坦具有最佳的耐受性,其次为西他生坦、马西替坦和波生坦。
肺动脉高压作为一类预后极差的疾病,病死率已被推荐为肺动脉高压药物治疗的重要终点结局指标。本研究中,直接Meta分析显示各种药物与安慰剂比较差异均无统计学意义,网状Meta分析结果与直接Meta分析结果一致,进一步证实肺动脉高压是一类威胁患者生命的严重疾病。等级概率图显示安贝生坦在降低患者病死率方面效果最好,其次依次为马西替坦、波生坦,最差为西他生坦。马西替坦是一种由波生坦改造的新型内皮素受体拮抗剂,在短期疗效观察中,本研究结果显示马西替坦并不能有效降低肺动脉高压患者的病死率,但在长期疗效观察中,SERAPHIN[21]研究显示马西替坦能显著降低患者的病死率。
临床恶化率是综合了住院、心血管问题、WHO/NYHA肺动脉高压分级恶化等多种不良事件的复合结局指标,被认为是衡量新药治疗肺动脉高压有效性和安全性的结局指标[7]。本研究的直接与网状Meta分析的结果显示不一致。在直接比较中,3种药物的临床恶化率均优于安慰剂,且安贝生坦效果最佳,但在网状Meta分析中,只有西他生坦和波生坦的效果优于安慰剂,且等级概率图显示安贝生坦临床恶化率最高,效果最差。可能原因是安贝生坦的研究数量较少且纳入样本量较小造成。
安贝生坦是一类非磺胺类的内皮素A受体拮抗剂,已被相关研究证实可有效降低肺动脉高压[17]。本网状Meta分析结果显示效果最佳的药物同时也具有最好的耐受性,此前有关药物治疗其他疾病的网状Meta分析也得出了同样的结论[33,34]。在药物治疗的费用方面,安贝生坦、波生坦每年的治疗费用都在5万元以上,西他生坦和波生坦的治疗费用暂无详细报道,由于内皮素受体拮抗剂费用较为昂贵,且无相关的药物经济学评价,我们并不能得出确切的结论。
本研究是首个内皮素受体拮抗剂治疗肺动脉高压的网状Meta分析,检索了国内外主要医学类数据库、相关专业杂志、临床试验注册平台、会议论文集及相关网站,全面收集并评价了4种内皮素受体拮抗剂的RCT并给出了不同结局指标的等级排名。但本研究仍存在以下局限性:①纳入研究的方法学质量不足,纳入的13个RCT均提及随机,但只有6个RCT具体描述了随机方法,4个RCT提及分配隐藏,此外,多项研究由药物公司资助,存在潜在的利益冲突;②由于纳入研究的治疗周期较短,且多数研究未进行长期随访,并不能明确内皮素受体拮抗剂治疗肺动脉高压的长期疗效;③由于纳入的各个研究报道的结局指标不同,且许多研究并未报道相关的重要结局指标(如WHO/NYHA功能分级),并不能全面评价所有的药物治疗肺动脉高压的相关结局指标。

表1 纳入文献基本特征

表2 疗效与耐受性的直接Meta分析结果
综上,在治疗肺动脉高压的4种内皮素受体拮抗剂中,安贝生坦在疗效和耐受性方面均优于其他3种药物,但在病死率和临床恶化率方面优势并不明显。在未来的研究中,应该更多关注安贝生坦及其他药物在病死率和临床恶化率方面的效果,此外,应注重探讨不同药物剂量、不同类型肺动脉高压患者的具体疗效。
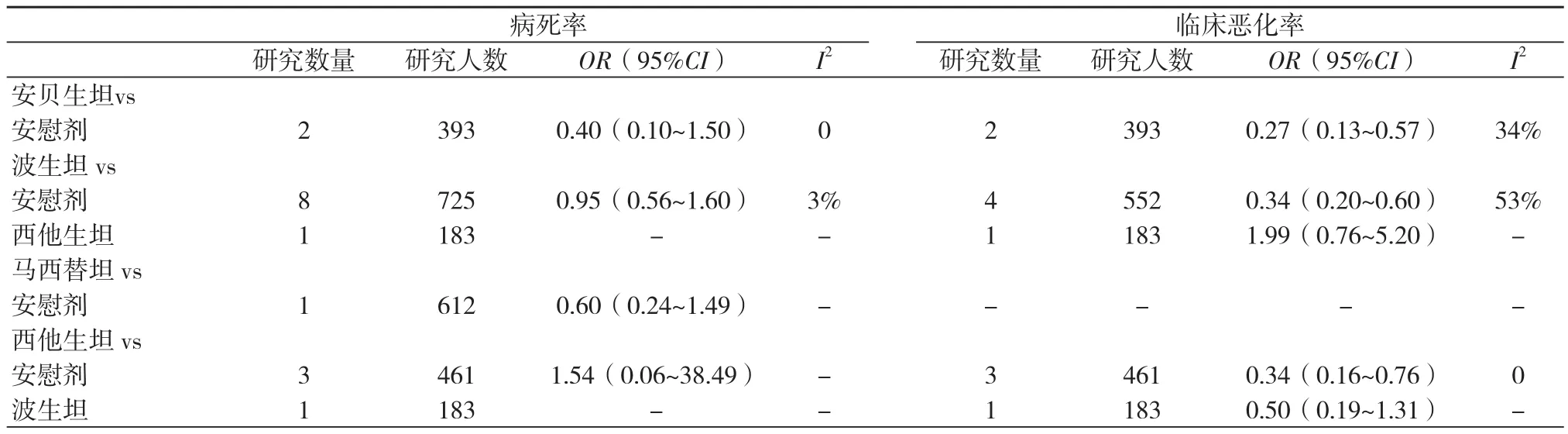
表3 病死率与临床恶化率的直接Meta分析结果

表4 疗效与耐受性的网状Meta分析结果
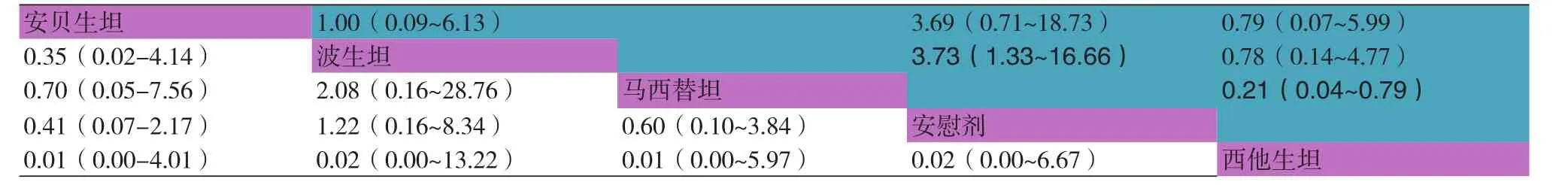
表5 病死率与临床恶化率的网状Meta分析结果
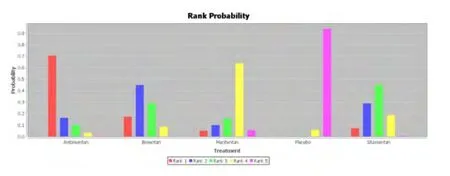
图3 疗效的等级概率图

图4 耐受性的等级概率图

图5 病死率的等级概率图

图6 临床恶化率的等级概率图
[1] McLaughlin VV,Archer SL,Badesch DB,et al. Accf/aha 2009 expert consensus document on pulmonary hypertension: A report of the american college of cardiology foundation task force on expert consensus documents and the american heart association: Developed in collaboration with the american college of chest physicians,american thoracic society, inc., and the pulmonary hypertension association[J]. Circulation,2009,119(16):2250-94.
[2] Farber HW,Loscalzo J. Pulmonary arterial hypertension[J]. N Engl J Med,2004,351(16):1655-65.
[3] Humbert M,Morrell NW,Archer SL,et al. Cellular and molecular pathobiology of pulmonary arterial hypertension[J]. J Am Coll Cardiol,2004,43(12 Suppl S):13S-24S.
[4] Humbert M,Sitbon O,Chaouat A,et al. Pulmonary arterial hypertension in france: Results from a national registry [J]. Am J Respir Crit Care Med,2006,173(9):1023-30.
[5] D'Alonzo GE,Barst RJ,Ayres SM,et al. Survival in patients with primary pulmonary hypertension[J]. Results from a national prospective registry[J]. Ann Intern Med,1991,115(5):343-9.
[6] Thenappan T,Shah SJ,Rich S,et al. A USA-based registry for pulmonary arterial hypertension:1982-2006[J]. Eur Respir J,2007,30(6):1103-10.
[7] He B,Zhang F,Li X,et al. Meta-analysis of randomized controlled trials on treatment of pulmonary arterial hypertension. Circ J,2010,74(7):1458-64.
[8] Liu C,Chen J,Gao Y,et al. Endothelin receptor antagonists for pulmonary arterial hypertension. The Cochrane database of systematic reviews,2013,2:CD004434.
[9] 曾宪涛,曹世义,孙凤,田国祥. Meta分析系列之六:间接比较及网状分析[J]. 中国循证心血管医学杂志,2012,4(5):399-402.
[10] Higgins JPT AD,Sterne, JAC (editors). Chapter 8: Assessing risk of bias in included studies. In: Higgins jpt, green s (editors). Cochrane handbook for systematic reviews of interventions. Version 5.1.0[updated march 2011]. The Cochrane Collaboration, 2011. Available from www.cochrane-handbook.org. 2011.
[11] 胡荣明,张超,曾宪涛. 应用GeMTC软件实现网状Meta分析[J]. 湖北医药学院学报, 2014, 33(1):36-40.
[12] 张超,徐畅,曾宪涛. 网状Meta分析中网状关系图的绘制[J]. 中国循证医学杂志,2013,13(11):1382-6.
[13] 张超,鄢金柱,孙凤,等. 网状Meta分析一致性的鉴别与处理方法[J]. 中国循证医学杂志,2014,14(7): 884-8.
[14] Badesch DB,Bodin F,Channick RN,et al. Complete results of the first randomized, placebo-controlled study of bosentan, a dual endothelin receptor antagonist, in pulmonary arterial hypertension [J]. Current Therapeutic Research, Clinical & Experimental,2002:227-46.
[15] Barst RJ,Langleben D,Badesch D,et al. Treatment of pulmonary arterial hypertension with the selective endothelin-a receptor antagonist sitaxsentan [J]. J Am Coll Cardiol,2006,47(10):2049-56.
[16] Barst RJ,Langleben D,Frost A,et al. Sitaxsentan therapy for pulmonary arterial hypertension[J]. Am J Respir Crit Care Med,2004,15,169(4):441-7.
[17] Barst RJ,Mubarak KK,Machado RF,et al. Exercise capacity and haemodynamics in patients with sickle cell disease with pulmonary hypertension treated with bosentan: Results of the asset studies [J].Br J Haematol,2010,149(3):426-35.
[18] Galie N,Beghetti M,Gatzoulis MA,et al. Bosentan therapy in patients with eisenmenger syndrome: A multicenter, double-blind,randomized, placebo-controlled study[J]. Circulation,2006,114(1):48-54.
[19] Galiè N,Olschewski H,Oudiz RJ,et al. Ambrisentan for the treatment of pulmonary arterial hypertension: Results of the ambrisentan in pulmonary arterial hypertension, randomized, double-blind, placebocontrolled, multicenter, efficacy (aries) study 1 and 2[J]. Circulation,2008,117(23):3010-9.
[20] Galiè N,Rubin L,Hoeper M,et al. Treatment of patients with mildly symptomatic pulmonary arterial hypertension with bosentan (early study): A double-blind, randomised controlled trial[J]. Lancet,2008,371(9630):2093-100.
[21] Pulido T,Adzerikho I,Channick RN,et al. Macitentan and morbidity and mortality in pulmonary arterial hypertension [J]. N Engl J Med,2013,29,369(9):809-18.
[22] Rubin LJ,Badesch DB,Barst RJ,et al. Bosentan therapy for pulmonary arterial hypertension [J]. N Engl J Med,2002,21,346(12):896-903.
[23] Sandoval J,Torbicki A,Souza R,et al. Safety and efficacy of sitaxsentan 50 and 100 mg in patients with pulmonary arterial hypertension [J].Pulm Pharmacol Ther,2012,25(1):33-9.
[24] 鲁一兵,李小婷,景舒南,等. 波生坦治疗先天性体-肺分流性心脏病患者肺动脉高压效果观察[J]. 昆明医学院学报,2010,31(8):93-5.
[25] 肖仁杰. 波生坦治疗特发性肺动脉高压的临床疗效[J]. 国际医药卫生导报,2012,18(9):1246-7.
[26] Giaid A,Yanagisawa M,Langleben D,et al. Expression of endothelin-1 in the lungs of patients with pulmonary hypertension [J]. N Engl J Med,1993,328(24):1732-9.
[27] Rubens C,Ewert R,Halank M,et al. Big endothelin-1 and endothelin-1 plasma levels are correlated with the severity of primary pulmonary hypertension[J]. Chest,2001,120(5):1562-9.
[28] Kim H,Yung GL,Marsh JJ,et al. Pulmonary vascular remodeling distal to pulmonary artery ligation is accompanied by upregulation of endothelin receptors and nitric oxide synthase[J]. Exp Lung Res,2000,26(4):287-301.
[29] Mansoor AM,Honda M,Saida K,et al. Endothelin induced collagen remodeling in experimental pulmonary hypertension[J]. Biochem Biophys Res Commun,1995,24,215(3):981-6.
[30] Wort SJ,Woods M,Warner TD,et al. Endogenously released endothelin-1 from human pulmonary artery smooth muscle promotes cellular proliferation: Relevance to pathogenesis of pulmonary hypertension and vascular remodeling [J]. Am J Respir Cell Mol Biol,2001,25(1):104-10.
[31] Gabler NB,French B,Strom BL,et al. Validation of 6-minute walk distance as a surrogate end point in pulmonary arterial hypertension trials [J]. Circulation,2012,126(3):349-56.
[32] Nakanishi N. 2009 esc/ers pulmonary hypertension guidelines and connective tissue disease [J]. Allergol Int,2011,60(4):419-24.
[33] Cipriani A,Barbui C,Salanti G,et al. Comparative efficacy and acceptability of antimanic drugs in acute mania: A multipletreatments meta-analysis[J]. Lancet,2011,378(9799):1306-15.
[34] Cipriani A,Furukawa TA,Salanti G,et al. Comparative efficacy and acceptability of 12 new-generation antidepressants: A multipletreatments meta-analysis[J]. Lancet,2009,373(9665):746-58.
