不同重金属离子对C-S-H 凝胶影响及其固化稳定性
2014-11-28颜碧兰
汪 澜,颜碧兰,王 昕,刘 晨,刘 晶
(中国建筑材料科学研究总院 绿色建筑材料国家重点实验室,北京 100024)
随着城市和工业固体废弃物的排放与日俱增,重金属元素(Pb,Cr,Cu,Zn,As,Cd等)的吸附固化已为世界各国所关注.水化硅酸钙凝胶(简称C-SH 凝胶)是硅酸盐水泥最主要的水化产物,具有极高比表面能和离子交换能力,可通过物理吸附、共生和层间化学置换控制多种金属阳离子移动[1].研究表明,C-S-H 凝胶可通过共沉淀方式或以离子交换方式实现对Cd2+的捕集[2];Ni2+可在C-S-H 凝胶结构内层表面反应形成复合物[3];Nd2+在1d内即可在CS-H 内层表面形成复合物,且Nd—Ca键和Nd—Si键的结合间距随时间延长而增大[1];Pb2+可在水泥颗粒表面形成沉淀,阻止水泥进一步水化,故很难对Pb2+进行有效固化[4-5];但是,也有研究者认为Pb2+可与C-S-H 凝胶形成稳定化合物,改变C-S-H的密度及其纳米结构,增强水泥28d抗压强度[6-7].
C-S-H 凝胶对重金属阳离子的俘获能力及固化稳定性也存在差异,然而在此方面的研究较少.本文现通过溶液法人工合成C-S-H 凝胶,就不同种类、不同价态重金属阳离子对C-S-H 凝胶影响进行了系统研究,同时对重金属离子在C-S-H 凝胶中固化稳定性差异进行了分析比较.
1 试验材料与方法
1.1 试验材料
硅质原料 Na2SiO3·9H2O 和 钙质原料Ca(NO3)2·4H2O,均为分析纯试剂;重金属盐试剂Cr(NO3)3·9H2O,K2Cr2O7·12H2O,Pb(NO3)2,Cu(NO3)2·3H2O,Zn(NO3)2·6H2O,Cd(NO3)2·4H2O,均为化学纯试剂;去离子水,其电导率在0.01μs/cm 以下,使用前沸煮30 min 去除溶解性CO2.
1.2 样品制备
1.2.1 纯C-S-H 凝胶的合成
本文通过溶液法化学合成了钙硅比n(Ca)/n(Si)为0.8,1.8的2种C-S-H 凝胶.具体方法是:称取一定量Na2SiO3·9H2O 溶于去离子水中,分别按一定钙硅比加入适量Ca(NO3)2·4H2O,水固比(质量比)为10∶1,并加入适量NaOH 控制溶液pH 值为13.0,将混合物充分搅拌后在60℃下养护7d,抽滤后用去离子水冲洗去除未反应的Na+,NO-3,并在真空干燥箱中烘干,得到纯C-S-H 凝胶样品.
1.2.2 掺杂不同重金属离子的C-S-H 凝胶合成
分别称取5种重金属盐试剂溶于去离子水中,然后将其分别滴入配制好的硅酸钠与硝酸钙混合溶液中,水固比为10∶1,并加入适量NaOH 控制溶液pH 值为13.0,混合物充分搅拌后在60 ℃下养护7d,并按上述方法制成含不同重金属元素的C-S-H凝胶样品.重金属离子掺量分别为硅酸钠与硝酸钙混合物溶质总质量的2%,4%.
1.3 试验方法
用D/MAX-ⅢA 型X 射线衍射仪对样品结构分析,扫描角度5°~60°,扫描速度2(°)/min.用S4800冷场发射扫描电子显微镜观测样品微观形貌,电流为75mA,电压为15kV;用EMJ 2100型透射电镜观测样品纳米级微观形态.用ESCALAB 250Xi型X 射线光电子能谱仪对样品结构变化进分析,单色化AlKα和Mg/Al双阳极光源,最佳能量分辨率≤0.45eV,灵敏度(Ag 3d5/2能量分辨率≤0.50eV)≥400 000 次/s,分析室真空度为2.9×10-7Pa,测射速率约为4nm/min.利用PLASMA SPEC-1 型电感耦合等离子发射光谱仪对C-S-H 凝胶样品不同龄期浸出液中重金属离子浸出量进行检测.
2 结果与分析
2.1 重金属离子对C-S-H 凝胶的影响
2.1.1 离子种类对C-S-H 凝胶的影响
图1为掺杂不同重金属离子前后不同钙硅比C-S-H 凝胶的XRD 图谱.
由XRD 图谱可见,水化液相中Cr3+,Pb2+,Cu2+,Zn2+,Cd2+等单独存在对不同钙硅比C-S-H凝胶的影响程度并不相同.对于低钙硅比(n(Ca)/n(Si)=0.8)C-S-H 凝胶,水化液相中存在重金属离子时,C-S-H 凝胶衍射主峰(d=0.302 8nm)宽度有所增大,结晶程度变差,且Zn2+,Cr3+,Cu2+的影响较明显.尤其是水化液相中存在Cu2+时,C-S-H 凝胶衍射峰位置(2θ=29.5°)会发生一定偏移δ(见图1(a)).这可能是Zn2+,Cr3+挤入C-S-H 凝胶硅酸盐结构夹层间隙,使C-S-H 结晶度降低,衍射峰变得更为弥散;而Cu2+挤入夹层间隙的数量相对较多,从而使C-S-H 凝胶衍射峰位置发生偏移.
对于高钙硅比(n(Ca)/n(Si)=1.8)C-S-H 凝胶,水化液相中Cr3+,Cu2+,Zn2+等单独存在时,C-S-H凝胶衍谢谱图中出现了较明显的Ca(OH)2特征峰(d=0.262 7nm,2θ=34°)(见图1(b)).这可能是由于高钙硅比C-S-H 凝胶中的硅氧四面体结构被Ca2+分割为短链,使Zn2+,Cu2+,Cd2+较容易取代Ca2+形成相对稳定的化合物,如Ca[Zn(OH)3H2O]3等[8-9],而水化液相中Ca2+的溶出又促进了Ca(OH)2高过饱和度的形成以及晶体成核生长,因此随着Ca2+被取代数量的增加,Ca(OH)2晶体含量及结晶程度有所提高.
2.1.2 离子价态对C-S-H 凝胶的影响
图2为Cr3+,Cr6+对C-S-H 凝胶的影响.
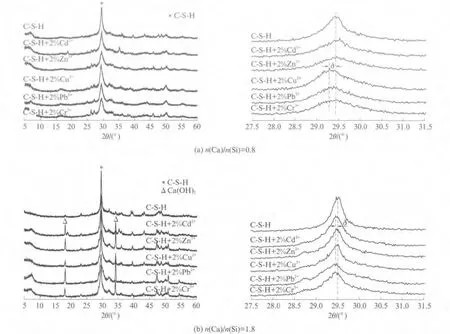
图1 掺杂不同重金属离子C-S-H 凝胶的XRD 图谱Fig.1 XRD of C-S-H gel with different heavy metal ions added
由图2 可见,Cr3+,Cr6+对C-S-H 凝胶的影响并不相同.当水化液相中存在Cr3+时,低钙硅比C-S-H凝胶的XRD 衍射主峰(d=0.302 8nm)宽度有所增大,结晶度有所降低;高钙硅比C-S-H 凝胶的XRD 衍射谱图中出现了较明显的Ca(OH)2特征峰,C-S-H 凝胶衍射主峰位置也发生了一定偏移.与前者相反,当水化液相中存在Cr6+时,无论低钙硅比还是高钙硅比,C-S-H 凝胶的XRD 衍射峰均未出现明显变化,也没有较明显的Ca(OH)2特征峰出现.由此可见,Cr3+对C-S-H 凝胶结构有一定影响,而Cr6+影响不大.
2.2 重金属离子对C-S-H 凝胶中Si,Ca原子芯层电子结合能的影响
由以上分析可以看出,重金属离子种类及其价态不同,对钙硅比不同的C-S-H 凝胶的影响程度不同.图3为掺杂不同重金属离子前后高钙硅比C-SH 凝胶的XPS图谱.
由图3可见,掺杂重金属离子后,C-S-H 凝胶中的Si2p,Ca2p电子结合能均发生了变化,且重金属离子种类不同,对电子结合能的影响存在一定差异.其中纯C-S-H 凝胶Si2p的结合能为101.0eV,掺杂Cr3+或Pb2+后,Si2p的结合能增至101.6eV,且谱峰明显变宽,链层中的Si—O 结合方式可能发生了一些变化;掺杂Zn2+后,Si2p的结合能变化不明显;而掺杂Cu2+后,Si2p的结合能虽变化不大,但其谱峰强度明显减弱.
在纯C-S-H 凝胶中,Ca2p的谱峰结合能分别为346.7,350.2eV.掺杂Cr3+或Pb2+后,C-S-H 凝胶中Ca2p的结合能也有较大变化,分别增至347.9,351.4eV;掺杂Zn2+后,Ca2p的结合能也有所增大,但不如前者显著;而掺杂Cu2+后,Ca2p的结合能反而有所降低,且其谱峰强度也明显减弱.由此可见,不同种类重金属离子在C-S-H 凝胶中的固化机制存在差异,其中Cr3+或Pb2+对链层结构的影响较为相近,Si2p,Ca2p的结合能均有较大增强;Cu2+的作用则相反.
此外,重金属离子价态不同,其对高钙硅比C-S-H凝胶硅氧四面体链层结构的影响也不同,如图4所示.由图4可见,C-S-H 凝胶中掺杂Cr6+后,Si2p,Ca2p的结合能均未明显变化,与Cr3+存在较大差别.
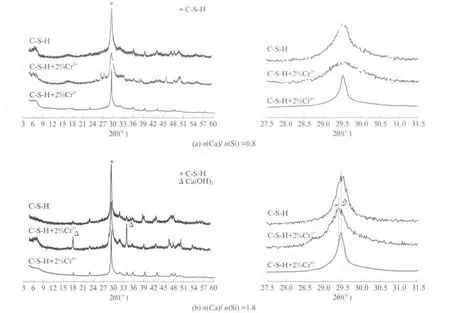
图2 Cr3+,Cr6+对C-S-H 凝胶的影响Fig.2 XRD of C-S-H gels to fix heavy metal ions with different valence states
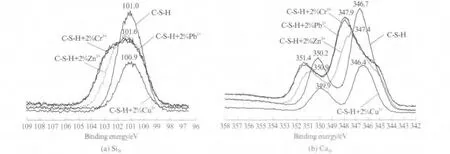
图3 掺杂重金属离子前后C-S-H 凝胶(钙硅比为1.8)的XPS图Fig.3 XPS of C-S-H gel(n(Ca)/n(Si)=1.8)before and after heavy metal ions added
综合以上可以看出,由于不同重金属离子在C-S-H凝胶中的结合方式存在差异,引起了硅氧四面体中Si2p,Ca2p结合能的变化波动,其中Cr3+或Pb2+在硅氧四面体链层结构中的原子结合方式较相近,Si2p,Ca2p的结合能均增大,Zn2+次之,而Cu2+对Si2p,Ca2p结合能的影响则与前者相反,且谱峰强度明显减弱.
3 形貌分析
在水化液相中存在重金属离子时,C-S-H 凝胶的早期水化形貌存在一定差异,如图5所示.由图5可见,未掺杂重金属离子的低钙硅比C-S-H 凝胶水化早期或为细小箔状薄片,或为板块状团聚;掺杂Zn2+,Cu2+,Cd2+,Cr3+后,其形貌发生了不同程度变化.掺杂Cd2+后,C-S-H(Ⅰ)凝胶水化早期形态除呈箔薄片状外,还有大量树叶状水化产物存在.

图4 掺杂Cr3+,Cr6+前后C-S-H 凝胶的XPS图Fig.4 XPS patterns of C-S-H gel before and after Cr3+and Cr6+added

图5 掺杂不同重金属离子前后C-S-H 凝胶水化7d的形貌比较Fig.5 Morphology of C-S-H with different n(Ca)/n(Si)before and after adding heavy metal ions with different valence states at 7d
高钙硅比C-S-H(Ⅱ)凝胶水化早期呈相互交织的凝胶网状结构,掺杂Zn2+后,多呈细小绒球状,这可能是由于Zn2+对C-S-H 凝胶形成具有一定延缓作用所致;而水化液相中存在Cu2+,Cd2+时,C-S-H凝胶形成量较前者多,且呈块状团聚.
图6为高钙硅比C-S-H(Ⅱ)凝胶掺杂Pb2+,Cd2+,Cu2+前后的微观形态比较.
由图6可见,纯C-S-H(Ⅱ)凝胶的纤维颗粒排列紧密,粒子分布均匀,相互交错层叠在一起;而掺杂重金属离子后,C-S-H 凝胶结构则出现了不同程度的变化.掺杂Pb2+后,C-S-H(Ⅱ)凝胶的纤维颗粒排列不均匀,粒子分布出现等粒径点状团聚;掺杂Cu2+后,C-S-H 凝胶的纤维颗粒团聚分布更加不均匀;掺杂Cd2+后,C-S-H(Ⅱ)凝胶的纤维颗粒分布也较不均匀,但其影响程度不如Cu2+明显.可 以 看 出,高 钙 硅 比C-S-H(Ⅱ)凝 胶 中Pb2+,Cd2+,Cu2+的掺入,使其硅氧四面体链层结构排列变得更加无规则,且重金属离子种类不同,其对CS-H(Ⅱ)凝胶的影响程度也不同,其中Pb2+的影响程度较小.
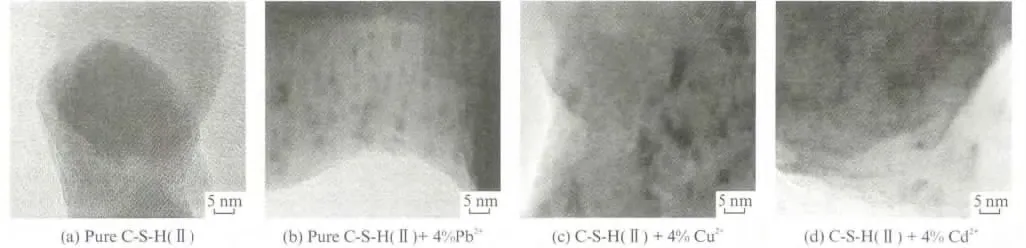
图6 高钙硅比C-S-H 凝胶掺杂重金属离子前后微观形态比较Fig.6 Morphology of C-S-H gel(n(Ca)/n(Si)=1.8)before and after heavy metal ions added
4 C-S-H 凝胶对不同重金属离子的固化稳定性
表1为C-S-H 凝胶对不同重金属离子固化稳定性比较.
由表1可见,无论钙硅比还是重金属掺量大小,C-S-H 凝胶水化早期(7d)对水化液相中的Cr3+,Cu2+,Zn2+均有较强固化能力,固化率(质量分数)在90%以上,但对Cr6+的俘获能力较弱(固化率仅50%~60%);水化后期(60 ℃条件下加速水化至28d),C-S-H 凝胶对各重金属离子的固化能力有所增强,但对Cr6+的固化能力变化不大.

表1 C-S-H凝胶对不同重金属离子固化稳定性比较Table 1 Comparison of ability of C-S-H gel to fix different heavy metal ions
C-S-H 凝胶对不同重金属离子俘获及其稳定性不同,可能是由于低钙硅比C-S-H(Ⅰ)凝胶结构类属-1.4nm Tobermorite(雪硅钙石)[10],其中的硅氧四面体以Q2形式存在,且每层硅氧四面体是两两相连的直链结构,层与层之间通过Ca相连接形成多层结构.低钙硅比C-S-H 结构中Ca结合能较高,降低了钙在化合物中的协调性[11],且C-S-H(Ⅰ)凝胶硅氧四面体链层结构中各直链间的桥氧四面体间距较小(仅0.56nm)[10],当水化液相中Cr3+,Pb2+,Cu2+,Zn2+共存时,少量电负性和离子半径较小的金属阳离子可挤入C-S-H(Ⅰ)凝胶的夹层空隙,而多数金属离子则吸附于C-S-H 凝胶表面,故C-S-H(Ⅰ)凝胶对重金属离子的固化稳定性相对较低.
高钙硅比C-S-H(Ⅱ)凝胶结构以类Jennite(羟基硅钙石)为主[11],类似于组群状硅酸盐结构,OH基团和Ca—O 键与低钙硅比C-S-H 不同,其硅氧四面体以Q1结构为主(约占质量分数的50%).由于钙硅比增大,使C-S-H 凝胶硅氧四面体的聚合度和桥氧数降低,硅氧四面体链逐渐变短[12],且桥氧四面体间距(1.00nm)较C-S-H(Ⅰ)大,故金属阳离子很容易挤入链层结构空间,与Ca发生离子置换反应形成稳定化合物;另外,C-S-H(Ⅱ)凝胶硅氧四面体的剩余负电荷也较C-S-H(Ⅰ)高,有利于金属阳离子吸附与稳定固化.因此,C-S-H(Ⅱ)凝胶对重金属离子的稳定固化能力较C-S-H(Ⅰ)高.
同时,由于Cr3+,Pb2+,Cu2+的离子半径、电负性存在差异及其在水化液相中交换作用影响,导致C-S-H 凝胶对水化液相中多种重金属离子固化稳定性与单一金属离子存在较大差异,尤其是对离子半径较大、活性较差的Pb2+稳定固化能力差异较明显.
5 结论
(1)C-S-H 凝胶对重金属离子有较强的固化作用,但由于重金属离子种类和价态不同,C-S-H 凝胶对其固化存在较大差异.其中C-S-H 凝胶对Cu2+,Cd2+,Cr3+,Zn2+的固化能力较强,对Cr6+的固化能力和稳定性较差.
(2)钙硅比不同,C-S-H 凝胶对重金属离子固化稳定性及固化机制均存在一定差异.
(3)Cu2+,Cd2+,Cr3+,Zn2+对C-S-H 凝胶形态和结构均有不同程度影响,且钙硅比不同,其影响程度不同.
(4)C-S-H 凝胶对多种重金属离子的固化稳定性与单一重金属离子存在较大差异.
(5)C-S-H 凝胶对价态不同的Cr离子固化能力及其稳定性有较大差异,且水化液相中Cr6+的存在,还会使C-S-H 凝胶对Pb2+的固化及稳定性产生巨大影响.
[1]MANDALIEV P,DÄHN R,TITS J,et al.EXAFS study of Nd(Ⅲ)uptake by amorphous calcium silicate hydrates(C-SH)[J].Journal of Colloid and Interface Science,2010,34(1):1-7.
[2]POMIÈS M P,LEQUEUX N,BOCH P.Speciation of cadmi-um in cement(PartⅠ):Cd2+uptake by C-S-H[J].Cement and Concrete Research,2001,31(4):563-569.
[3]VESPA M,WIELAND E,DAHN R,et al.Determination of the elemental distribution and chemical speciation in highly heterogeneous cementitious materials using synehrotron based micro-spectroseopic techniques[J].Cement and Concrete Researeh,2007,37(11):1473-1482.
[4]IVEY D B,HEINMANN R B,NEUWIRTH M,et al.Electron microscopy of heavy metalin cement materials[J].Journal Material Science Letters,1990,98(5):5055-5062.
[5]HERRERA J E,TITTLEBAUM M,CARTLEDGE F,et al.Evaluation of the leaching properties of solidified heavy metal wastes[J].Journal of Environmental Science and Health,1992,27(4):983-998.
[6]THEVENIN G,PERA J.Interaction between lead and different binders[J].Cement and Concrete Research,1999,29(10):1605-1610.
[7]GINEYS N.Managing trace elements in Portland cement(PartⅠ):Interactions between cement paste and heavy metals added during mixing as soluble salts[J].Cement and Concrete Composites,2010,32(8):563-570.
[8]KAKALI G,TSIVILIS S,TSIALTAS A.Hydration of ordinary cement made from raw mixcontaining transition element osides[J].Cement and Concrete Research,1998,28(2):335-340.
[9]STUMM A,GARBEV K,BEUCHLE G,et al.Incorporation of zinc into calcium silicate hydrates(PartⅠ):Formation of C-S-H(Ⅰ)with C/S=2/3and its isochemical counterpart gyrolite[J].Cement and Concrete Research,2005,35(9):1665-1675.
[10]TAYLOR H F W.Cement chemistry[M].London:Academic Press:1990,142-152.
[11]BLACKA L,GARBEVA K,STEMMERMANNA P,et al.Characterisation of crystalline C-S-H phases by X-ray photoelectron spect roscopy[J].Cement and Concrete Research,2003,33(6):899-911.
[12]KWAN S,LAROSA-THOMPSON J,GRUTZECK M W.Structure and phase relations of aluminum-substituted calcium silicate hydrate[J].J Am Ceram Soc,1996,79(4):967-971.
