两种方法建立兔VX2肝癌模型的比较及影像学评估
2014-11-01陈茂振尹化斌
钱 亭, 陈茂振, 高 峰, 尹化斌
VX2肝癌模型已广泛应用于介入治疗的实验研究,其造模方法有多种,常用的有开腹包埋及穿刺种植两种[1]。本实验对两种建模方法进行比较,筛选简单、有效的模型制作方法,并探讨其影像学表现。
1 材料与方法
1.1 实验动物及分组
新西兰白兔40只,雌雄不限,体重2.0~3.0 kg,购自上海国睿生命科技有限公司。荷瘤兔由上海市第九人民医院提供。将动物随机分成A、B两组,每组20只。A组采用开腹包埋植入VX2瘤块,B组采用CT引导下穿刺种植VX2瘤块。
1.2 VX2瘤株的制备
采用盐酸氯胺酮 (福建古田药业有限公司)∶陆眠宁Ⅱ(1.5 ml∶30 mg,吉林省华牧动物保健品有限公司)1∶1混合液(0.2~0.3 ml/kg)肌肉注射麻醉荷瘤兔,常规备皮、消毒、铺洞巾,于兔后肢外侧逐层分离至肌肉,完整剥离出肿瘤组织,放入盛有少量生理盐水的换药碗中。用生理盐水冲洗瘤块3~4次,剪去多余的筋膜、肌肉组织及瘤块内坏死组织,随后放入另一无菌换药碗内,倒入少量生理盐水,将瘤块剪成1~2 mm3小块备用。
1.3 兔VX2肝癌模型的建立
VX2肝癌模型制备前,所有实验兔禁食12 h,盐酸氯胺酮:陆眠宁Ⅱ1∶1混合液 (0.2~0.3 ml/kg)肌肉注射麻醉。
1.3.1 开腹包埋植入VX2瘤块 A组兔取仰卧位,四肢固定于手术台上。上腹部常规备皮、消毒、铺巾,于剑突下偏左2 cm处沿肋间隙开腹2~3 cm,暴露肝左叶,在较厚处用穿刺针尖沿肝门方向插入肝实质内做成深约1 cm切口,取2块组织块植入,压迫止血,确认无活动性出血后逐层缝合。术后肌内注射青霉素40万u,连续3 d。
1.3.2 CT引导下穿刺种植VX2瘤块 B组兔仰卧位固定于CT检查床上(自制相关简易工具),根据CT平扫确定进针位置及深度,明确接种位置 (均选用肝左叶)。接种时,用细针尖(5 ml注射器针尖折断制成)在皮肤上定位,再用18 G穿刺针(NIPRO)经皮肋间穿刺至肝左外叶,深度约10 mm,拔出针芯,注意有无出血,用眼科剪夹取2块瘤组织塞入鞘内,再用穿刺针将瘤块推入肝实质内,需多次重复推注针芯,确定所取瘤块均接种于肝左叶,见图1。

图1 CT引导下经皮穿刺瘤块植入
1.4 影像学检查
1.4.1 CT检查 两组实验兔均于术后2周行16排螺旋 CT 检查(LightSpeed,GE),扫描前禁食 12 h,全麻后将实验兔固定于自制检查板上。仰卧位,头先进。平扫的扫描参数为:120 kV,200 mA,FOV 20,Pitch 1.375,层厚 5 mm,1.25 薄层重建;增强扫描:采用耳缘静脉高压团注方式,对比剂为碘佛醇注射液(加拿大),剂量为2 ml/kg,注入速度为1 ml/s,分别于注入对比剂后12、25、50及150 s时行动脉早期、动脉晚期、门脉期及延迟期扫描。
1.4.2 DSA血管造影 实验兔全麻,备皮,仰卧位固定,腹股沟区常规消毒、铺巾,触摸右侧股动脉搏动最强处,经右侧腹股沟下方沿股动脉搏动处做与股动脉走行一致的长约4 cm的手术切口,分离和暴露股动脉约2 cm。在已分离的股动脉远端和近端分别放置2条3.0丝线,先把动脉远端用丝线结扎,然后提起近端丝线使两丝线间的股动脉充盈,用20 G穿刺针穿刺股动脉,利用微导丝引导微导管插管[2],在透视情况下将微导管选择性插入腹腔干,推注碘化油注射液(法国加柏公司)约1 ml造影,然后超选择性插入肝左动脉,再次推注对比剂造影,以确定微导管的位置及肿瘤血供情况。术后拔除导管,同时结扎股动脉近端,缝合包扎切口。
1.5 观察指标
记录两组实验兔种植所需时间、术后感染及死亡情况,2周后根据CT和DSA图像记录两组肝内、外成瘤情况、肿瘤体积(CT增强分别测得肿瘤的最大层面长径L,与L垂直的最宽径W,用公式:V=L × W2/2)[3],观察有无腹腔种植性转移及腹腔积液,并比较术前、术后实验兔体重变化情况。观察肿瘤在不同影像学检查中的表现。
1.6 统计学分析
应用SPSS17.0软件进行统计学分析。计量资料采用独立样本t检验,计数资料采用Fisher检验,P<0.05为差异有统计学意义。
2 结果
2.1 模型制备情况
A组中4只于术后3 d死亡,2只经CT检查均未见肝内、肝外成瘤,10只肝内成瘤,2只腹壁浸润,2只腹腔种植性转移并见腹腔积液(图2a)。B组2周内未见死亡,2只经CT检查均未见肝内、肝外成瘤,17只肝内成瘤,1只腹壁浸润(图 2b),未见腹腔种植性转移。
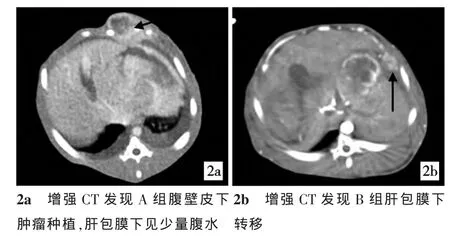
图2 增强CT所见肝外成瘤
种植操作时间A组为(32±5)min,B组为(8±2)min,组间差异有统计学意义(P<0.05)。术后实验兔体重 A组为 (2.37±0.25)kg,B组为 (2.26±0.34)kg,组间差异无统计学意义(P > 0.05)。 肝内肿瘤体积 A组为 (4 739.29±530.2)mm3,B组为(4 789 ± 626.27)mm3,组间差异无统计学意义(P >0.05)。 死亡率 A 组为 20%(4/20),B 组为 0(0/20),组间差异有统计学意义(P=0.037)。肝内成瘤率A组为 50%(10/20),B 组为 85%(17/20),组间差异有统计学意义(P=0.02)。
2.2 CT 表现
两组建模成功,实验兔在CT上均表现为局灶孤立结节,CT平扫为低密度结节影,A组平扫CT值约为(42.3 ± 5.4)Hu,B 组为(45.6 ± 3.7)Hu。 增强扫描肿瘤周边环形强化,动脉早期、动脉晚期、门脉期及延迟期扫描A组CT值分别为 (89.6±7.2)、(111.3 ± 6.4)、(108 ± 6.7)和(92.5 ± 9.3)Hu,B 组分别为(83.5 ± 4.7)、(120.7 ± 6.3)、(113.2 ± 3.7)和(93.2±5.8)Hu,肿瘤于增强动脉早期即出现强化,动脉晚期进一步强化,门脉期与肝实质强化水平一致,到延迟期对比剂部分退出,见图3。两组平扫及增强各期比较差异均无统计学意义(P>0.05)。

图3 B组各期CT增强扫描所见
2.3 血管造影表现
两组模型兔肝动脉造影均可见肿瘤供血动脉增粗,分支被肿瘤推压形成“抱球征”,肿瘤呈环形染色(图4)。两组模型兔腹腔干动脉均自T12~L1水平由腹主动脉前壁稍偏右侧发出。腹腔干造影寻找肝总动脉,可见肝总动脉向右水平发出胃十二指肠动脉,向上发出肝固有动脉。肝固有动脉发出肝左、右叶动脉。供血的肝动脉增粗,显影较浓,向肿瘤中心发出肿瘤血管,形成抱球状肿瘤染色。其中2只实验兔插管造影未成功。
3 讨论
3.1 兔VX2肝癌模型制备
VX2瘤株是由Shope病毒诱发的兔乳头状瘤衍生的鳞状细胞癌经70次传代而建立的肿瘤细胞株,具有很强的侵袭转移性[4]。接种2周后行相关检查,原因为此阶段肿瘤生长最旺盛,体积迅速增大,切面多呈实质性,转移及坏死较少。此阶段为肿瘤血管形成期,毛细血管大量形成,易实施介入手术。

图4 兔肝固有动脉动脉造影,可见肿瘤供血丰富,瘤区呈环形染色
本实验中,B组操作过程简单,操作时间明显短于A组,成瘤率高于A组,部分原因为缩短了瘤块离体的时间,减少了瘤块缺血再灌注损伤,同时降低了瘤块感染性。A组术后4只死亡,由于手术对实验动物创伤大,术中麻醉要求高,肿瘤可沿手术切口向腹腔蔓延,且实验兔术后免疫力下降,易发生腹腔种植性转移。本实验A组中有2只发生腹腔转移,而B组未见转移。实验中共有4只接种2周后未见肝内及肝外肿瘤生长,考虑与瘤块取材有关,因此取材时应尽可能选取肿瘤边缘生长旺盛的鱼肉样组织,尽量去除坏死及结缔组织,以提高接种成功率。另一方面原因可能与实验兔免疫防御机制有关。
两组实验兔术后体重及肿瘤体积未见明显差别,表明两种种植方式对实验兔的体重及肿瘤体积无显著影响。
CT引导下经皮穿刺较开腹种植简单、实用,但对操作者要求高,进针要快且不易太浅(1.0~1.5 cm),否则组织块易沿窦道流出或由于供血不足而生长缓慢。肿瘤组织块注入针芯后,需多次重复推注,确定瘤块接种于肝左叶。拔出针芯后按压穿刺点30 s,防止瘤块溢出。
3.2 CT表现
两组兔VX2肝癌模型CT表现一致,平扫上均表现为低密度。增强检查扫描4期,可使动脉血管清晰显示,利于指导血管造影检查。增强检查发现不同于人类肝细胞性肝癌“快进快出”的强化特点[5],表现为动脉早期环形强化,动脉晚期进一步强化,到延迟期部分退出。
3.3 血管造影表现及技术要点
两组实验兔血管造影均显示肿瘤供血动脉增粗,分支被肿瘤推压形成“抱球征”,肿瘤环形染色。其中,腹腔干动脉多开口于T12~L1水平,应先行腹主动脉造影明确腹腔干动脉开口,之后直接用导管头端指向腹侧稍偏右于T12~L1水平反复探寻腹腔干动脉,可缩短手术时间及减少对比剂的用量,进而减轻对实验兔肾功能的影响。行腹腔干动脉造影时,可将球管向右侧倾斜10°~15°,能较好的辨认肝固有动脉,肝固有动脉迂曲纤细,微导管在微导丝配合下可进入肝固有动脉,但如果进一步超选择肝左右动脉则较困难。如进行血管内介入治疗,导管头位于肝固有动脉,由于肿瘤供血动脉较正常肝动脉增粗且血流较快,缓慢注药可优先进入肿瘤供血动脉。因此,介入治疗时,如超选肝左动脉困难,不可强行进入,否则易引起血管痉挛、损伤,导致实验失败。实验中2只血管造影未成功,原因可能为肝固有动脉起源异常。其中1只实验兔肿瘤较小,直径约1.2 mm,供瘤血管少而细小也是实验失败的原因之一。
本实验通过比较开腹及穿刺植入瘤块法,证实开腹包埋法制作动物模型创伤大,动物死亡率高,易发生腹腔种植性转移,对手术者手术技巧要求高,同时手术切口不利于后续观察与研究。CT引导下经皮穿刺VX2瘤块植入操作简单,创伤小,成瘤率高,可重复性强,优于开腹包埋法。VX2肝癌模型血供丰富,类似人类肝转移癌模型,在肝癌介入治疗研究中将得到越来越广泛的应用。
[1] Lee KH,Liapi E,Buijs M,et al.Percutaneous US-guided implantation of VX-2 carcinoma into rabbit liver:a comparison with open surgical method[J].J Surg Res, 2009, 155: 94-99.
[2] 江雄鹰,罗荣光,黄金华,等.兔VX2肝癌模型建立与经兔股动脉微导管超选择性肝左动脉插管技术的探讨[J].介入放射学杂志,2011,20:214-217.
[3] Watanabe D, Ueo H, Inoue H, et al.Antitumor effects of intraarterial infusion of tumor necrosis factor/lipiodol emulsion on hepatic tumor in rabbits[J].Oncology, 1995, 52: 76-81.
[4] Swistel AJ, Bading JR, Raaf JH.Intraarterial versus intravenous adriamycin in the rabbit VX-2 tumor system [J].Cancer,1984,53:1397-1404.
[5] 史东宏,曹建民,许 健,等.CT引导下兔VX2肝癌模型的制作及综合评估[J].介入放射学杂志,2008,17:725-728.