基于壳聚寡糖的黄芩苷固体分散体的研究
2014-10-25翟文婷史红军
翟文婷,史红军
(南京市高淳人民医院,江苏 南京211300)
黄芩苷(baicalin)是从中药黄芩中提取的一种黄酮类化合物,具有清热、消炎、抗氧化和清除自由基、抗肿瘤等作用[1,2],在临床上具有广阔应用前景。然而黄芩苷溶解性能差,口服制剂体内吸收缓慢、生物利用度低,从而影响了在临床上的应用[3],因此必须通过有效的方法提高其溶出速率。应用固体分散体技术可改善难溶性药物的溶解性能,提高溶出速率,从而提高生物利用度[4,5]。
壳聚寡糖(chitooligosaccharide),又名葡萄糖胺寡糖,是壳聚糖降解后聚合度为2~10的产物[6]。作为自然界中唯一大量存在的碱性氨基多糖,具有分子量小、水溶性好、易吸收等特性[7],壳聚寡糖在医药、保健品、化妆品、农药、饲料添加剂等方面具有广阔的应用前景[8,9]。壳聚寡糖的制剂应用较少,本实验尝试以壳聚寡糖为载体制备黄芩苷固体分散体,并进行物相鉴别,以期能有效提高药物的溶出度。
1 材料与仪器
1.1 材料 黄芩苷(西安小草植物科技有限公司,含量为98%,批号:xc121225);黄芩苷对照品(中国食品药品检定研究院,批号:110715-200815);壳聚寡糖(浙江金壳药业有限公司,平均分子量1 000 Da,批号:D130227020);甲醇、磷酸为色谱纯,水为高纯水,其余试剂均为分析纯。
1.2 仪器 Agilent 1200高效液相色谱仪;B-295小型喷雾干燥仪(瑞士BUCHI公司);DSC 60差示扫描量热仪(日本岛津);S-4700扫描电子显微镜(日本电子公司);X Pert Pro型X射线衍射仪(荷兰Philips公司);Nicoiet 8700红外光谱仪(美国热电公司);FA-2004型电子天平(上海精密仪器厂);KQ-100E超声波清洗器(昆山超声仪器有限公司);Mastersizer激光粒度仪(英国马尔文仪器有限公司)。
2 方法与结果
2.1 样品的制备
2.1.1 黄芩苷-壳聚寡糖固体分散体的制备 按照药物与载体质量比 1∶4、1∶6、1∶8 的比例,分别称取黄芩苷与壳聚寡糖,溶解于适量50%乙醇,进行喷雾干燥(进风温度120℃,进料速度10 mL·min-1),干燥粉过80目筛,即得黄芩苷-壳聚寡糖固体分散体,置干燥器内保存备用。
2.1.2 物理混合物的制备 按1∶6质量比例称取黄芩苷和壳聚寡糖,混合均匀,制得物理混合物,置干燥器内保存备用。
2.2 体外溶出试验
2.2.1 色谱条件 Zorbax SB-C18色谱柱(4.6 mm×250 mm,5 μm);柱温为30℃;流动相为甲醇 -水 - 磷酸(47∶53∶0.2);流速为 1 mL· min-1;检测波长为 280 nm;进样量:10 μL。
2.2.2 对照品溶液的制备 精密称取黄芩苷对照品8.11 mg,置50 mL量瓶中,用甲醇溶解并稀释至刻度,摇匀,得 162.20 μg·mL-1黄芩苷对照品溶液。
2.2.3 线性关系考察 分别精密吸取黄芩苷对照品溶液0.1、0.2、0.5、1.0、2.0、5.0 mL 各置 10 mL量瓶中,加甲醇稀释至刻度,摇匀,分别量取10 μL注入高效液相色谱仪,测定峰面积(A),将质量浓度(C)与A值进行线性回归,按外标法计算得标准曲线方程 A=48.757C+21.852,r=0.999 6;线性范围1.622 ~81.10 μg·mL-1。
2.2.4 精密度试验 取同一浓度黄芩苷对照品溶液,连续进样5次,测得黄芩苷峰面积的RSD分别为 0.89%。
2.2.5 稳定性试验 取黄芩苷对照品溶液,于配制后0、2、4、8、12、24 h 进样,黄芩苷峰面积 RSD 为1.45%,表明黄芩苷溶液在室温下24 h内稳定。
2.2.6 加样回收率试验 精密称取已知黄芩苷含量的固体分散体各约8 mg,平行9份,分别置25 mL量瓶中,分别精密加入黄芩苷对照品适量,甲醇稀释至刻度,滤过,制成低、中、高质量浓度的供试品溶液,按上述色谱条件测定含量,计算回收率,结果见表1。黄芩苷平均回收率为 100.27%,RSD为1.25%,表明此测定方法回收率良好。
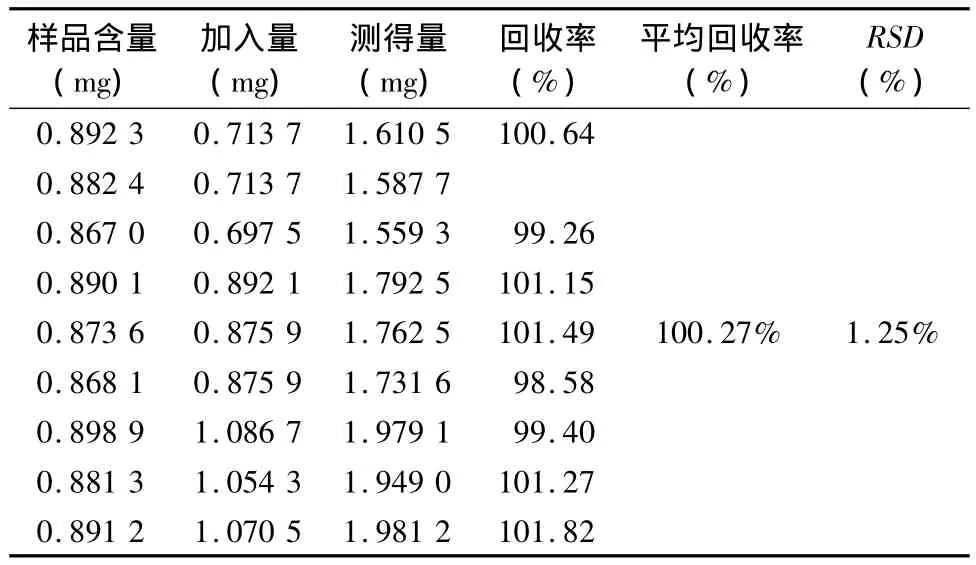
表1 黄芩苷加样回收率试验
2.2.7 药物的溶出度测定 溶出度测定方法为《中国药典》2010年版(二部)附录Ⅹ C篮法,转速50 rpm,温度(37±0.5)℃,溶出介质为900 mL蒸馏水。精密称取黄芩苷、物理混合物和不同比例的固体分散体适量(含黄芩苷10 mg),分别装于胶囊中,置于转篮中,在上述溶出条件下,分别于5、10、15、30、45、60、90、120 min 取样 5 mL(同时补加同温同体积的溶出介质),以0.45 μm微孔滤膜过滤,取续滤液10 μL注入液相色谱仪进行测定,测定结果代入标准曲线计算浓度,并换算成累积溶出百分率,结果见图1。
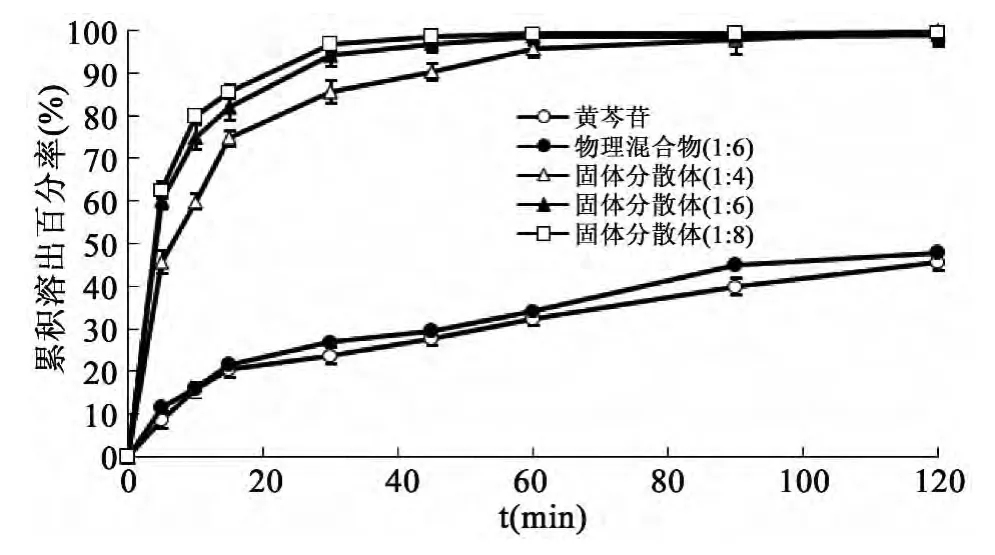
图1 不同比例壳聚寡糖对黄芩苷溶出度的影响(n=6)
由图1的溶出曲线可以看出壳聚寡糖作为固体分散体的载体材料,可明显提高黄芩苷的溶出速率和程度。且壳聚寡糖所占比例越大,黄芩苷溶出度越好,当黄芩苷与壳聚寡糖比例为1∶6、1∶8时,在30 min时药物溶出度分别为94.25%和96.77%,显著性高于其物理混合物和原料药。从载药量方面考虑,载药量高相应地可以减少给药剂量,故选择药物与载体比例为1∶6制备黄芩苷固体分散体。
2.3 粒径分布 采用Mastersizer激光粒度仪对黄芩苷原料药和黄芩苷-壳聚寡糖固体分散体(1∶6)的粒度进行分析,结果见表2。
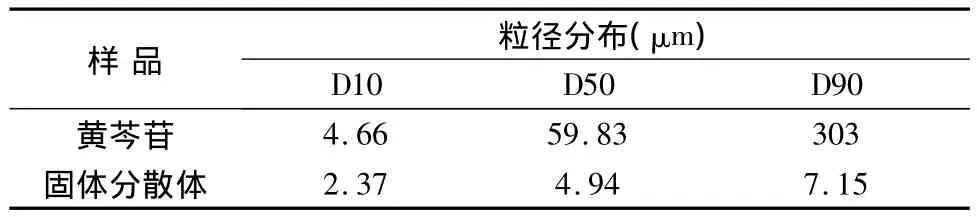
表2 粉末的粒径分布(n=3)
表2结果表明,黄芩苷原料药粒径大,分布范围比较广,经喷雾干燥制备的固体分散体粒径减小,且粒度分布均匀。
2.4 固体分散体物相表征
2.4.1 差示量热扫描分析(DSC) 测试条件为铝坩埚;气氛:氮气;升温速率:10.00℃· min-1;升温范围:0~400℃。分别对黄芩苷原料药、壳聚寡糖、黄芩苷/壳聚寡糖(1∶6)物理混合物(以下简称物理混合物)和黄芩苷/壳聚寡糖(1∶6)固体分散体(以下简称固体分散体)进行DSC分析,结果见图2。
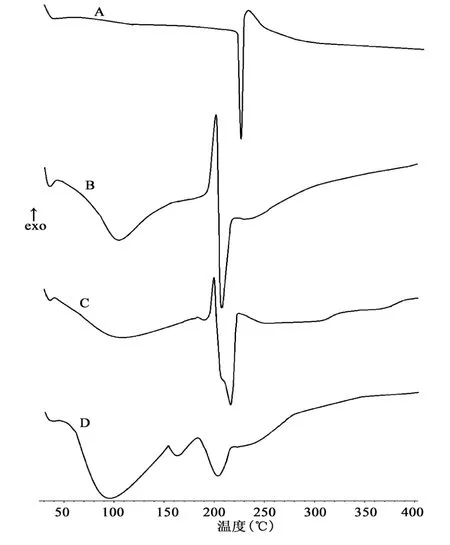
图2 差示量热扫描图
DSC曲线图显示:黄芩苷原料药在227℃处出现一个明显吸热峰;壳聚寡糖在201℃、208℃处各有一明显放热峰和吸热峰;在物理混合物中,黄芩苷在227℃吸热峰存在,说明药物晶型未改变;而在固体分散体中原料药的特征峰消失,提示黄芩苷可能以非晶体形式存在。
2.4.2 扫描电镜法分析(SEM) 测试条件为真空镀金70 s,用扫描电镜分别观察黄芩苷原料药和固体分散体的表面结构特征,结果见图3。

图3 扫描电镜图
从图3可知黄芩苷原料是一种细长晶体,晶体形态清晰。固体分散体为球状或类球状的颗粒,黄芩苷结晶消失,提示固体分散体中黄芩苷以非晶形态高度分散。
2.4.3 X-射线粉末衍射法分析 (XRD) 测试条件为 Cu 靶(40 kV,40 mV);步进扫描:0.01°/步;扫描范围:10 ~90°;扫描速度:4°·min-1,分别对黄芩苷原料药、壳聚寡糖、物理混合物和固体分散体进行分析,结果见图4。
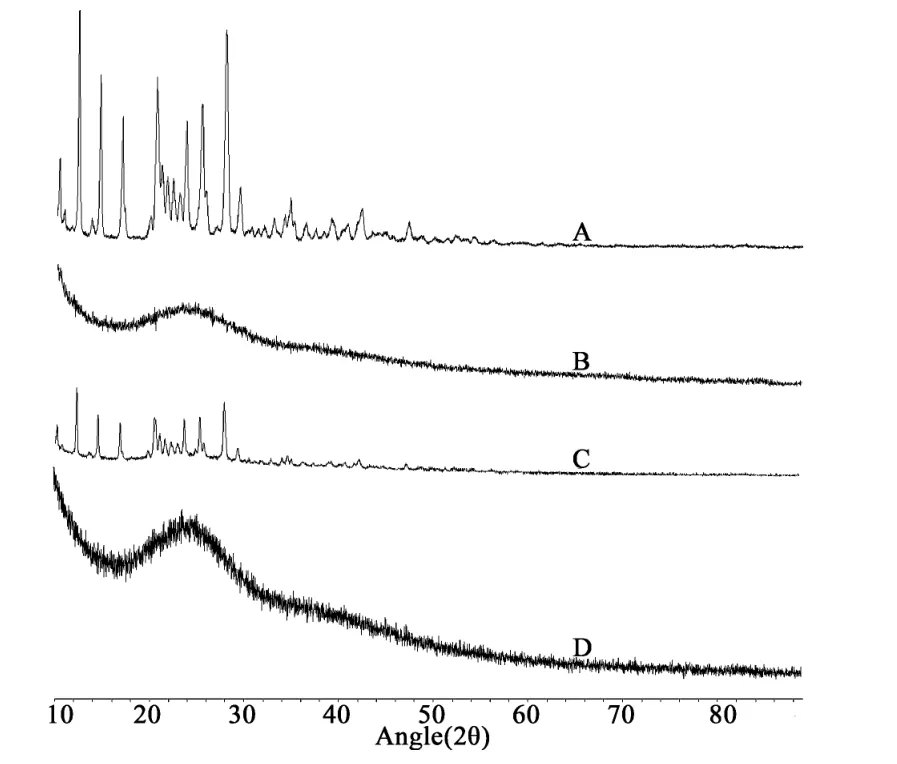
图4 X-射线衍射图
X-射线衍射谱图显示:黄芩苷在10~60°范围内有多个强的结晶峰;壳寡糖是一种无定形粉末,其衍射图谱没有明显的特征衍射峰;物理混合物中保留了黄芩苷原料药的晶体特征衍射峰,而在固体分散体中黄芩苷的晶体特征峰均消失,提示药物以非晶形态存在。
2.4.4 傅里叶变换红外光谱(FTIR) 采用KBr压片法测定红外光谱,将样品与KBr在干燥环境下混合制片后,分辨率为 4 cm-1,4 000 ~500 cm-1全谱扫描,结果见图5。
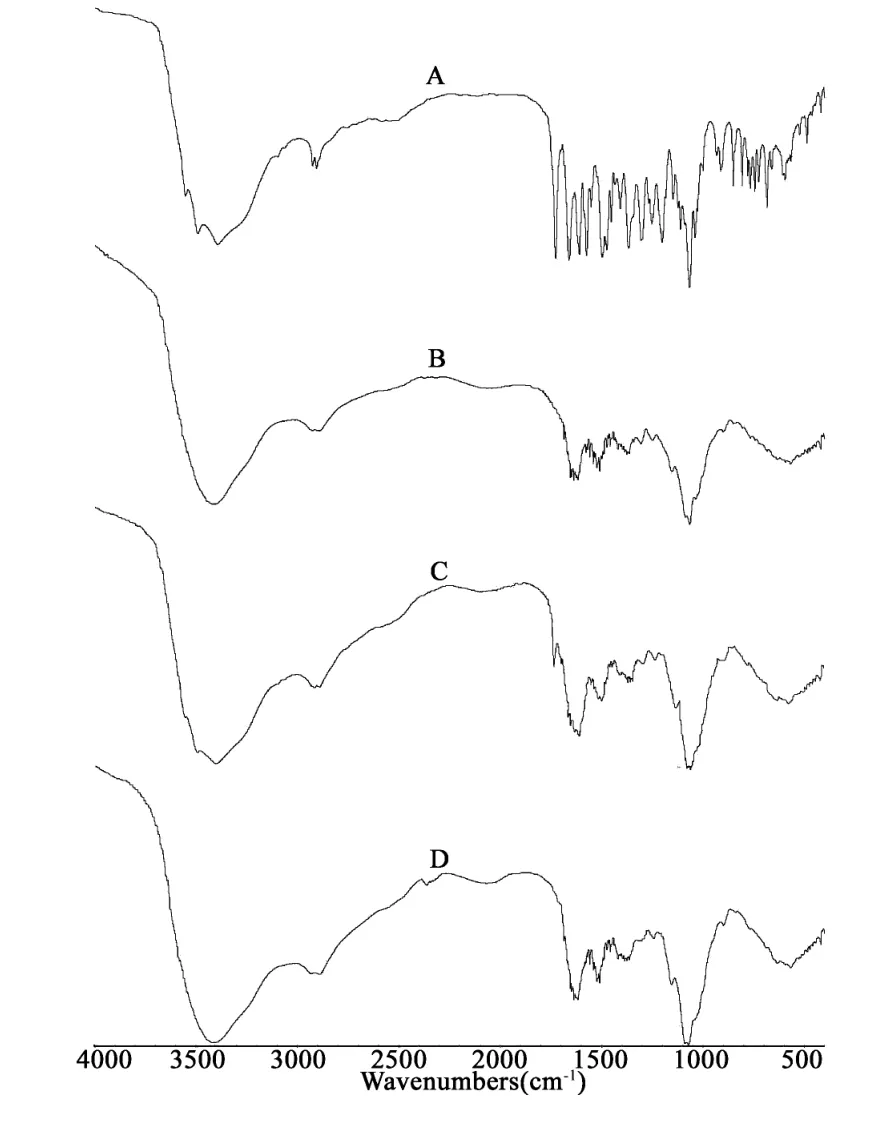
图5 红外光谱图
物理混合物图谱主要是壳寡糖与黄芩苷主要吸收峰的叠加。而在固体分散体中,黄芩苷在3 300~3 600 cm-1区域的羟基伸缩振动峰及1 729.46 cm-1处的-COOH中羰基特征吸收峰消失;壳寡糖在1 636.86 cm-1处的酰胺Ⅰ特征吸收峰消失,及在1 523.32 cm-1处的酰胺Ⅱ的特征吸收峰减弱,提示黄芩苷的羧基和壳寡糖的氨基可能存在相互作用。
4 讨论
喷雾干燥因瞬间蒸发、干燥过程迅速,避免了传统蒸发干燥工艺耗时长、温度高等缺点,提高了生产效率;其产品为形状均匀、膨松的粉末状物质,可以直接供片剂、颗粒剂、胶囊剂的成型。因此,在制药行业喷雾干燥技术已得到广泛应用。本实验选择壳聚寡糖作为载体材料,采用喷雾干燥技术制备壳寡糖-黄芩苷固体分散体,显著增加了黄芩苷的溶出度。粒径分布测定结果表明,与黄芩苷原料药相比,固体分散体粉末粒径显著减小,促进了药物的体外溶出。同时DSC、XRD结果表明黄芩苷以非晶形态分布于固体分散体中,进一步增加了药物的体外溶出度。本实验的研究结果证实以壳聚寡糖为载体制备固体分散体能提高药物的溶出度,为难溶性药物的制剂前处理提供了新的途径。
[1]叶玉杰,钱敏.黄芩苷固体分散体的制备及其体外溶出情况[J].中国医院药学杂志,2010,30(22):1905-1908.
[2]汤立建,赵良才,李庆林,等.黄芩黄酮类成分抗肿瘤作用及机制研究进展[J].中国中药杂志,2007,32(1):21-23.
[3]陈莉,龙晓英,黄嗣航,等.黄芩苷及其磷脂复合物、自微乳的Caco-2细胞跨膜转运研究[J].中药材,2012,33(5):757-761.
[4]徐璐,朱澄云,李三鸣.布洛芬固体分散体的制备[J].中国医院药学杂志,2012,32(1):22 -26.
[5]蒋艳荣,张振海,陆艳,等.丹参酮ⅡA二元载体固体分散体的研究[J].中国中药杂志,2012,37(10):1383-1387.
[6]陈虹,臧素敏,侯伟革.不同浓度壳寡糖对蛋用鹌鹑免疫功能的影响[J].中国畜牧兽医,2013,40(1):108-109.
[7]张沛,韩宝芹,陈列欢,等.用酶解法制备壳寡糖及其对机体免疫功能的调节作用[J].中国免疫学杂志,2013,29(2):191 -195.
[8]邓培昌,胡杰珍,侯庆华,等.壳寡糖制备方法研究进展[J].中国免疫学杂志,2012,40(6):22 -24.
[9]李峻峰,邹琴,赖雪飞.壳聚糖微球药物释放机制研究进展[J].生物医学工程学杂志,2011,28(4):843-846.
