基于多重氢键的寡聚芳酰胺自组装囊泡
2014-10-18贺有周袁立华
贺有周 刘 云 刘 鹏 冯 文 袁立华
(四川大学化学学院,原子核科学技术研究所,辐射物理及技术教育部重点实验室,成都 610064)
1 引言
囊泡因其在生物模拟、1-3纳米材料4-6以及药物和基因传递7-10等方面的重要意义而受到日益广泛关注.早期的研究主要是通过磷脂分子、11表面活性剂12,13和嵌段共聚物14等作为主体分子来设计和构筑囊泡体系.随着超分子化学的深入发展,相继出现了以杯芳烃、15,16葫芦脲、17环糊精18,19和芳酰胺分子20-23等为主体的自组装超分子囊泡体系.
近年来发展起来了一类结构独特的寡聚芳酰胺分子,是基于多重氢键作用形成自互补或异互补双股分子链.24-27利用这种双股分子链,可构筑超分子二嵌段共聚物28或者有效地提高有机反应的产率.29近几年我们报道了一种基于四重氢键寡聚芳酰胺双股分子链的凝胶,通过改变侧链可以对凝胶的稳定性和组装形貌等进行调控;30设计了一系列可以通过改变氢键结合位点间距来调控结合强度和专一性的寡聚萘芳酰胺分子链;31并用含有端烯烃的寡聚芳酰胺分子,在Grubbs催化剂的催化下形成了基于氢键和烯烃复分解共价偶联的拉链分子;32发现了基于六重氢键异互补寡聚芳酰胺双股分子链构建的氢键型超分子接枝共聚物可以存在于中等极性的溶剂环境中;33探讨了基于酰胺和脲结构的自互补和异互补两类新型的四重氢键结合单元,及其吸电效应、预组织效应以及位阻效应等对结合能力的影响.34,35我们已研究了氢键编码顺序为ADAADA-ADAADA的寡聚芳酰胺分子2,能组装成微纳米实心球;36而我们在设计合成与其能互补配对的氢键编码顺序为DADDAD-DADDAD的寡聚芳酰胺分子1时,意外地发现其能自组装成囊泡结构.
本文首先合成了寡聚芳酰胺分子1,并用SEM、TEM和DLS等手段研究了其形成囊泡的自组装行为,以及加入异互补分子2后的形貌变化,并运用荧光显微镜探讨了其包裹性能.
2 实验部分
2.1 试剂和仪器
采用CaH2对CH2Cl2进行干燥;其它试剂均为市售分析纯,除特殊说明外直接使用.仪器使用日本日立公司Hitachi S-450型扫描电镜(加速电压为20 kV);日本电子株式会(JEOL)的JEM-100CX型透射电镜(加速电压为80 kV);美国Brookhaven公司Malvern Zetasizer Nano S动态光散射仪,扫描角度为90°,采用氦氖激光光源(532 nm);Bruker AV II-400 MHz和Bruker AV II-600 MHz核磁共振波谱仪;日本SHIMADZU公司生产的UV-2450型号的紫外可见分光光度计;日本尼康公司生产的型号为Nikon Eclipse Ti-E倒置荧光显微镜.
2.2 寡聚芳酰胺自组装测试制样方法
先配成一定浓度的四氢呋喃/甲醇溶液(5.00 mmol·L-1)或者丙酮溶液(0.10-5.00 mmol·L-1),加热至50°C摇匀,冷却至室温,静置1 h滴加到云母上,溶剂自然挥发干燥后进行SEM测试.TEM制样方法:配成0.20 mmol·L-1的丙酮溶液,加热至50 °C,震荡摇匀,冷却至室温,静置1 h,用滴管吸取溶液滴于纯碳膜铜网上,用滤纸吸去余液,在45°C下真空干燥2 h后滴加磷钨酸(质量分数为2%)进行染色,5 min后吸去多余的染液,烘干进行测试.
DLS测试制样采用丙酮,配制成一定浓度的溶液,用孔径为220 nm的过滤筛进行过滤.测试温度25°C,入射光波长532 nm,扫描时间3 min,扫描角度90°.
2.3 囊泡荧光染料包裹测试制样方法
将化合物1和罗丹明B按照相同物质的量的浓度(0.5 mmol·L-1)溶解于3 mL四氢呋喃/甲醇(体积比为95/5)混合溶剂中,加热到60°C,冷却至室温形成澄清的溶液,然后转移至透析袋(截留分子量MW(CO)=3500)中,用1 L四氢呋喃/甲醇溶剂透析三天后,得到的溶液再用四氢呋喃/甲醇溶剂稀释后进行荧光测试.
2.4 合成路线
化合物1的合成路线见示意图1.
2.5 合成步骤
2.5.1 化合物3的合成
化合物3参照以前发表的文献37,38进行合成.
2.5.2 化合物1的合成
将0.70 g(0.74 mmol)化合物3溶于四氢呋喃中,加入0.14 g Pd/C氢气还原,得到的产品直接进行下步反应.将64.4 mg(0.37 mmol)辛二酸和189.0 mg(1.50 mmol)草酰氯溶于干燥的二氯甲烷中,加10µL N,N-二甲基甲酰胺(DMF),室温反应.在冰浴的条件下,滴加到含有化合物3的还原生成的677.0 mg(0.74 mmol)胺和182.0 mg(1.8 mmol)三乙胺的二氯甲烷溶液中,室温搅拌过夜.柱层析分离(V(CHCl3)/V(CH3OH)=30/1)得到浅黄色固体产物(0.55 g,76%).核磁共振氢谱(1H NMR)(600 MHz,DMSO-d6):δ 10.37(s,4H),9.94(s,2H),9.88(s,2H),8.55(t,J=5.2 Hz,4H),8.10(s,2H),8.08-8.04(m,8H),7.87-7.72(m,4H),7.16(dd,J=9.1,4.7 Hz,4H),4.26-4.17(m,12H),4.05-3.97(m,8H),2.33-2.24(m,4H),2.03(s,6H),1.85(m,4H),1.68(m,2H),1.65-1.54(m,4H),1.54-1.23(m,52H),0.94-0.77(m,36H).13C NMR(100 MHz,DMSO-d6):δ 171.43,168.44,167.95,165.99,164.96,164.93,153.14,153.10,139.92,134.55,133.15,131.26,124.13,124.06,122.33,122.26,121.93,115.31,114.49,113.96,79.64,72.31,67.16,63.10,46.08,44.04,38.97,38.78,36.71,34.82,34.14,33.97,31.74,30.89,30.45,30.34,29.48,29.15,28.93,28.85,25.52,24.96,24.23,23.88,23.75,22.95,22.84,22.53,14.29,14.27,11.29,11.25,9.03.HRESIMS(m/z)计算值[C110H158N12O20+H]+1969.1827,实验值:1969.1859;计算值[C110H158N12O20+Na]+1991.1647,实验值:1991.1689.
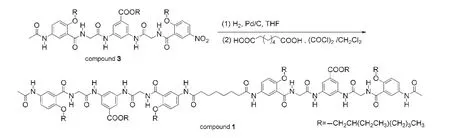
示意图1 寡聚芳酰胺1的合成路线Scheme 1 Synthetic route of oligoaramide 1 THF:tetrahydrofuran
3 结果与讨论
3.1 自组装囊泡形貌分析
将化合物1溶于四氢呋喃溶剂中,滴加到云母片上并干燥,通过SEM观察没有发现其组装形貌.Zang课题组39曾报道适当添加不良溶剂有利于自组装发生.于是向良溶剂四氢呋喃中加入5%的不良溶剂甲醇制样,惊讶地发现其组装形成了球形结构(图1),但其形状不太规整,微球上有小孔,暗示其可能为囊泡结构;加入15%(w)的甲醇时,得到了较为规整的球形结构,微球上同样存在小孔;加入30%的甲醇时,发现微球上的小孔明显增多;当加入50%的甲醇时,分散的微球开始连在了一起,有的形成了整块的膜状结构.溶剂组成改变对组装结构产生了影响,适当添加不良溶剂甲醇有利于自组装发生.
改用丙酮作为溶剂,化合物1也能组装成大小较均匀的球形结构(图2),与混合溶剂中的情况一样,球状物上也有小孔,表明此球状物很可能为囊泡结构.当浓度为0.10 mmol·L-1时,囊泡的平均直径大约变为了0.48 μm;当浓度增加到0.25 mmol·L-1时,囊泡的平均直径也增大为0.50 μm;当浓度进一步增加到5.00 mmol·L-1时,囊泡的平均直径变为了2.18 μm.这说明了溶液浓度对囊泡大小的影响,浓度越浓囊泡越大.
TEM实验发现(图3),球体中间颜色浅、边沿深,进一步证实其为囊泡结构,直径在250 nm左右.囊泡的壁厚为3.0 nm左右,这与其双分子层囊泡模型(CPK)计算值2.6 nm十分接近,推测囊泡表现为双分子层结构.
3.2 化合物1的核磁共振氢谱1H NMR分析

图1 化合物1(5.0 mmol·L-1)在四氢呋喃/甲醇不同比例混合溶剂中的扫描电镜图Fig.1 SEM images of compound 1(5.0 mmol·L-1)in tetrahydrofuran/methanol volume ratio of tetrahydrofuran/methanol:(a)95/5;(b)85/15;(c)70/30;(d)50/50

图2 不同浓度化合物1在丙酮中的扫描电镜图Fig.2 SEM images of compound 1 with different concentrations in acetone

图3 化合物1在丙酮中的透射电镜图(磷钨酸染色)Fig.3 TEM images of compound 1 in acetone(phosphotungstic acid staining)
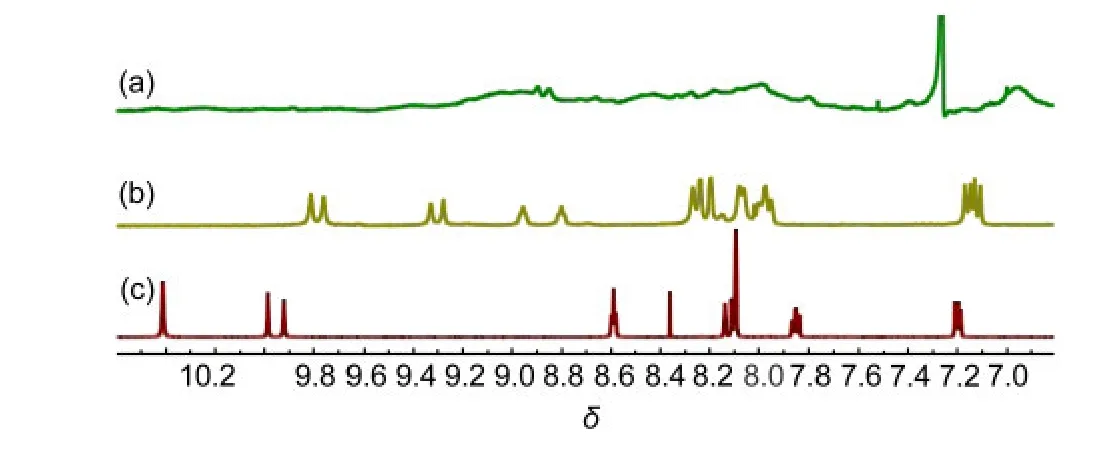
图4 化合物1(5 mmol·L-1)在不同溶剂中的局部叠加1H NMR谱图Fig.4 Stacked partial1H nuclear magnetic responance(1H NMR)spectra of compound 1(5 mmol·L-1)in different solutions
通过变极性核磁研究了化合物1的聚集行为.实验结果(图4)表明:在弱极性溶剂氯仿中,化合物1呈现出很宽的峰,可能是由于分子间氢键作用形成了超分子聚合物导致聚集作用非常强;在中等极性溶剂丙酮中,化合物1的峰开始变得较为清晰,分子间氢键作用被削弱了,从而导致超分子聚合物的聚合能力减弱了;在强极性溶剂二甲基亚砜(DMSO)中,分子间的氢键作用彻底被破坏了,化合物1峰形变得非常尖锐.所以通过变极性核磁实验暗示化合物1在丙酮中可能形成了超分子聚合物或者超分子寡聚体.
二维核磁共振(2D NOESY)实验是研究化合物1是否发生自组装的一种很好的方法.2D NOESY实验(图5)显示,苯环质子j和亚甲基质子d之间有明显的相互作用,说明化合物1通过氢键作用发生了自组装,可能形成了线性超分子寡聚体或聚合物.TEM实验已经推测囊泡为双分子层结构,化合物1自组装形成囊泡可能的组装模型如图6所示.

图5 化合物1的二维核磁(2D NOESY)谱图Fig.5 Partial two-dimensional nuclear overhauser enhancement(2D NOESY)spectra of compound 1
3.3 自组装囊泡动态光散射(DLS)分析
DLS实验进一步提供了化合物1在溶液状态中发生自组装的证据(图7).新配制的溶液经静置2 h后,平均粒径为229.0 nm,这与TEM实验发现的囊泡直径在250 nm左右相近;而静置24 h,平均粒径增大到383.0 nm左右.静置的时间越久其粒径越大,说明化合物在丙酮中的聚集程度随着静置时间的延长而加强,这可能是囊泡相互融合造成的.

图6 化合物1自组装形成囊泡的示意图Fig.6 Schematic representation of self-assembled vesicles of compound 1
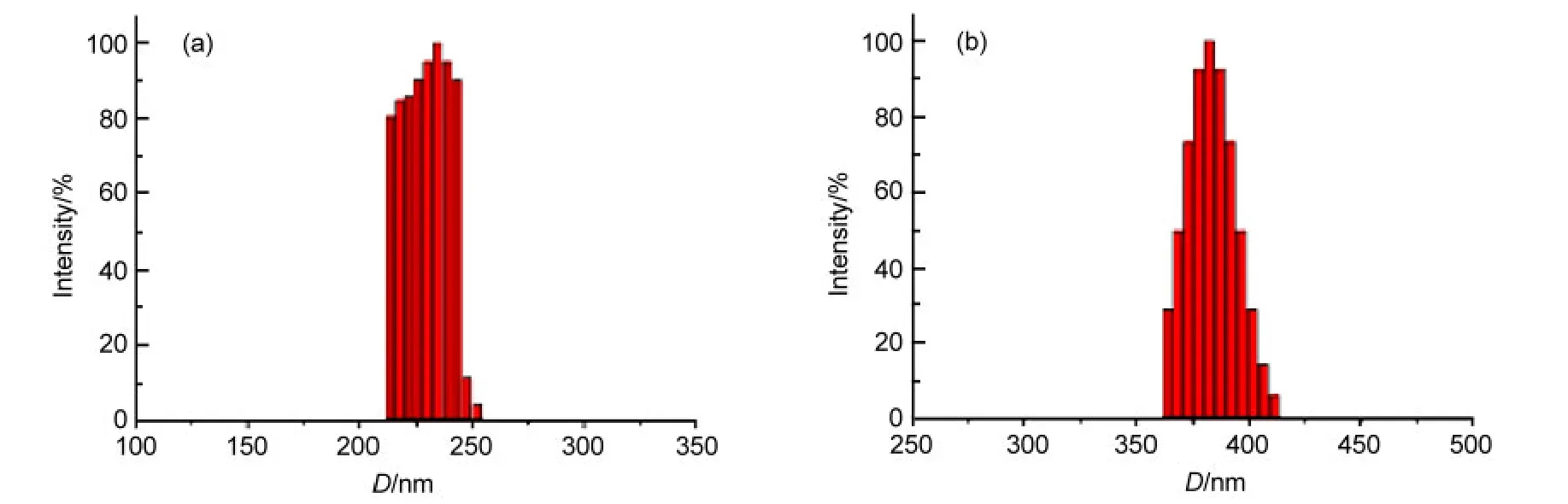
图7 化合物1(0.2 mmol·L-1)在丙酮中的动态光散射(DLS)图Fig.7 Dynamic laser scattering(DLS)patterns of compound 1(0.2 mmol·L-1)in acetone(a)2 h;(b)24 h

图8 化合物2的结构36Fig.8 Structure of compound 236

图9 (a)复合物1·2的扫描电镜图;(b)复合物1·2的透射电镜图Fig.9 (a)SEM image of complex 1·2;(b)TEM image of complex 1·2
3.4 自组装形貌调控
加入等物质的量的异互补链2(图8),对自组装形貌进行调控.通过SEM(图9(a))发现,复合物1·2自组装形成了球状物,但与化合物1形成的囊泡相比较,其球形结构上没有出现小孔,暗示此球状物可能为实心球.通过TEM(图9(b))证实其球状物的确为实心结构.当加入异互补分子2后,对自组装形貌产生了影响,使囊泡转变成了实心球,达到了自组装形貌调控的目的.

图10 化合物1(0.005 mmol·L-1)和化合物2(0.005 mmol·L-1)及其复合物1·2(0.005 mmol·L-1)在氯仿中的紫外-可见光谱Fig.10 UV-Vis absorption spectra of compounds 1(0.005 mmol·L-1),2(0.005 mmol·L-1)and complex 1·2(0.005 mmol·L-1)in CHCl3

图11 化合物1(C)和化合物2(A)及其复合物1·2(B)的薄层色谱图Fig.11 Thin-layer chromatography(TLC)of compounds 1,2(C,A)and complex 1·2(B)
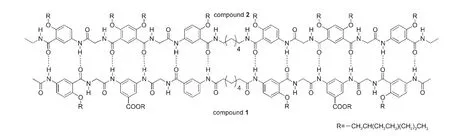
图12 复合物1·2的组装模式示意图Fig.12 Illustration of complex 1·2

图13 化合物1自组装囊泡包裹罗丹明B的荧光显微镜图Fig.13 Fluorescence microscopy image of Rhodamine B-entrapped vesicles of compound 1
紫外测试显示(图10),复合物1·2的吸光度远大于化合物1和2的吸光度,并非简单二者强度的加和,且观察到复合物1·2的最大吸收峰有红移现象发生,说明通过氢键配对的化合物1和2之间发生了自组装.
在对化合物1和2及其复合物1·2进行薄层色谱(TLC)板检测时,发现了一个更直接的证据.如图11所示,复合物1·2(点B)在TLC板上显示了与化合物1(点C)和化合物2(点A)不同的比移值(Rf).复合物1·2在TLC板上形成的新点直观地说明了复合物1·2自组装体的形成.
加入的互补化合物2和化合物1可能形成了如图12所示的二聚体结构,使其不能再形成线性的超分子寡聚体或聚合物,二聚体再通过侧链的范德华力与苯环之间的ππ堆积作用聚集在一起,从而形成了实心球.
3.5 囊泡包裹性能
为了进一步对囊泡进行研究,我们运用荧光显微镜探讨了其包裹性能.实验表明(图13)化合物1自组装成的囊泡结构可以很好地包裹荧光分子(罗丹明B),可以看到其包裹的罗丹明B分子.
4 结论
合成了氢键编码顺序为DADDAD-DADDAD的寡聚芳酰胺分子1,通过SEM和TEM对其自组装形貌进行了研究,发现化合物1组装结构会受到混合溶剂比例改变的影响,在四氢呋喃溶剂中没有发现其组装形貌,当适当加入不良溶剂甲醇有利于自组装发生,加入15%的甲醇得到了较为规整的囊泡结构;分子1也能在单一溶剂丙酮中组装成大小均匀的双分子层囊泡结构.DLS实验表明在丙酮中的聚集程度随着静置时间的延长而加强.通过加入异互补分子2(ADAADA-ADAADA)对自组装形貌进行调控,使囊泡转变成了实心球结构.最后运用荧光显微镜证实化合物1自组装成的囊泡结构可以很好地包裹荧光分子(罗丹明B).本文提供了一种通过含多重氢键的寡聚芳酰胺体系构筑囊泡的方法,通过进一步分子结构修饰,有可能实现在药物包埋和释放方面的应用.
(1)Graff,A.;Sauer,M.;Gelder,P.V.;Meier,W.Proc.Natl.Acad.Sci.U.S.A.2002,99,5064.doi:10.1073/pnas.062654499
(2)Stoenescu,R.;Meier,W.Chem.Commun.2002,3016.
(3)Wang,Y.Y.;Hua,W.;Liu,T.Q.Acta Phys.-Chim.Sin.2011,27,1907.[王元有,华 伟,刘天晴.物理化学学报,2011,27,1907.]doi:10.3866/PKU.WHXB20110822
(4)Stanish,I.;Lowy,D.A.;Hung,C.W.;Singh,A.Adv.Mater.2005,17,1194.
(5)Yan,Q.;Yuan,J.Y.;Cai,Z.N.;Xin,Y.;Kang,Y.;Yin,Y.W.J.Am.Chem.Soc.2010,132,9268.doi:10.1021/ja1027502
(6)Yan,Q.;Zhou,R.;Fu,C.K.;Zhang,H.J.;Yin,Y.W.;Yuan,J.Y.Angew.Chem.,Int.Edit.2011,50,4923.doi:10.1002/anie.v50.21
(7)Discher,D.E.;Eisenberg,A.Science 2002,297,967.doi:10.1126/science.1074972
(9)Duan,Q.P.;Cao,Y.;Li,Y.;Hu,X.Y.;Xiao,T.X.;Lin,C.;Pan,Y.;Wang,L.Y.J.Am.Chem.Soc.2013,135,10542.doi:10.1021/ja405014r
(10)Li,S.;Qiu,Y.Q.;Zhang,S.H.;Gao,Y.H.Acta Phys.-Chim.Sin.2011,27,2167.[李 爽,邱玉琴,张锁慧,高云华.物理化学学报,2011,27,2167.]doi:10.3866/PKU.WHXB20110833
(11)Menger,F.M.;Gabrielson,K.D.Angew.Chem.Int.Edit.1995,34,2091.
(12)Moss,R.A.;Bizzigotti,G.O.J.Am.Chem.Soc.1981,103,6512.doi:10.1021/ja00411a049
(13)Zhao,G.X.;Huang,J.B.Acta Phys.-Chim.Sin.1992,8,583.[赵国玺,黄建滨.物理化学学报,1992,8,583.]doi:10.3866/PKU.WHXB19920503
(14)Discher,B.M.;Won,Y.Y.;Ege,D.S.;Lee,J.C.M.;Bates,F.S.;Discher,D.E.;Hammer,D.A.Science 1999,284,1143.doi:10.1126/science.284.5417.1143
(15)Lee,M.;Lee,S.J.;Jiang,L.H.J.Am.Chem.Soc.2004,126,12724.doi:10.1021/ja045918v
(16)Guan,B.;Jiang,M.;Yang,X.;Liang,Q.;Chen,Y.Soft Matter 2008,4,1393.doi:10.1039/b805312j
(17)Kim,K.;Selvapalam,N.;Ko,Y.H.;Park,K.M.;Kim,D.;Kim,J.Chem.Soc.Rev.2007,36,267.doi:10.1039/b603088m
(18)Ravoo,B.J.;Darcy,R.Angew.Chem.Int.Edit.2000,39,4324.
(19)Lim,C.W.;Crespo-Biel,O.;Stuart,M.C.A.;Reinhoudt,D.N.;Huskens,J.;Ravoo,B.J.Proc.Natl.Acad.Sci.U.S.A.2007,104,6986.doi:10.1073/pnas.0611123104
(20)Zhang,K.D.;Zhou,T.Y.;Zhao,X.;Jiang,X.K.;Li,Z.T.Langmuir 2012,28,14839.
(21)Xu,Y.X.;Wang,G.T.;Zhao,X.;Jiang,X.K.;Li,Z.T.Langmuir 2009,25,2684.doi:10.1021/la8034243
(22)Xu,Y.X.;Wang,G.T.;Zhao,X.;Jiang,X.K.;Li,Z.T.Soft Matter 2010,6,1246.doi:10.1039/b917576h
(23)Du,P.;Wang,G.T.;Zhao,X.;Li,G.Y.;Jiang,X.K.;Li,Z.T.Tetrahedron Lett.2010,51,188.doi:10.1016/j.tetlet.2009.10.115
(24)Gong,B.Accounts Chem.Res.2012,45,2077.doi:10.1021/ar300007k
(25)Li,M.F.;Yamato,K.;Ferguson,J.S.;Gong,B.J.Am.Chem.Soc.2006,128,12628.doi:10.1021/ja064515n
(26)Li,M.F.;Yamato,K.;Ferguson,J.S.;Singarapu,K.K.;Szyperski,T.;Gong,B.J.Am.Chem.Soc.2008,130,491.doi:10.1021/ja072567m
(27)Yuan,L.H.;Zhang,P.H.;Feng,W.;Gong,B.Curr.Org.Chem.2011,15,1250.doi:10.2174/138527211795378236
(28)Yang,X.W.;Hua,F.J.;Yamato,K.;Ruckenstein,E.;Gong,B.;Kim,W.;Ryu,C.Y.Angew.Chem.Int.Edit.2004,43,6471.
(29)Yang,X.W.;Gong,B.Angew.Chem.Int.Edit.2005,44,1352.
(30)Cao,R.K.;Zhou,J.J.;Wang,W.;Feng,W.;Li,X.H.;Zhang,P.H.;Deng,P.C.;Yuan,L.H.;Gong,B.Org.Lett.2010,12,2958.doi:10.1021/ol100953e
(31)Zhang,P.H.;Chu,H.Z.;Li,X.H.;Feng,W.;Deng,P.C.;Yuan,L.H.;Gong,B.Org.Lett.2011,13,54.doi:10.1021/ol102522m
(32)Zeng,J.S.;Wang,W.;Deng,P.C.;Feng,W.;Zhou,J.J.;Yang,Y.Y.;Yuan,L.H.;Yamato,K.;Gong,B.Org.Lett.2011,13,3798.doi:10.1021/ol201282d
(33)Pan,X.S.;Chen,C.;Peng,J.;Yang,Y.A.;Wang,Y.H.;Feng,W.;Deng,P.C.;Yuan,L.H.Chem.Commun.2012,48,9510.doi:10.1039/c2cc35004a
(34)Li,X.H.;Fang,Y.Y.;Deng,P.C.;Hu,J.C.;Li,T.;Feng,W.;Yuan,L.H.Org.Lett.2011,13,4628.doi:10.1021/ol2018455
(35)Li,X.H.;Jia,Y.M.;Ren,Y.;Wang,Y.J.;Hu,J.C.;Ma,T.;Feng,W.;Yuan,L.H.Org.Biomol.Chem.2013,11,6975.doi:10.1039/c3ob40998h
(36)Liu,Y.;He,Y.Z.;Yuan,L.H.;Feng,W.Acta Phys.-Chim.Sin.2011,27,918.[刘 云,贺有周,袁立华,冯 文.物理化学学报,2011,27,918.]doi:10.3866/PKU.WHXB20110403
(37)Jin,Y.D.;Liu,Y.;Yang,Y.A.;Zhang,D.;Dan,G.P.;Du,J.;Yuan,L.H.;Feng,W.Chin.J.Org.Chem.2011,31,1864.[金永东,刘 云,杨永安,张 东,但贵萍,杜 鹃,袁立华,冯 文.有机化学,2011,31,1864.]
(38)Zeng,H.Q.;Miller,R.S.;Flowers,R.A.;Gong,B.J.Am.Chem.Soc.2000,122,2635.doi:10.1021/ja9942742
(39)Balakrishnan,K.;Datar,A.;Naddo,T.;Huang,J.L.;Oitker,R.;Yen,M.;Zhao,J.C.;Zang,L.J.Am.Chem.Soc.2006,128,7390.doi:10.1021/ja061810z
