MnO2/NiCo2O4的静电自组装合成及其电化学性能
2014-10-18胡中爱杨玉英吴红英崔璐娟
李 丽 胡中爱 杨玉英 吴红英 崔璐娟
(1西北师范大学化学化工学院,甘肃省高分子材料重点实验室,生态环境相关高分子材料教育部重点实验室,兰州 730070;2西北民族大学化工学院,兰州 730030)
1 引言
自组装技术能够自发并有效地将纳米结构单元集合成宏观材料,同时还可将纳米结构的特性转移到具有层状微结构的宏观材料中.1,2与其它方法制得的化合物或是大块材料不同,自组装技术制备的具有层状结构的材料拥有大的比表面积、易于反应的位点、快速的离子或电子转输能力以及机械完整性等特性,3故而在电化学储能研究方面受到了研究者们的关注.4目前,这一方法大多运用在了石墨烯基复合材料的制备上.3,5-8氧化石墨是一种层状物,它具有离子交换特性并且能够被剥离成单层的纳米片形成二维纳米材料.9常见的无机层状化合物有层状金属氧化物、层状双氢氧化物和金属磷酸盐等.10-14
作为一种廉价、环境友好的无机材料,金属氧化物MnO2由于其良好的电化学特性,有望替代RuO2成为超级电容器的电极材料.15,16插入四甲基铵离子(TMA+)后层状MnO2容易被剥离成带负电荷的二维纳米片,其表面能够提供稳定的负电荷,可作为一种特殊的结构单元吸附带有正电荷的结构单元或基团,形成具有特殊功能的复合体.Yu等17利用静电吸附层-层自组装方法制备了层状二氧化锰/2,2'-联吡啶铁自组装膜材料;Oh等18利用带负电的[Mn1/3Co1/3Ni1/3]O2纳米片与阳离子导电聚合物的自组装制得了异质层状薄膜;而Lee等19将Li+与带负电的MnO2和[Mn1/3Co1/3Ni1/3]O2纳米片静电自组装制得了异质层状复合物,并将其运用在了锂离子电池中.与此同时,能够剥离成带正电荷的层状双氢氧化物.由于其化学多样性、可调层组成和阴离子交换特性逐渐受到研究者们的关注.20,21Kang等22对Mg-Al LDHs(层状双氢氧化物)与羧甲基纤维素进行了自组装;Wang等10利用带正电荷的Co-Al LDHs纳米片与带负电荷的氧化石墨纳米片的静电自组装制得了Co-Al LDHs/GO复合物,其电化学性能得到了很大的提升;Li等9,20分别采用插层/还原法和层层自组装的方法制备出MnO2/Ni2+-Fe3+LDHs复合物,在5 mV·s-1的扫描速率下其比电容分别达到190和104 F·g-1.然而,由于双氢氧化物高的层电荷密度和层间氢键,上述工作中双氢氧化物都是在甲酰铵中剥离的.
本文采用静电自组装的方法将剥离成负电荷的MnO2纳米片与正电荷的Co-Ni LDHs纳米片有序复合,外加后续热处理后得到了具有异质层状堆垛结构的MnO2/NiCo2O4复合物.值得一提的是,在两种纳米片的剥离过程中均以廉价无毒的水溶液取代了昂贵且有毒的有机溶剂,这使得该方法简便、廉价且绿色环保.
2 实验部分
2.1 试剂和仪器
硝酸钴(天津市科密欧化学试剂开发中心,分析纯),硝酸镍(天津市化学试剂六厂三分厂,分析纯),氯化锰(天津市致远化学试剂有限公司,分析纯),对氨基苯甲酸(天津市光复精细化工研究所,分析纯),四甲基氢氧化铵(天津市光复精细化工研究所,分析纯),30%双氧水(烟台市双双化工有限公司,分析纯),氨水(西安化学试剂厂,分析纯),氢氧化钾(天津市致远化学试剂有限公司,分析纯),无水乙醇(天津市兴复科技发展有限公司,分析纯),所用溶液全部用二次水配制.
日本理学D/max-2400X射线衍射仪(铜靶Kα辐射);美国Thermo S2 AA System原子吸收光谱仪(AAS);美国Nicolet 380傅里叶变换红外(FTIR)光谱仪;德国BRUKER RTS 100/S拉曼光谱仪(Raman);日本JEM-5600LV低真空扫描电子显微镜(FESEM);日本电子JEM-2100高分辨透射电子显微镜(TEM);CHI860D电化学工作站(北京华科普天科技有限责任公司);CT 2001A LAND电池测试系统(武汉市金诺电子有限公司).
2.2 MnO2/NiCo2O4复合物的制备
对氨基苯甲酸(PABA)-Co-Ni LDHs胶状悬浮液的制备:将0.9248 g PABA加入到200 mL蒸馏水中,强力搅拌至完全溶解,加入一定量的硝酸钴和硝酸镍(质量比为2:1),搅拌1 h后在恒速搅拌下滴加浓氨水至pH=9,反应30 min后静置12 h.用大量的蒸馏水洗涤至上清液为中性后加蒸馏水超声分散1 h得带正电的PABA-Co-Ni LDHs胶状悬浮液.就PABA-Co-Ni LDHs的制备而言,已有文献报道,23在本实验中,我们对试剂的添加顺序做了调整,改进后的方法能够更好地提高PABA的插层效果.
TMA-MnO2胶状悬浮液的制备:通过文献报道貌岸然的方法合成TMA+插层的MnO2,24得棕黑色胶状悬浮溶液,加蒸馏水稀释分散(体积比1:20)得带负电的TMA-MnO2胶状悬浮液.
自组装及热处理:在恒速搅拌下将上述TMAMnO2悬浮液滴加到PABA-Co-Ni LDHs悬浮液中,搅拌1 h后,40°C下搅拌12 h.所得沉淀用大量的水和乙醇反复洗涤,过滤得到的棕黑色前驱体在60°C下真空干燥12 h.将所得前驱体在空气气氛下分别于250、300、350和400 °C热处理5 h获得样品.作为对比,将单纯的MnO2和双氢氧化物按照相同的方法进行热处理.
2.3 样品表征
对所得样品采用日本理学D/max-2400X射线衍射仪(XRD)进行晶型结构分析,衍射条件:Cu靶,Kα辐射(λ=0.15418 nm),管电压 40 kV,管电流 60 mA,扫描范围为 4°-80°.选用美国 Thermo S2 AA System原子吸收光谱仪(AAS)对所得样品进行元素分析.对粉末样品与KBr混合压片后,采用Nicolet 380傅里叶变换红外光谱仪测定其红外光谱,光谱范围为4000-400 cm-1.采用日本JEM-5600LV低真空扫描电子显微镜和日本电子JEM-2100高分辨透射电子显微镜观察样品的形貌及尺寸.
2.4 电极材料的制备及电化学测试
将75%(质量分数,下同)的样品、10%的乙炔黑以及10%的导电石墨充分研磨并滴加几滴无水乙醇再加入5%的聚四氟乙烯乳液,调和成糊状物后涂在1 cm×l cm泡沫镍集流体上,60°C干燥12 h压片得工作电极,铂网和饱和甘汞电极(SCE)分别作为辅助电极和参比电极,1 mol·L-1的KOH溶液作为电解液组成三电极体系.利用CHI860D电化学工作站在-0.6-0.45 V电位范围内进行电化学测试.
3 结果与讨论
3.1 MnO2/NiCo2O4复合物的合成
金属氧化物的法拉第反应不仅仅发生在电极表面,更会渗入到整个电极内部发生,因此可以获得比双电层电容更高的比电容.25目前,用作电极材料的金属氧化物其制备方法主要是基于化学共沉淀或氧化还原法,其优异的电化学性能因有限的表面活性位点利用率而难以得到充分体现.在此,我们采用了一种新方法(示意图1),利用带相反电荷的二维纳米片静电自组装,经后续热处理得到了具有高电容性能的多孔层状堆垛的异质复合物.由图1a可以看到,水中剥离的TMA插层MnO2(TMAMnO2)呈黄色胶体分散液,其zeta电位值为-33.6 mV(图1c),在水溶液中TMA+不仅能阻止纳米片的絮凝,而且还能剥离悬浮液中局部团聚的纳米片.24对氨基苯甲酸插层Co-Ni LDHs(PABA-Co-Ni LDHs)在水中剥离后呈淡绿色胶体分散液,其zeta电位值为+20.8 mV(图1b),在水溶液中带正电的PABA末端胺基使得氢氧化物层层之间相互排斥,进而剥离出带正电的二维纳米片.23当这两种带相反电荷的组分混合后生成了絮状沉淀,这是因为静电作用驱使它们自组装成异质结构的纳米复合物.在后续热处理过程中,Co-Ni LDHs纳米片在复合物中转化为NiCo2O4.MnO2纳米片和NiCo2O4纳米片相互堆垛形成了一种多孔层状分布的异质结构(将250、300、350和400°C热处理5 h后得到的样品分别标记为MNC250、MNC300、MNC350和MNC400).
3.2 XRD分析
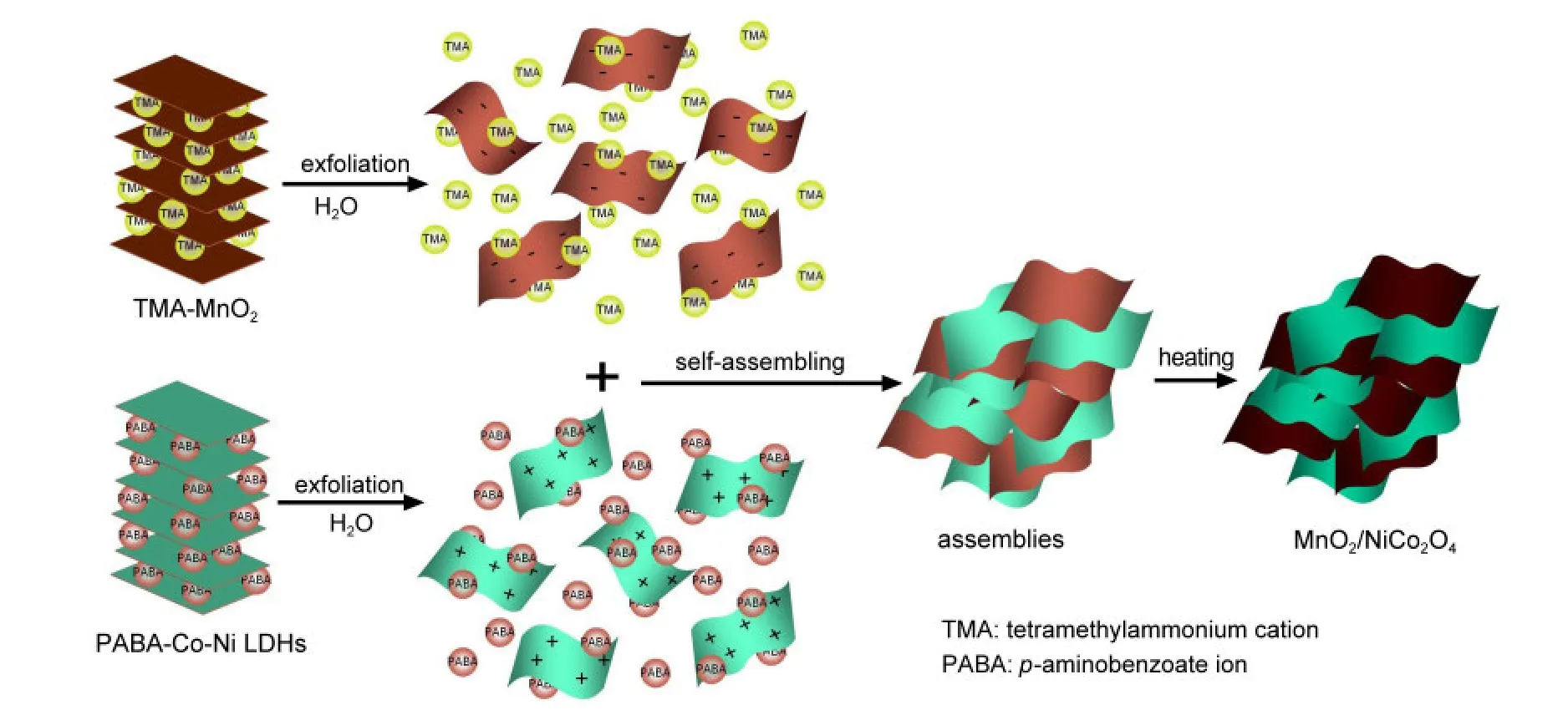
示意图1 MnO2/NiCo2O4复合物的制备过程Scheme 1 Preparing process of the MnO2/NiCo2O4composite

图1 (a)(左)PABA-Co-Ni LDHs,(中)TMA-MnO2水分散液和(右)混合溶液的照片;(b)PABA-Co-Ni LDHs和(c)TMA-MnO2的zeta电位图Fig.1 (a)Photographs of(left)an aqueous dispersion of PABA-Co-Ni LDHs,(middle)an aqueous dispersion of TMA-MnO2,and(right)a mixture of PABA-Co-Ni LDHs and TMA-MnO2;the zeta potential plots of(b)PABA-Co-Ni LDHs and(c)TMA-MnO2
图 2a分别为 TMA-MnO2、PABA-Co-Ni LDHs和组装物的XRD图谱.TMA-MnO2在2θ为9.0°处的衍射峰对应于(001)晶面,0.98 nm的层间距证明了TMA是插于二氧化锰纳米片层间的.24,26PABA-Co-Ni LDHs在2θ=5.6°处的衍射峰对应于(003)晶面,其层间距为1.58 nm,这一值也表明了PABA离子存在于氢氧化物纳米片层间.23静电自组装后,组装物对应于(003)晶面的特征峰在2θ=11.5°处,在向大角度方向偏移的同时其层间距减小为0.77 nm,该值的减小表明两种插层离子均不在组装体中,这个结果可以间接地证明二氧化锰纳米片和氢氧化物纳米片通过静电吸附作用组装在一起.图2b为300°C热处理5 h后MnO2、NiCo2O4和复合物MNC300的XRD图谱.从图中可以看到,复合物显示出NiCo2O4的衍射峰(JCPDS,No.20-0781),27-29但MnO2(JCPDS,No.44-0141)的特征峰不甚明显.15,30,31我们推断这可能是因为在复合物中MnO2的含量较NiCo2O4的少,且被尖晶石钴酸镍所包覆.此外,复合物的XRD图较纯NiCo2O4的XRD图向小角度方向发生了偏移,这可能是由于MnO2的相近衍射所致.
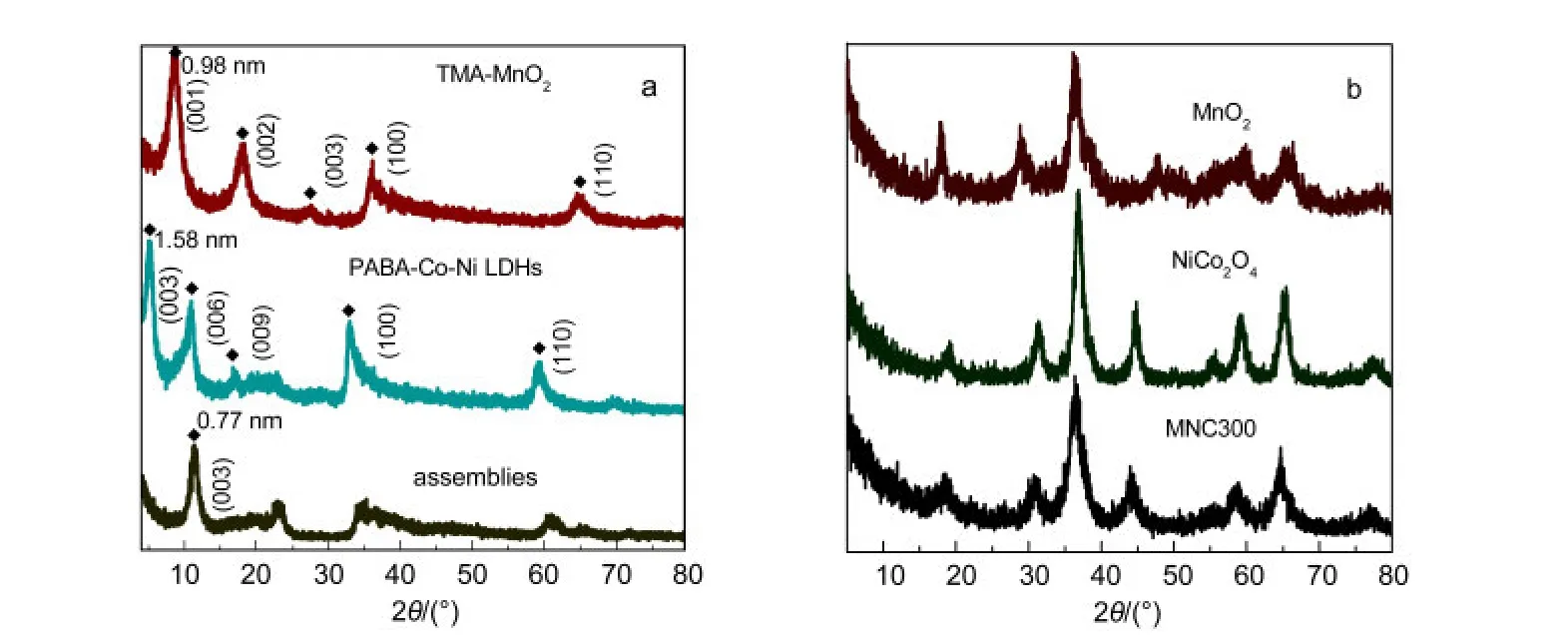
图2 (a)TMA-MnO2,PABA-Co-Ni LDHs和组装物的XRD图谱;(b)300°C热处理5 h后MnO2,NiCo2O4和复合物MCN300的XRD图谱Fig.2 XRD patterns of(a)TMA-MnO2,PABA-Co-Ni LDHs,and assemblies;and(b)MnO2,NiCo2O4,and composite MCN300 annealed at 300°C for 5 h
3.3 傅里叶变换红外及拉曼光谱分析
组装物及MNC300的红外光谱图如图3a所示,组装物在3420和1629 cm-1两处的峰是由插入晶格层间的水分子以及样品层内―OH基团的伸缩和弯曲振动引起的;32,331357 cm-1处的吸收峰对应于组装物层间NO3-离子中N―O的伸缩振动;23,33800 cm-1以下的峰归属于Mn―O、Ni―O和Co―O的振动吸收;34-36此外,组装物中没有出现TMA和PABA离子的特征峰,表明MnO2纳米片和Co-Ni LDHs可能存在于彼此层间.32,37在MNC300中,3429和1629 cm-1两处的吸收峰仍然存在,但强度减弱了很多,表明复合物中含有少量吸附水;1357 cm-1处的吸收峰消失,说明加入的NO3-受热分解;33800 cm-1以下的吸收峰为MnO2中Mn―O键20,32和NiCo2O4中Co―O和Ni―O键的伸缩振动.33,38
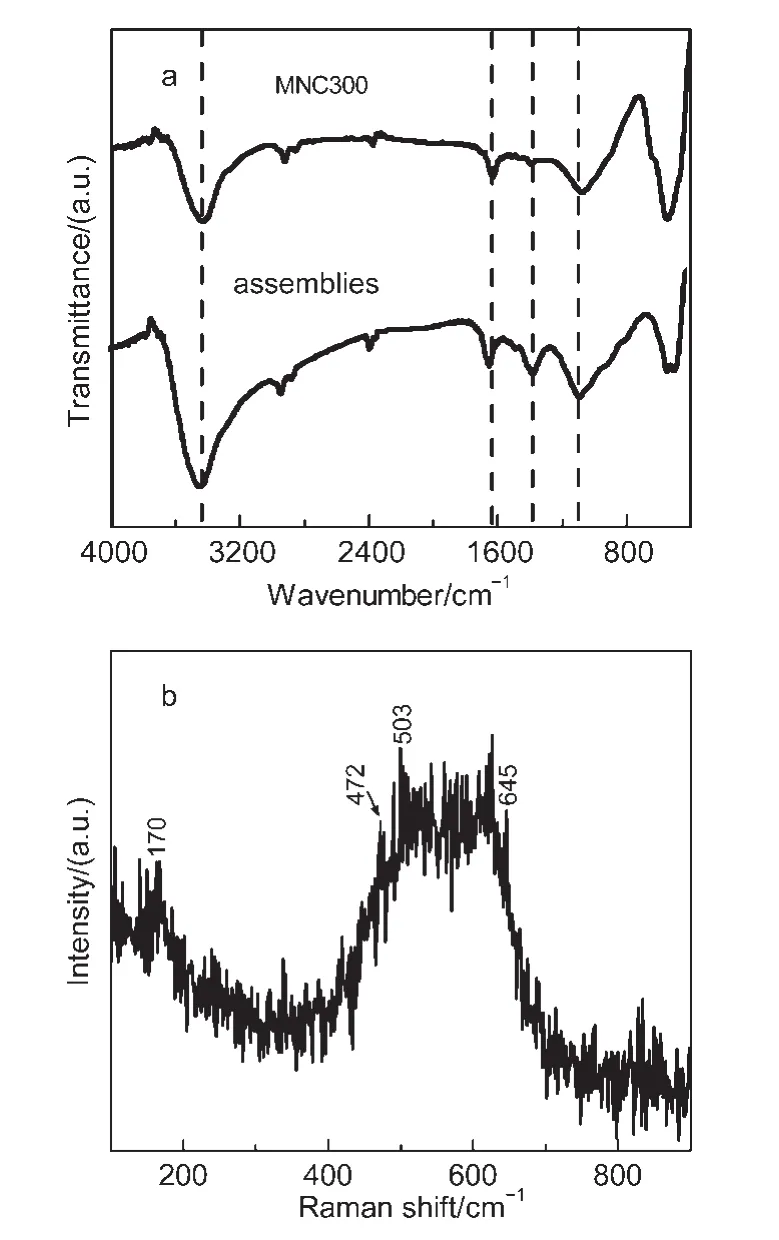
图3 (a)组装物和复合物MNC300的FTIR谱图;(b)复合物MCN300的Raman谱图Fig.3 (a)FTIR spectra of assemblies and MNC300 composite;(b)Raman spectrum of MNC300 composite
图3b是MNC300的拉曼谱图,在170、472、503和645 cm-1处的特征峰归属于NiCo2O4的F2g,Eg,F2g和A1g振动模式;39,40500-650 cm-1范围内的特征峰归属于层状MnO2晶格中MnO6八面体Mn―O键的对称伸缩振动.41然而,由于MnO2与NiCo2O4的相互作用,使得具有不同键强度的Mn―O键、Ni―O键和Co―O键分散了彼此的振动能量,进而加宽了拉曼谱图,在400-700 cm-1范围内形成了峰包.19,41
3.4 FESEM/TEM和AAS分析
为了进一步了解复合物的微观结构,我们对其进行了FESEM和TEM研究.图4(a,b)分别为PABACo-Ni LDHs和TMA-MnO2的FESEM图,由图可见两者均以片状结构存在.自组装后组装物的断面图(图4c)清晰地展现出卷曲的纳米片较为疏松地堆叠在一起,形成了多孔层状结构,这一结构不仅扩大了电极材料与电解液离子的接触面积,而且还利于其扩散进入到材料内的孔道里.样品经300°C热处理5 h后,其形貌基本没有发生变化,延续了前驱体的形貌(图4d).BET测试表明,热处理后复合物MNC300的比表面积(135 m2·g-1,图S1c,见Supporting Information)大于单纯的 MnO2(95.6 m2·g-1,图S1a)和NiCo2O4(77.3 m2·g-1,图S1b),其平均孔径约为6.5 nm(图S1d),说明复合物具有更多的外露活性点位,这有利于提升其电容性能.从TEM形貌(图4e)中看到,复合物呈片状堆叠,结果与SEM相一致.这种特殊的结构证明了带正电的PABA-Co-Ni LDHs纳米片与带负电的TMA-MnO2纳米片进行了自组装.此外,我们对样品进行了Mn、Ni和Co三种元素的空间分布测试.图4(f,g)分别为MNC300断面和粉末的元素分布图,由图可以看到Mn、Ni和Co三种元素均匀地分布在选定的垂直区域上,这进一步说明了复合物是由两种带相反电荷的纳米片经有序自组装而成,而不是随机混合而成.此外,Co元素的信号强于Mn和Ni元素,表明在复合物中Co元素的含量要高于Mn和Ni元素的含量.根据EDS和AAS分析(表1),复合物MnO2/NiCo2O4中Mn、Ni、Co三种元素的摩尔比约为1.00:0.97:2.06,这一结果佐证了XRD和元素分布的推断.
3.5 电化学性能测试
3.5.1 循环伏安测试
图5a为在不同热处理温度(250、300、350和400°C)下复合物在1 mol·L-1KOH溶液,-0.6-0.45 V(vs SCE)电势范围内,扫描速率为5 mV·s-1时的循环伏安曲线.从图中可以看出,循环伏安曲线的面积随热处理温度的升高呈现先增大后减小的趋势,当温度为300°C时曲线面积达到最大即电容活性最佳,这可能是因为高温利于晶形的转化或MnO2完整晶格的形成,但是,过高的处理温度又会使产物的结晶度增加,不利于电解质溶液的渗透,电极材料的实际利用率降低,结果导致比电容减小.MnO2、NiCo2O4和MNC300在扫描速率为5 mV·s-1时的循环伏安曲线如图5b所示,复合物MNC300的曲线面积远大于单纯组分MnO2和NiCo2O4的曲线面积.图中,-0.6-0 V范围内的氧化还原峰对应于MnO2的氧化还原过程,42而0-0.45 V范围内的氧化还原峰则对应于NiCo2O4的氧化还原过程.27,43由此可见,通过静电自组装这种特殊方式的复合,MnO2和NiCo2O4的电化学活性在协同作用下得到了充分的发挥,复合物在其电容提高的同时电位窗口也扩大到了1.05 V.图5c为复合物MNC300在不同扫描速率下的循环伏安曲线,随着扫描速率增加,各氧化还原峰的比电流也随之增大,并表现出较好的响应关系;此外,氧化峰和还原峰也随之分别向正方向和负方向移动,但偏移幅度较小且峰形基本保持不变,这表明复合物MNC300有着良好的倍容特性.

表1 复合物MNC300的X射线能量色散谱(EDS)和原子吸收光谱(AAS)测试结果Table 1 Energy dispersive X-ray spectroscopy(EDS)and atomic absorption spectrometry(AAS)data of composite MNC300

图5 (a)复合物MNC250、MNC300、MNC350和MNC400与(b)MnO2、NiCo2O4和复合物MNC300在扫描速率为5 mV·s-1时以及(c)复合物MNC300在不同扫描速率下的CV曲线Fig.5 CV curves of(a)the MNC250,MNC300,MNC350,and MNC400 at the scan rate of 5 mV·s-1,(b)MnO2,NiCo2O4,and composite MNC300 at the scan rate of 5 mV·s-1;and(c)the composite MNC300 at different scan rates
3.5.2 恒流充放电测试
图6A为在1 A·g-1电流密度下,MNC300、NiCo2O4和MnO2在1 mol·L-1KOH溶液中,-0.6-0.45 V(vs SCE)电势范围内的恒电流放电曲线.由图可以看出,复合物MNC300的比电容大于单纯组分的.复合物的恒电流放电曲线中出现的两处放电平台(-0.6-0 V和0-0.45 V)分别归属于复合物中MnO2和NiCo2O4的赝电容特性,这与循环伏安曲线的分析相一致.根据比电容的计算公式:
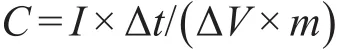
其中,I(A)为放电电流,Δt(s)为放电时间,ΔV(V)为放电过程的电位降,m(g)为电活性物质的质量,C(F·g-1)为比电容.经计算得到复合物MNC300在1 A·g-1时的比电容为482 F·g-1,大于单纯组份MnO2(242 F·g-1)和NiCo2O4(304 F·g-1)的比电容.
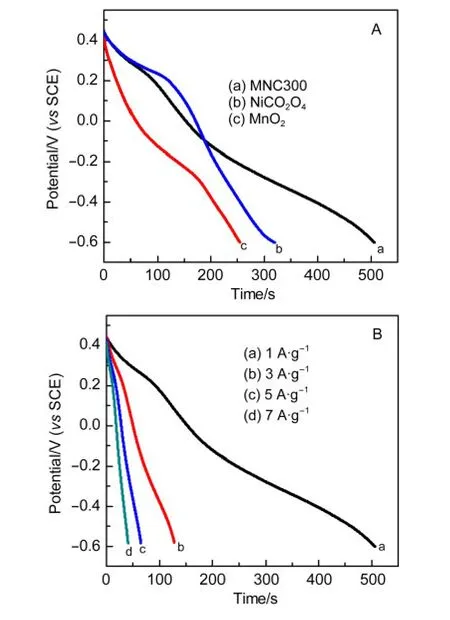
图6 (A)复合物MNC300、NiCo2O4和MnO2在电流密度为1 A·g-1及(B)复合物MNC300在不同电流密度下的恒电流放电曲线Fig.6 Galvanostatic discharge curves of(A)the MNC300 composite,NiCo2O4and MnO2at the current density of 1 A·g-1 and(B)the MNC300 composite at different specific current densities
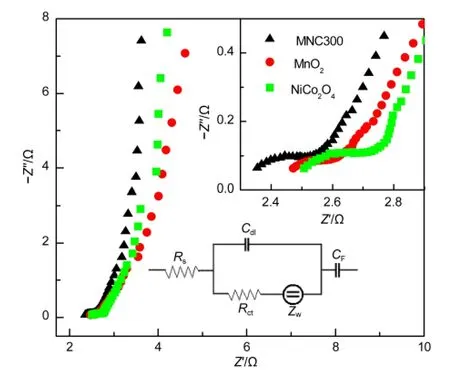
图7 复合物MNC300、MnO2和NiCo2O4的交流阻抗图及其等效电路Fig.7 Nyquist plots of the MNC300 composite,MnO2and NiCo2O4and the equivalent circuit
图6B为复合物MNC300在不同电流密度下的恒电流放电曲线,当电流密度为1、3、5、7 A·g-1时,其相应的比电容值分别为482、367、310、271 F·g-1.随着电流密度的不断增加,体系所要求的离子迁移速率也在随之提高.因此,在较大电流下充放电时,短时间内电解液中的离子或质子来不及渗透和潜出电极材料本体,使得电极材料中活性物质不能得到最大程度的利用,充放电不完全,故而比电容会发生一定程度的降低.在7 A·g-1时,复合物的比电容仍然能达到271 F·g-1,说明其具有较好的倍容率性质.
3.5.3 交流阻抗测试
图7 是复合物 MNC300、MnO2和 NiCo2O4的交流阻抗图,三者都由高频区的不规则半圆和低频区的斜线组成.对交流阻抗谱拟合后的等效电路图如图7插图所示.各电极的拟合数据和相对误差见表S1.在高频区,复合物MNC300的曲线与实部的截距最小,说明对应的电极具有最小的等效串联电阻(Rs);此外,复合物MNC300的电荷传递电阻也很小.这些特性归因于静电自组装后形成的特殊结构为离子提供了畅通无阻的传输通道和易于利用的活性位点.3
4 结论
在水溶液中剥离出带正电荷的PABA-Co-Ni LDHs纳米片和带负电荷的TMA-MnO2纳米片,将二者静电自组装外加后续热处理制得了MnO2/NiCo2O4复合物,方法简便且绿色环保.SEM观察表明,复合物呈现出卷曲层的堆垛结构,形成了有利于电解液存储的微孔.电性能测试表明,热处理温度对组装物电容性能的影响呈现先增加后减小的趋势,当热处理温度达到300°C时,该复合物表现出最佳的电容性能及良好的倍容特性,单电极比电容达482 F·g-1,优于单纯组分MnO2和NiCo2O4的.此外,1.05 V较宽的电位窗口则有利于材料能量密度的提高.
Supporting Information∶Nitrogen adsorption-desorption isotherms and BJH pore size distributions plot of CNTs,MnO2,and composite and the fitting results to equivalent circuits for different electrodes have been included.This information is available free of charge via the internet at http://www.whxb.pku.edu.cn.
(1)Cong,H.P.;Ren,X.C.;Wang,P.;Yu,S.H.ACS Nano 2012,6,2693.doi:10.1021/nn300082k
(2)Whitesides,G.M.;Grzybowski,B.Science 2002,295,2418.doi:10.1126/science.1070821
(3)Choi,B.G.;Huh,Y.S.;Hong,W.H.;Kim,H.J.;Park,H.S.Nanoscale 2012,4,5394.doi:10.1039/c2nr31215h
(4)Yuan,C.Z.;Gao,B.;Shen,L.F.;Yang,S.D.;Hao,L.;Lu,X.J.;Zhang,F.;Zhang,L.J.;Zhang,X.G.Nanoscale 2011,3,529.doi:10.1039/c0nr00423e
(5)Wang,H.W.;Hu,Z.A.;Chang,Y.Q.;Chen,Y.L.;Wu,H.Y.;Zhang,Z.Y.;Yang,Y.Y.J.Mater.Chem.2011,21,10504.doi:10.1039/c1jm10758e
(6)Park,J.S.;Cho,S.M.;Kim,W.J.;Park,J.;Yoo,P.J.ACS Appl.Mater.Interfaces 2011,3,360.doi:10.1021/am100977p
(7)Yu,D.S.;Dai,L.M.J.Phys.Chem.Lett.2009,1,467.
(8)Zhou,Y.Z.;Yang,J.;Sun,L.;Zhao,N.;Cheng,X.N.Chin.J.Inorg.Chem.2012,28,137.[周亚洲,杨 娟,孙 磊,赵南,程晓农.无机化学学报,2012,28,137.]
(9)Li,H.J.;Deng,L.J.;Zhu,G.;Kang,L.P.;Liu,Z.H.Materials Science and Engineering:B 2012,177,8.doi:10.1016/j.mseb.2011.09.012
(10)Wang,L.;Wang,D.;Dong,X.Y.;Zhang,Z.J.;Pei,X.F.;Chen,X.J.;Chen,B.;Jin,J.Chem.Commun.2011,47,3556.doi:10.1039/c0cc05420h
(11)Shan,D.;Cosnier,S.;Mousty,C.Anal.Chem.2003,75,3872.doi:10.1021/ac030030v
(12)Liu,Z.H.;Wang,Z.M.;Yang,X.J.;Ooi,K.Langmuir 2002,18,4926.doi:10.1021/la011677i
(13)Nakato,T.;Furumi,Y.;Terao,N.;Okuhara,T.J.Mater.Chem.2000,10,737.doi:10.1039/a908139i
(14)Liu,Z.P.;Ma,R.Z.;Ebina,Y.;Takada,K.;Sasaki,T.Chem.Mater.2007,19,6504.doi:10.1021/cm7019203
(15)Chen,S.;Zhu,J.W.;Wu,X.D.;Han,Q.F.;Wang,X.ACS Nano 2010,4,2822.doi:10.1021/nn901311t
(16)Tian,Y.;Yan,J.W.;Liu,X.X.;Xue,R.;Yi,B.L.Acta Phys.-Chim.Sin.2010,26,2151.[田 颖,阎景旺,刘小雪,薛 荣,衣宝廉.物理化学学报,2010,26,2151.]doi:10.3866/PKU.WHXB201311262
(17)Yu,S.P.;Xi,M.J.;Han,K.F.;Wang,Z.M.;Zhu,H.Acta Chim.Sin.2010,68,374.[于书平,席铭俊,韩克飞,汪中明,朱 红.化学学报,2010,68,374.]
(18)Oh,E.J.;Kim,T.W.;Lee,K.M.;Song,M.S.;Jee,A.Y.;Lim,S.T.;Ha,H.W.;Lee,M.Y.;Choy,J.H.;Hwang,S.J.ACS Nano 2010,4,4437.doi:10.1021/nn100286u
(19)Lee,K.M.;Lee,Y.R.;Kim,I.Y.;Kim,T.W.;Han,S.Y.;Hwang,S.J.J.Phys.Chem.C 2012,116,3311.doi:10.1021/jp210063c
(20)Li,H.J.;Zhu,G.;Yang,Z.P.;Wang,Z.L.;Liu,Z.H.J.Colloid Interface Sci.2010,345,228.doi:10.1016/j.jcis.2010.01.061
(21)Yang,Q.Z.;Zhang,C.G.;Sun,D.J.;Guo,P.Z.;Zhang,J.Acta Chim.Sin.2002,60,1712.[杨亲正,张春光,孙德军,郭培志,张 洁.化学学报,2002,60,1712.]
(22)Kang,H.L.;Huang,G.L.;Ma,S.L.;Bai,Y.X.;Ma,H.;Li,Y.L.;Yang,X.J.J.Phys.Chem.C 2009,113,9157.
(23)Nethravathi,C.;Viswanath,B.;Sebastian,M.;Rajamathi,M.J.Colloid Interface Sci.2010,345,109.doi:10.1016/j.jcis.2010.01.047
(24)Kai,K.;Yoshida,Y.;Kageyama,H.;Saito,G.;Ishigaki,T.;Furukawa,Y.;Kawamata,J.J.Am.Chem.Soc.2008,130,15938.doi:10.1021/ja804503f
(25)Lokhande,C.D.;Dubal,D.P.;Joo,O.S.Curr.Appl.Phys.2011,11,255.doi:10.1016/j.cap.2010.12.001
(26)Brock,S.L.;Sanabria,M.;Suib,S.L.;Urban,V.;Thiyagarajan,P.;Potter,D.I.J.Phys.Chem.B 1999,103,7416.doi:10.1021/jp991009u
(27)Gupta,V.;Gupta,S.;Miura,N.J.Power Sources 2010,195,3757.doi:10.1016/j.jpowsour.2009.12.059
(28)Wang,X.;Han,X.D.;Lim,M.F.;Singh,N.D.;Gan,C.L.;Jan,M.;Lee,P.S.J.Phys.Chem.C 2012,116,12448.doi:10.1021/jp3028353
(29)Wu,H.Y.;Wang,H.W.Acta Phys.-Chim.Sin.2013,29,1501.[吴红英,王欢文.物理化学学报,2013,29,1501.]doi:10.3866/PKU.WHXB201304241
(30)Gao,T.;Fjellvåg,H.;Norby,P.Anal.Chim.Acta 2009,648,235.doi:10.1016/j.aca.2009.06.059
(31)Cheng,F.Y.;Zhao,J.Z.;Song,W.N.;Li,C.S.;Ma,H.;Chen,J.;Shen,P.W.Inorg.Chem.2006,45,2038.doi:10.1021/ic051715b
(32)Yang,X.J.;Makita,Y.J.;Liu,Z.H.;Sakane,K.;Ooi,K.Chem.Mater.2004,16,5581.doi:10.1021/cm049025d
(33)Verma,S.;Joshi,H.M.;Jagadale,T.;Chawla,A.;Chandra,R.;Ogale,S.J.Phys.Chem.C 2008,112,15106.doi:10.1021/jp804923t
(34)Julien,C.M.;Massot,M.;Poinsignon,C.Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy 2004,60,689.doi:10.1016/S1386-1425(03)00279-8
(35)Hu,Z.A.;Xie,Y.L.;Wang,Y.X.;Xie,L.J.;Fu,G.R.;Jin,X.Q.;Zhang,Z.Y.;Yang,Y.Y.;Wu,H.Y.J.Phys.Chem.C 2009,113,12502.doi:10.1021/jp8106809
(37)Nethravathi,C.;Rajamathi,J.T.;Ravishankar,N.;Shivakumara,C.;Rajamathi,M.Langmuir 2008,24,8240.doi:10.1021/la8000027
(38)He,G.Y.;Wang,L.;Chen,H.Q.;Sun,X.Q.;Wang,X.Mater.Lett.2013,98,164.doi:10.1016/j.matlet.2013.02.035
(39)Liu,Z.Q.;Xiao,K.;Xu,Q.Z.;Li,N.;Su,Y.Z.;Wang,H.J.;Chen,S.RSC Advances 2013,3,4372.doi:10.1039/c3ra23084h
(40)Huang,L.;Liu,M.Nano Lett.2013,13,3135.doi:10.1021/nl401086t
(41)Julien,C.;Massot,M.;Baddour-Hadjean,R.;Franger,S.;Bach,S.;Pereira-Ramos,J.P.Solid State Ionics 2003,159,345.doi:10.1016/S0167-2738(03)00035-3
(42)Zhang,S.W.;Peng,C.;Ng,K.C.;Chen,G.Z.Electrochim.Acta 2010,55,7447.doi:10.1016/j.electacta.2010.01.078
(43)Liu,M.C.;Kong,L.B.;Lu,C.;Li,X.M.;Luo,Y.C.;Kang,L.ACS Appl.Mater.Interfaces 2012,4,4631.doi:10.1021/am301010u
