Fenton法处理垃圾渗滤液的研究*
2014-09-28李晶晶董泽琴
潘 军,李晶晶,董泽琴
(1.贵州省环境科学研究设计院, 贵阳 550081;2.贵州师范大学地理与环境科学学院, 贵阳 550001)
垃圾渗滤液中含有大量腐殖酸、氨氮、“三致”有机物和重金属,这种废水具有成分复杂、毒性强,有机物、氨氮含量高,可生化性差,微生物营养元素比例严重失调,对生态环境危害很大,水质状况随“场龄”发生很大的变化等特点,国内外专家学者对垃圾渗滤液的理化特性和处理技术进行了广泛研究,垃圾渗滤液的无害化处理一直是个世界性的难题[1-3]。
高级氧化技术(advanced oxidation processes,AOPs)因其能够产生极强氧化性的·OH自由基而被认为是处理有机污染物的一种重要替代方法,Fenton法的氧化机理[4]是因为Fenton试剂具有很强的氧化能力,其中含有Fe2+和H2O2,H2O2被亚铁离子催化分解生成羟基自由基(·OH),并引发更多的其他自由基,·OH与有机物RH反应生成游离基R·,R·进一步氧化生成CO2和H2O,从而使废水的COD大大降低。Fenton法作为高级氧化技术的一种,由于它操作简便、费用低廉而受到人们的重视。本文以实际的垃圾渗滤液为研究对象,考察Fenton试剂氧化法处理垃圾渗滤液的效果及影响因素。
1 实验材料和测定方法
1.1 实验用水
实验用水取自贵州省某市的垃圾填埋场,该市人口在100万人左右,渗滤液取自填埋场进入调节池的出水口,渗滤液颜色呈黑褐色,有恶臭味,水质如表1所示:
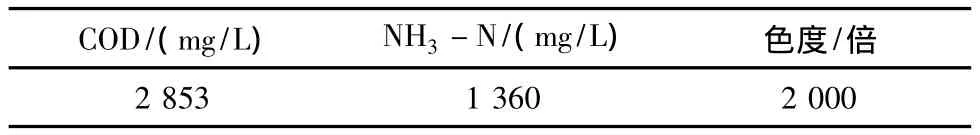
表1 垃圾填埋场垃圾渗滤液水质
1.2 实验仪器和药品
YHNH-100A型COD快速测定仪(江苏姜堰银河仪器有限公司),紫外可见分UV1601型光光度计(日本岛津),78-1型磁力搅拌器。
30% 的 H2O2,FeSO4·7H2O,NaOH,H2SO4,HgI2等均为分析纯,来自中国医药(集团)上海化学试剂公司和贵阳瑞晟化玻有限公司。
1.3 测试方法
量取100 ml垃圾渗滤液于200 ml的烧杯中,在BDS-307A型酸度计上用H2SO4或NaOH调节pH到一定值,再向溶液中加入一定量的FeSO4·7H2O和H2O2,迅速混合,控制反应温度为25±2℃,置于磁力搅拌器上反应一定时间后取出,调节其pH至8以上,静置一段时间后,取上清液测其COD和氨氮值。
2 结果与讨论
2.1 pH对处理效果的影响
控制实验参数 n(H2O2)∶n(Fe2+)=4∶1,反应时间设定为 1h,调节 pH=3、4、5、6、7,反应 1h 后调节其pH至8以上,静置一段时间后,取上清液测其COD值,结果如表2、图1所示。
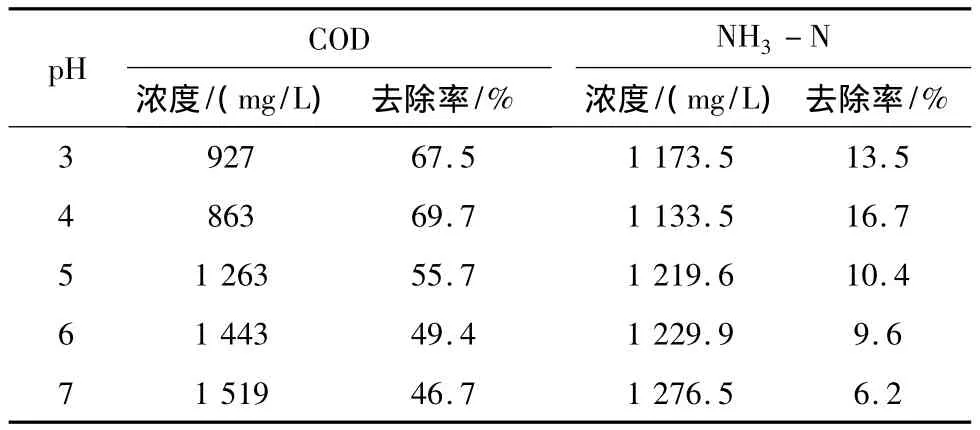
表2 不同pH条件下垃圾渗滤液COD和氨氮处理效果
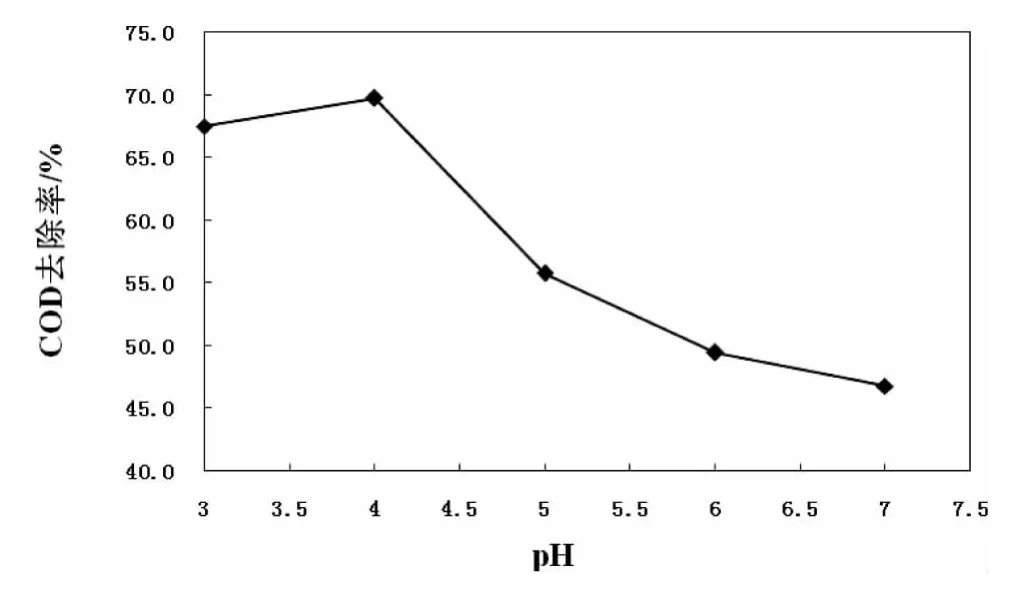
图1 不同pH条件下对COD去除率的影响
从图1可以看出,当pH=4时,反应的COD去除效果明显,去除率达到69.7%,但是随着pH的增大,去除效率在不断的下降。Fenton试剂主要是通过·OH自由基的氧化能力来处理污染物。Fenton试剂产生的Fe2+与H2O2反应产生·OH自由基,从而提高H2O2的分解速率。废水的pH过高和过低都会对COD的去除效果产生影响。当pH过高时,过量的OH-使溶液中的Fe2+以氢氧化物的形式沉淀而失去催化能力,并且抑制了·OH的产生,同时使得H2O2的氧化电势会降低,影响污染物的处理效果;当pH过低时,H+浓度会增高,Fe3+不能快速的被还原为 Fe2+,催化反应受阻。Fe2+、Fe3+的络合平衡体系会受到pH值变化的影响,从而影响Fenton试剂的氧化能力[5]。
2.2 时间对处理效果的影响
控制实验参数n(H2O2)∶n(Fe2+)=4∶1。反应 pH 设定为 4,反应时间为:0.5、1、1.5、2、2.5 h,反应1 h后调节其pH至8以上,静置一段时间后,取上清液测其COD值,结果如表3、图2所示。
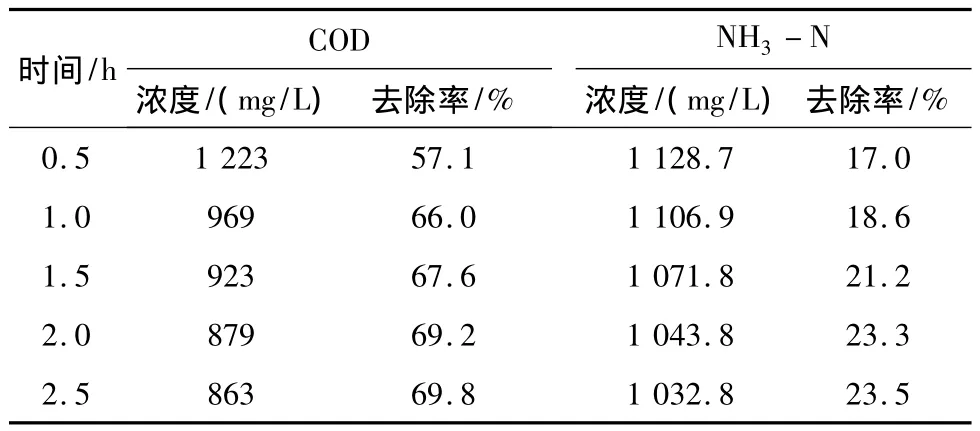
表3 不同时间条件下垃圾渗滤液COD和氨氮处理效果
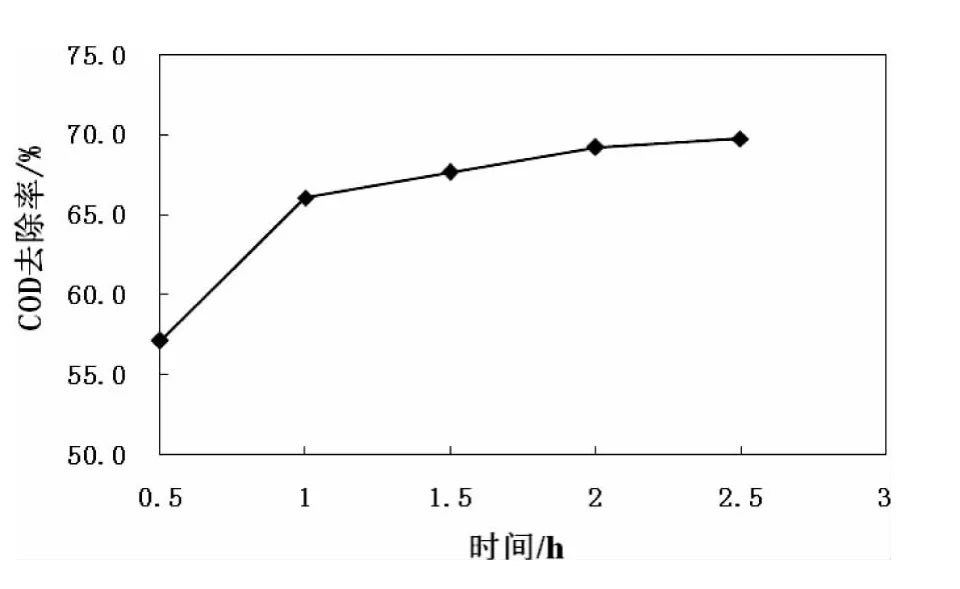
图2 反应时间对COD去除率的影响
从图2可以得到,COD去除效率随着反应时间的增加而增大,时间在0.5~1 h之间的去除率变化最大,反应时间1 h之后,COD去除率的上升趋势平缓,所以选定1 h为最佳反应时间。
2.3 双氧水用量对处理效果的影响
控制实验参数时间设定为1 h、pH设定为4,n(H2O2)∶n(Fe2+)=2、4、6、8、10,其中固定 Fe2+的量为 174 mg,改变 H2O2的用量:0.125、0.25、0.375、0.5、0.625 ml,反应 1h 后调节其 pH 至 8 以上,静置一段时间后,取上清液测其COD值,结果如表4、图3所示。

表4 双氧水用量变化的处理效果

图3 H2O2添加量对COD去除率的影响
从图3中得知,当n(H2O2)∶n(Fe2+)=4∶1时COD去除效果较好,达到63.7%。固定Fe2+的量,增加H2O2的投加量,COD去除率不仅没有无限增大,反而还会下降。这主要是因为,当H2O2投加量较低时,产生的·OH自由基较少,导致COD去除率较低;当H2O2投加量逐渐增大,COD去除率会提高;当投加的H2O2过量后,在反应开始阶段H2O2就将Fe2+迅速地氧化为Fe3+,抑制了·OH的生成。过量的H2O2破坏已经生成的·OH自由基,造成H2O2分解后并没有产生预想的效果[6]。
2.4 Fe2+用量对处理效果的影响
控制实验参数时间设定为1 h、pH设定为4,n(H2O2)∶n(Fe2+)=2、4、6、8、10,其中固定H2O2的量为 0.25 ml,改变 Fe2+的用量:348、174、116、87、69.6 mg,反应 1h 后调节其 pH 至 8 以上,静置一段时间后,取上清液测其COD值,结果如表5、图4所示。
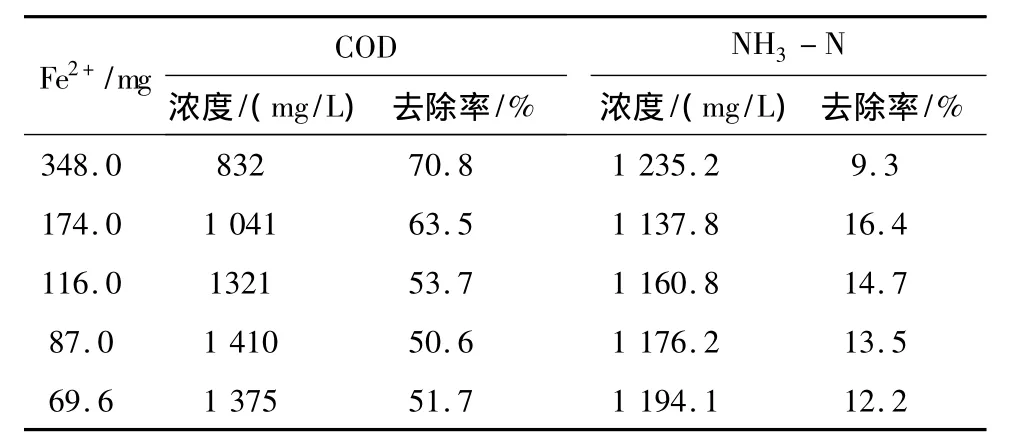
表5 Fe2+量变化的处理效果
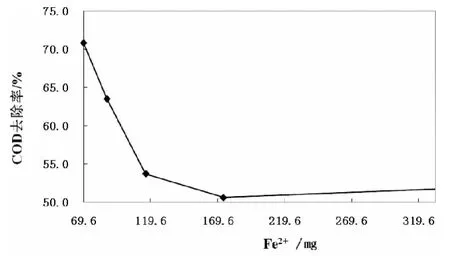
图4 Fe2+添加量对COD去除率的影响
由图4可知,当n(H2O2)∶n(Fe2+)=2时,H2O2的用量为2.5 ml/L,Fe2+的用量为3.48 g/L。此时的处理效果比其它比例的都好,达到了70.8%。随着Fe2+投加量的减少,COD去除率在不断地下降。开始的时候,投加的Fe2+过量,过量的Fe2+导致H2O2快速分解产生·OH自由基,造成·OH自由基之间快速反应,抑制了·OH自由基对有机物物质的降解作用;当Fe2+的投加量过低时,H2O2的分解速度极慢,分解产生·OH自由基的产生量和产生速度都会降低,降解过程受到抑制[7]。
2.5 氨氮去除率
氨氮的去除率较低可能是由多种情况共同影响产生的:Fenton法的pH值较低,影响了铵离子平衡体系。产生的羟基自由基在氧化过程中,首先与C-H键接触发生反应,对于氨氮的氧化也会产生影响。具体的氧化机理还要通过进一步的研究来取得。
3 结论
Fenton试剂处理垃圾渗滤液取得了良好的效果,可将原水的COD从2 853 mg/L降到832 mg/L,去除率达到70.8%。通过实验确定反应的最佳条件为:初始pH为4,反应时间为1 h,H2O2加入量为2.5 ml/L,FeSO4·7H2O 加入量为3.48 g/L。Fenton试剂法对氨氮的去除效果不明显,尚值得进一步深入研究。
[1]Poznyak T,Bautista G L,Chairez I,et a1.Decomposition of toxic pollutants in landfill leachate by ozone after coagulation treatment[J].Journal of Hazardous Materials,2008,152(3):1108-1114.
[2]Primoo,Rueda A,Rivero M J,et a1.An integrated process,Fenton reaction- ultrafiltration,for the treatment of landfill leachate:pilot plant operation and analysis[J].Ind Eng Chem Res,2007.47(3).
[3]唐琼瑶,何品晶,徐苏云,等.新鲜渗滤液与长填埋龄渗滤液的Fenton处理过程特征[J].环境科学,2008,29(11):3258-3264.
[4]Pigllatello J J.Dark and photoasisited Fe3+—Catalyzed Degradation of Chlorophenoxy Herbicides by Hydrogen Peroxide[J].Enviro.Sci.Techno1,1992,26(6):944 -951.
[5]张萍.Fenton试剂处理垃圾渗滤液技术进展的研究[J].环境卫生工程,2004,12(1):28 -31.
[6]许海燕,李义久,刘亚菲.Fenton-混凝催化氧化法处理焦化废水的影响因素[J].复旦学报,2003,42(3):440-444.
[7]李晋,刘丹.Fenton法处理模拟生物反应器填埋场“老龄”渗滤液的实验[J].环境卫生工程,2005,13(3):30-32.
