[Co(NTB)Cl]2[CoCl4]·4CH3OH的合成、晶体结构和超氧化物歧化酶模拟活性
2014-09-07张若璇陈世明马志刚陈雪梅
张 勇,张若璇,陈世明,王 强,李 伟,马志刚,陈雪梅
(1湖北理工学院 化学与材料工程学院,湖北 黄石 435003;2黄石市中心医院,湖北 黄石 435000)
[Co(NTB)Cl]2[CoCl4]·4CH3OH的合成、晶体结构和超氧化物歧化酶模拟活性
张 勇1,张若璇1,陈世明2,王 强1,李 伟1,马志刚1,陈雪梅1
(1湖北理工学院 化学与材料工程学院,湖北 黄石 435003;2黄石市中心医院,湖北 黄石 435000)

超氧化物歧化酶;晶体结构;NBT光照还原法;模拟活性
超氧化物歧化酶(Superoxide Dismutase,SOD)广泛存在于各类动物、植物和微生物中,它能够清除超氧化物,保护细胞免受氧化损伤,是一种体内免除自由基损伤的主要防御酶。研究表明,SOD与某些癌症或糖尿病等疾病有关,能延缓人和动物衰老,具有提高植物的抗寒、抗旱和抗病害能力[1-3]。天然SOD具有分子量大、易透过细胞膜、保存期短和价格昂贵等缺点,难以在工农业等方面推广应用,因此,用化学方法来合成小分子量的SOD模拟物成为当前研究的热点之一[4-7]。SOD以多种常见形式存在, 根据金属辅基的不同可将超氧化物歧化酶分为Cu-Zn-SOD, Mn-Fe-SOD, Fe-SOD 和Ni-SOD等。钴是人体必需的一种微量元素,在生物体内均以配合物的形式存在。它可作为一种优良的探针离子取代金属蛋白和金属酶中Zn(Ⅱ)、Fe(Ⅱ)、Cu(Ⅱ)等离子而具有载氧、氧化还原、水解等作用,这使得钴配合物的研究在药理学、配位化学以及生物无机化学方面具有重要意义[8-10]。本文选用含有苯并咪唑的配体(2-苯并咪唑亚甲基)胺(C24H21N7,NTB) 来模拟SOD活性中心的组氨酸残基,合成和表征了一种没有报道过的以钴(Ⅱ)为中心的SOD模型化合物,并用NBT光照还原法对它进行了SOD的活性检测。
1 实验部分
1.1仪器与试剂
除邻苯二胺和氨三乙酸为化学纯以外,实验所用试剂均为市售分析纯。所用仪器为PHS- 3C酸度计,Perkin-Elmer 2400元素分析仪, Perkin-Elmer 1700 红外光谱仪(KBr 压片法),HP 8453 UV-Vis紫外光谱仪, 722型分光光度计,晶体结构测定使用Brucker Smart-2000 CCD 单晶衍射仪。
1.2配合物的合成
配体NTB参照文献[11]的方法合成。称取0.26 g (1.1 mmol) CoCl2·6H2O和0.41 g (1 mmol)配体NTB,将它们一起加入到40 mL甲醇溶液中,然后在搅拌条件下于60 ℃加热反应3 h,冷却至室温后,过滤,静置数天后得到了适合X射线单晶衍射测试的红色块状晶体,产率:45%. mp 142~143 ℃.UV-Vis spectra [λmax,nm (ε,L mol-1cm-1)]:(MeOH solution)282(22750). IR (KBr, cm-1):3325,1668,1465,1386,748 cm-1.Anal.Calcd for C52H58Cl6N14O4Co3:C,46.85;H,4.35;N,14.71;Found:C,46.55;H,4.58;N,15.02。
1.3晶体的测定
选取大小为0.23 mm × 0.12 mm × 0.10 mm 的红色块状标题化合物单晶置于Brucker Smart-2000 CCD单晶衍射仪上, 采用石墨单色化的Mo Kα射线(λ=0.071 073 nm),于298(2) K, 以ω/2θ方式扫描, 在1.93°<θ<25.00°范围内共收集到衍射点37 578个, 其中独立衍射点10 967个(Rint=0.048 5),I>2σ(I)的可观测的衍射点9 446个。全部衍射数据经Lp因子和经验吸收校正。晶体结构由直接法解出,非氢原子坐标在以后的数轮差值Fourier合成中陆续确定。对全部氢原子的坐标及各向异性参数用SHELXS-97程序,以最小二乘法对结构进行精修。标题化合物的剑桥晶体数据库编号:CCDC 933484。
1.4 SOD模拟活性实验
NBT光照还原法测定配合物的SOD模拟活性参照文献[12]的方法。 用0.05 mol·L-1磷酸缓冲溶液(pH 7.8)配制含6.80×10-6mol·L-1的核黄素,1.0×10-4mol·L-1的四甲基乙二胺,9.32×10-5mol·L-1的NBT和系列浓度(0~1.0×10-4mol ·L-1)的标题配合物溶液。室温下,用恒定光强(50 500±500 lx)的冷光灯照射, 固定测定波长560 nm,用722型分光光度计测定混合溶液每光照一分钟的吸光度。实验温度用水浴锅控制为25 ℃,每个样品平行测定3个数据,然后取平均值,每种浓度测定10个点,以不加配合物的作为空白对照实验。
2 结果与讨论
2.1配合物的结构
配合物紫外光谱图中282 nm处的吸收归属为苯并咪唑环π-π*跃迁。配合物的红外光谱图中,3 325 cm-1归属为溶剂分子甲醇的υ(O-H),1 668,1 465归属为苯环骨架振动,1 386 cm-1为溶剂分子甲基的C-H弯曲振动,748 cm-1为苯环面外伸缩振动。标题配合物的结构示意图见图 1,其晶体参数列于表 1,重要键长和键角列于表 2。在标题配合物的晶体结构中(图 2),中心离子Co2+的配位构型有2种:一种是在[CoCl4]2-中,Co2+与4个Cl-形成近似于正四面体的构型(Cl(3)-Co(3)-Cl(4),Cl(3)-Co(3)-Cl(6),Cl(3)-Co(3)-Cl(5),Cl(6)-Co(3)-Cl(5),Cl(4)-Co(3)-Cl(5),Cl(4)-Co(3)-Cl(6)的键角分别为111.8(3)°,110.2(2)°,109.97(19)°,107.5(3)°,109.30(18)°,107.94(19)°);另一种是在[Co(NTB)Cl]-中,中心离子Co2+的配位构型为变形的三角双锥结构,其中苯并咪唑N2,N4,N6(或N9,N11,N3)形成三角平面,烷氨氮N1(或N8)和氯原子Cl1(或Cl2)处于三角双锥的2个顶点,其中Cl(1)-Co(1)-N(1)和Cl(2)-Co(2)-N(8)的键角分别为176.4(2)°和176.3(2)°,稍微偏离了理想的180°键角。在分子中有2个[Co(NTB)Cl]-,这是由于它们不对称导致的。配合物中心离子Co2+与烷胺氮之间的距离[Co(1)-N(1),Co(2)-N(8)]明显长于其与苯并咪唑氮的距离[Co(1)-N(4),Co(1)-N(2),Co(2)-N(11),Co(2)-N(9)]。此外,配合物的阴离子[CoCl4]-的4个Co-Cl键长分别为2.272(4),2.294(4),2.236(6),2.252(5),这也从键长的角度表明它为不规则的四面体构型。从化合物的晶胞堆积图(图3)可以看出,相邻分子间苯并咪唑环存在π-π堆积作用;此外,溶剂甲醇的氧原子、氯离子和苯并咪唑的氮原子相互作用形成O-H…Cl,C-H…Cl,N-H…O,N-H…Cl等多种氢键,这使得化合物彼此形成三维网络结构(表 3)。
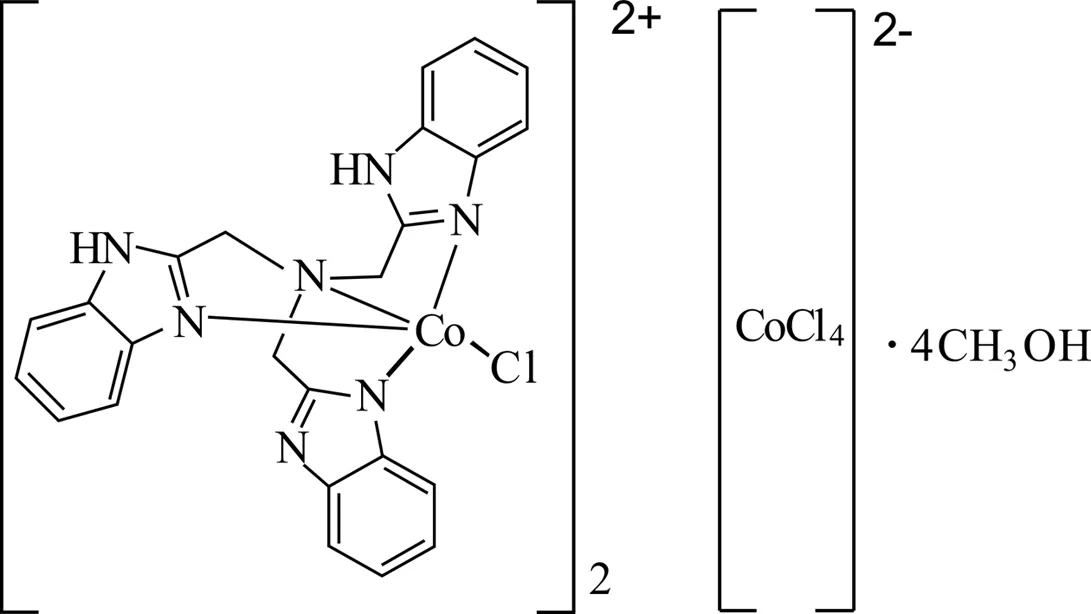
图1 标题配合物的结构示意图

图2 标题配合物的晶体结构

表1 标题配合物的晶体学数据和精修参数

表2 标题配合物的部分键长和键角(°)数据
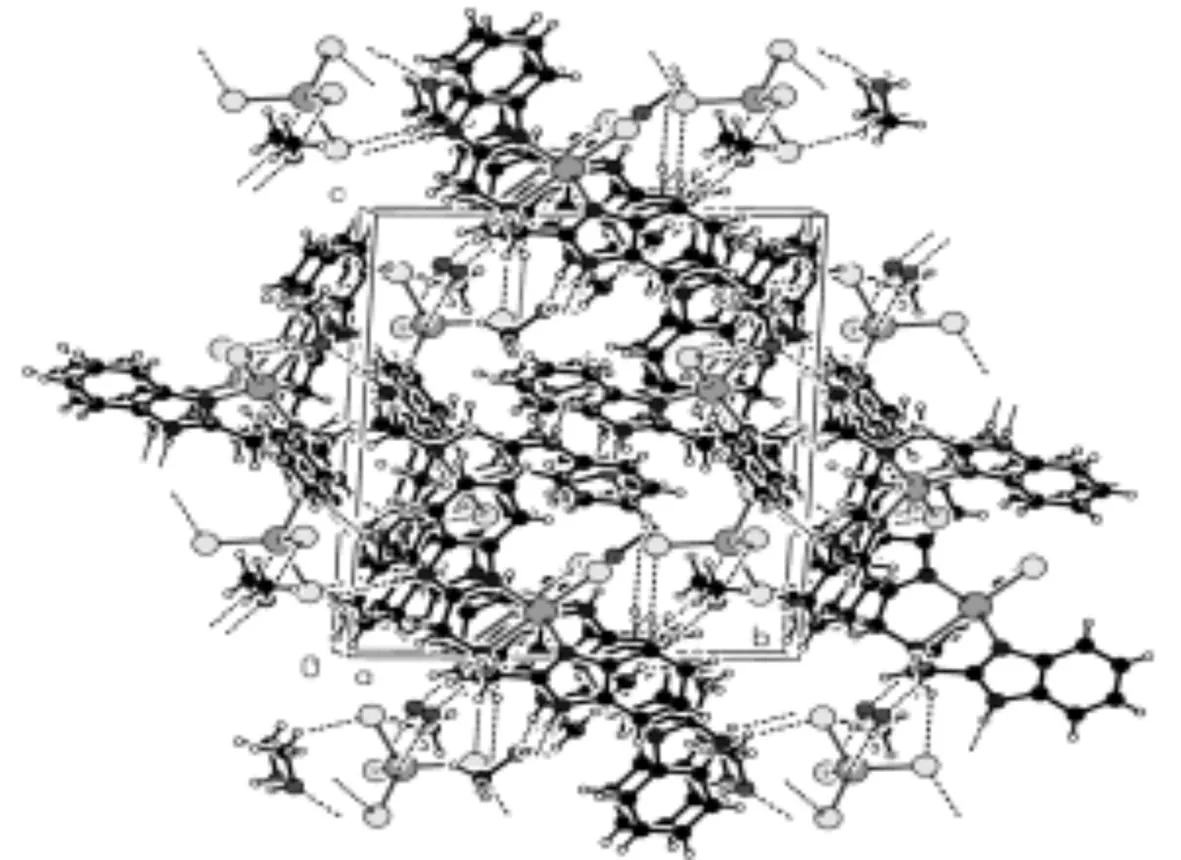
图3 标题配合物的晶胞堆积图

表3 标题配合物的氢键数据
注:#1 -x,-y,-z+1;#2 -x+1,-y+1,-z+1;#3x,y-1,z;#4 -x+1,-y+1,-z。
2.2 SOD模拟活性


图4 标题配合物在不同浓度时溶液的吸光度随时间变化([complex]a-e=0,6.0×10-5,8.0×10-5,1.0×10-4,1.2×10-4 mol ·L-1)
3 结论
用X射线单晶衍射等方法表征了单核钴配合物[Co(NTB)Cl]2[CoCl4]·4CH3OH,它具有一定的SOD模拟活性,IC50为0.884 μmol·L-1,而且催化O2歧化分解速度随着其浓度增加而增加。
[1] 廖展如,陈战芬,孟祥高,等.金属拟酶抗逆剂的设计与合成[J].华中师范大学学报(自然科学版),2003,37(3):336-342.
[2] 魏文树,曾昭全,刘锡钧.超氧化物歧化酶模拟物研究进展[J].药物生物技术,2003,10(4):256-260.
[3] Lin L,Jiang D,Alex M,et al.Copper Redox Cycling in the Prion Protein Depends Critically on Binding Mode[J].J.Am.Chem.Soc.,2011,133(31):12229-12237.
[4] 孙薇,杨晓虹,周小平.锰超氧化物歧化酶模拟物的研究进展[J].中国药物化学杂志,2005,15(1):55-59.
[5] 李晨,杨征,厍梦尧,等.超氧化物歧化酶化学模拟的新进展[J].高等学校化学学报,2011,32(9):2046-2061.
[6] 赵绘,高鹏,慕向宾,等.不同离子型超氧化物歧化酶模拟物(SODM)对水稻产量与品质的影响[J].安徽农学通报,2012,18(1):54-55.
[7] 吕静,韩莉梅,张所有.超氧化物歧化酶模拟物(SODM)对大豆保护酶系统的影响[J].黑龙江农业科学,2013(1):23-26.
[8] Kaushik G,Varun M,Pramod K,et al.DNA binding, nuclease and superoxide scavenging activity studies on mononuclear cobalt complexes derived from tridentate ligands[J].Polyhedron,2013,49(1):167-176.
[9] 朱莉,廖展如.钴配合物的合成表征及超氧化物歧化酶活性的研究[J].湘潭大学自然科学学报,2001,23(4):63-66.
[10] Zhang Y,Meng X G,Liao Z R,et al.Synthesis,structures and polyphenol oxidase activities of dicopper and dicobalt Complexes[J].J.Coord.Chem.,2009,62:876-885.
[11] 郭洪声,王敏,王瑾玲.三(2-苯并咪唑亚甲基)胺的合成及其晶体结构的测定[J].武警医学院学报,1997,6(1):23-24.
[12] 古琴,林庆斌,乐学义.TATP-铜(Ⅱ)-L-氨基酸配合物的合成、表征及其SOD活性[J].化学通报,2007,70(6):450-455.
[13] 丁杨,邓剑生,乐学义.(甘氨酰-β-丙氨酸)(二吡啶[3,2-d:2',3'-f]喹喔啉)铜(II)配合物合成、结构及其超氧化物歧化酶活性[J].有机化学,2011,31(7):1081-1086.
(责任编辑吴鸿霞)
Synthesis,Crystal Structure of [Co(NTB)Cl]2[CoCl4]·4CH3OH and Its Superoxide Dismutase Mimic Activity
ZhangYong1,ZhangRuoxuan1,ChenShiming2,WangQiang1,LiWei1,MaZhigang1,ChenXuemei1
(1School of Chemical and Materials Engineering,Hubei Polytechnic University,Huangshi Hubei 435003;2Huangshi Central Hospital,Huangshi Hubei 435000)
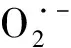
superoxide dismutase;crystal structure;NBT photoreduction method;mimic activity
2013-09-05
国家自然科学基金项目(项目编号51173060)。
张勇(1978— ),男,讲师,博士,研究方向:金属模拟酶, 小分子螯合药物和荧光探针的设计、合成和应用。
10.3969/j.issn.2095-4565.2014.01.012
O614.81+2
A
2095-4565(2014)01-0048-05
