新型气相毛细管柱的制备及对苯系位置异构体的色谱分离
2014-08-28贾成俊郑盛润章伟光
贾成俊, 颜 霞, 范 军, 郑盛润, 章伟光
(华南师范大学化学与环境学院,广州 510006)
1958年,Golay首先发展了毛细管气相色谱技术[1]. 毛细管气相色谱使用简单、快速和高效,在科学研究和工业技术中应用广泛[2-3].目前常用的气相色谱固定相有聚硅氧烷型[4]、冠醚类[5]、聚乙二醇类[6]、高分子液晶[7]、离子液体[8-9]、环糊精衍生物[10-11]和金属有机骨架材料[12-13]等. 其中,环糊精(CD)呈外部亲水、内部疏水结构,可作为主体包合客体,如有机分子、无机离子和气体分子等. König等[14]最早应用环糊精衍生物液相色谱法分离氨基酸和二醇等对映异构体,它们对手性化合物展现了良好的拆分性能[15-16].另一方面,páanik等[17]采用环糊精衍生物作为固定相气相色谱法分离苯系和烷烃同系物. 傅若农等[18-19]开发了一系列涂覆环糊精衍生物的气相毛细管柱,比较了它们对10种苯系物位置异构体的分离性能的差异. 本课题组研究了多叠氮对氯苯氨基甲酰化-β-环糊精、全取代对氯苯氨基甲酰化-β-环糊精和单叠氮乙酰化-β-环糊精等3种固定相在气相色谱中对二氯苯、硝基氯苯和硝基甲苯等位置异构体的分离性能[20].
本研究分别将羟丙基-β-环糊精(HP-β-CD)和七-(2,6-O-二戊基-3-O-三氟乙酰基)-β-环糊精(DP-TFA-β-CD)(图1)静态涂覆在毛细管内得到了2种涂覆环糊精衍生物的气相毛细管柱,研究它们对硝基甲苯、硝基氯苯、二氯苯、二甲苯和苯二甲酸二甲酯等的位置异构体的分离性能. DP-TFA-β-CD是一款商品化涂覆型毛细管柱的固定相材料,文献报道其对许多手性化合物具有很好的拆分性能[21].
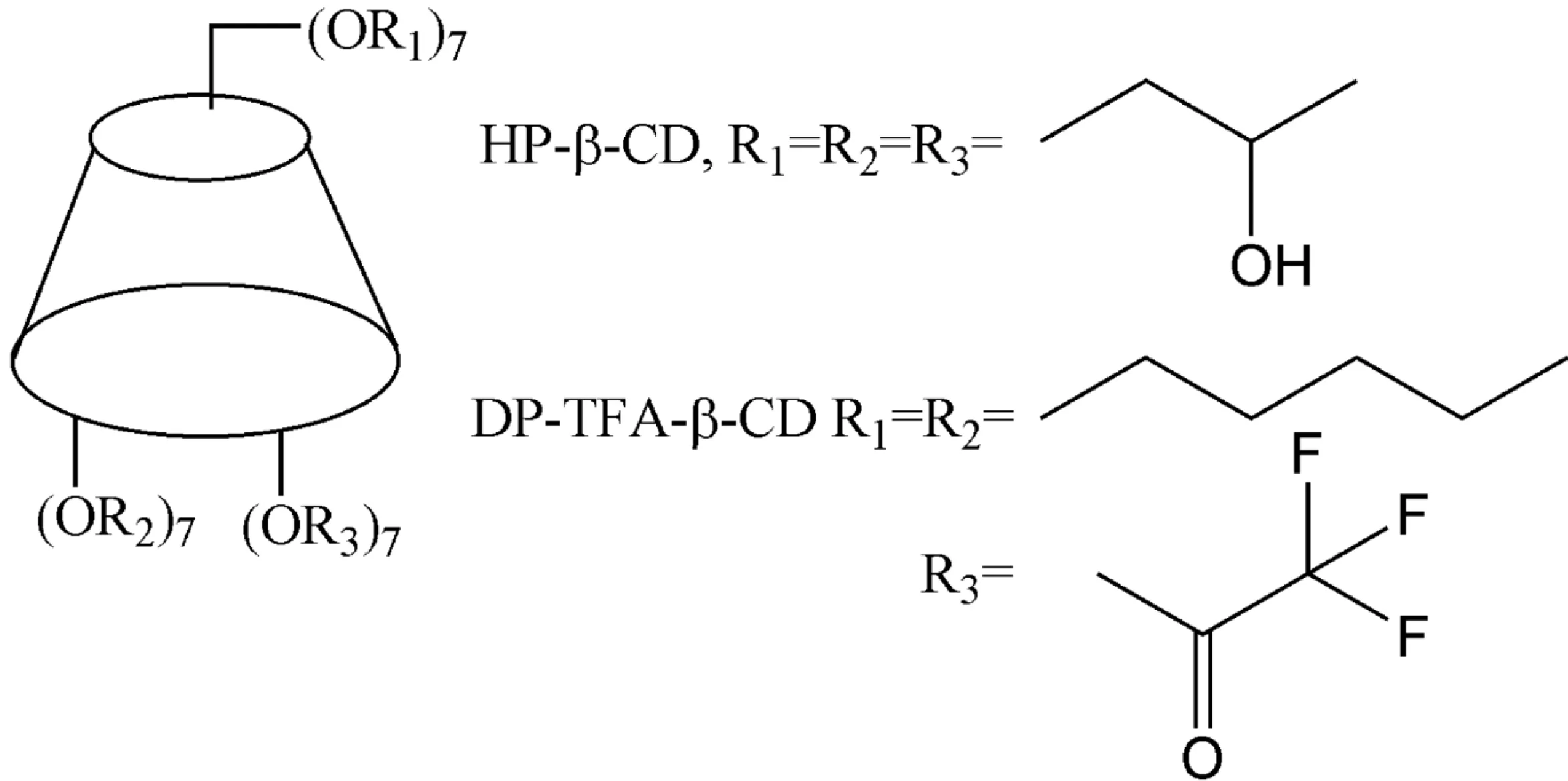
图1 HP-β-CD和DP-TFA-β-CD的结构示意图
Figure 1 Molecular structures of HP-β-CD and DP-TFA-β-CD
1 实验部分
1.1 仪器与试剂
GC1690型气相色谱仪(广州科晓仪器公司),配备氢火焰离子化检测器(带N3000工作站);弹性石英毛细管柱(10 m×φ0.32 mm,河北永年光纤厂).
羟丙基-β-环糊精(HP-β-CD)购于广东郁南县永光环状糊精有限公司.七-(2,6-O-二戊基-3-O-三氟乙酰基)-β-环糊精(DP-TFA-β-CD)参考文献[21]方法制备,产率为86%.其他试剂为分析纯,直接使用.
1.2 气相毛细管柱的制备
将弹性石英毛细管柱在240~260 ℃、通N2预加热处理2 h;然后将0.5%的环糊精衍生物的CH2Cl2溶液静态涂渍在毛细管内表面,真空脱去溶剂;再从40 ℃起梯度升温至180 ℃,保持6 h. 根据涂渍的固定相不同,分别标记为HP-β-CD柱和DP-TFA-β-CD柱.
1.3 色谱条件
载气为高纯氮气(纯度99.99%),载气流速为25.5 cm/s;柱温低于180 ℃,气化室温度为250 ℃,检测器温度为250 ℃;溶质质量浓度为1.00 g/L,进样量为0.5 μL,分流比为80∶1.
2 结果与讨论
2.1 色谱柱的理论塔板数和极性
在柱温120 ℃下,用正十二烷为标准物分别对HP-β-CD柱和DP-TFA-β-CD柱进行评价.正十二烷在HP-β-CD柱和DP-TFA-β-CD柱上的保留时间分别为7.975、8.292 min,计算得到色谱柱的理论塔板数分别为2 337/m和2 562/m,不对称因子分别为1.121和1.017,说明这2种毛细管柱具有较高的柱效. 但由于DP-TFA-β-CD在CH2Cl2中的溶解性能比HP-β-CD好,在毛细管内更容易涂覆成膜,因而DP-TFA-β-CD柱具有更高的柱效.
图2中,正构烷烃(C6-C12)在毛细管柱的出峰顺序与其分子量和沸点顺序一致.配制1-硝基丙烷、吡啶、2-戊酮、1-丁醇和苯溶液,考察其在HP-β-CD柱和DP-TFA-β-CD柱的保留行为.根据文献[22-23]计算得到2种毛细管柱的麦氏常数(表1). 在5种底物中,苯的麦氏常数最小,说明苯与2种毛细管柱上涂覆的环糊精间的作用力较小;2-丁醇在HP-β-CD柱上的麦氏常数最大,说明2-丁醇与HP-β-CD的分子间作用强,保留较强.另外,HP-β-CD柱的麦氏常数平均值为212.2,对于DP-TFA-β-CD柱,其平均值为183.9,说明它们均为中等极性的固定相.
2.2 毛细管柱对Grob试剂的分离性能
Grob试剂由1-正壬醛、正十二烷、癸酸甲酯、二环己胺和十二酸甲酯等按比例混合而成,常用其来考察毛细管柱对不同底物的分离性能. 图3中,HP-β-CD 柱和DP-TFA-β-CD柱对Grob试剂中的5种组分都实现基线分离,且在2种柱上出峰顺序相同,1-正壬醛最先被洗脱,然后依次是正十二烷、癸酸甲酯和二环己胺,最后十二酸甲酯被洗脱,说明2种毛细管柱对酯类和胺类化合物有很强的保留作用,可解释为这些分析物易与环糊精衍生物上的官能团(如羟基和酯羰基)形成较强的氢键作用,分析物在色谱柱上的保留增强. 正十二烷和1-正壬醛与环糊精衍生物间主要通过疏水相互作用和范德华力产生作用,故保留较弱,最容易被洗脱.
2.3 对苯系位置异构体的分离
各种苯系位置异构体是重要的工业原料和化学试剂,也是造成环境污染的主要化学物质,对其进行分离检测具有重要的理论意义和应用前景. 本文以硝基甲苯、硝基氯苯、二氯苯、二甲苯和苯二甲酸二甲酯等为分析物,分别考察HP-β-CD柱和DP-TFA-β-CD柱对它们的分离性能(表2).
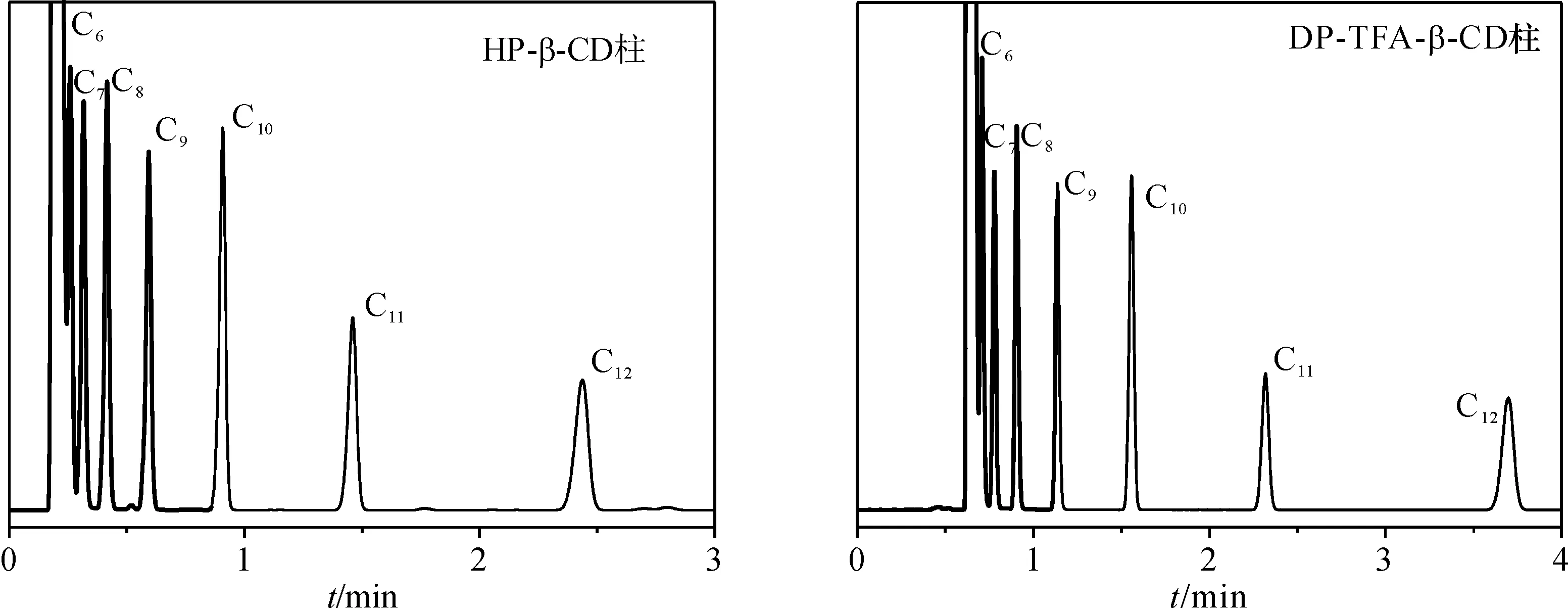
图2 正构烷烃(C6-C12)在2种环糊精衍生物气相毛细管柱上的色谱图

毛细管柱种类固定相 X'Y'Z'U'S'总和平均值HP-β-CD柱74.8284.8261.8265.5173.91 060.8212.2DP-TFA-β-CD柱60.8173.1280.5259.7145.5949.5183.9
注:X′:苯;Y′:1-丁醇;Z′:2-戊酮;U′:1-硝基丙烷;S′:吡啶.
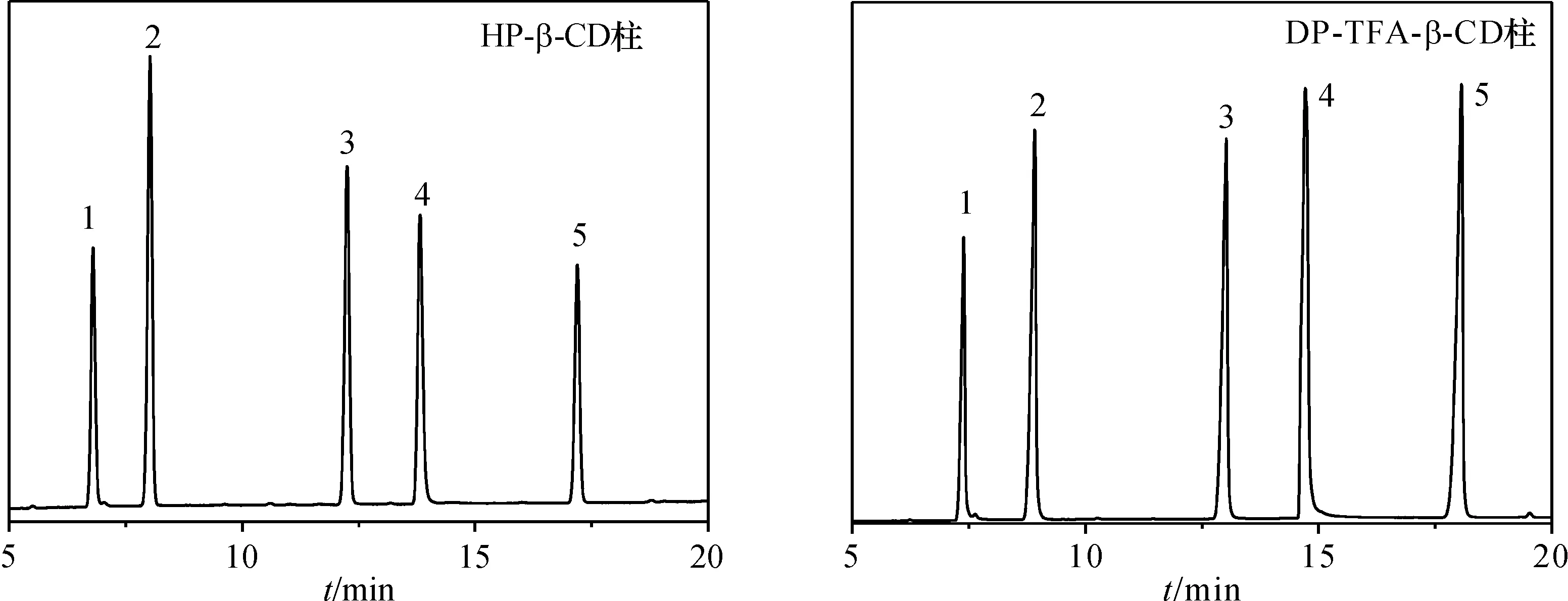
(1: 1-正壬醛; 2: 正十二烷; 3: 癸酸甲酯;4: 二环己胺;5:十二酸甲酯)
结果表明,5种苯系化合物的位置异构体(邻、间和对位)在HP-β-CD 柱和DP-TFA-β-CD柱上的洗脱顺序相同. 分析物的结构对保留行为和分离产生了明显影响. 在5种分析物中,含有硝基(如硝基甲苯和硝基氯苯)或酯基的化合物(如苯二甲酸二甲酯)在柱上的保留时间较长,从柱上洗脱困难,这与2.1和2.2部分中底物在柱上的保留行为一致;而二氯苯和二甲苯等在柱上的保留较弱,保留因子较小. 尽管适宜样品分离的最佳温度存在差异,但它们在柱上的保留行为变化趋势一致. 同时,底物在毛细管柱上过强的保留反而使位置异构体的分离效果变差,如苯二甲酸二甲酯在2种柱上的分离因子仅为1.06/1.09 (对于HP-β-CD柱)和1.15/1.06 (对于DP-TFA-β-CD柱);二氯苯在HP-β-CD柱的分离因子分别为1.28和1.13,在DP-TFA-β-CD柱上的分离因子分别为1.14和1.08,相同温度条件下,二氯苯在HP-β-CD柱上的保留比DP-TFA-β-CD柱上弱.

表2 5种苯系位置异构体在2种毛细管柱上的分离结果Table 2 Chromatographic separation results of five disubstituted benzene compounds on two capillary columns by GC
2.4 环糊精衍生物结构对二甲苯分离性能的影响
环糊精上衍生基团的结构对分析物的分离产生影响. 将本文中二甲苯位置异构体在环糊精柱上的分离结果与文献结果进行对比(表3).
邻和间二甲苯在HP-β-CD柱的分离因子为1.26,在表3中列出的6种环糊精衍生物中为最大值,HP-β-CD柱对邻和间二甲苯的分离表现出优势;在涂覆全甲基-β-环糊精和全戊基-β-环糊精上的柱上的分离效果次之,而涂覆七-(2, 6-O-月桂基-3-O-乙酰基)-β-环糊精和七-(2, 6-O-月桂基-3-O-三氟乙酰基)-β-环糊精的毛细管柱对其没有分离能力. 这意味着在环糊精上2, 6-位引入体积过大的取代基(如月桂基)会增大空间位阻,进而影响环糊精与二甲苯间的相互作用,使其分离能力减弱.
表3二甲苯位置异构体在不同环糊精衍生物气相
毛细管柱的分离因子
Table 3 Separation factors (α) of xylene positional isomers on different capillary columns by gas chromatography

涂覆的环糊精衍生物种类分离因子(α)HP-β-CD柱羟丙基-β-环糊精1.08, 1.26柱 1全甲基-β-环糊精[24]1.03, 1.19柱 2全戊基-β-环糊精[18]1.06, 1.19柱 3七-(2,6-O-月桂基-3-O-甲基)-β-环糊精[18]1.10, 1.13柱 4七-(2,6-O-月桂基-3-O-乙酰基)-β-环糊精[18]inseparable柱 5七-(2,6-O-月桂基-3-O-三氟乙酰基)-β-环糊精[18]inseparable柱 6七-(2,6-O-戊基-3-O-苄基)-β-环糊精[25]1.06, 1.05
3 结论
将羟丙基-β-环糊精(HP-β-CD)作为固定相静态涂覆于毛细管内壁,得到了一种新型毛细管气相色谱柱. 柱的理论塔板数为2 337/m,呈中等极性,对一些二取代苯系位置异构体(如硝基甲苯、硝基氯苯、二氯苯、二甲苯和苯二甲酸二甲酯)表现出了较好的分离性能;将其与商品化气相固定相七-(2, 6-O-二戊基-3-O-三氟乙酰基)-β-环糊精(DP- TFA-β-CD)相比,对二氯苯和二甲苯的分离显现了一定优势.
参考文献:
[1] Golay M J E. Theory and practice of gas liquid partition chromatography with coated capillaries[M]. New York: Academic Press, 1978: 17.
[2] Clement R E. Gas chromatography: Biochemical, biomedical, and clinical applications[M]. New York: Wiley-Interscience, 1990: 256.
[3] Maštovská K, Hajšlová J, Godula M, et al. Fast temperature programming in routine analysis of multiple pesticide residues in food matrices[J]. Journal of Chromatography A, 2001, 907(1/2): 235-245.
[4] Wu C Y, Cheng J S, Zeng Z R. The selectivity of crown ether polysiloxane stationary phases[J]. Chromatographia,1993, 35(1/2):33-37.
[5] Jing P, Fu R N, Dai R, et al. Consequence of diluting modified β-cyclodextrins in a side-chain crown ether polysiloxane and in a side-chain liquid-crystalline polysiloxane-containing crown ether as stationary phases in capillary gas chromatography[J]. Chromatographia, 1996, 43(9/10): 546-550.
[6] Silva B J, Tranchida P Q, Purcaro G, et al.Evaluation of comprehensive two-dimensional gas chromatography coupled to rapid scanning quadrupole mass spectrometry for quantitative analysis[J]. Journal of Chromatography A, 2012,1255(14):177-183.
[7] Kelker H. Kristallin-flüssige schmelzen als stationäre phasen in der gas-flüssigkeits-verteilungs chromatographie[J]. Fresenius Journal of Analytical Chemistry, 1963, 198(3):254-266.
[8] Grisales J O, Lebed P J, Keunchkarian S. Permethylated β-cyclodextrin in liquid poly(oxyethylene) as a stationary phase for capillary gas chromatography[J]. Journal of Chromatography A, 2009, 1216 (40): 6844-6851.
[9] Poole C F, Poole S K.Ionic liquid stationary phases for gas chromatography[J]. Journal of Separation Science, 2011, 34(8): 888-900.
[10] Liang M M, Qi M L, Zhang C B, et al. Peralkylated-β-cyclodextrin used as gas chromatographic stationary phase prepared by sol-gel technology for capillary column[J]. Journal of Chromatography A, 2004, 1059(1/2): 111-119.
[11] Shi X Y, Guo H C, Wang M. Enantioseparation of chiral epoxides using four new cyclodextrin derivatives as chiral stationary phases of capillary gas chromatography[J]. Analytica Chimica Acta, 2005, 553(1/2): 43-49.
[12] Gu Z Y, Yang C X, Chang N, et al. Metal-organic frameworks for analytical chemistry: From sample collection to chromatographic separation[J].Accounts of Chemical Research, 2012, 45(5): 734-745.
[13] Fang Z L, Zheng S R, Tan J B, et al. Tubular metal-organic framework-based capillary gas chromatography column for separation of alkanes and aromatic positional isomers[J]. Journal of Chromatography A, 2013, 1285: 132-138.
[14] König W A, Lutz S, Wenz G, et al. Cyclodextrins as chiral stationary phase in capillary gas chromatography: Part II: Heptakis(3-O-acetyl-2, 6-di-O-pentyl)-β-cyclodextrin[J]. Journal of High Resolution Chromatography, 1988, 11(7): 506-509.
[15] Lin C, Liu W N, Fan J, et al. Synthesis of a novel cyclodextrin-derived chiral stationary phase with multiple urea linkages and enantioseparation toward chiral osmabenzene complex[J]. Journal of Chromatography A, 2013, 1283: 68-74.
[16] 林纯,章伟光,范军,等.手性分子识别与分离研究进展[J].华南师范大学学报:自然科学版,2014,46(3):1-9.
Lin C,Zhang W G,Fan J, et al. Progress in recognition and resolution of enatiomers[J]. Journal of South China Normal University: Natural Science Edition, 2014, 46(3):1-9.
[18] Xiao D Q, Ling Y, Fu R N, et al. Investigation on five novel substituted β-cyclodextrins used as GC stationary phases[J]. Chromatographia,1998, 47(9/10): 557-564.
[19] Xiao D Q, Ling Y, Wen Y X, et al. Synergistic effect of resorcarene and cyclodextrin mixed stationary phase in gas chromatography[J]. Chromatographia,1997, 46(3/4):177-182.
[20] 颜霞, 方智利, 林纯, 等. 环糊精衍生物涂渍毛细管柱的制备及分离性能[J]. 应用化学, 2013, 30(8):957-962.
Yan X, Fang Z L, Lin C, et al. Preparation and separation performance of three new gas chromatography capillary columns coated with cyclodextrin derivatives[J]. Chinese Journal of Applied Chemistry, 2013, 30(8):957-962.
[21] Li W Y, Jin H L, Armstrong D W. 2,6-Di-O-pentyl-3-O-trifluoroacetyl cyclodextrin liquid stationary phases for capillary gas chromatographic separation of enantiomers[J]. Journal of Chromatography A, 1990, 509(2): 303-324.
[22] McReynolds W O. Characterization of some liquid phases[J]. Journal of Chromatographic Science, 1970, 8(12): 685-691.
[23] 傅若农, 刘虎威. 高分辨气相色谱及高分辨裂解气相色谱[M]. 北京: 北京理工大学出版社, 1992: 83-84.
[24] 何林,尹红锋,黄爱今,等. 用全甲基化β-环糊精石英毛细管色谱柱分离苯的多元取代物异构体[J]. 北京大学学报:自然科学版, 1993, 29(4):423-427.
He L, Yin H F, Huang A J, et al. Permethylated β-cyclodextrin as a stationary phase of fused-silica open tubular column for the separation of substituted benzene[J]. Acta Scientiarum Naturalium Universitatis Pekinensis, 1993, 29(4): 423-427.
[25] 史雪岩,邵青龙, 陶丹妮,等. 一种苄基取代的环糊精衍生物的合成及其气相色谱性能研究[J]. 高等学校化学学报, 2001, 22(7):1098-1101.
Shi X Y, Shao Q L, Tao D N, et al. Synthesis and GC properties of heptakis(2,6-di-O-pentyl-3-O-benzyl) -β-cyclodextrin[J]. Chemical Journal of Chinese Universities, 2001, 22(7):1098-1101.
