参蛇软膏的质量标准研究
2014-08-20石小鹏毕琳琳第四军医大学西京医院药剂科西安7003第四军医大学药学系天然药物学教研室西安7003
石小鹏,缪 珊,李 捷,毕琳琳,苗 青,栗 艳*(.第四军医大学西京医院药剂科,西安 7003;.第四军医大学药学系天然药物学教研室,西安 7003)
参蛇软膏剂型为软膏剂,由苦参、蛇床子、地肤子、土茯苓等中药组成。作为外用制剂,临床主要用于蚊虫叮咬、皮肤瘙痒等。为了有效地控制制剂质量,笔者对处方中的苦参、黄柏、蛇床子、土茯苓进行定性鉴别[1-5],采用HPLC法测定蛇床子中的有效成分蛇床子素的含量[6-8],为该制剂的质量控制和评价指标提供实验依据。
1 仪器与试药
1.1仪器 LC-20AT高效液相色谱仪(日本岛津);薄层色谱成像系统(瑞士CANAG公司);R200D电子分析天平(德国Sartorius公司);HH-S4型电热恒温水浴锅(北京科伟永兴仪器有限公司);SB5200型超声波仪(上海必能信超声仪器有限公司)。
1.2试药 蛇床子、黄柏对照药材,苦参碱对照品(批号110805-200507)、蛇床子素对照品(批号110822-200406)、盐酸小檗碱对照品(批号110713-200910)、落新妇苷对照品(批号111798-200901),以上均由中国药品生物制品检定所提供;硅胶G板(青岛海洋化工厂);参蛇软膏(第四军医大学药物研究所提供,批号130301,130302,130303);甲醇、乙腈为色谱纯试剂,水为超纯水,其他均为分析纯试剂。
2 定性鉴别
2.1苦参的薄层色谱鉴别 称取本品3 g,置于圆底烧瓶中,加水30 mL,水浴上加热回流30 min,取出,放冷,滤过,滤液用浓氨水调节pH至11,用氯仿萃取3次(30,15和15 mL),合并氯仿萃取液,蒸干,残渣加甲醇1 mL使其溶解,作为供试品溶液。取苦参阴性对照(按处方及制备工艺制备成不含苦参的阴性对照样品)2 g,按上述制备方法制成苦参阴性对照溶液。另取苦参碱对照品,加甲醇制成1 mg·mL-1的对照品溶液。照薄层色谱法(《中国药典》2010年版一部附录ⅥB)实验,吸取上述3种溶液各8 μL,分别点于同一以5 g·L-1羧甲基纤维素钠溶液为黏合剂的硅胶G薄层板上,展开剂为苯-丙酮-乙酸乙酯-浓氨水(10∶15∶20∶1),展开,取出,晾干,再喷以稀碘化铋钾试液,置于日光下检视。供试品溶液色谱中,在与对照品溶液相应的位置上,显相同颜色的斑点,阴性对照无干扰。
2.2蛇床子的薄层色谱鉴别 称取本品2 g,置于圆底烧瓶中,加入甲醇20 mL,水浴上加热回流30 min,取出,放冷,滤过,滤液浓缩至1 mL,作为供试品溶液。取蛇床子阴性对照样品(按处方及工艺制备成不含蛇床子的阴性对照样品)2 g,按上述制备方法制成蛇床子阴性对照溶液。另取蛇床子对照药材0.3 g,同法制成对照药材溶液。再取蛇床子素对照品,加甲醇制成1 mg·mL-1的对照品溶液。照薄层色谱法进行实验,吸取上述4 种溶液各8 μL,分别点于同一以5 g·L-1羧甲基纤维素钠溶液为黏合剂的硅胶G薄层板上,展开剂为甲苯-乙酸乙酯-正己烷(3∶3∶2),展开,取出,晾干,于365 nm紫外光灯下检视。供试品溶液色谱中,在与对照药材溶液和对照品溶液相应的位置上,显相同颜色的荧光斑点,阴性对照无干扰。
2.3黄柏的薄层色谱鉴别 称取本品2 g,加入甲醇20 mL,超声处理30 min,取出,放冷,滤过,取滤液作为供试品溶液。取黄柏阴性对照(按处方及工艺制备成不含黄柏的阴性对照样品)2 g,按上述制备方法制成黄柏阴性对照溶液。另取黄柏对照药材0.5 g,同法制成对照药材溶液。再取盐酸小檗碱对照品,加甲醇制成1 mg·mL-1的对照品溶液。照薄层色谱法进行实验,吸取上述4种溶液各10 μL,分别点于同一以5 g·L-1羧甲基纤维素钠溶液为黏合剂的硅胶G薄层板上,展开剂为正丁醇-冰醋酸-水(7∶1∶2),展开后,取出,晾干,置于365 nm紫外光灯下检视。供试品溶液色谱中,在与对照药材溶液和对照品溶液相应的位置上,显相同颜色的荧光斑点,阴性对照无干扰。
2.4土茯苓的薄层色谱鉴别 称取本品5 g,置于具塞锥形瓶中,加水30 mL,于水浴上加热回流1 h,取出,放冷,滤过,滤液用乙醚提取3次。每次15 mL,弃去乙醚液,用氯仿提取3次,每次15 mL,弃去氯仿液,再用乙酸乙酯提取3 次(30,15和15 mL),合并提取液,浓缩至1 mL,作为供试品溶液。再取土茯苓阴性对照(按处方及工艺制备成不含土茯苓的阴性对照样品)2 g,按上述制备方法制成土茯苓阴性对照溶液。另取落新妇苷对照品,加甲醇制成1 mg·mL-1的对照品溶液。照薄层色谱法进行实验,吸取上述3种溶液各10 μL,分别点于同一以5 g·L-1羧甲基纤维素钠溶液为黏合剂的硅胶G薄层板上,以苯-乙酸乙酯-甲酸(13∶32∶19)为展开剂,展开,取出,晾干,喷以20 g·L-1三氯化铝乙醇溶液,于365 nm紫外光灯下检视。供试品溶液色谱中,在与对照品溶液相应的位置上,显相同颜色的荧光斑点,阴性对照无干扰。
3 含量测定
3.1色谱条件 Kromasil C18色谱柱(250 mm×4.6 mm,5 μm);乙腈-水(65∶35)为流动相;检测波长:320 nm;流速:1.0 mL·min-1;进样量:20 μL;理论板数按蛇床子素计不低于3 000。
3.2对照品溶液的配制 精密称取4.40 mg蛇床子素对照品,置于50 mL量瓶中,加乙醇溶解,稀释并定容至刻度,摇匀,得质量浓度88.0 mg·L-1的溶液,作为对照品溶液。
3.3供试品溶液的制备 精密称取本品5 g,置于圆底烧瓶中,精密加入50 mL甲醇,密塞,精密称定质量,水浴加热回流40 min,取出,放至室温,再精密称定质量,用乙醇补足减失的质量,摇匀,过0.45 μm微孔滤膜,作为供试品溶液。
3.4阴性对照溶液的制备 按处方比例称取处方药材,再按制备工艺制成缺蛇床子的阴性样品,精密称取阴性样品5 g,按2.3项下的制备方法制成阴性对照溶液。
3.5专属性实验 精密吸取上述溶液,按2.1项下的色谱条件进行测定,结果供试品溶液在与对照品溶液相对应的位置上有相同的色谱峰,而阴性对照则无色谱峰出现,说明样品中其他成分对蛇床子素无干扰,其专属性强,色谱图见图1。
3.6标准曲线制备和线性范围考察 精密量取对照品溶液1,2,3,4和5 mL,置于不同的5 mL量瓶中,加乙醇稀释并定容至刻度,摇匀,依次得到质量浓度为17.6,35.2,52.8,70.4和88.0 mg·L-1的对照品溶液,按2.1项下的色谱条件进行测定,记录峰面积,以质量浓度为横坐标(X),峰面积为纵坐标(Y),绘制线性回归方程:Y=69 485X+38 475(r=0.999 9),结果蛇床子素在17.6~88.0 mg·L-1范围内呈良好的线性关系。

图1 HPLC图
3.7精密度实验 精密吸取质量浓度为35.2 mg·L-1的对照品溶液和同一批号(130301)的供试品溶液各20 μL,按2.1项下的色谱条件进行测定,结果对照品RSD为0.15%(n=5),样品RSD为0.23%(n=5),结果表明,其精密度良好。
3.8稳定性实验 精密吸取质量浓度为52.8mg·L-1的对照品溶液和同一批号(130302)的供试品溶液各20 μL,按2.1项下的色谱条件分别间隔0,1,2,4和8 h进行测定,结果对照品RSD为0.51%(n=5),样品RSD为0.23%(n=5),结果表明,蛇床子素在15 h内稳定。
3.9重复性实验 精密称取同一批号(130303)样品5份,按2.3项下的制备方法制成供试品溶液,按上述色谱条件进行检测,蛇床子素的平均含量为0.297 mg·g-1,RSD=0.61%(n=5)。
3.10加样回收率实验 精密称取已知含量的样品6份,分别加入蛇床子素对照品1.0,1.0,1.5,1.5,2.0和2.0 mg,按2.3项下的制备方法制成供试品溶液,再按2.1项下的色谱条件进行测定,测得平均加样回收率为99.6%,RSD为0.4%,测定结果如表1所示。
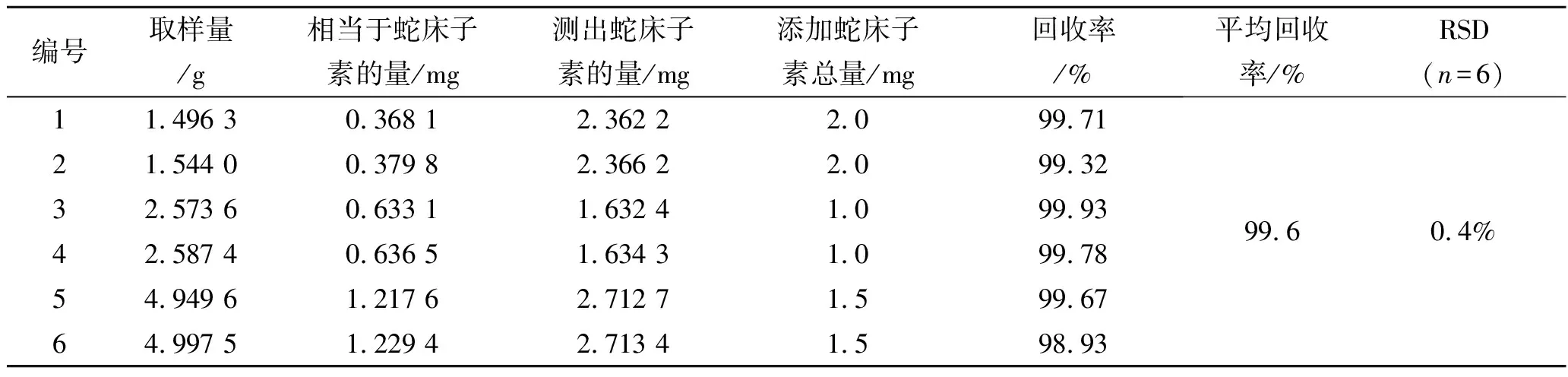
表1 蛇床子素加样回收率测定结果
3.11样品含量测定 精密称取3批参蛇软膏样品各5 g,按2.3项下的制备方法制成供试品溶液,再按2.1项下的色谱条件进行测定,结果如表2所示。
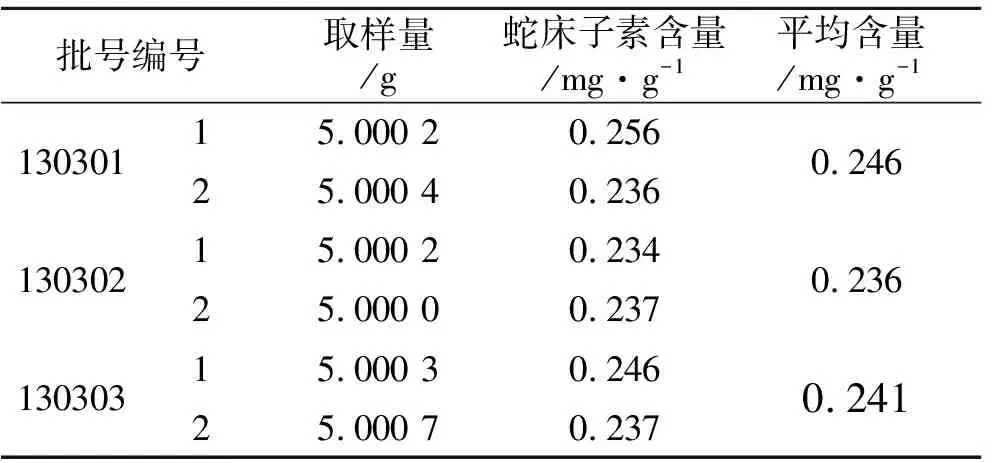
表2 参蛇软膏中蛇床子素的含量测定结果
4 讨论
在薄层色谱中,曾对苦参、蛇床子、黄柏和土茯苓的供试品制备及展开系统的方法优选,经过多次实验研究,最终优选的制样方法过程简单,分离度好,不受其他成分干扰,专属性强,重复性好,结果可靠,可作为参蛇软膏的定性指标。
蛇床子为处方君药,主要含有香豆素类成分,蛇床子素为主要活性成分之一,近代药理研究证实,蛇床子素对抑制乳腺癌细胞的增殖、诱导细胞凋亡有明显作用,另外还有降血脂、抑制血栓形成及抗菌止痒等作用[9-10]。因此,将其作为含量测定指标之一,能直接影响到药品的疗效。通过文献查询及预实验,我们采用了适用于本品的HPLC法对蛇床子素的含量进行了研究[6-8]。曾选择不同色谱条件进行实验,结果表明,流动相为乙腈-水(65∶35)、流速为1.0 mL时,蛇床子素与其他组分得到较好地分离,且峰形对称,能准确测得其含量。在实验中,采用甲醇、乙醇2种不同的溶剂以及不同的溶剂量,选择超声波提取和回流提取的方法制备供试品溶液。结果表明,甲醇50 mL回流提取的含量明显较高,故选择甲醇回流提取;对回流提取时间的考察:分别选择提取15,30,40和60 min,结果提取30 min时所测得蛇床子素的含量明显高于15 min,提取40 min时所测得蛇床子素的含量则高于30 min时的含量,而提取40 min与提取60 min时的含量没有明显差别,故选择40 min为最佳提取时间。经过方法学研究,该方法样品处理简单,测得的结果回收率高,精密度好,可以有效控制制剂的质量。
参考文献:
[1] 刘冰,熊代琴,艾克拜尔·阿斯良. 乳痛宁糖浆的制备及质量标准[J]. 西北药学杂志,2010,25(5):105-107.
[2] 张格,张俊,程璐. 紫草解毒软膏质量标准研究[J]. 医药导报,2012,31(4):486-488.
[3] 刘志刚,邓伟杰,孙维峰. 复方土茯苓颗粒定性定量方法研究[J]. 药物分析杂志,2011,3(1):119-123.
[4] 邹渭洪,付成效,龙宇,等. RP-HPLC法测定三皮止癣酊中蛇床子素的含量[J]. 中国药房,2012,23(47):4484-4485.
[5] 国家药典委员会. 中国药典2010年版[S].一部.北京:中国医药科技出版社, 2010:17.
[6] 李小安,张军科,史关佳,等. HPLC法同时测定阿娜尔妇洁液中蛇床子素和欧前胡素的含量[J]. 西北药学杂志,2008,23(3):139-141.
[7] 李华荣,高逢喜,孙鑫. HPLC法测定妇舒能洗剂中蛇床子素的含量[J]. 中国药师,2010,13(8):1180-1181.
[8] 曹霞,斐周琳. 高效液相色谱法测定独活寄生丸中蛇床子素的含量[J]. 中国实用医药,2010,5(9):36-37.
[9] 杨大朋,王海啸,彭延廷,等. 蛇床子素对人乳腺癌细胞增殖、细胞周期及凋亡的影响[J].南京师范大学学报:自然科学版,2010,33(2):76-80.
[10] 陈蓉,谢梅林. 蛇床子素抑制血栓形成及其作用机制研究[J]. 中国现代医药杂志,2008,10(10):50-52.