HPLC法测定复方氯霉素醇溶液中氯霉素和水杨酸的含量
2014-08-15吴海伟贾燕花王晓青薛谟斐刘皈阳
吴海伟,贾燕花,王晓青,高 磊,薛谟斐,刘皈阳
0 引言
复方氯霉素醇溶液是《中国人民解放军医疗机构制剂规范》[1](2002年增补版)(以下简称“军队制剂规范”)中收载的一种外用制剂,具有抗菌、软化角质作用,临床上主要用于治疗脂溢性皮炎、皮疹、瘙痒症等。复方氯霉素醇溶液中含有氯霉素、水杨酸两种主成分,用75%乙醇作为溶剂配制而成。在《军队制剂规范》中,采用了高效液相法和中和滴定法分别测定复方氯霉素醇溶液中氯霉素、水杨酸的含量,该方法操作较繁琐、耗时;因此,为了简化复方氯霉素醇溶液中氯霉素、水杨酸的含量测定方法,提高专属性、准确性;本实验拟建立高效液相法同时测定复方氯霉素醇溶液中氯霉素、水杨酸的含量,参考2010版《中国药典》[2]进行方法学验证,结果,该方法能够较准确地测量复方氯霉素醇溶液的含量,为该制剂的质量标准控制提供了参考。
1 仪器与试药
1.1 主要仪器 Aglient1200型高效液相色谱仪,Eclips XDB-C18(4.6 mm×250 mm,5 μm)色谱柱,美国Aglient公司;紫外分光光度仪,U-3000,日本日立株式会社;电子天平,Mettler AE200,梅特勒-托利多仪器有限公司。
1.2 试药 氯霉素对照品(批号:100508-200902,中国药品生物制品鉴定所),水杨酸对照品(批号:100106-201104,中国药品生物制品鉴定所),氯霉素原料药(批号:CH130313,南京白敬宇制药有限责任公司),水杨酸原料药(批号:10092,山东新华制药股份有限公司),乙酸(分析纯,北京化工厂),甲醇(色谱级,赛默飞世尔科技有限公司),复方氯霉素醇溶液(本院自制,批号:130911-1、130911-2、130911-3,规格:100 mL/瓶)。
2 方法与结果
2.1 溶液配制
2.1.1 对照品液液的制备 称取氯霉素对照品约50.0 mg,水杨酸对照品约50.0 mg,精密称定,置于50 mL容量瓶中,用适量甲醇溶解,加流动相稀释至刻度,摇匀,作为对照品贮备液;精密量取5 mL置于50 mL容量瓶中,加流动相稀释至刻度,摇匀,即为对照品溶液。
2.1.2 供试品溶液的制备 精密量取复方氯霉素醇溶液2.5 mL,置于50 mL容量瓶中,加流动相稀释至刻度,摇匀,再精密量取5 mL置于50 mL容量瓶中,加流动相稀释至刻度,摇匀,作为供试品溶液。
2.1.3 空白溶液的制备 根据处方比例,配制不含氯霉素、水杨酸的空白样品,并按“2.1.2”项配制空白溶液。
2.2 最大吸收波长的确定 称取等量氯霉素、水杨酸对照品适量,用适量甲醇溶解,流动相稀释成适当浓度,在紫外分光光度仪下,400~200 nm范围内进行全波长扫描,结果,氯霉素与水杨酸混合溶液在293.2 nm处有最大吸收值(见图1);因此,检测波长确定为293 nm。
2.3 色谱条件 色谱柱为Eclipse XDB-C18(4.6 mm×250 mm,5 μm);以1%冰醋酸-甲醇(60∶40)为流动相;检测波长为293 nm;流速1.0 mL/min,进样量10 μL。
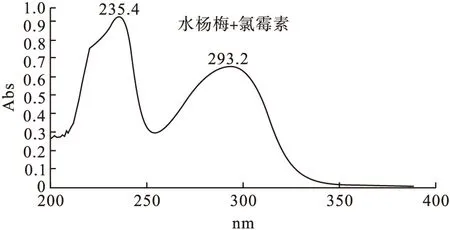
图1 氯霉素、水杨酸混合溶液全波长扫描
2.4 专属性试验 取本品制剂2.5 mL,置于50 mL容量瓶中,共3份;分别加入10 mL 1 mol/L HCl溶液、10 mL 1 mol/L NaOH溶液及10 mL双氧水,室温放置60 h,用流动相稀释至刻度,摇匀;精密量取适量,用流动相稀释10倍,即为供试品溶液;分别取上述供试品溶液、对照品溶液及空白溶液10 μL,注入色谱仪,记录色谱图。结果,该制剂在酸、碱及氧化条件下,均有杂质峰出现,但均不干扰主峰,且两主峰分离较好,分离度大于2,如图2所示。
2.5 线性关系考察 精密量取对照品贮备液3、4、5、6、7、8 mL置于50 mL容量瓶中,加流动相稀释至刻度,摇匀,分别进样10 μL以对照品峰面积(A)对浓度(C)进行线性回归,氯霉素、水杨酸线性回归方程分别为:A=14.42C-2.101,r=1;A=11.97C-53.21,r=1。表明氯霉素、水杨酸在60~160 μg/mL浓度范围内峰面积与浓度线性关系良好。
2.6 样品测定
2.6.1 精密度试验 精密量取对照品贮备液2.5 mL,置25 mL容量瓶中,加流动相稀释至刻度,摇匀;取上述溶液10 μL注入液相色谱仪,连续进样6次,记录色谱图,计算得氯霉素峰面积RSD值为0.11%(n=6),水杨酸峰面积RSD值为0.08%(n=6);表明仪器精密度良好。
2.6.2 稳定性试验 按“2.1.2”项下方法制备供试品溶液,于室温下放置24 h,每隔2 h进样一次,每次进样10 μL,记录色谱图,计算氯霉素、水杨酸峰面积的RSD值分别为0.12%、0.10%;表明本溶液在24 h内稳定,其峰面积基本不变。
2.6.3 重复性实验 选择同一批复方氯霉素醇溶液,按“2.1.2”项下方法制备6份供试品溶液,分别取10 μL注入液相色谱仪,记录色谱图,计算得氯霉素峰面积RSD值为0.80%(n=6),水杨酸峰面积RSD值为0.34%(n=6);表明样品含量测定重复性较好。
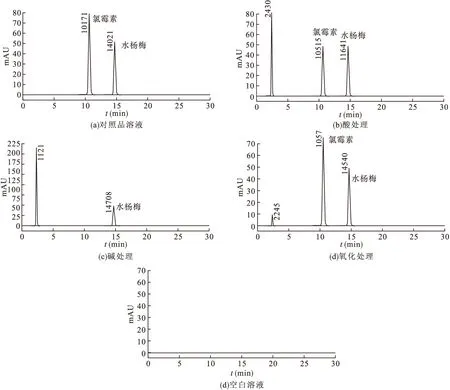
图2 对照品及样品高效液相色谱图
2.6.4 加样回收率试验 称取氯霉素、水杨酸原料药各约40、50、60 mg,精密称定,分别置50 mL容量瓶中,按处方比例加入辅料,适量甲醇溶解,加流动相稀释至刻度,摇匀,再精密量取2.5 mL溶液,置于25 mL容量瓶中,加流动相稀释至刻度,即制得浓度为80%、100%、120%的供试品溶液,每个浓度组制备3份。按“2.3”项下色谱条件,分别进样,记录色谱图;结果氯霉素平均回收率为99.45%,RSD值为0.46%,水杨酸平均回收率为100.32%,RSD值为0.97%。结果见表1、表2。
2.7 耐用性考察 为考察该色谱条件对测定结果的影响,拟在改变下列色谱条件的情况下,对供试品进行含量测定,并计算每个条件下含量测定的RSD值。(1)改变流速±0.2 mL/min:0.8 mL/min;1.0 mL/min;1.2 mL/min。(2) 改变流动相比例±2%:1%冰醋酸∶甲醇=58∶42;1%冰醋酸∶甲醇=60∶40;1%冰醋酸∶甲醇=62∶38。(3)改变波长±5 nm:288 nm;293 nm;298 nm。(4)色谱柱:①Eclipse plus-C18(4.6 mm×250 mm,5 μm)。②ZORBAX SB-C18(4.6 mm×250 mm,5 μm);③Eclipse XDB-C18(4.6 mm×250 mm,5 μm)

表1 氯霉素
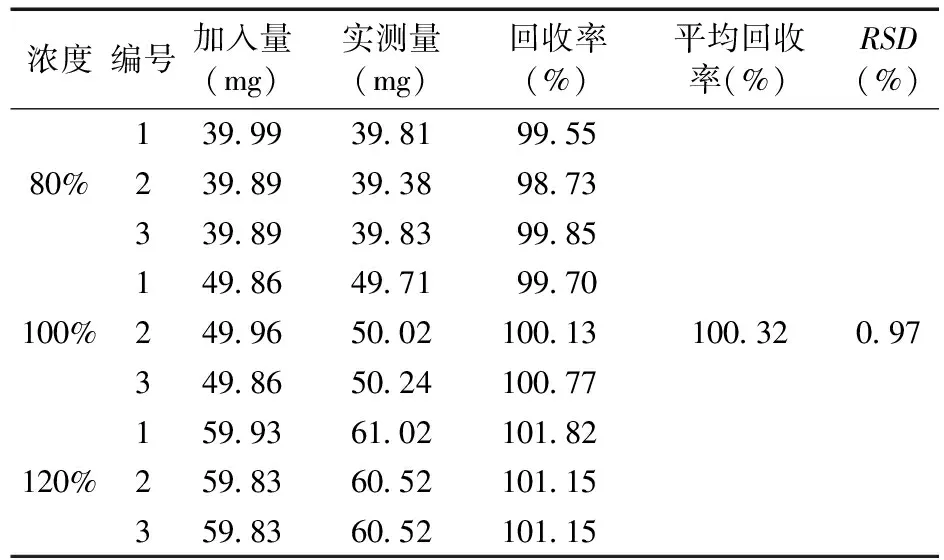
表2 水杨酸
取复方氯霉素醇溶液,按“2.1.2”项下方法制备供试液,在上述色谱条件,进样10 μL,记录色谱图。试验结果表明:在改变流动相比例、流速、波长及色谱柱条件下,供试品的测定含量均符合要求,各条件下含量测定的RSD值均小于2%,说明该方法用于样品含量测定,耐用性较好。结果见表3。
2.8 样品含量测定 取复方氯霉素醇溶液三批(批号:130911-1、130911-2、130911-3),按“2.1.2”项下方法制备供试液,取10 μL注入液相色谱仪,记录色谱图,按外标法计算含量,测定3批样品中氯霉素含量分别为98.52%、99.76%、98.92%,水杨酸的含量分别为99.06%、100.97%、99.27%。结果表明:三批样品中氯霉素和水杨酸的含量均符合要求,结果见表4。
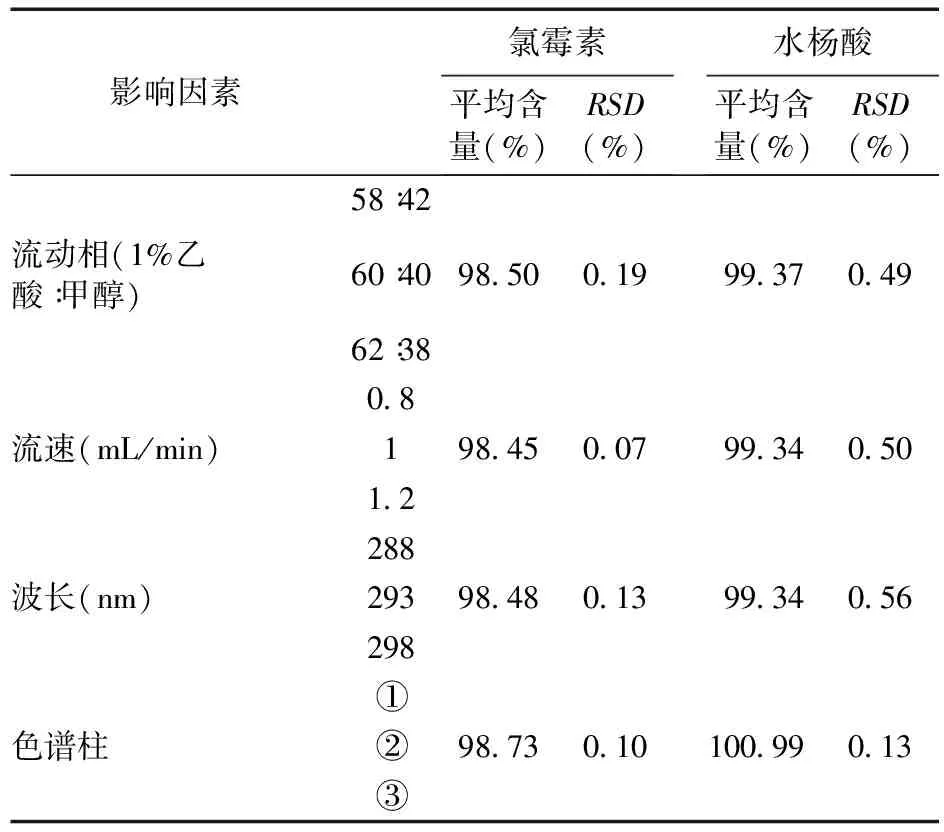
表3 耐用性试验结果

表4 样品含量测定结果
3 讨论
本实验建立高效液相法同时测定复方氯霉素醇溶液中氯霉素、水杨酸的含量,该方法简单、方便,避免了《军队制剂规范》中分别测定水杨酸、氯霉素含量的繁琐步骤。该方法与《军队制剂规范》中氯霉素含量测定项下色谱条件相比,流动相配制更简单,对主成分出峰时间影响较小,提高了含量测定的准确度。另外,有文献报道[3-5],HPLC法同时测定复方氯霉素醇溶液中氯霉素和水杨酸的含量,采取单一检测波长,例如278 nm,但水杨酸的最大吸收波长为301 nm(经紫外分光光度仪检测),在278 nm处氯霉素与水杨酸的吸收强度差别较大,不适合作为两者的共同检测波长;也有文献报道[6],采用双波长双通道法检测该制剂中氯霉素和水杨酸的含量,即在278和300 nm处分别检测氯霉素和水杨酸的色谱峰;而王敏等[7]人采用了单波长切换的方法测定复方氯霉素醇溶液的含量,但考虑基层设备条件问题,均不适合作为制剂标准规范收载。因此,本实验选取氯霉素、水杨酸混合液的最大吸收波长293 nm,作为本品制剂含量测定的检测波长;在293 nm处,氯霉素与水杨酸的吸收值相近,能同时满足两者检测的需要,有利于提高含量测定的灵敏度和准确度。本方法应用于复方氯霉素醇溶液的含量测定,并做了重复性、耐用性等试验的考察,结果均较好,可用于该制剂质量的控制。
参考文献:
[1] 中国人民解放军总后勤部编.中国人民解放军医疗机构制剂规范2002年版增补本[M].人民军医出版社,2007:28-29.
[2] 国家药典委员会.中华人民共和国药典(二部)[S].北京:中国医药科技出版社,2010:附录XIXA.
[3] 郭胜才,谷娜,李华.高效液相色谱法测定复方氯霉素醇溶液中水杨酸与氯霉素含量[J].医药导报,2010,29(6):783-785.
[4] 刘晋华,李玉萍,尤光甫.复方氯霉素醇溶液含量测定方法的改进[J].解放军药学学报,2007(3):228-230.
[5] 陶建亮,张崇生.高效液相色谱法测定复方氯霉素醇溶液的含量[J].海峡药学,2006,18(4):87-88.
[6] 谷娜,邢旺兴,郭胜才.高效液相色谱法同时测定复方氯霉素醇溶液中水杨酸与氯霉素含量[J].健康研究,2009,29(3):177-179.
[7] 王敏,张瑞麟,王逢春,等.高效液相色谱法单波长切换测定复方氯霉素醇溶液中水杨酸、氯霉素含量[J].解放军医药杂志,2013(8):94-96.
