加红生化汤中阿魏酸的含量测定
2014-08-15赖水容陈行愉韩丽萍
赖水容,陈行愉,韩丽萍
0 引言
加红生化汤是本院临床科室在长期临床实践和用药经验总结下,根据著名古方生化汤[1]组方原理,进一步完善配方和改进生产工艺技术生产的纯中药制剂,处方由当归、川芎、桃仁、姜炭、炙甘草、红花6味中药药材所组成,具有活血去瘀、温经止痛的功效,临床常用于产后子宫收缩痛、子宫复旧不良及常见妇科疾病。其中当归与川芎均为加红生化汤中主药,两味药的功效主治[2]与制剂功效有密切关系。研究表明,阿魏酸是川芎、当归等多种中药的有效成分之一,具有多方面的生物活性[3-4],许多生药及其制剂常选用阿魏酸的含量作为其质量控制指标[5]。目前该制剂质量标准草案中尚未建立相关含量测定方法控制其质量。所以,本研究建立了加红生化汤中阿魏酸的高效液相色谱含量测定,保证该制剂质量,实现临床用药安全有效。
1 仪器与试药
Agilent 1100型高效液相色谱仪(美国Agilent公司,配有G1315B 紫外检测器、G1312A双泵、G1313A自动进样器和CAG Bootp Server色谱工作站);BP211D型电子天平(Made by Sartorius)等;阿魏酸对照品(中国药品生物制品检定所,批号:11073-201012);甲醇为色谱纯,水为超纯水,乙酸乙酯、冰醋酸均为分析纯;加红生化汤(本院制剂,0.86 g/mL,批号:110311、110715、120113)。
2 方法
2.1 色谱条件 色谱柱:Agilent TC-C18色谱柱(4.6 mm×250 mm,5 μm);流动相为甲醇-0.3%冰乙酸溶液(30∶70);流速:1.0 mL/min;检测波长:323 nm;柱温:25 ℃;进样量:10 μL。在此条件下对阿魏酸溶液进行分离,用外标法按峰面积定量计算。
2.2 对照品溶液的制备 精密称取阿魏酸对照品约10 mg,置50 mL棕色量瓶中,加甲醇溶解并稀释至刻度,摇匀,作为储备液。实验时吸取储备液1 mL,置10 mL棕色量瓶中,加甲醇稀释至刻度,摇匀,即制成含阿魏酸19.76 μg/mL的对照品溶液。
2.3 供试品溶液的制备 取加红生化汤(批号:110715),摇匀,精密量取10 mL,置分液漏斗中,精密加乙酸乙酯20 mL,轻微振摇,放置至分层,分离乙酸乙酯层提取液。按上述操作重复3次,合并乙酸乙酯层提取液,置水浴锅上(100 ℃)蒸干,残渣用甲醇溶解,转移至10 mL量瓶中,加甲醇至刻度,摇匀,用微孔滤膜(0.45 μm)滤过,即得。
2.4 阴性对照溶液的制备 按该制剂处方称取不含当归、川芎的其他药材,按制剂的制备工艺制成汤剂,然后按供试品溶液的制备方法制成阴性对照溶液,即得。
3 结果
3.1 系统适用性试验 按“2.1”项色谱条件,精密吸取上述对照品溶液、供试品溶液和阴性对照溶液各10 μL进样测定,结果阴性对照在与对照品、供试品相同保留时间处,无干扰峰出现(见图1),因此确定处方中其他中药材成分对阿魏酸的含量测定不产生干扰。

图1 加红生化汤中阿魏酸的HPLC色谱分析图
3.2 线性关系考察 分别精密吸取储备液0.5、1.0、1.5、2.0、3.0、5.0 mL置于10 mL量瓶中,用甲醇稀释并定容,摇匀,精密吸取上述对照品溶液各10 μL进样测定。以进样量为横坐标(X)、峰面积值为纵坐标(Y),绘制标准曲线,计算回归方程。结果,计算得线性方程为Y=57 765 X-47.898(R2=0.999 8),线性范围为9.88~98.8 μg/mL。
3.3 精密度试验 精密吸取供试品溶液10 μL,按“2.1”项色谱条件测定,连续进样6次,记录各色谱图的峰面积。结果计算得峰面积相对标准偏差RSD为0.94%(n=6),表明仪器精密度良好。
3.4 稳定性试验 取同一供试品溶液,分别于室温下放置0、1、2、3、4、5、6、8、10 h,由同一操作人员精密吸取10 μL进样测定。测得供试品中阿魏酸峰面积的相对标准偏差RSD=1.3%(n=9),表明供试品中阿魏酸在10 h内比较稳定。
3.5 重复性试验 取同一批(批号:110715)的加红生化汤适量,按供试品溶液的制备方法操作,按“2.1”项色谱条件测定,进行7次平行试验,计算得供试品中阿魏酸的平均含量为28.43 μg/mL,其相对标准偏差RSD为2.1%(n=7),表明本方法重复性良好。
3.6 加样回收试验 精密量取已测定含量的供试品6份(测得阿魏酸含量为28.43 μg/mL)5 mL,精密吸取上述储备液各1.0 mL,超纯水各4.0 mL,按供试品溶液的制备方法制备样品溶液。精密吸取上述样品溶液各10 μL进样测定,计算得样品中阿魏酸的平均回收率为99.07%,RSD为1.4%(n=6)。见表1。
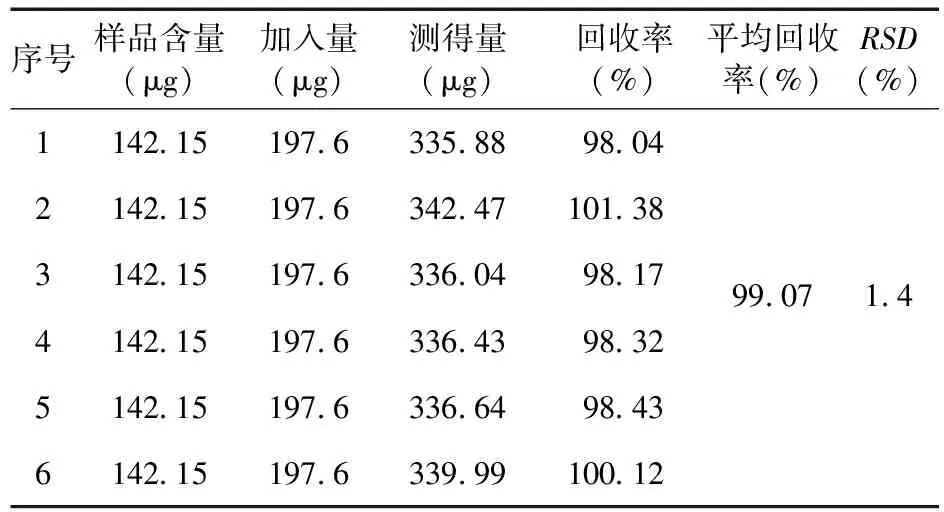
表1 加样回收试验结果
3.7 样品含量的测定 取3批加红生化汤,按供试品溶液的制备方法处理,每批制备3份供试品溶液,按“2.1”项色谱条件测定,计算得供试品中阿魏酸的平均含量,见表2。

表2 样品测定结果
4 讨论
4.1 测定方法的考察 《中华人民共和国药典》2010年版一部“当归”项下含量测定项采用高效液相色谱法测定阿魏酸的含量。关于阿魏酸的含量测定方法文献报道较多,如高效液相色谱法[6-8]、气相色谱法[9]、薄层扫描法[10]、毛细管电泳法[9]等,由于高效液相色谱法具有快速、方便、灵敏、专属性强等特点,已经被广泛应用于药物的含量测定、组成分析、质量控制等方面。因此,本研究参照《中华人民共和国药典》2010年版一部“当归”项下含量测定项下的方法测定了该制剂提取物中阿魏酸的含量,并进行了方法学考察。
4.2 预处理方法的选择 参考文献[10-11],提取阿魏酸的方法主要有超声提取法和溶剂萃取法,本研究考察了上述两种方法,通过试验结果选择溶剂萃取法作为加红生化汤中阿魏酸的提取方法;同时还考察了提取溶媒的种类和用量,用乙酸乙酯与乙醚比较,试验结果表明,乙酸乙酯的提取效率明显优于乙醚。
4.3 检测波长的选择 按紫外分光光度法,用甲醇作为空白对照溶液,制备阿魏酸对照品的甲醇溶液,在190~400 nm波长范围内进行扫描。结果显示,阿魏酸在323 nm波长处有最大吸收,故选择323 nm作为检测波长。
4.4 流动相的选择 本研究参照中国药典2010版一部川芎和当归含量测定项下的方法,对色谱条件中的流动相进行了考察,选择甲醇-1%冰醋酸溶液(30∶70)和乙腈-0.085%磷酸溶液(17∶83)作为流动相进行试验。结果显示,用甲醇-1%冰醋酸溶液(30∶70)的分离度比用乙腈-0.085%磷酸溶液(17∶83)的分离度大,且拖尾因子较小。通过进一步实验,调整流动相的酸度使阿魏酸成分保持稳定。结果表明,用甲醇-0.3%冰醋酸溶液(30∶70)作为流动相时,出峰时间适中,且基线平稳,故选择其作为本研究的流动相。
参考文献:
[1] 刘影,张伟娟,任亚娟,等.生化汤的临床应用及实验药理[J].河南中医,2013,33(4):603-604.
[2] 国家药典委员会.中华人民共和国药典(一部)[S].北京:中国医药科技出版社,2010.
[3] 郑维兵.HPLC法测定归芪生血颗粒中阿魏酸的含量[J].海峡药学,2013,25(8):88-89.
[4] 俞永梅,张平,牟娜.HPLC法测定参芪生肌颗粒中阿魏酸的含量[J].中国药师,2012,15(6):826-828.
[5] 陈阿丽,杨永霞,梁生旺,等.高效液相色谱法测定妇康宁片中阿魏酸的含量[J].中国当代医药,2013,20(28):71-75.
[6] 申睿,郭琪.HPLC法测定活血止痛液中阿魏酸的含量[J].解放军药学学报,2013,29(6):547-549.
[7] 郑维兵.HPLC法测定归芪生血颗粒中阿魏酸的含量[J].海峡药学,2013,25(8):88-89.
[8] 姜建萍,陈晨,马雯芳.生化汤实验研究进展[J].中药材,2008,31(10):1590-1595.
[9] 李全斌,何开勇,吴建萍.阿魏酸含量测定方法研究进展[J].中医药导报,2011,17(3):117-119.
[10]冯艺戎.TLCS法测定安中养血合剂中阿魏酸的含量[J].安徽医药,2010,14(6):654-656.
[11]钟露苗,彭艳梅.醒脑通络片中阿魏酸含量测定方法学研究[J].中南药学,2010,8(2):135-138.
