利用酚型木素模型物研究硫酸盐法蒸煮过程中LCC的形成
2014-08-15杨志勇谢益民
杨志勇 谢益民 周 燕
(1.潍坊科技学院,山东寿光,262700;2.湖北工业大学化学与环境工程学院,湖北武汉,430068)
制浆造纸过程中,高效率地将纤维素纤维从植物细胞壁中分离出来是首要任务,然而,植物原料和未漂纸浆中的相当一部分木素大分子通过化学键与多糖结合在一起,并以木素-碳水化合物复合体(Lignin-Carbohydrate Complexes,简称LCC)的形式存在,这阻碍了木素的脱除,使得制浆和漂白过程消耗大量的化学药品和能源,同时造成严重的环境污染[1]。如何选择性地破坏木素和碳水化合物之间的化学键连接是发展新的制浆和漂白技术时要解决的关键问题。目前,LCC的形成机理、化学结构以及反应特性的研究是木材化学和制浆造纸领域中一个很重要的研究方向,也是国际公认的跨世纪研究课题之一。
迄今为止,人们已经对LCC做了大量的研究工作,但是对制浆蒸煮过程中LCC形成机理的研究却很少。虽然聚木糖沉积在纤维表面的现象可以从实际蒸煮实验过程中观察得到,但对于这种沉积在纤维表面的聚木糖是否与残留在纸浆中的木素形成新LCC的研究却很少。如果能对制浆、漂白过程中形成的LCC有一个明确的认识,就会更好地指导脱木素过程。利用木素模型物研究木素在制浆、漂白等处理过程中的变化规律是不可缺少的研究手段[2]。本研究在以往研究工作的基础上,充分利用木素侧链的同位素示踪技术[3],合成了带13C同位素标记的酚型β-O- 4型木素模型物愈创木基丙三醇-β-愈创木基醚-[α-13C],并将合成的木素模型物和聚木糖作为蒸煮对象,利用硫酸盐法蒸煮过程,从分子水平上探讨了传统硫酸盐法制浆过程中LCC的形成情况。本研究有助于进一步解释硫酸盐法蒸煮后纸浆中残余木素存在的原因,为新型制浆技术及纸浆全无氯漂白技术提供理论指导和依据。
1 实 验
1.1 β-O- 4型木素模型物的合成
酚型β-O- 4型木素模型物——愈创木基丙三醇-β-愈创木基醚-[α-13C]按照文献[4]所述方法合成,并分析确认。
1.2 蒸煮实验
将400 mg愈创木基丙三醇-β-愈创木基醚-[α-13C]和400 mg聚木糖放入12 mL不锈钢反应釜内,在硫化度25%、活性碱用量17%(以Na2O计)、液比1∶4的条件下进行硫酸盐法蒸煮,油浴加热,以2℃/min的速度加热到160℃,并在160℃保温1 h,取出反应釜放置室温下冷却,然后按图1所示方法将蒸煮产物分离,并对分离后的各个组分进行红外光谱(FT-IR)、13C-核磁共振波谱(13C-NMR)、异核多量子相干谱(二维HMQC)分析。

图1 蒸煮产物的分离
在无聚木糖的情况下,将400 mg愈创木基丙三醇-β-愈创木基醚-[α-13C])放入12 mL不锈钢反应釜内,相同蒸煮条件下进行空白蒸煮实验。

图2 蒸煮产物碱不溶物的13C-NMR谱图
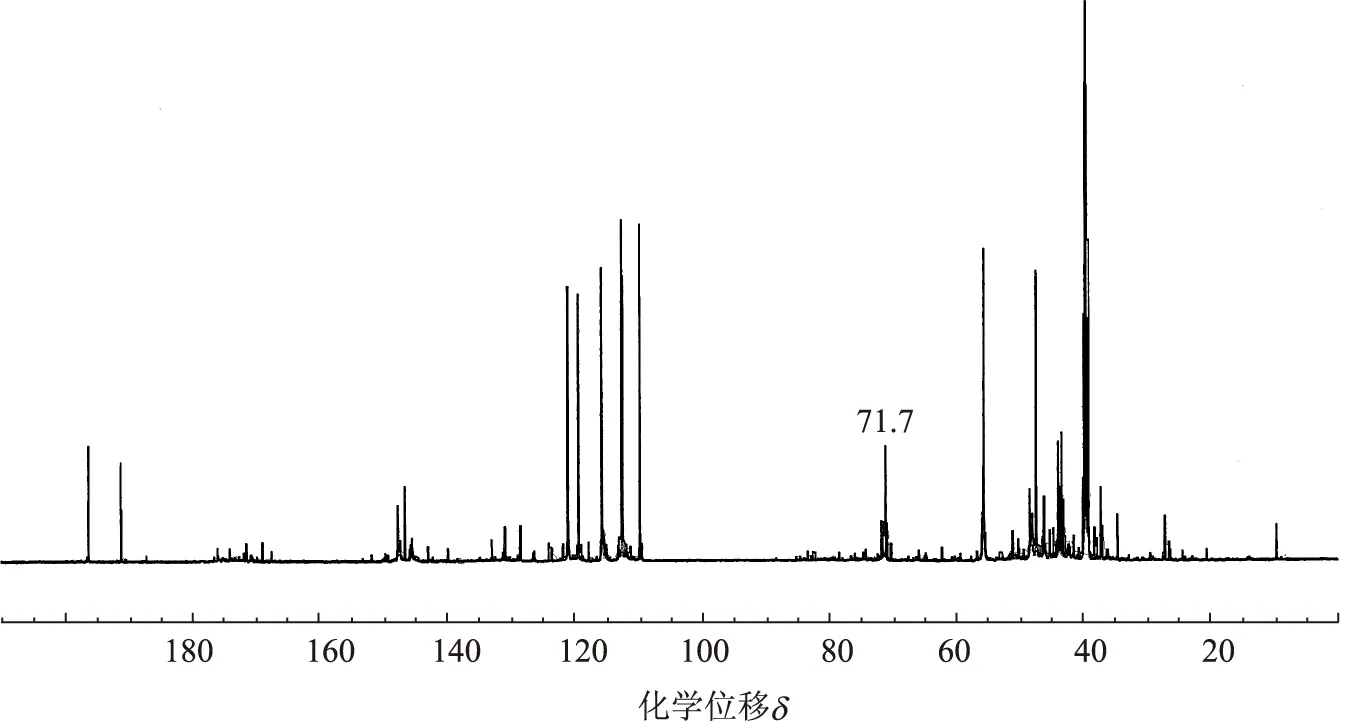
图3 蒸煮产物乙酸乙酯抽提物的13C-NMR谱图
1.3 分析方法
1.3.1FT-IR分析
将样品经溴化钾压片后利用BRUKER Tensor 27型FT-IR光谱仪进行分析。
1.3.2核磁分析
将样品溶于DMSO-d6,并置入直径5 mm的试样管内,然后利用BRUKER advance- 600核磁共振仪进行13C-NMR、二维HMQC分析。
2 结果与讨论
2.1 蒸煮产物碱不溶物的分析
愈创木基丙三醇-β-愈创木基醚-[α-13C]和聚木糖经硫酸盐法蒸煮后的蒸煮产物离心分离得到了110 mg的碱不溶物。由该碱不溶物的13C-NMR谱图(见图2)可知,峰1(δ为127.6)、峰2(δ为120.9)、峰3(δ为112.5)、峰4(δ为109.6)、峰5(δ为71.1)分别来自于愈创木基上的C3/C6、C5/C6、C2/C5、C2/C5和Cα(β-O- 4)[5-8],但是这些峰的强度较弱,可见碱不溶物中仅含有少量的芳香类物质。这说明在硫酸盐法蒸煮过程中大部分β-O- 4型木素结构发生了降解。另外,图2中没有明显的来自于聚木糖的吸收信号(即δ在60~80范围内没有明显的吸收峰[5]),这说明碱不溶物中几乎没有聚木糖,所以碱不溶物中不可能形成新的LCC。
2.2 蒸煮产物乙酸乙酯抽提物的分析
由愈创木基丙三醇-β-愈创木基醚-[α-13C]和聚木糖经硫酸盐法蒸煮后的蒸煮产物乙酸乙酯抽提物的13C-NMR谱图(见图3)可以看出,δ为71.7处的信号来自于β-O- 4中的Cα[8]。如图3所示,由于δ在60~100范围内没有明显的来自聚木糖的吸收信号[7],所以该抽提物内没有聚木糖。由此可见,该乙酸乙酯抽提物中不可能形成新的LCC。
2.3 蒸煮产物酸可溶物的分析
由愈创木基丙三醇-β-愈创木基醚-[α-13C]和聚木糖经硫酸盐法蒸煮后的蒸煮产物酸可溶物的FT-IR谱图(见图4)可知,酸可溶物内没有典型的木素吸收[5](即FT-IR谱图在波数1600、1500 cm-1处附近均没有出现吸收峰),所以其不含芳香类物质,更不会形成新的LCC。
2.4 蒸煮产物酸不溶物的分析
由愈创木基丙三醇-β-愈创木基醚-[α-13C]和聚木糖的硫酸盐法蒸煮产物酸不溶物的13C-NMR谱图(见图5)可知[5-9],该酸不溶物含有聚木糖成分和未降解的木素结构,其中,信号峰1~9主要来自于未降解的木素结构,而峰10(δ为102.2)、峰14(δ为75.7)、峰15(δ为74.2)、峰16(δ为72.8)、峰17(δ为69.7)、峰18(δ为66.0)、峰19(δ为63.4)处的信号分别来自于聚木糖上的C1、C3、C2、C2/C3、C4、C5、C5。另外,图5在δ为84.3(峰11)处出现了来自于苯甲醚键型结构的Cβ的吸收信号[10],而δ为83.3(峰12)、82.1(峰13)处也出现了苯甲醚键型结构Cα或愈创木基Cβ的吸收信号[3,9],这说明该酸不溶物中可能出现了苯甲醚键型的LCC。但是根据文献[10]可知,13C-NMR谱图中δ在82~84范围内的吸收信号也有可能来自于聚木糖上的C4或非结晶区纤维素上的C4,可见仅依靠单一的13C-NMR谱图很难确定苯甲醚键型LCC的存在。

图4 蒸煮产物酸可溶物的FT-IR谱图
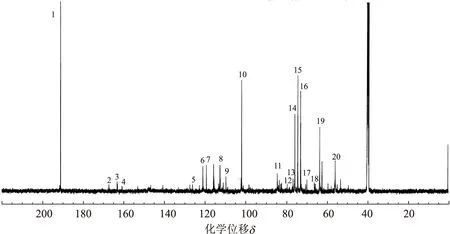
图5 蒸煮产物酸不溶物的13C-NMR谱图
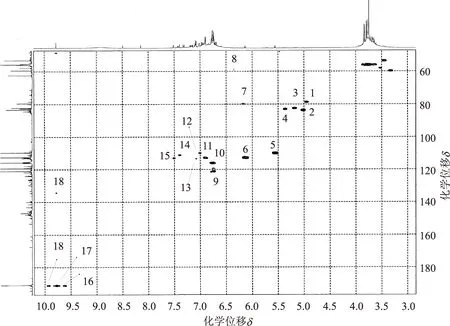
图6 空白实验蒸煮产物酸不溶物的二维HMQC图
为了进一步确认苯甲醚键型LCC是否存在,将在不加入聚木糖情况下进行愈创木基丙三醇-β-愈创木基醚-[α-13C]硫酸盐法蒸煮(即空白实验)所得蒸煮产物酸不溶物,与加入聚木糖情况下进行愈创木基丙三醇-β-愈创木基醚-[α-13C]蒸煮所得蒸煮产物酸不溶物进行了二维HMQC比较,其谱图分别见图6和图7。由图6和图7可知,当δ在82~84范围内,图6中的峰2、峰3、峰4与图7中的峰12、峰13、峰15相同,说明两组酸不溶物中都有未降解的木素结构。另外,图7的峰比图6的峰多,显然,这些多出的峰与添加的聚木糖成分或新形成的苯甲醚键型LCC有关,其中,图7中的峰1(δC/δH 72.8/3.05)、峰2(δC/δH 63.4/3.16)、峰3(δC/δH 74.2/3.28)、峰5(δC/δH 76.5/3.5)、峰6(δC/δH 69.7/3.52)、峰9(δC/δH 102.2/4.25)分别来自于聚木糖上的C2/C3、C5、C2、C3、C4、C1。而图7中的峰18(δC/δH 84.3/5.71)和峰20(δC/δH 83.3/6.02)是来自于苯甲醚键型LCC结构的Cα-Hα[9,11]。综上可知,愈创木基丙三醇-β-愈创木基醚-[α-13C]和聚木糖的硫酸盐法蒸煮所得的酸不溶物中含有新形成的苯甲醚键型LCC。这与图5所示结果一致。
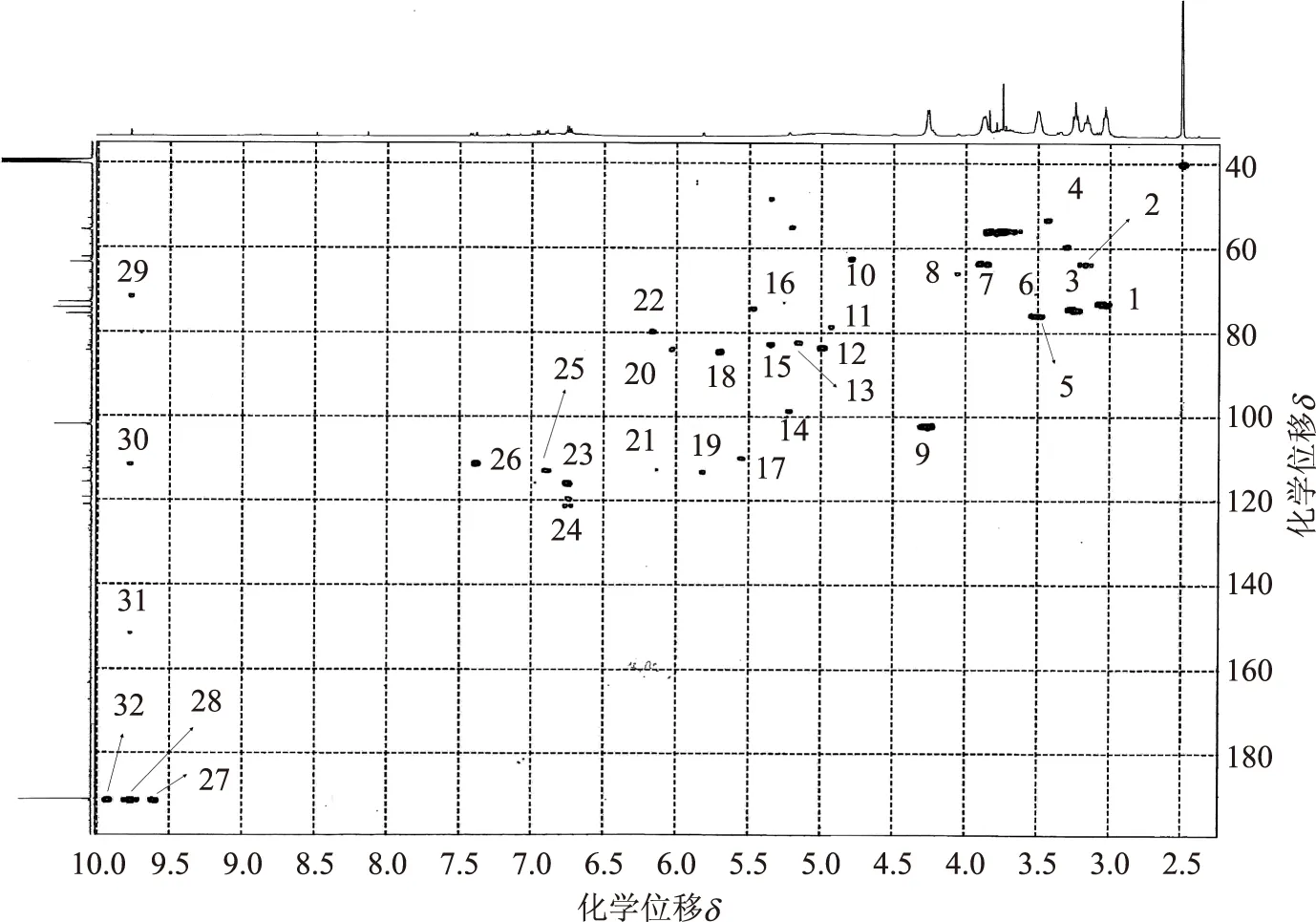
图7 加入聚木糖情况下蒸煮产物酸不溶物的二维HMQC图

图8 蒸煮过程中酚型木素模型物和聚木糖形成LCC的途径
2.5 蒸煮过程中LCC的形成机理
根据硫酸盐法和碱法蒸煮的反应机理,假设蒸煮过程中酚型木素模型物和聚木糖形成LCC的途径如图8所示。其形成的过程总结如下:在碱性介质中,酚型木素模型物Cα上的羟基首先被断裂脱除,酚型木素模型物加成硫氢根离子(或氢氧根离子)后得到了苯甲基硫醇盐产物,而硫阴离子诱导β-芳基醚的基团裂开,经过硫乙烷中间体,将其中的结合硫释放出来,从而形成愈创木基苯乙烯,而愈创木基苯乙烯中带有未共享电子对的酚氧原子可以与芳环上的π电子云重叠,这使得不同位置上的碳原子具有不同的电子密度,带有芳环连接的愈创木基苯乙烯具有碳碳双键,因而由于酚羟基的存在而引起的高电子密度就存在于该双键中的Cβ上,这样就形成了缺电子的Cα,此缺电子的Cα也就成为亲电基团进攻的主要位置,这种缺电子的中心会随缺电子的Cα被其他基团攻占而消除。作为半纤维素的重要组分,聚木糖含有丰富的羟基基团,在硫酸盐法蒸煮过程中很容易脱氢生成氧游离基成为亲电基团而与此缺电子的木素中间体形成LCC。由此可见,结构Ⅰ和结构Ⅱ可能存在。由于Cγ很容易消除,所以LCC的最终结构是结构Ⅱ(见图8)。另外,碱法制浆过程中松柏醇型中间体也有可能形成,聚木糖可以被添加到侧链的双键上,故在硫酸盐法制浆过程中可能形成另外一种苯甲醚键型LCC(结构Ⅰ,见图8)。
3 结 语
在加入聚木糖的情况下,硫酸盐法蒸煮酚型β-O- 4型木素模型物——愈创木基丙三醇-β-愈创木基醚-[α-13C]的过程中,大部分β-O- 4型木素结构发生了降解,而降解过程的中间产物和聚木糖形成了苯甲醚键型LCC,这些LCC主要存在于酸不溶物中,碱不溶物、乙酸乙酯抽提物和酸可溶物组分内没有苯甲醚键型LCC。
参 考 文 献
[1] Xiao B, Sun X F, Sun Run Cang. The chemical modification of lignins with succinia anhydride in arpucous system[J]. Polymer degradation and stahility,2001, 71(2): 223.
[2] 周 燕, 谢益民, 甘定能, 等. 缩合型木素模型物的合成及LCC的变化情况[J]. 中国造纸学报, 2006, 21(1): 9.
[3] 范建云, 谢益民, 杨海涛, 等.13C-同位素示踪法研究木素与纤维素连接键的形成[J]. 中国造纸学报, 2006, 21(1): 1.
[4] 周 燕, 谢益民, 杨志勇, 等. 愈创木基丙三醇-β-愈创木基醚-[α-13C]的合成新方法及结构分析[J]. 化学研究与应用, 2006, 18(8): 921.
[5] 李 坚. 木材波谱学[M]. 北京: 科学出版社, 2003: 109.
[6] 中野準三. 木质素的化学——基础与应用[M]. 高 洁, 鲍 禾, 李忠正, 译. 北京: 轻工业出版社, 1988: 239.
[7] 陈家翔, 余家鸾. 植物纤维化学结构的研究方法[M]. 广州: 华南理工大学出版社, 1989: 155.
[8] 杨海涛.13C同位素示踪法研究木素与LCC的化学结构及形成机理[D]. 广州: 华南理工大学, 2004: 44.
[9] Taneda H, Nakano J, Hosoya S, et al. Stability ofα-Ether Type Model Compounds During Chemical Pulping Processes[J]. Journal of Wood Chemistry and Technology, 1987, 7(4): 485.
[10] 刘传富, 孙润仓, 叶 君. 固体核磁CP/ MAS13C-NMR在植物纤维原料研究中的应用[J]. 中国造纸学报, 2005, 20(2): 184.
[11] Nobutaka Fukagawa, Gyosuke Meshitsuka, Atsushi Ishizu. A Two-dimensional NMR Study of Birch Milled Wood Lignin [J]. J.Wood Chemistry and Technology, 1991, 11(3): 373.
