放化疗联合Ommaya囊置入化疗治疗囊性 脑转移瘤的临床观察
2014-08-08许德志王勇徐军朱玉方陶荣杰
许德志,王勇,徐军,朱玉方,陶荣杰
论著·临床
放化疗联合Ommaya囊置入化疗治疗囊性 脑转移瘤的临床观察
许德志,王勇,徐军,朱玉方,陶荣杰
目的观察放化疗联合Ommaya囊置入治疗囊性脑转移瘤的有效性及安全性。方法40例囊性脑转移瘤患者随机分为2组:Ommaya组24例,对照组16例。Ommaya组行Ommaya囊置入术,同时进行同步放化疗及瘤内化疗;对照组仅进行同步放化疗,均4周为1个疗程。2组均随访至2013年6月,比较2组的近期疗效、中位生存时间(MOS)、生存率及治疗相关不良反应。结果Oommaya组治疗后客观有效率为91.7%,高于对照组62.5%(P<0.05)。Oommaya组的中位生存期为16月,对照组的中位生存期为6月。Ommaya组6个月、1年、2年生存率分别为83.3%、75.0%和25.0%,明显高于对照组的50.0%、18.8%和0(P<0.05)。患者的耐受性好,2组相关不良反应比较差异无统计学意义(P<0.05)。结论放化疗联合Ommaya囊内化疗治疗囊性脑转移瘤,其疗效优于单纯放化疗,且不良反应轻,患者耐受性好。
Ommaya囊;放射疗法;化学疗法;脑转移瘤,囊性
脑转移瘤是颅外恶性肿瘤累及脑实质、脑神经、脑血管的转移性肿瘤。25%~40%的颅外恶性肿瘤在病程中发生脑转移,常见的原发肿瘤为肺癌、乳腺癌、恶性黑色素瘤、消化道肿瘤以及肾癌,脑转移瘤的预后非常差,不经治疗者中位生存期为3个月。由于恶性肿瘤的发病率越来越高,恶性肿瘤的治疗疗效的改善和生存期的延长,脑转移瘤的发生率也在增加,脑转移瘤生长迅速, 中心部位血供较差, 常发生坏死囊变, 而当脑转移瘤内坏死液化严重仅剩一薄壁时, 则称之为囊性脑转移瘤, 临床并不少见。囊性脑转移瘤多见于中老年患者, 原发灶以肺癌最为多见, 瘤灶多位于幕上, 以额、顶叶多见, 男性多于女性。由于囊性转移瘤往往有明显的颅高压的症状,且患者身体状况较差,因此给治疗增加了难度。囊性脑转移瘤患者的单一治疗疗效有限,因此联合治疗成为必然趋势, 经过Ommaya囊置入术后,既可减轻颅压,改善患者的症状,同时也能瘤内化疗。现对我院2008年6月—2011年 6月收治的24例囊性脑转移瘤患者进行Ommaya置入加放射治疗、化疗治疗,观察并比较其疗效和不良反应,现报道如下。
1 资料与方法
1.1 临床资料 囊性脑转移瘤患者均经手术病理或细胞学诊断证实,脑内病灶与原发病灶病理类型一致,将符合筛选条件的40例患者按随机数字法分成2组:Ommaya组24例,男15例,女9例,年龄42~70岁,中位年龄56岁;单个转移瘤10例,多个转移瘤14例;肺癌16例,乳腺癌6例,结肠癌2例;KPS评分50~80(64±10)分;幕上转移瘤19例,幕下转移瘤5例,肿瘤直径25~70(47.0±7.3)mm;发现原发灶至出现颅内转移瘤1~20(6.0±3.7)个月。对照组16例,男10例,女6例;年龄40~75岁,中位年龄59岁;单个转移瘤9例,多个转移瘤7例;肺癌10例,乳腺癌4例,结肠癌2例;KPS评分50~90(67±12)分;幕上转移瘤13例,幕下转移瘤3例,肿瘤直径23~68,(45.0±15.7)mm;发现原发灶至出现颅内转移瘤2~21(7.0±4.8)个月。2组患者在性别、年龄、转移瘤数目、肿瘤来源、肿瘤部位、KPS评分、肿瘤直径、发现原发灶至出现颅内转移瘤时间等比较,差异无统计学意义(P>0.05),具有可比性。
1.2 治疗方法 Ommay组患者行Ommaya囊置入术,根据CT和MR图像显示, 利用三维立体定向原理, 确定手术切口, Dandy 钻颅, 打开硬脑膜, 穿刺囊性病变, 抽取囊内液送化验后,将化疗泵的脑内端放在囊腔中心, 储液泵放在帽状腱膜下并且固定, 缝合切口。待切口愈合后行同步放化疗+瘤内化疗;对照组患者仅行同步放化疗。放疗方案:采用6MeVX线照射,全脑照射每次2 Gy,每周5次,4周为1疗程;根据患者具体情况行大孔径CT定位后局部脑转移灶缩野加量照射8~20Gy。放疗期间给予同步替莫唑胺75 mg·m2·d-1净化疗,持续至放疗结束。瘤内化疗方案为:先将瘤内液放至不外流,再将阿糖胞苷50mg/m2+地塞米松5 mg稀释后经Ommaya囊瘤腔内给药,每周1次,直至完全缓解。
1.3 观察指标 所有患者均定期随访,于放化疗前10天内及放化疗后每3个月行头颅增强MR检查,定期复查血常规、血生化、进行神经系统体格检查,记录客观有效率、生存期、症状及不良反应,评价药物毒性,调整用药。依据WHO关于肿瘤对治疗敏感性的标准评价肿瘤治疗的近期客观疗效:(1)完全缓解(CR),所有可见病灶完全消失并至少维持4周以上; (2) 部分缓解(PR),肿瘤最大径及其最大垂直径的乘积与治疗前相比较减少50%以上,并维持4周以上,无新病灶出现,神经系统症状稳定或改善; (3) 稳定(SD),病灶两径乘积减小50%以下,或增大25%以内,维持4周以上,无新病灶出现; (4) 疾病进展(PD),病灶两径乘积与治疗前相比较增大25%以上或出现新病灶,神经系统症状恶化或死亡。其中CR、PR、SD为治疗有效,客观有效率(ORR)=(CR+PR+SD)/总例数×100%。放化疗期间出现的不良反应,参考WHO制定的抗肿瘤药物毒性反应分度标准。远期疗效按患者6个月、1年、2年生存率评价(失访病例按失访事件计算为死亡)。

2 结 果
2.1 近期疗效 全部患者均随访至2013年6月1日,全组患者有2例因病情迅速进展而未完成放化疗治疗。2组患者根据治疗前后CT或MR检查所示肿瘤的变化来评价患者的近期疗效,近期疗效为同步放化疗结束后2个月,Ommaya组24例中CR 5例(20.8%),PR 13例(54.2%),Sd4例(16.7%),Pd2例(8.3%),ORR为91.7%;对照组16例中,PR 5例(31.2%),Sd5例(31.3%),Pd6例(37.5%),ORR为62.5%。2组ORR比较差异有统计学意义(P<0.05)。
2.2 生存率与生存期 Ommaya组6个月、1年、2年生存率及中位生存期均高于对照组(P<0.05)。见表1。2组总生存期比较,差异有统计学意义(P<0.05)。见图1。
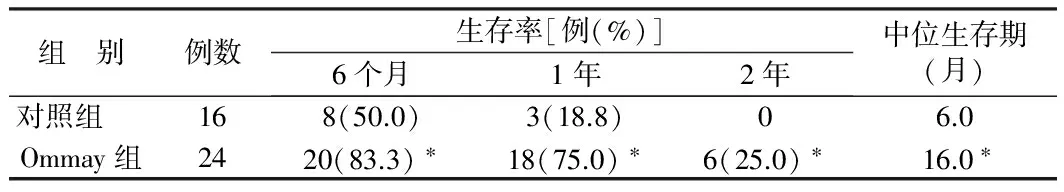
表1 2组生存率与生存期比较
注:与对照组比较,*P<0.05
2.3 不良反应 Ommaya组中术后无1例出现Ommaya囊堵塞、出血等相关并发症。出现颅脑感染1例,给予泰能治疗后治愈。治疗中的主要不良反应为胃肠反应、血液毒性和肝肾毒性, 且不良反应多只限于I~II级,均在给予对症药物处理后恢复。Ommaya组与对照组比较差异无统计学意义(P>0.05)。见表2。
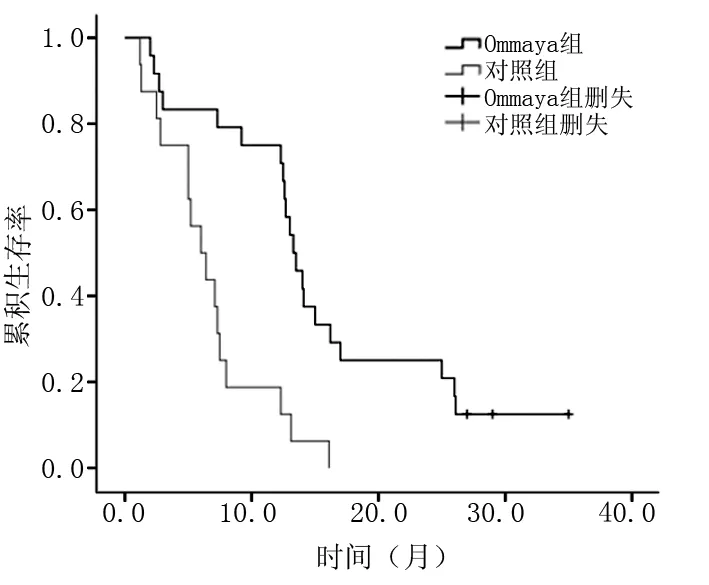
图1 2组患者总生存期曲线

表2 2组不良反应比较
3 讨 论
脑转移瘤最早于1898年由Bucholz[1]首先报道,是全身性肿瘤致残、致死的主要原因,脑转移瘤是一类原发于中枢神经系统以外,通过不同途径播散进入脑组织的肿瘤。脑转移瘤是目前为止成年人最常见的颅内肿瘤。脑转移瘤患者处于恶性肿瘤晚期,治疗已十分困难,生存期相当有限,不经任何治疗者中位生存期只有3个月[2]。目前对脑转移瘤的主要治疗手段包括全脑放疗(WBRT)、开颅肿瘤切除术以及立体定向放射外科手术。囊性脑转移瘤可发生在脑内任何部位,但最多发生于大脑中动脉供应的颞顶枕交界区,通常位于或邻近功能区脑皮质,如中央前后回、角回及颞上回或颞中回。由于多数囊性脑转移瘤的患者一般情况较差,不能耐受手术及手术全切,术后并发症较多,因此手术治疗十分有限。
囊性转移瘤由于肿瘤生长迅速,患者往往有明显的颅高压症状,肿瘤的占位效应明显,且患者身体状况较差,直接性放射治疗并不合适,因为囊性脑转移瘤放射治疗后囊液不能马上吸收,同时伴有脑水肿,不但不能缓解颅高压症状,反而增加了治疗的风险。Ommaya囊由巴基斯坦神经外科医生于1963年发明[3],因其有可反复抽吸、损伤小的特性,在神经外科逐步取得广泛应用。据报道[4],Ommaya囊的病死率和并发症发生率均较低,Ommaya囊留置比手术治疗创伤小、痛苦少,患者易接受,且术后并发症少、患者恢复快,使治疗具有重复性及连续性,对于许多囊液消退不明显的患者可经Ommaya囊进行抽吸囊液,避免了再次手术。经Ommaya囊抽吸囊液后,可将化疗药物注入瘤腔内,行瘤内化疗,既减少了化疗的不及反应,同时局部给药也提高了化疗的疗效。Ommaya囊常见并发症有颅内出血、继发感染、置管位置不正及堵塞等[5,6],为了减少并发症,在置入Ommaya囊时应偏向肿瘤的底部,并且尽量避开囊壁最厚处,避免穿刺失败,在经Ommaya囊放液或注入药物时,应缓慢操作,以免颅内压力急剧改变引起颅内出血,颅内感染常发生于Ommaya囊的使用过程中,其发生率为4%~9%,其发生与Ommaya囊使用频率无关,而与使用时无菌操作有关,严格的无菌操作有利于降低感染率。在操作时建议用葡萄糖酸洗必泰清洗头皮,用聚维酮碘小心消毒。本组病例中有1例发生颅内感染,给予抗生素治疗后治愈。
放疗在脑转移瘤的治疗中一直起着主要作用,Chao等[7]于1954年首先报道在脑转移瘤治疗中应用WBRT。根据肿瘤放射治疗组(RTOG)报道,1~4周内经20~40Gy剂量的全脑放疗可使脑转移瘤的中位生存期达到4~6个月,全脑放疗后症状改善率为70%~90%[8,9],50%的患者放疗后头痛、癫痫和颅高压症状改善,65%患者症状改善维持时间达到1年以上,而40%的患者脑神经功能障碍也得以改善。全脑放疗的急性并发症包括轻度疲劳、可逆性脱发、轻度头皮红斑和过度色素沉着。大多数并发症在6周内可自行缓解,一些回顾研究结果显示,一般日分割剂量1.8~2 Gy,总剂量40~45 Gy的WBRT方案较合理,可降低放疗的并发症而且预后良好。放疗中我们同步替莫唑胺作为全身化疗的主要药物,因其不但能很好地透过血脑屏障而且不良反应小,且更加适合于恶性肿瘤晚期患者。伽玛刀采用高能射线聚焦一次性大剂量定向照射靶区治疗病灶,其特点是定位准确,靶体积小,靶区周围正常组织剂量跌落梯度大。将高能射线一次性大剂量集中照射靶区,产生边界清晰的损伤灶,甚至放射性坏死,而对靶区周围正常组织损伤较小。国内伽玛刀治疗囊性脑肿瘤的总有效控制率为70%~90%,术后3d~1个月有明显症状改善[10~12]。但是伽玛刀治疗后脑水肿明显,患者的神经系统症状明显,降低了患者的生存质量。郑耕宇等[13]采用1次WBRT加多次立体定向32P囊内放疗21例,疗效较好,局部肿瘤控制率达89.2%,中位生存期13个月。本组患者总体局部肿瘤控制率为91.7% ,中位生存期16个月,不良反应较少,患者均可耐受。
综上所述,放化疗联合Ommaya囊置入化疗治疗囊性脑转移瘤可取得较好的疗效,可改善患者的生存质量,延长患者的生存时间。
1 Bucholz A.Kasuistischer Beitrag zur Kenntis der Karzinome des Zentralnervensystems[J].Monatsschr Psychiatr Neurol,1898,4:183-210.
2 于飞,杨进,聂歆闻.脑转移瘤立体定向放射治疗疗效分析[J].中国微创外科杂志, 2003, 3(5): 404-405.
3 Ammaya AK.Subcutaneous reservoir andpump for sterile access to ventricular cerebrospinal fluid[J].Lancct,1963,2(7315):983-988.
4 Amanaka Y,Shuto T,Kato Y,et al.Ommaya reservoir placement followedby Gamma knife surgery for large cystic mctastatic brain tumors[J].J Ncurosurg, 2006,105(Suppl):79-81.
5 邵宇权,胡兴越,程源深,等.ommaya管在中枢神经系统疾病中的应用[J].中国临床神经科学,2000,8(3):215-216.
6 王勇,高烨,许德志,等.经Ommaya囊脑室内化学治疗肺腺癌脑膜转移[J].中国临床神经外科杂志,2013, 18(4):209-212.
7 Chao J, Phillips R, Nickson J.Roentgen-ray therapy of cerebral metastases[J]. Cancer, 1954,7(4):682-689.
8 Borgelt B, Gelber R, Kramer S, et al.The palliation of brain metastases: final results of the first two studies by the Radiation Therapy Oncology Group[J]. Int J Radiat Oncol Biol Phys,1980,6(1):1-9.
9 Coia LR. The role of radiation therapy in the treatment of brain metastases[J].Int J Radiat Oncol Biol Phys,1992,23(1):229-238.
10 厉民,黄润生,卢刚,等. 80例多发性脑转移瘤的伽玛刀治疗.浙江创伤外科, 2001, 6(4): 234-235.
11 李文涛,孟喜军,刘昊,等.伽玛刀治疗脑转移瘤105例临床报告[J].山西医学杂志, 2001, 30(10): 616-617.
12 郭裕天,许建新,田新华,等.应用旋转式伽玛刀治疗脑转移瘤[J].立体定向和功能性神经外科杂志, 2002, 15(3): 171-172.
13 郑耕宇,严吕琬,梁 权,等.囊肿型脑转移瘤全脑放射加囊内放疗[J].中国神经精神疾病杂志, 2000, 26(4): 249-250.
ClinicalobservationontreatmentofcysticmetastaticbraintumorwithOmmayasacimplantationchemotherapycombinedwithchemoradiotherapy
XUDezhi*,WANGYong,XUJun,ZHUYufang,TAORongjie.
*ShandongAcademyofMedicalSciences,SchoolofMedicineandLifeSciences,AffiliatedwithUniversityofJinan,Jinan250022,China
ObjectiveTo observe the efficacy andsafety of chemoradiotherapy combinedOmmaya sac placement for treatment of cystic brain metastases.Methods40cases of cystic brain metastases were randomly dividedinto two groups: Ommaya group of 24patients, control group of 16patients, Ommaya group underwent Ommaya capsule implantation, concurrent chemoradiotherapy andintratumoral chemotherapy; control group for concurrent chemoradiotherapy are four weeks of a course of treatment. Two groups were followedup to June 2013, comparedtwo groups of short-term effect, the median survival time (MOS), survival, andtreatment-relatedadverse reactions.ResultsThe Ommaya group after treatment, objective response rate was 91.7%, higher than 62.5% of the control group (P<0.05).Ommaya group, the median survival time was 16months, in the control group, the median survival time was 6months. Ommaya group at 6months, 1-year, 2-year survival rates were 83.3%, 75.0% and25.0%, significantly higher than 50.0%, 18.8%, and0(P<0.05). Well toleratedby patients, two groups of relatedadverse reactions was no significant difference (P<0.05).ConclusionChemoradiotherapy combinedOmmaya sac placement for treatment of cystic brain metastases, its efficacy is superior to chemotherapy alone, andthe adverse reactions were mildly, patients toleratedwell.
Ommaya sac; Radiotherapy; Chemotherapy; Metastatic brain tumors,cystic
250022 济南大学/山东省医学科学院医学与生命科学学院(许德志);250117 济南,山东省肿瘤医院神经外科 (王勇、徐军、朱玉方、陶荣杰)
10.3969 / j.issn.1671-6450.2014.01.011
2013-08-28)
