Ti/Sb-SnO2电极电解后的表面状态变化
2014-08-08徐浩邵丹杨鸿辉延卫
徐浩,邵丹,杨鸿辉,延卫
(西安交通大学环境科学与工程系, 710049, 西安)
Ti/Sb-SnO2电极电解后的表面状态变化
徐浩,邵丹,杨鸿辉,延卫
(西安交通大学环境科学与工程系, 710049, 西安)
针对电极表面发生电化学反应而影响电极稳定性的问题,研究了0.1 mol·L-1的Na2SO4溶液中以5×10-3A·cm-2恒电流电解300 h后Ti/Sb-SnO2电极表面状态的变化,同时采用扫描电镜、元素分析和X射线衍射检测了该表面的状态,用电感耦合等离子体发射光谱仪检测了电解后溶液中的金属含量。结果表明:经长时间电解后的Ti/Sb-SnO2电极表面出现了氧化物层局部溶解及脱落的情况;电解完成后的溶液中检测到Sn元素;电极表层的物质仍为Sb-SnO2,但衍射峰强度有所降低,Ti峰强度大幅度升高。由此推测,表层氧化物层的溶解、局部区域的脱落以及基底与表面层之间的钝化可能是造成Ti/Sb-SnO2电极在长时间使用后失稳的主要原因。该结果可为改善Ti/Sb-SnO2电极表面形貌、提高表层氧化物负载量和电极稳定性研究提供参考。
Sb-SnO2电极;电解;表面;稳定性
电化学处理技术作为一种新颖的废水物化处理技术,具有操作参数简单、易于自动化、处理条件温和及对生物难降解废水具有较好处理效果等特点,受到越来越多科研工作者的关注与重视[1-4]。
电极的稳定性能一直是电化学水处理技术研究中的重要内容[5-6]。钛基体金属氧化物电极的稳定性更是决定其实用性的重要因素,从该种类电极被称为形稳阳极也可见其稳定性能的重要性[7]。作为钛基体金属氧化物电极的典型代表,Ti/Sb-SnO2电极由于表层Sb-SnO2氧化物性质的原因,其稳定性尚不能达到实用的要求[8-11]。
电极表面是发生电化学反应的主要场所,其表面形态的变化直接影响到电极的各种性质,尤其是其稳定性能[12]。如果能够将Ti/Sb-SnO2电极在长时间电解前后的表面状态进行对比,将有可能发现电极表面在形貌、氧化物晶型、元素分布等方面的差异,揭示电极在长时间电解过程中的反应历程,为分析其可能的失效原因奠定基础。
本文通过对Ti/Sb-SnO2电极在长时间电解反应前后的表面形貌、表层氧化物晶型、表面元素分布及电解液中金属元素浓度进行检测表征,获知电解过程对电极表面的影响,并由此分析电极表面的电解反应历程,揭示电极失效的可能原因。在此基础上,结合文献资料,提出改善Ti/Sb-SnO2电极稳定性的途径。
1 实验部分
1.1 电极制备
钛基体为2.5 cm×3 cm×0.5 mm的钛片(纯度为99.6%,宝鸡钛业股份公司),经600目砂纸打磨后用去离子水洗净;置于由质量分数为10%的NaOH和丙酮以体积1∶1混合成的洗涤液中超声除油1 h。将钛基体洗净后浸入微沸的质量分数为10%的草酸溶液中刻蚀2 h,取出后用去离子水洗净,备用。
配制含等体积无水乙醇、异丙醇、正丁醇的有机溶剂,Sn、Sb按摩尔比10∶1将所需的金属氯化物溶解在上述有机溶剂中,用浓盐酸调节液体的酸度为pH=1,即获得所用刷涂液[13]。此刷涂液需在使用前配制。
将前处理过的钛基体自然晾干,称重。将刷涂液均匀刷涂在钛基体上,放入120 ℃的烘箱中烘烤15 min,后放入450 ℃的马福炉(CMF1100,合肥科晶科技有限公司)中烧结15 min,取出后自然冷却,重复上述步骤共10次,最后一次在马福炉中450 ℃条件下烧结1 h,并在马福炉中自然冷却至室温后取出备用,此时的电极基体表面呈现蓝灰色。
1.2 电极性能测试
电极表面形貌使用扫描电子显微镜(FESEM,JSM-6700F,JEOL)观察,电极表面元素分布情况采用FESEM自带能谱测试仪(EDS)来分析;电极表面材料组成与结构使用X射线衍射仪(XRD,Rigaku D/MAX-2400X,Cu-Ka靶)来测定。
电化学测试在两电极体系中进行,以Ti/Sb-SnO2电极为阳极,相同尺寸的铜片为阴极,采用LK3200A型电化学工作站(天津兰立科公司)。长时间电解测试以0.1 mol·L-1的Na2SO4溶液为电解质,在电流密度恒定为5×10-3A·cm-2条件下进行,共进行300 h。长时间电解测试结束后,取电解液进行Sn及Sb元素浓度测试(ICP-OES,ICPE-9000,SHIMADZU)。
2 结果与讨论
2.1 电极表面形貌
图1为Ti/Sb-SnO2电极在长时间电解测试前后电极表面扫描电镜(SEM)图。由图1a可知,在电解测试前,其表面为典型的Sb-SnO2泥裂状多层重叠结构,存在大量明显的裂纹,裂纹宽度在0.2~0.3 μm范围内[8,11,14]。裂纹是由于表面Sb-SnO2层的热膨胀系数与钛基体不一致,导致在高温热处理及后续冷却过程中Sb-SnO2层开裂所造成。多层结构则是由于多次刷涂热解、氧化物层相互叠加导致,这样有利于提高基体表面氧化物的负载量。图1b~1d所示为电解测试完成后Ti/Sb-SnO2电极表面形貌。由图1b可知,表面Sb-SnO2泥裂状态依然存在,但出现大量氧化物溶蚀斑块,表明表层氧化物在电化学反应后溶解进入到电解液中,造成上述溶蚀斑块现象。溶蚀斑块较深处,能清晰看到下一层氧化物层(图1c中白框部分)。除溶蚀现象外,表面氧化物层的完整性也已被破坏,部分区域出现明显Sb-SnO2层脱落(图1d中白框部分)。
2.2 电极表面元素分布
表1为对图1a及图1b所示Ti/Sb-SnO2电极表面元素的EDS分析结果。由表1可知,电解前Sn与Sb的原子数之比n(Sn/Sb)为34.59,Ti与Sn的原子数之比n(Ti/Sb)为0.12,电解后n(Sn/Sb)为30.88,n(Ti/Sn)为0.33。
电解前电极表面n(Sn/Sb)的实测比值明显高于刷涂液中n(Sn/Sb) 值的原因可能在于热解过程中Sn与Sb两元素的挥发速度不一致。电解前能够检测到Ti元素则表明电极表面有些裂纹的深度已经达到钛基体。n(Sn/Sb)值在电解后有所降低,表明电解过程中Sn氧化物存在部分溶解的可能。n(Ti/Sn)值在电解后有一定程度的上升,表明电极表面的裂纹加深,破损处增加,导致钛基底(或是钛氧化物层)暴露的比率增大。

(a)电解测试前

(c)电解测试后表层溶解区

(b)电解测试后

(d)电解测试后表层脱落区
表1 Ti/Sb-SnO2电极长时间电解前后的 表面元素EDS分析结果
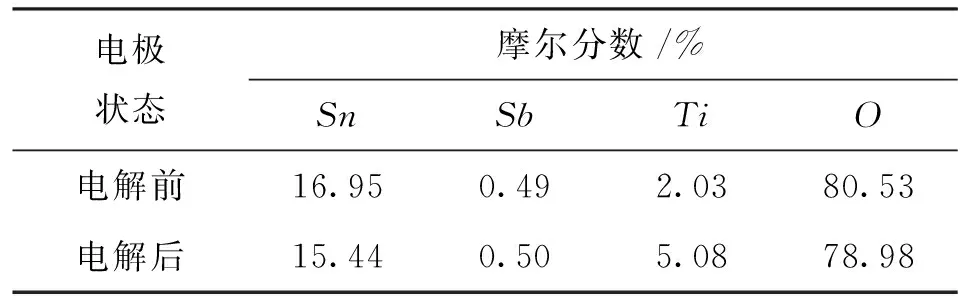
电极状态摩尔分数/%SnSbTiO电解前16.950.492.0380.53电解后15.440.505.0878.98
表2为对图1d所示Ti/Sb-SnO2电极表面未脱落处与脱落处的元素EDS分析。由表2可知,相比于未脱落处,脱落处的Ti元素量大幅度增加,n(Ti/Sn)值达到3.69,远高于未脱落处的0.06,表明氧化物层的脱落使得底层的钛氧化物层甚至钛基底暴露出来。
表2 Ti/Sb-SnO2电极表面未脱落和 脱落处元素分析
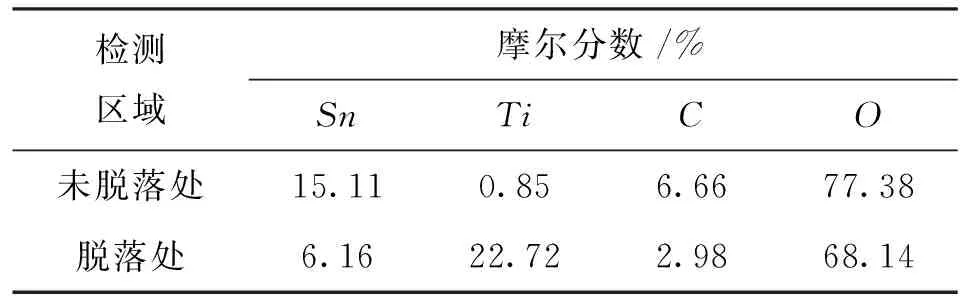
检测区域摩尔分数/%SnTiCO未脱落处15.110.856.6677.38脱落处6.1622.722.9868.14
2.3 电解液中元素含量
电感耦合等离子体发射光谱仪(ICP-OES)检测长时间电解完成后的电解液发现,其中Sn元素含量为0.013 2 mg·L-1,表明表层Sb-SnO2氧化物中的Sn元素由于表层电化学反应而溶解进入到电解液中,进而造成图1b、1c所示的溶蚀斑块现象。测试并没有检测到Sb元素,可能是由于其含量非常微小低于仪器的检测限所致。
2.4 电极表面XRD分析
图2为Ti/Sb-SnO2电极长时间电解测试前后X射线衍射(XRD)谱图。由图2可知,长时间电解前的电极衍射曲线在2θ为26.5°、33.8°与51.8°处出现的3处峰为SnO2特征衍射峰,没有出现Sb氧化物的特征峰;在2θ为38°、40°和71°处出现的3处衍射峰为Ti的特征峰。出现Ti特征峰可能是由于氧化物表层存在大量裂纹所致。
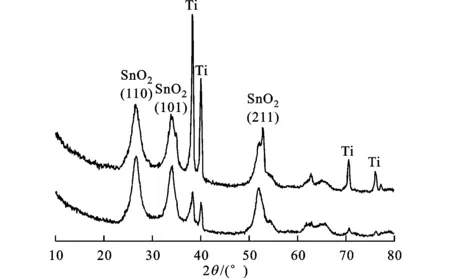
图2 Ti/Sb-SnO2电极测试前后XRD图
通过对比可知:电解后Sb-SnO2电极表面2θ为26.5°、33.8°与51.8°这3处SnO2特征衍射峰强度有所降低,可能是由于表面氧化物层部分溶解并进入溶液中,使得其负载量及结晶度减小,从而导致衍射峰强度下降;而38°、40°和71°这3处Ti特征峰的衍射强度均升高,表明由于电极长时间电解,使得表层Sb-SnO2氧化物出现溶蚀与破损现象,表面裂纹增大,甚至有部分区域出现Sb-SnO2氧化层脱落,暴露出更多钛基体。
2.5 电极表面状态改变历程分析
根据上述实验测试结果,可推测Ti/Sb-SnO2电极表面状态改变历程如下:当Ti/Sb-SnO2电极加电运行后,在电极/溶液界面处发生析气反应,不同的电解质溶液中所发生的反应如下

(1)

(2)
图1显示出Ti/Sb-SnO2电极表面有大量裂纹存在,电解液会沿着电极表面裂纹向基体方向扩散。式(1)、式(2)所示的析气反应不仅发生在涂层外表面,也会发生在电极内部的裂纹处。由图1可知,氧化物电极表面的缝隙及裂纹都在微米尺度,其缝隙内传质条件非常差。在如此狭小的空间内,所产生的气体压力将非常大,由此而带来的冲击作用,直接作用于涂层裂纹处,使得涂层与基体之间出现缝隙,进而导致涂层的机械脱落与崩离,如图1d所示。
根据式(1)、式(2)可知,随着电解反应的进行,溶液中H+不断积累,OH-不断消耗,由此会在阳极区域逐渐形成一个明显的酸性环境,处于其中的表层活性涂层组分会发生如反应式(3)所示的电化学反应,造成电极表面氧化物层溶解,如图1c所示。同时由于传质条件的限制,将使得裂纹及缝隙内的pH值远低于本体溶液的pH值,势必加速涂层氧化物的溶解。

(3)
在电化学溶解和机械脱落崩离的共同作用下,底部钛基体暴露在电解液中的比例显著增加,如表1与表2所示EDS测试数据以及图2所示XRD图所示。暴露的钛基体在电解液中很快会被氧化成为TiO2,造成电极在使用过程中电阻上升。除此之外,电极表面由于电化学反应而生成新生态氧,其中一部分转化为氧气,另外一部分则会吸附于电极表面。由于电场的作用,吸附部分的新生态氧将通过扩散的方式向基体方向迁移,进而氧化氧化物与钛基体界面处的Ti使之变为TiO2。此种氧化过程会随时间的推移而逐渐加深,导致TiO2绝缘层的范围越来越大,进而使得氧化物与钛基体界面处的导电通道逐渐缩小,直至消失。当电极使用时间达到一定值后,上述原因会导致表面氧化物层与底层钛基体之间的电阻不断增大,电极使用过程中的槽压不断升高,直至达到规定的氧化物电极失效标准。Ti/Sb-SnO2层电极长时间电解过程中表面层的变化趋势可由图3所示的过程来表示。
由上述数据结果、分析及图3可知,造成Ti/Sb-SnO2电极失稳的可能原因有以下几点:①氧化物层溶解/溶蚀,即表层金属氧化物由于电极/溶液界面处的环境而逐渐溶解到溶液中;②氧化物层脱落,即由于裂纹内大量释放的气体冲击基体与Sb-SnO2氧化物层而导致的表层脱落;③形成TiO2钝化层,使得表层与基体间之间的接触电阻随使用时间的延长而不断增加,直至电极失效。
2.6 技术改性方向
由上述分析可知,为提高Ti/Sb-SnO2电极的稳定性,可以从以下方面进行技术改性:①提高电极表面Sb-SnO2层的负载量,改善Sb-SnO2层的溶蚀性能,使得氧化物溶蚀的过程能够延长;②改善电极表面形貌,提高其Sb-SnO2层致密性,减少甚至阻断电解液向基体方面的渗透和扩散,使得氧化物层内部进行电化学反应的概率降低;③改善Sb-SnO2电极结构形式,阻断钛基体与电解液直接接触反应的通道。
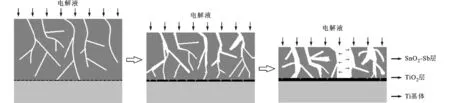
图3 Ti/Sb-SnO2层电极长时间电解过程中变化趋势示意图
要达到提高稳定性的目的,有以下几条路线可行:①采用新的Ti/Sb-SnO2电极制备方法,如电沉积法[15]、超声喷雾热解法[16]、溶剂热合成法[17]、梯度功能法[18]、旋转涂布法[19]和微波热解法[20]等;通过新方法来减少Ti/Sb-SnO2电极表面的裂纹,提高其负载量,进而提高电极稳定性;②采用其他元素或组分进行掺杂改性,使得涂层组分多元化,以提高电极的稳定性。最常用的掺杂元素是稀土金属元素[21-22];③改变电极的结构形式,即在Sb-SnO2层与钛基体之间引入中间层[23],或是利用TiO2纳米管阵列来作为新的Sb-SnO2电极基体,使得电极变成三维立体电极[24],进而提高稳定性。也可结合上述3条技术线路中的2条或是全部来进行Ti/Sb-SnO2电极改性,以进一步提高其稳定性。
3 结 论
本文采用SEM、XRD、EDS分析以及ICP-OES元素浓度检测等手段,测试了Ti/Sb-SnO2电极在长时间电解测试前后表面层性质的变化。SEM测试结果表明:Ti/Sb-SnO2电极在长时间电解后,电极表面存在区域氧化物层溶解及脱落的情况,表层元素分析表明使用后电极表面Ti元素量有所上升。ICP-OES检测发现,电解后溶液中Sn元素含量达到0.013 2 mg·L-1。XRD测试表明,在电极表层的物质仍为Sb-SnO2,但其衍射峰强度下降,Ti峰强度大幅度升高。由此推测造成Ti/Sb-SnO2电极失稳可能存在3种方式:表层氧化物层的溶解、表层氧化物层的脱落及基底与表面层之间的钝化。因此,Ti/Sb-SnO2电极的表面氧化物溶蚀性能、负载量,表面形貌以及电极结构形式对于该电极的稳定性存在较大影响。
[1] RAJESHWAR K, IBANEZ J G, SWAIN G M. Electrochemistry and the environment [J]. Journal of Applied Electrochemistry, 1994, 24(11): 1077-1091.
[2] MARTINEZ-HUITLE C A, FERRO S. Electrochemical oxidation of organic pollutants for the wastewater treatment: direct and indirect process [J]. Chemistry Society Reviews, 2006, 35(12): 1324-1340.
[3] MARTINEZ-HUITLE C A, BRILLAS E. Decontamination of wastewaters containing synthetic organic dyes by electrochemical methods: a general review [J]. Applied Catalysis: B Environmental, 2009, 87(3/4): 105-145.
[4] MARCO P, GIACOMO C. Direct and mediated anodic oxidation of organic pollutants [J]. Chemical Review, 2009, 109(12): 6541-6569.
[5] 孔德生, 吕文华, 冯媛媛, 等. DSA电极电催化性能研究及尚待深入探究的几个问题 [J]. 化学进展, 2009, 21(6): 1107-1117. KONG Desheng, LU Wwenhua, FENG Yuanyuan, et al. Advances and some problems in electrocatalysis of DSA electrodes [J]. Progress in Chemistry, 2009, 21(6): 1107-1117.
[6] LI Xiaohong, PLETCHER D, WALSH F C. Electrodeposited lead dioxide coatings [J]. Chemical Society Reviews, 2011, 40(7): 3879-3894.
[7] 张招贤. 钛电极工学 [M]. 第2版. 北京: 冶金工业出版社, 2003.
[8] SO Y Y, YEON S C, KIM S, et al. Boosting the electrocatlytic activities of SnO2electrodes for remediation of aqueous pollutants by doping with various metals [J]. Applied Catalysis: B Environmental, 2012, 111/112(12): 317-325.
[9] LI Peiqiang, ZHAO Guohua, CUI Xiao, et al. Constructing stake structured TiO2-NTs/Sb-doped SnO2electrode simultaneously with high electrocatalytic and photocatalytic performance for complete mineralization of refractory aromatic acid [J]. Journal of Physic and Chemistry: C, 2009, 113(6): 2375-2383.
[10]ADAMS B, TIAN M, CHEN A C. Design and electrochemical study of SnO2-based mixed oxide electrodes [J]. Electrochimica Acta, 2009, 54(5): 1491-1498.
[11]FENG Yujie, CUI Yuhong, LIU Junfeng, et al. Factors affecting the electro-catalytic characteristics of Eu doped SnO2/Sb electrode [J]. Journal of Hazardous Materials, 2010, 178(1/2/3): 29-34.
[12]SHAHRAM G, MIR F M, MOITABA S. Electrochemical deposition of lead dioxide in the presence of polyvinylpyrrolidone: a morphological study [J]. Electrochimica Acta, 2007, 53(2): 459-467.
[13]徐浩, 延卫, 游莉. 不同酸处理对钛基体性能的影响研究 [J]. 稀有金属材料与工程, 2011, 40(9): 1550-1554. XU Hao, YAN Wei, YOU Li. Effects of various acids treatment on the properties of titanium substrate [J]. Rare Metal Materials and Engineering, 2011, 40(9): 1550-1554.
[14]KONG Haishen, LU Haiyan ZHANG Wenli, et al. Performance characterization of Ti substrate lead dioxide electrode with different solid solution interlayers [J]. Journal of Material Science, 2012, 47(18): 6709-6715.
[15]DING Haiyang, FENG Yujie, LIU Junfeng. Preparation and properties of Ti/SnO2-Sb2O5electrodes by electrodeposition [J]. Materials Letters, 2007, 61(27): 4920-4923.
[16]YAO Peidong, JIN Qiannan, CHEN Xueming, et al. Ti/SnO2-Sb electrodes for pollutant degradation prepared using ultrasonic spray pyrolysis [J]. Electrochemical and Solid-State Letters, 2008, 11(5): J37-J39.
[17]HUANG Aisheng, ZHAO Guohua, LI Hongxu. High quality Sb-doped SnO2electrodes with high oxygen evolution potential prepared by in situ hydrothermal synthesis method [J]. Chinese Chemical Letters, 2007, 18(8): 997-1000.
[18]邹忠, 李杰, 丁凤其,等. 梯度功能型金属氧化物涂层阳极(DSA)的制备 [J]. 功能材料, 2001, 32(4): 431-433. ZOU Zhong, LI Jie, DING Fengqi, et al. Preparation of the functionally gradient metal oxide anode coating (DSA) [J]. Journal of Functional Materials, 2001, 32(4): 431-433.
[19]XU Hao, YAN Wei, TANG Chengli. A novel method to prepare metal oxide electrode: spin-coating with thermal decomposition [J]. Chinese Chemical Letters, 2011, 22(3): 354-357.
[20]XU Hao, TANG Chengli, ZHANG Qian, et al. A microwave approach to the preparation of Sb-doped SnO2electrode [J]. Journal of Inorganic Materials, 2012, 27(6): 667-672.
[21]BERENGUER R, QUIJADA C, MORALLON E. Electrochemical characterization of SnO2electrodes doped with Ru and Pt [J]. Electrochimica Acta, 2009, 54(22): 5230-5238.
[22]CUI Yuhong, FENG Yujie, LIU Zhengqian. Influence of rare earths doping on the structure and electro-catalytic performance of Ti/Sb-SnO2electrodes [J]. Electrochimica Acta, 2009, 54(21): 4903-4909.
[23]崔玉虹, 冯玉杰, 刘峻峰. 含Mn中间层钛基二氧化锡电催化电极的性能 [J]. 材料研究学报, 2005, 19(1): 47-53. CUI Yuhong, FENG Yujie, LIU Junfeng. Performance of Ti-base SnO2electrode with an inter layer containing Mn element [J]. Chinese Journal of Materials Research, 2005, 19(1): 47-53.
[24]ZHAO Guohua, CUI Xiao, LIU Meichuan, et al. Electrochemical degradation of refractory pollutant using a novel microstructured TiO2nanotubes/Sb-doped SnO2electrode [J]. Environmental Science and Technology, 2009, 43(5): 1480-1486.
[本刊相关文献链接]
吴春,陈刚,彭勃.中温固体氧化物燃料电池LaNiO2.5-Ba(Zr0.1Ce0.7Y0.2)O3-δ阴极的制备和表征.2013,47(2):92-96.[doi:10.7652/xjtuxb201302016]
马扬洲,徐友龙,肖芳,等.影响脉冲电流法制备MnO2超级电容器电极性能的因素.2011,45(9):114-118.[doi:10.7652/xjtuxb201109021]
燕子鹏,蔡舒,武卫兵.电化学法制备p型Cu2O半导体薄膜及其性能的表征.2011,45(3):121-124.[doi:10.7652/xjtuxb201103023]
连芩,刘红忠,丁玉成,等.TiO2光阳极有序微结构的纳米压印工艺.2009,43(11):90-94.[doi:10.7652/xjtuxb2009110 19]
钞书哲,丁玉成,叶向东,等.电子束直写模版电沉积制备图案化磁记录介质.2009,43(3):27-30.[doi:10.7652/xjtuxb 200903006]
Liang F U,卢天健,J.K.LUO.一种微型锌/空气电池的开发.2008,42(7):791-754.[doi:10.7652/xjtuxb200807001]
苗鹤,刘永锋,高明霞,等.Co替代Ni对钛钒基储氢电极合金循环稳定性的影响.2008,42(5):630-633.[doi:10.7652/xjtuxb200805026]
(编辑 刘杨 苗凌)
SurfaceAnalysisofTi/Sb-SnO2ElectrodeafterElectrolysis
XU Hao,SHAO Dan,YANG Honghui,YAN Wei
(Department of Environmental Science and Engineering, Xi’an Jiaotong University, Xi’an 710049, China)
The change in the surface morphology in electrochemical processes can directly affect the stability of the electrode. Ti/Sb-SnO2, the target electrode, was electrolyzed in the Na2SO4solution (0.1 mol·L-1) under constant current density condition (5×10-3A·cm-2) for 300 h. scanning electron microscope, energy dispersive spectrometer and X-ray diffraction (XRD) were used to determine the change in the surface morphology. Inductively coupled plasma optical emission spectrometry was used to determine the metal content in the electrolyte. Then the possible reason for the deactivation of the Ti/Sb-SnO2electrode after long time running was proposed. The SEM results show that the surface layer of the Ti/Sb-SnO2electrode was partially dissolved and some parts were even detached from the titanium base after electrolysis. The Sn element was detected in the electrolyte after electrolysis, suggesting that Sb-SnO2was indeed dissolved in the electrolyte. The XRD analysis indicates that the surface layer was still Sb-SnO2but the diffraction peak intensity decreased. It appears that the anode deactivation may result from the dissolution and detachment of the oxide layer and the passivation of substrate. The result can be useful for the enhancement of the electrode stability.
Sb-SnO2electrode; electrolysis; surface; stability
2013-05-06。 作者简介:徐浩(1984—),男,博士,讲师;延卫(通信作者),男,教授,博士生导师。 基金项目:中国博士后科学基金资助项目(2013M532053);教育部高等学校博士学科点专项科研基金资助项目(20120201120058);中央高校基本科研业务费资助项目。
时间:2013-12-10 网络出版地址:http:∥www.cnki.net/kcms/detail/61.1069.T.20131210.1438.005.html
10.7652/xjtuxb201402016
TQ150
:A
:0253-987X(2014)02-0093-06
