应用经验模式分解去除近红外光的运动伪迹
2014-08-08魏颖雯闫相国
魏颖雯,闫相国
(西安交通大学生物医学信息工程教育部重点实验室, 710049, 西安)
应用经验模式分解去除近红外光的运动伪迹
魏颖雯,闫相国
(西安交通大学生物医学信息工程教育部重点实验室, 710049, 西安)
针对近红外光谱(NIRS)技术对运动十分敏感和运动伪迹会严重影响后续分析处理结果这一问题,提出了一种利用经验模式分解去除运动伪迹的方法(EMD-MAR)。首先计算NIRS信号的移动标准偏差,根据其概率分布特性自动选取阈值和确定运动伪迹范围,然后利用经验模式分解(EMD)将信号分解成多个固有模式,对在运动伪迹范围具有明显异常的固有模式置0来消除运动伪迹,最后将处理后的固有模式加和得到校正后的信号。仿真与实测结果表明,EMD-MAR方法可有效检测和消除NIRS测量中常见的基线漂移、瞬时脉冲以及短暂低频振荡3种运动伪迹,并且极大提高了运动伪迹的自动检测程度,利用经验模式分解可以在去除运动伪迹的同时有效保留NIRS信号中的生理信息,为NIRS信号预处理提供了一种有效手段。
运动伪迹;近红外光谱;经验模式分解
近红外光谱(NIRS)技术可以无损地探测脑组织中含氧血红蛋白和脱氧血红蛋白浓度的变化量,是一种测量大脑局部血液动力学信息以及新陈代谢状况的有效手段[1]。与其他的脑功能测量设备如正电子发射型计算机断层成像(PET)和磁共振成像(MRI)等相比,NIRS具有舒适安全、操作简单、成本低廉等突出优点,使之成为连续监测大脑血液动力学状况的绝佳手段[2-4]。近年来,NIRS技术在新生儿脑氧监测、手术过程监测、危重病人监测以及睡眠呼吸暂停监测等医学领域[5-7]得到了广泛应用。
NIRS测量对皮肤和探头的接触情况较为敏感,因此容易引入一些运动伪迹(MA)影响测量信号的质量,并最终影响后续分析处理结果的可靠性[8]。如何有效检测和去除NIRS中包含的运动伪迹,是NIRS应用研究中关注的重要内容。现有的NIRS运动伪迹检测方法主要有两种:一是基于近红外数据的检测方法;另一种是基于附加信号(如加速度传感器信号)的检测技术[9]。前者比较有代表性的是运动伪迹消除(MARA)算法[10],它通过计算近红外信号的移动标准差(MSD),根据预先设定的阈值来检测运动伪迹;后者需要在采集NIRS数据时同步采集一路加速度传感器信号,利用加速度传感器信号反映头部的运动信息,以此为基础判别NIRS信号是否含有干扰。但是,这两类运动伪迹检测方法一般都需要人工设定阈值,为实际应用带来很大困难。此外,对含有运动伪迹的NIRS信号进行校正时,MARA算法要求运动伪迹的变化幅度远大于NIRS信号本身,持续时间也要远长于NIRS信号的一个周期,对剧烈波动的尖峰处理效果并不理想;而基于附加信号的自适应滤波方法又完全依赖于外加信号的质量,校正结果极不可靠。
本文研究检测和去除NIRS中运动伪迹的有效方法,以MSD为基础,根据NIRS信号的概率分布特点,研究检测运动伪迹的自动阈值选取方法,然后利用运动伪迹检测结果并结合经验模式分解(EMD)技术,消除NIRS信号中的运动伪迹。
1 基于EMD的运动伪迹去除方法
本文提出的基于EMD的运动伪迹去除方法(EMD-MAR)包括以下5个步骤:①计算NIRS信号的MSD值;②自动选取阈值标记运动伪迹的存在区域;③对NIRS信号进行经验模式分解;④在EMD分解所产生的不同固有模式(IMF)中进行伪迹消除;⑤信号重构。
1.1 计算MSD
采用MARA算法中的运动伪迹探测方法,计算NIRS信号的MSD值s(t)[10]。其定义为
s(t)=
(1)
式中:t=k+1,k+2,…,N-k,其中N为NIRS信号x(t)的长度。每一时刻纳入计算的信号长度为2k+1,称之为滑动窗口宽度W,W=2k+1。
1.2 自动标记运动伪迹区域
NIRS测量得到的血液动力学信号具有缓慢变化的特征,NIRS信号中包含运动伪迹时,其s(t)远大于正常信号的s(t)。对计算所得的s(t)做频数分布直方图,s(t)较大的区域出现频数极低,见图1a。因此,可以根据信号本身的概率分布特性确定阈值的大小,以此来辨别信号是否含有运动伪迹。
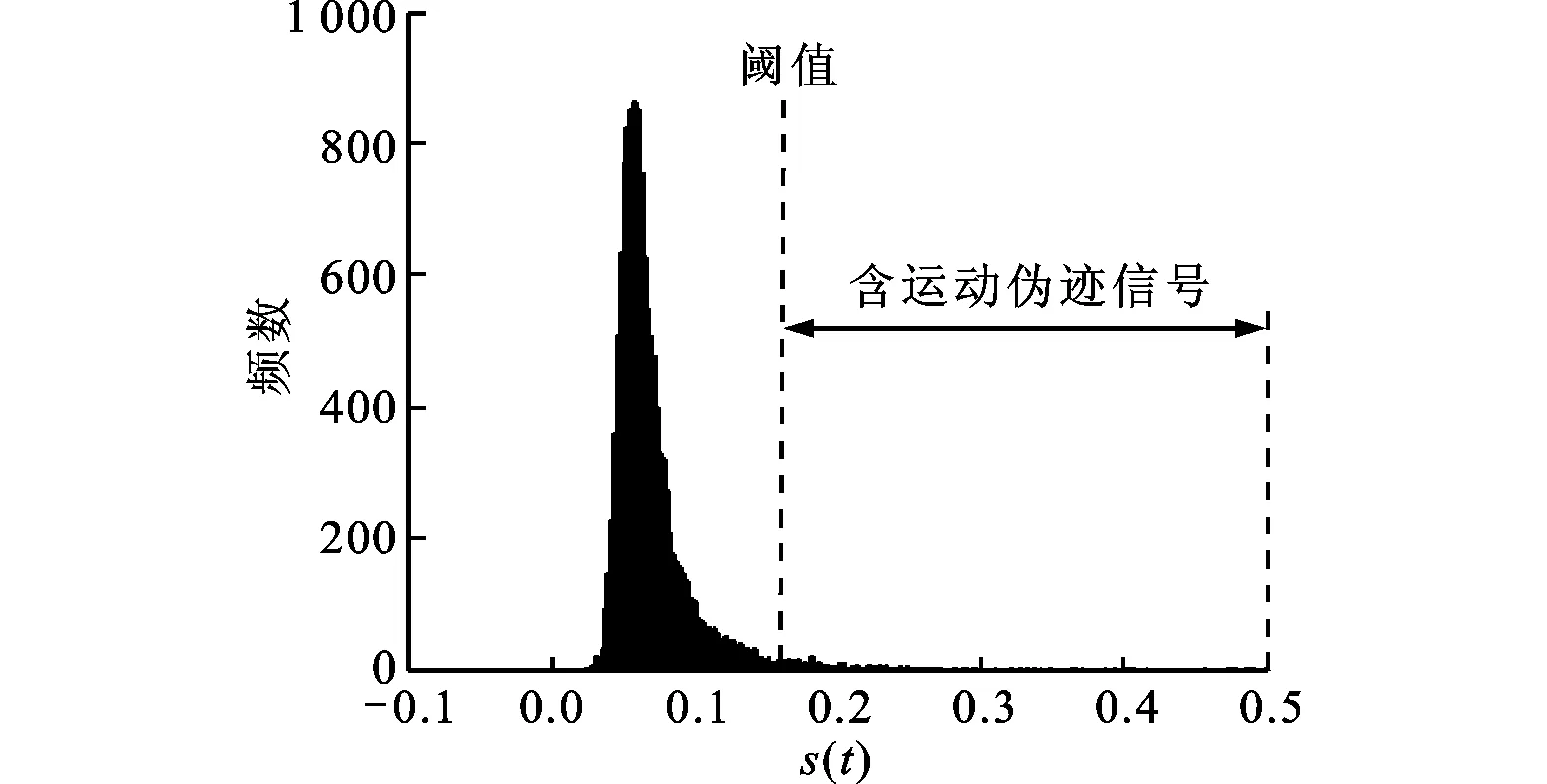
(a)s(t)的概率分布直方图
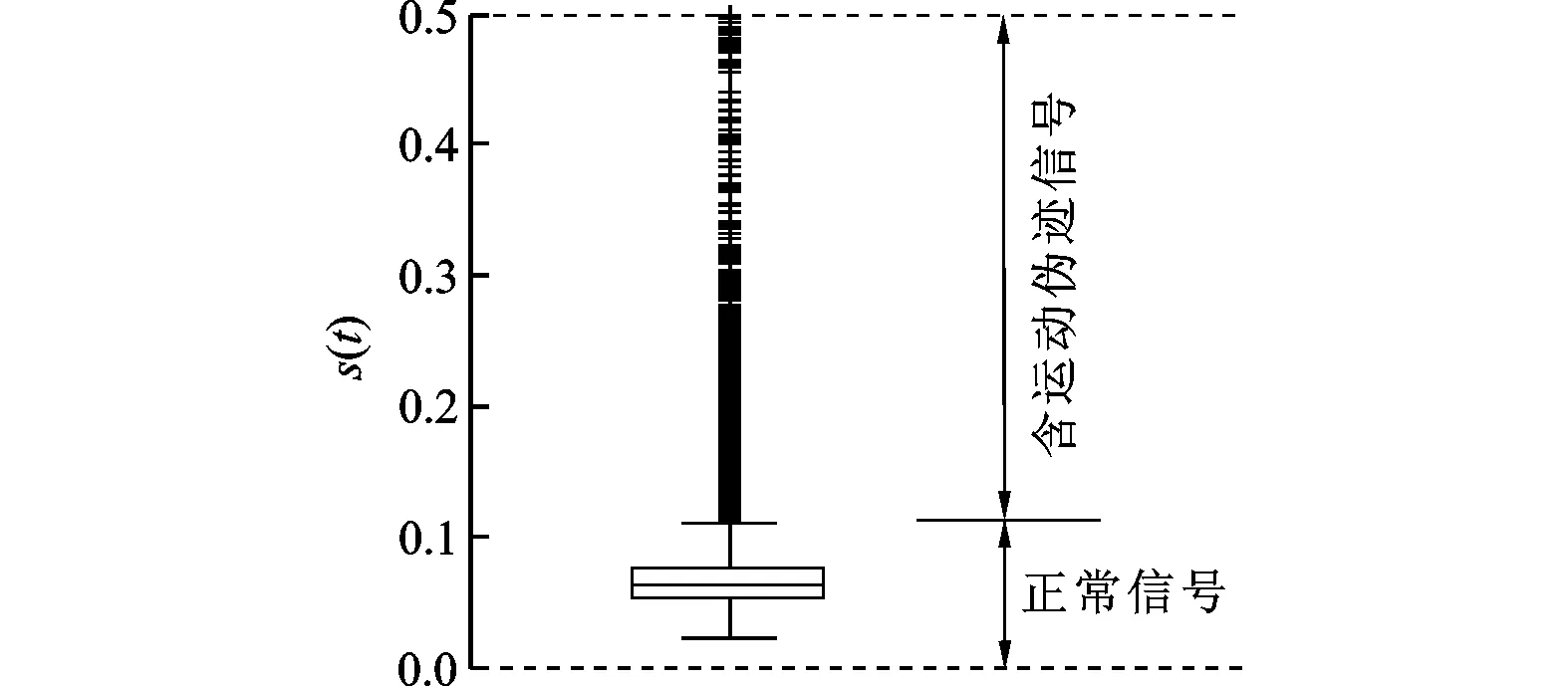
(b)s(t)的概率分布箱图
为了自动计算检测运动伪迹的MSD阈值T,对s(t)进一步做箱图分析,如图1b所示。图1b中矩形中间的横线表示s(t)的中位数,矩形上、下两条边分别表示s(t)的上四分位和下四分位,其余两条较短的横线表示的是上、下边界,上、下边界以外的部分为整个概率分布的离群值,如图中上边界外的点状重叠部分。因为含运动伪迹信号的MSD是整体数据的离群值,那么箱图中的上边界就可以作为区分正常信号和运动伪迹的阈值T。NIRS信号中MSD大于阈值T的部分为运动伪迹存在区域,小于T的为正常信号。将第i处运动伪迹的开始和结束位置分别标记为ma-start(i)和ma-end(i)。
1.3 经验模式分解
经验模式分解可以根据信号自身的时间尺度特征将信号分解成有限多个固有模式IMF,且不需要设立基函数,这是由信号本身驱动的一种自适应分析方法[11]。EMD可以将信号x(t)分解为
(2)
式中:cj是分解所得的第j个IMF;r是减去全部IMF后所得的残差项。
对含有运动伪迹的NIRS信号进行经验模式分解,所得固有模式分别为IMF1,IMF2,…,IMFn(n为EMD所得固有模式个数),和残差项r。NIRS信号是一种包含有呼吸、脉搏以及神经血管耦合相关的低频震荡等多种生理信息的多组分信号。EMD可将NIRS信号分解成与这些生理信息相关的成分,具有很好的生理学意义。图2所示为对实际采集的NIRS信号的分解结果,对各个固有模式进行频谱分析可得,IMF1和IMF2主要集中在1 Hz左右,表征脉搏效应;IMF3处于低频段0.2 Hz左右,表征呼吸效应;IMF4和IMF5表征0.1 Hz及以下的神经血管耦合相关的低频震荡;其余固有模式和残差为测量系统噪声和其他测量干扰的变化趋势。图2中虚线所示区域为标记所得的含运动伪迹的数据段。
1.4 运动伪迹的消除
由经验模式分解后,运动伪迹会以不同的强度分布于一些固有模式中,波形不规则且变化剧烈。观察EMD分解所得的各固有模式中运动伪迹区域(图2中所示的虚线区域)是否存在明显的异常波动,若存在则将此固有模式中对应区域的值置0,其余位置保持不变;若不存在,则该固有模式保持不变。

(a)时域 (b)频域
以图2为例,固有模式IMF3、IMF4和IMF5中的虚线标记区域存在变化剧烈的异常波动,因此将IMF3、IMF4、IMF5虚线区域对应的数值置0,虚线区域以外的值保持不变,其余固有模式受运动伪迹影响不大,不作改变。经伪迹消除以后的各固有模式分别记为IMF1’,IMF2’,…,IMFn’。EMD-MAR方法将信号细化后去除运动伪迹,最大限度地保证了生理信息的完整性。
1.5 信号重构
信号重构过程是把具有明确生理意义的固有模式IMF1’,IMF2’,…,IMFn’相加,舍弃测量系统噪声和其他测量干扰成分,重新建立起不含各种运动伪迹的真实信号。
2 结果及分析
我们用仿真信号和实际测量的NIRS信号对EMD-MAR方法进行分析研究。
2.1 NIRS信号仿真
NIRS信号含有多种生理信息,通过用4个正弦波信号外加高斯白噪声来模拟真实的NIRS信号xNIRS[10]

(3)
式中:ω=2πf;μ为正弦波的幅值;γ为高斯白噪声σ(t)的幅值。根据真实NIRS信号的统计平均值选择各信号成分的参数值[12-14],分别为:①超高频振荡,f=1 Hz,μ=0.6,γ=0.01,代表脉动效应;②高频振荡,f=0.25 Hz,μ=0.2,γ=0.01,代表呼吸效应;③低频振荡,f=0.1 Hz,μ=0.9,γ=0.01;④超低频振荡,f=0.04 Hz,μ=1,γ=0.05。第3和第4路信号共同表征神经血管耦合相关的周期性低频振荡。对以上4路信号合成的波形进行归一化处理,并平移至[-1,1]区间。仿真所产生的NIRS信号采样频率为10 Hz,取6 000点即10 min的信号对运动伪迹去除效果进行验证。
定义3种与xNIRS信号长度相同的信号xMA1(t)、xMA2(t)和xMA3(t)分别模拟实际NIRS信号中出现的典型运动伪迹:基线漂移(MA1)、瞬时脉冲(MA2)以及短暂的低频振荡(MA3)。在模拟xNIRS信号上分别叠加不同类型的运动伪迹生成对应的仿真NIRS信号,如图3所示。
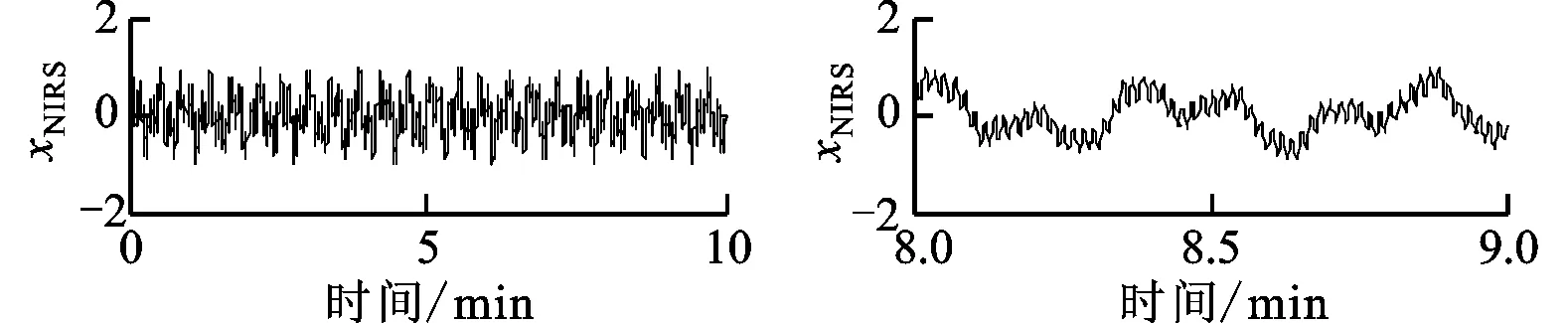
(a)仿真NIRS信号 (b)局部放大图
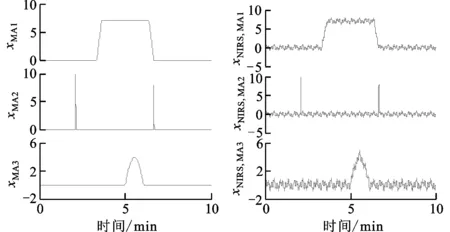
(c)3种运动伪迹信号 (d)运动伪迹信号与仿真信号叠加
2.2 运动伪迹检测
分别计算含有3种运动伪迹NIRS信号的移动标准差s(t)。根据数据的概率分布特性,采用箱图的上边界值作为阈值来界定信号含有运动伪迹的区域。窗口宽度和阈值分别如下:①W=151,T=0.050 7;②W=51,T=0.086;③W=401,T=0.033 8。运动伪迹探测结果如图4所示,其中阈值以上为含运动伪迹信号,阈值以下为正常信号,竖直的虚线表示运动伪迹的开始和结束位置。由图4可得,本文所述的自动阈值选取方法可以准确探测出NIRS信号中所存在的各类运动伪迹。
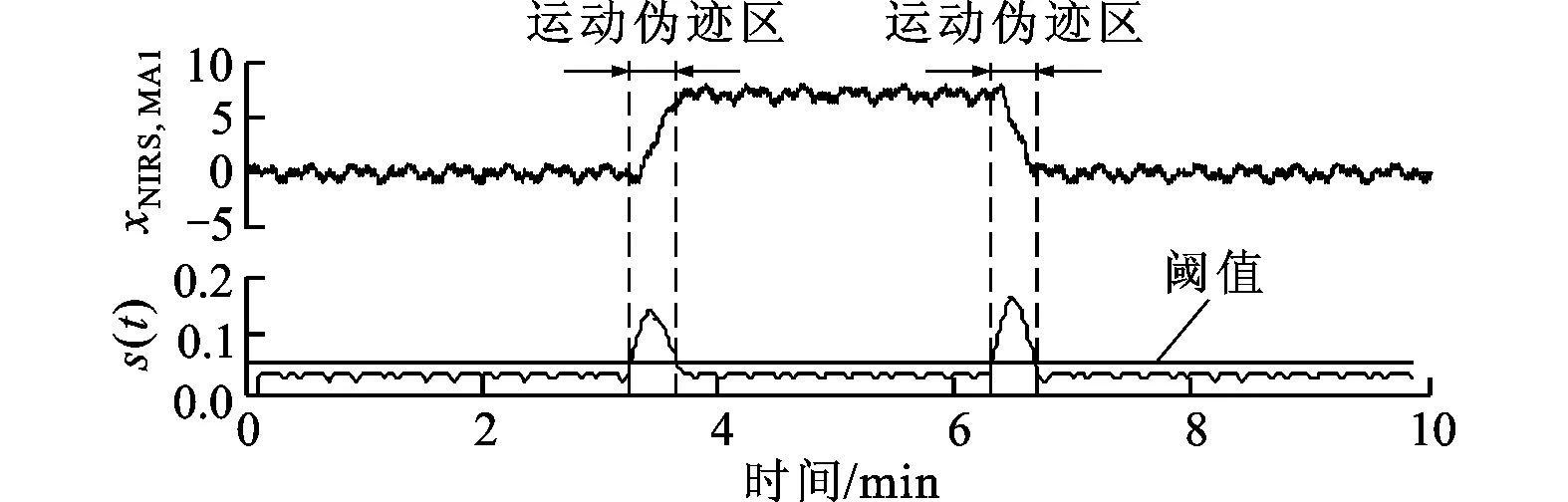
(a)基线漂移的s(t)及探测结果
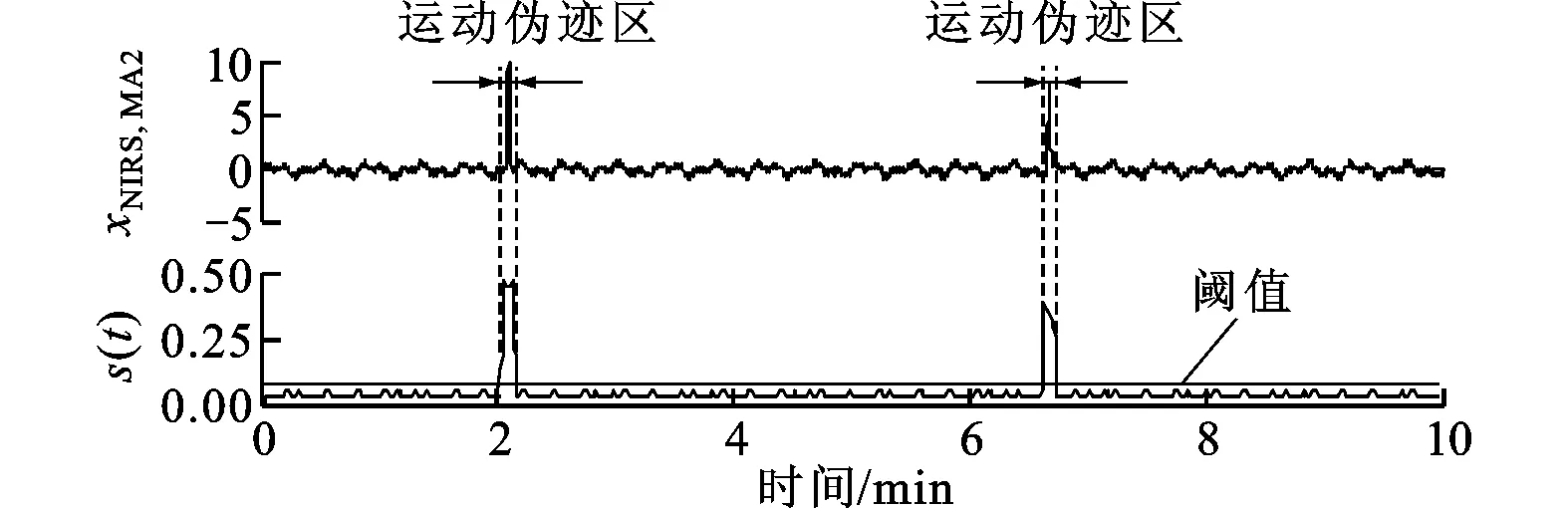
(b)瞬时脉冲的s(t)及探测结果
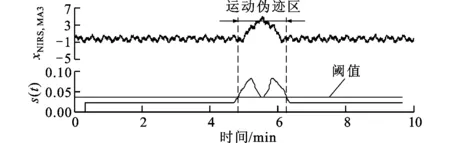
(c)低频振荡的s(t)及探测结果
2.3 经验模式分解消除运动伪迹
对仿真产生的含3种运动伪迹的NIRS信号进行经验模式分解,消除个别固有模式中运动伪迹区域所存在的异常波动。
运动伪迹去除前后的对比如图5所示,xNIRS,MA1、xNIRS,MA2、xNIRS,MA3为含运动伪迹的NIRS信号,yNIRS,MA1、yNIRS,MA2、yNIRS,MA3为运动伪迹去除校正后的信号。可以看出,无论是基线漂移、剧烈尖峰还是缓慢波动,本文所述方法均可以使之得到很好的校正,并且最大限度的保留有用的生理信号。
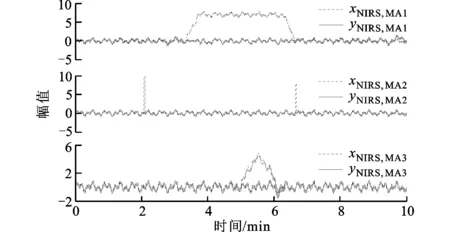
图5 3种仿真信号和经运动伪迹去除后的信号对比
2.4 仿真结果评价
为了评价去除运动伪迹后的信号质量,用信噪比n、均方根误差m和皮尔森相关系数r比较运动伪迹去除前后的信号与原始信号的相近程度,分别定义如下
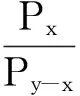
(4)
(5)
(6)
式中
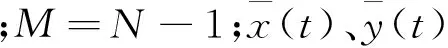
x(t)与y(t)越接近,均方根误差就越小,信噪比和皮尔森相关系数越大,其中r为区间[-1,1]中的数值,其绝对值越大表明信号的相关性越好。当信号x(t)和自身作对比时,n=∞,m=0,r=1。用以上参数对我们提出的EMD-MAR方法与文献[10]的MARA方法进行对比评价,结果如表1所示。其中,原始信号为xNIRS,含运动伪迹信号为xNIRS,MA1、xNIRS,MA2、xNIRS,MA3,MARA校正以后的信号为yMARA,MA1、yMARA,MA2、yMARA,MA3,EMD-MAR校正后的信号为yEMD,MA1、yEMD,MA2、yEMD,MA3。由表1可得,与MARA算法相比,EMD-MAR去除上述3种运动伪迹的效果更为突出,尤其是对于瞬时脉冲,经校正后,数据信噪比和皮尔森相关系数显著增加,均方误差明显减小,信号质量大幅提高。
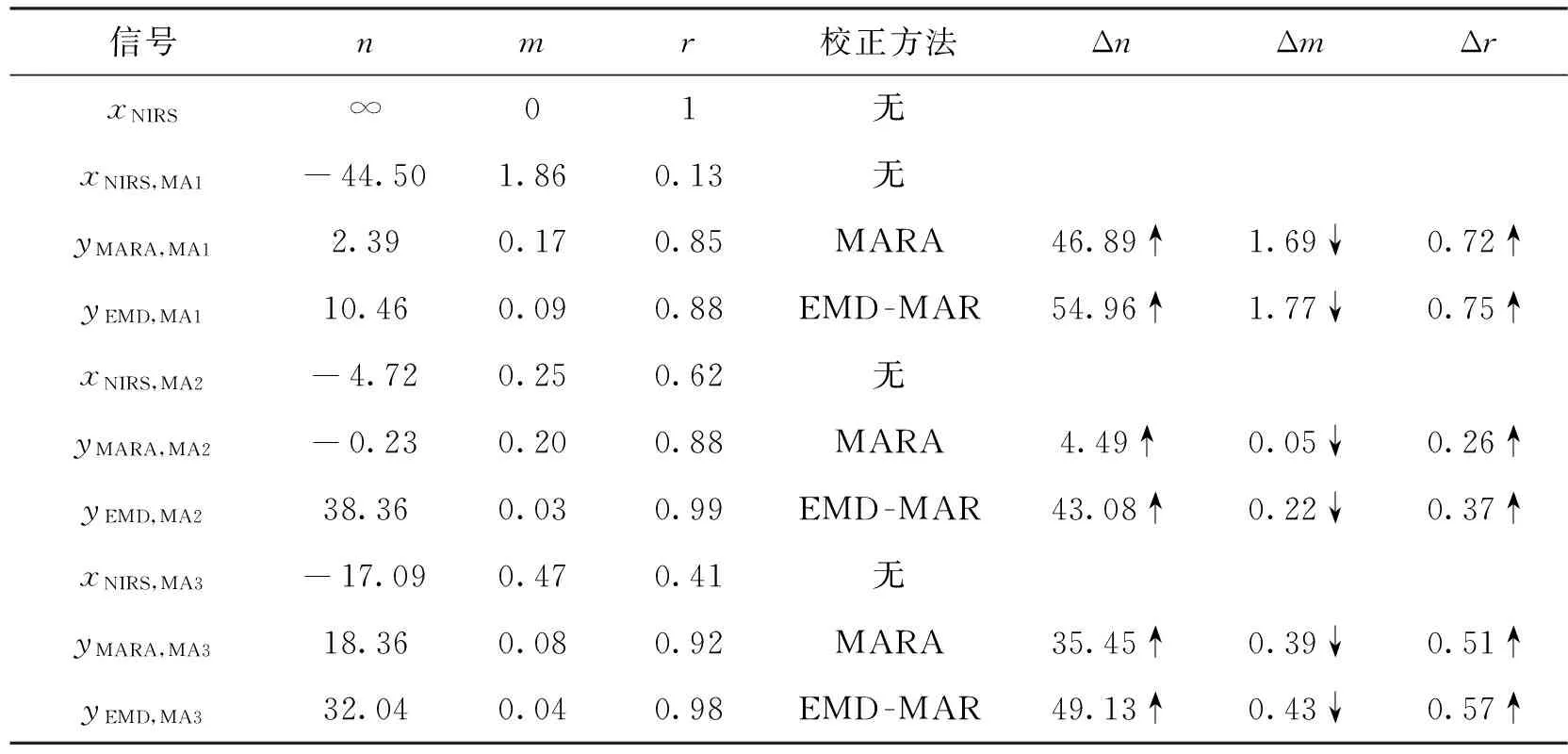
表1 运动伪迹消除算法的客观评价指标对比
2.5 实际NIRS信号校正结果
用实际采集的NIRS信号对EMD-MAR方法进行验证。本文使用连续光强度测量系统(CW)对受试者进行脑氧信号的提取。系统含有一个双波长LED光源,两个距光源位置为2 cm和3 cm的探测器,分别用来探测大脑浅层和深层信息。在测量时,将探头置于受试者前额,LED光源分时发出735 nm和850 nm波长的光,利用修正朗伯-比尔定理确定含氧血红蛋白和去氧血红蛋白的浓度变化量Δc(HbO2)、Δc(Hb),单位为μmol/L,采样率为10 Hz。
在实际的NIRS信号中各种运动伪迹通常不是单一出现的,相较于模拟仿真的运动情况更为复杂。图6所示为近端探测器所采集的含氧血红蛋白浓度的变化量ΔcHbO2和两种方法的校正结果,图中虚线区域为MSD自动阈值选取所探测出的含运动伪迹信号段。用MARA方法和本文EMD-MAR方法对同一段含运动伪迹信号进行去噪,结果显示相对于MARA算法,EMD-MAR方法对短暂的剧烈波动的尖峰有更好的去除效果,同时信号的基线漂移情况也得到有效消除。图7所示为另一时刻采集的近端ΔcHbO2信号,采用EMD-MAR方法同时校正其中所含有的多种运动伪迹,波形图显示信号恢复良好,且局部图形并没有发生明显变形。

图6 EMD-MAR和MARA方法校正结果对比
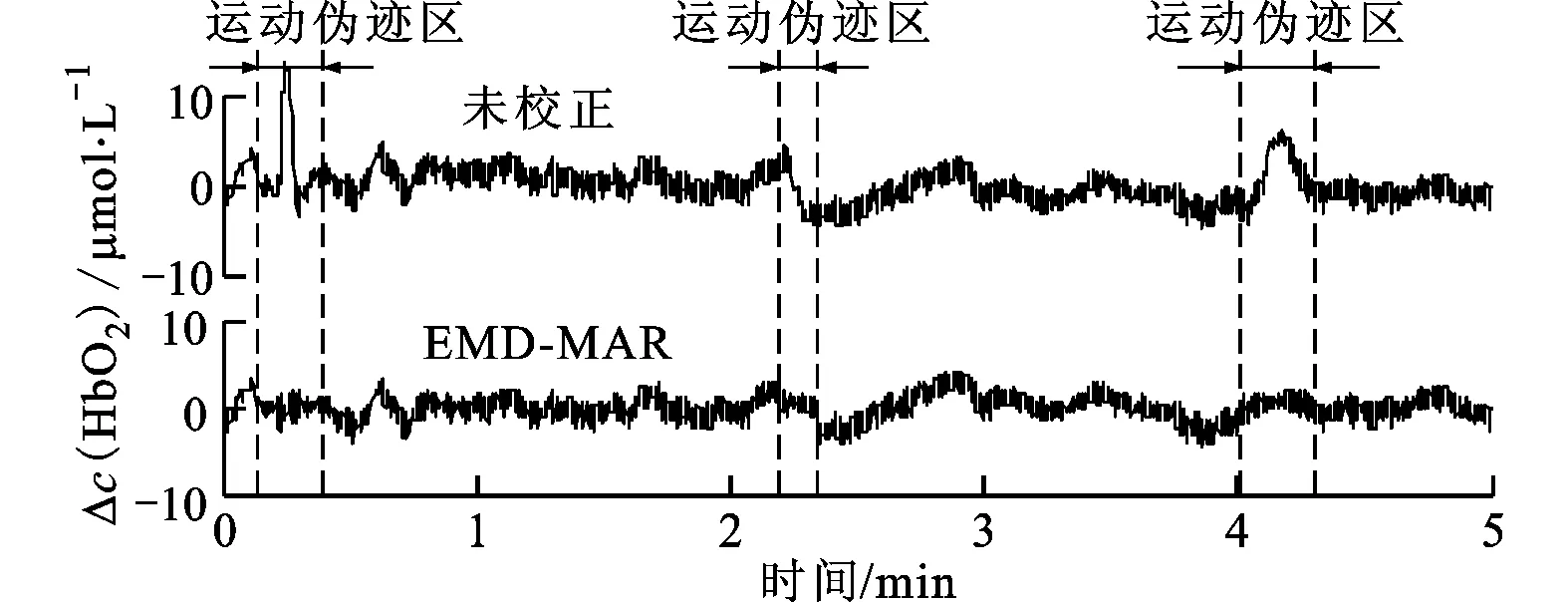
(a)校正结果
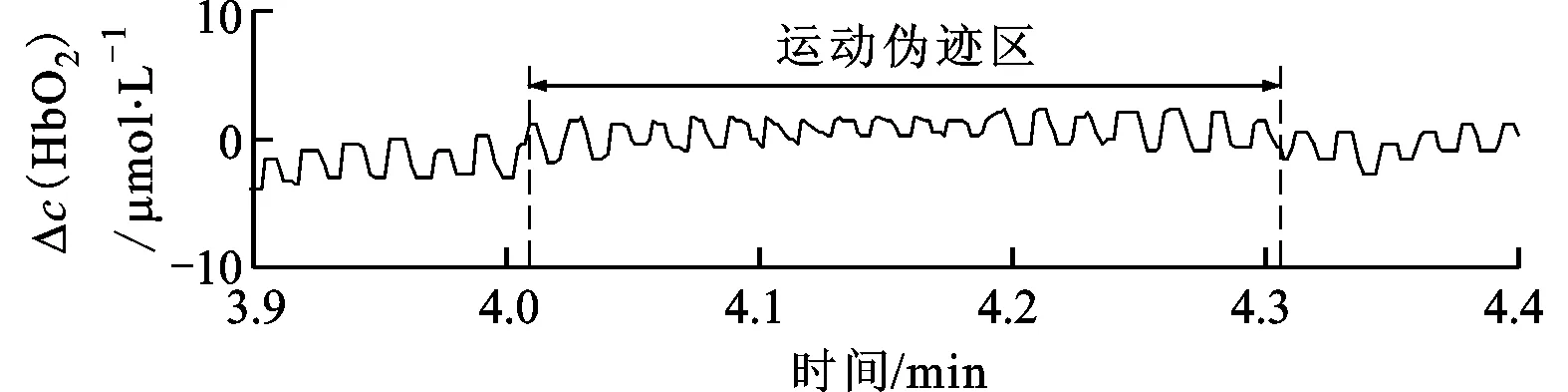
(b)局部波形
3 讨论与结论
本文提出了一种基于经验模式分解的近红外信号运动伪迹去除方法。此方法利用信号的MSD概率分布特性,自动选取阈值和检测含运动伪迹的数据段。与文献[10]的MARA方法相比,EMD-MAR方法极大地提高了运动伪迹的自动检测程度。对NIRS信号进行经验模式分解往往可得到具有明确生理意义的固有模式分量,通过对表现出明显异常的固有模式分量进行处理,可以在去除运动伪迹的同时有效保留NIRS信号中的生理信息,为后续处理打下了坚实基础。EMD-MAR方法同时也摒弃了MARA方法中要求运动伪迹的变化幅度、持续时间远大于NIRS信号的假设,即使是2~3 s的剧烈波动也具有很好的去除效果。对于NIRS信号发生基线漂移的情况,大部分已有算法都需要先进行运动伪迹消除再进行信号的拼接,算法复杂而且计算量大。EMD-MAR方法可以在去除运动伪迹的过程中同步消除基线漂移,在数据量较大的情况下具有明显优势。本文用模拟仿真和真实采集到的NIRS信号对运动伪迹的探测以及消除方法进行了验证和评价,结果证明EMD-MAR方法可有效检测和消除NIRS信号中存在的运动伪迹,在极大地改善了信号质量的同时又不影响到信号本身的特性,最大可能地保留了信号中的生理信息。EMD-MAR方法还存在一定的缺陷,有待进一步完善。首先,本文虽然解决了MSD方法中阈值T的自动选取,然而窗口宽度W还需要根据不同的运动伪迹多次尝试以作调整;其次,运动伪迹去除过程中经验模式分解所得的各固有模式中是否含有运动伪迹需要人工观察以作判定。因此,如何自动选取窗口大小,以及如何自动判别含运动伪迹的固有模式是我们下一步工作的方向。
[1] WALL P. Non-invasive optical spectroscopy and imaging of human brain function [J]. Trends Neurosci, 1997, 20(10): 324-325.
[2] OLOPADE CO, MENSAH E, GUPTA R, et al. A noninvasive determination of brain tissue oxygenation during sleep in obstructive sleep apnea: a near-infrared spectroscopic approach [J]. Sleep, 2007, 30(12): 1747-1755.
[3] IZZETOGLU K, BUNCE S, ONARAL B, et al. Functional optical brain imaging using near-infrared during cognitive tasks [J]. International Journal of Human-Computer Interaction, 2004, 17(2): 211-227.
[4] IZZETOGLU M, IZZETOGLU K, BUNCE S, et al. Functional near-infrared neuroimaging [J]. IEEE Transactions on Neural Systems and Rehabilitation Engineering, 2005, 13(2): 153-159.
[5] WOLF M, VON SIEBENTHAL K, KEEL M, et al. Tissue oxygen saturation measured by near infrared spectrophotometry correlates with arterial oxygen saturation during induced oxygenation changes in neonates [J]. Physiol Meas, 2000, 21(4): 481-491
[6] DAUBENEY P E F, SMITH D C, PILLINGTON S N, et al. Cerebral oxygenation during paediatric cardiac surgery: identification of vulnerable periods using near infrared spectroscopy [J]. European Journal of Cardio-Thoracic Surgery, 1998, 13(4): 370-377
[7] KIRHPATRICK P J, SMIELEWSLI P, CZOSNYKA M, et al. Near-infrared spectroscopy use in patients with head injury [J]. Journal of Neurosurgery, 1995, 83(6): 963-970.
[8] 赵一博, 韩妙飞, 闫相国. 几种漫射光学成像图像重建算法的比较研究 [J]. 西安交通大学学报, 2012, 46(4): 106-111. ZHAO Yibo, HAN Miaofei, YAN Xiangguo. Comparative research on several kinds of reconstruction algorithms for diffuse optical tomography [J]. Journal of Xi’an Jiaotong University, 2012, 46(4): 106-111.
[9] VIRTANEN J, NOPONEN T, KOTILAHTI K, et al. Accelerometer-based method for correcting signal baseline changes caused by motion artifacts in medical near-infrared spectroscopy [J]. Journal of Biomed Optics, 2011, 16(8): 087005.
[10]SCHLKMANN F, SPICHTIG S, MUEHLEMANN T, et al. How to detect and reduce movement artifacts in near-infrared imaging using moving standard deviation and spline interpolation [J]. Physiol Meas, 2010, 31(5): 649-662.
[11]HUANG N E, SHEN Z, LONG S R, et al. The empirical mode decomposition and the Hilbert spectrum for nonlinear and non-stationary time series analysis [J]. Proceedings of the Royal Society of London: Series A Mathematical, Physical and Engineering Sciences, 1998, 454(1971): 903-995.
[12]ELWELL C, SPRINGETT R, HILLMAN E, et al. Oscillations in cerebral haemodynamics [J]. Advances in Experimental Medicine and Biology, 1999, 471: 57-65.
[13]OBRIG H, NEUFANG M, WENZEL R, et al. Spontaneous low frequency oscillations of cerebral haemodynamics and metabolism in human adults [J]. Neuroimage, 2000, 12(6): 623-639.
[14]MULLER T, TIMMER J, REINHARD M, et al. Detection of very low-frequency oscillations of cerebral haemodynamics is influenced by data detrending [J]. Medical and Biological Engineering and Computing, 2003, 41(1): 69-74.
[本刊相关文献链接]
赵敏,郑崇勋,赵春临,等.利用Fisher判别式和事件相关电位的心理意识真实性识别.2010,44(8):132.[doi:10.7652/xjtuxb201008026]
赵敏,郑崇勋,赵春临.利用小波分解和支持向量机的心理意识真实性识别研究.2010,44(4):119-124.[doi:10.7652/xjtuxb201004025]
高军峰,郑崇勋,王沛.基于独立成分分析和流形学习的眼电伪差去除.2010,44(2):113-118.[doi:10.7652/xjtuxb2010 02023]
裴晓梅,郑崇,徐进.基于信息积累技术的大脑运动意识任务分类.2008,42(6):756-759.[doi:10.7652/xjtuxb200806023]
王晶,徐光华,张庆.经验模态分解和Kolmogorov测度的癫痫预测算法.2007,41(11):1364-1367.[doi:10.7652/xjtuxb 200711026]
于晓琳,张建保,王珏.基于功率谱分析的头皮电位和心率变异性关系研究.2007,41(8):991-994.[doi:10.7652/xjtuxb 200708025]
(编辑 杜秀杰)
MotionArtifactRemovalforNearInfraredSpectroscopybyEmpiricalModeDecomposition
WEI Yingwen,YAN Xiangguo
(MOE Key Laboratory of Biomedical Information Engineering, Xi’an Jiaotong University, Xi’an 710049, China)
Near infrared spectroscopy (NIRS) is very sensitive to the movement of a body. The motion artifacts (MA) coupled to the optical measurement seriously affect the subsequent analysis results. Aiming at this problem, a method by empirical mode decomposition (EMD) to remove the motion artifacts (EMD-MAR) is presented. The moving standard deviation (MSD) of a NIRS signal is evaluated. From the characteristics of the probability distribution of the MSD, the thresholds of MA detection are determined and the ranges of the MAs are detected automatically. Then EMD is adopted to decompose the signal into intrinsic mode functions (IMF). The values of the IMFs with obvious abnormal patterns within the detected range are set to zero to eliminate the MAs. All the IMFs treated are employed to reconstruct the corrected signal. The EMD-MAR is validated with simulated and real NIRS signals. The results show that it can effectively detect and eliminate the three kinds of MAs:baseline drift, transient impulse and transient oscillation, and a significant reduction of MAs and an increase in signal quality are achieved. The EMD-MAR method greatly improves the degree of automatic detection of motion artifacts to effectively keep the physiological information in a NIRS signal while the MAs are removed by the empirical mode decomposition.
movement artifacts; near-infrared spectroscopy; empirical mode decomposition
2013-08-21。 作者简介:魏颖雯(1989—),女,硕士生; 闫相国(通信作者),男,教授。 基金项目:国家“863计划”资助重大项目(2012AA02A604); 陕西省自然科学基础研究资助项目(2011JM4049)。
时间:2013-12-24 网络出版地址:http:∥www.cnki.net/kcms/detail/61.1069.T.20131224.0939.002.html
10.7652/xjtuxb201402022
R318.51
:A
:0253-987X(2014)02-0131-06
