固本抑瘤Ⅲ号方联合吉西他滨对人胰腺癌裸鼠异位移植瘤的抑瘤作用
2014-07-25刘炬钱海利徐志坚张立生叶霈智田爱平杨宏丽
刘炬,钱海利,徐志坚,张立生,叶霈智,田爱平,杨宏丽
(中国医学科学院北京协和医学院肿瘤医院,肿瘤研究所,1.防癌科,2.分子肿瘤学国家重点实验室,3.中医科,北京 100021)
胰腺癌是严重威胁人类健康的常见恶性肿瘤之一,也是常见实体瘤中预后最差的恶性肿瘤。随着人们生活水平的提高,胰腺癌的发病率呈明显上升趋势。虽然上个世纪80年代以来,各种常见实体瘤的治疗都取得了长足的进步,但胰腺癌的治疗水平无明显的提高。一项国际多中心临床研究代表了现代医学治疗胰腺癌的疗效:靶向治疗药物特罗凯联合化疗药物吉西他滨治疗不能手术的胰腺癌患者,中位生存期仅由吉西他滨治疗的5.9个月延长至6.4个月[1]。因此,迫切需要探索新的治疗思路和方法。
固本抑瘤Ⅲ号方是郁仁存主任医师治疗恶性肿瘤的经验方,经过多年的临床应用,证明其治疗常见癌症具有提高患者免疫力、改善患者生活质量的作用[2,3]。因此,尝试应用于胰腺癌动物模型研究。虽然观察药物临床疗效最直接的办法是进行临床试验,但由于患者之间的个体差异大、影响临床疗效的因素多等原因使临床药物疗效评价研究即临床试验花费巨大且耗时较长。动物实验研究周期短,可以设各种不同治疗组,恰好能够弥补临床研究的缺欠,能够在较短时间内得出一定的疗效结论,为临床研究和治疗提供有意义的线索和依据[4]。
裸鼠是免疫缺陷小鼠,人源性肿瘤细胞能够在其体内生长,人恶性肿瘤细胞裸鼠移植瘤模型能够较好地反应药物对人体癌症的治疗效果[5]。
因此,采用裸鼠人胰腺癌移植瘤模型探索固本抑瘤Ⅲ号方以及其与吉西他滨联合应用对裸鼠人胰腺癌移植瘤的抑瘤作用,以期指导临床实践,提高临床胰腺癌的治疗水平。
1 材料和方法
1.1 材料
1.1.1 人胰腺癌细胞株
采用PANC-1细胞株,冻存于中国医学科学院北京协和医学院肿瘤研究所药检中心。
1.1.2 实验动物及分组
SPF级BALB/c-nu裸小鼠40只,6周龄,雄性,体重17~18.5 g,来源于北京华阜康生物科技股份有限公司【SCXK(京)2009-0004】。无菌手术在中国医学科学院肿瘤医院SPF级动物实验室【SYXK(京)2008-0025】超净台内进行,并按实验动物使用的3R原则给予人道的关怀。
1.1.3 药品
吉西他滨(商品名:健择),美国礼来公司生产,批号:A731260A,以生理盐水配制成4 mg/mL溶液,每次给药前配制。固本抑瘤Ⅲ号方:生黄芪30 g、太子参30 g、白术 10 g、茯苓 10 g、女贞子 10 g、枸杞子 10 g、山萸肉 10 g、白英 20 g、龙葵 15 g、蛇莓 15 g、鸡内金 10 g、土茯苓 30 g、草河车10 g、鸡血藤30 g、焦三仙30 g。以上中药采用广州一方制药厂生产的免煎颗粒,颗粒混匀后,每付汤药加纯净水配制成90 mL中药汤剂,每毫升汤剂相当于生药3 g。中药复方灌胃给药,每日1次,每次0.5 mL。按每千克体重计算约相当于临床用药剂量的16倍。
1.2 实验方法
1.2.1 接种及分组方法
将冻存的PANC-1细胞复苏、传代、培养,接种于裸鼠右腋下,连续传代3代后,当第4代移植瘤生长至3周时,处死荷瘤裸鼠,取新鲜瘤组织,切成体积约8 mm3瘤块,接种于实验裸鼠右侧腋下,以上操作全部于超净台内无菌条件下进行。移植后第8天肿瘤于局部成活并生长至直径约0.5 cm,将动物随机分组为4组:对照组、吉西他滨组、固本抑瘤Ⅲ号联合吉西他滨组、固本抑瘤Ⅲ号组,每组10只裸鼠。
1.2.2 给药方式
自接种第8天起对各组给予不同治疗,①对照组每日灌胃给药0.5 mL纯净水,于吉西他滨组进行腹腔注射的同日,每周两次腹腔注射生理盐水0.5 mL。②吉西他滨组按照100 mg/kg剂量,以生理盐水配制成4 mg/mL,每周2次腹腔注射给药。③固本抑瘤Ⅲ号组为口服给药,每日1次,每次0.5 mL,共给药22 d。④固本抑瘤Ⅲ号联合化疗组每日灌胃给药0.5 mL固本抑瘤Ⅲ号汤药,同时按照100 mg/kg每周2次腹腔注射吉西他滨。
1.3 观察指标
1.3.1 抑瘤率
接种后第30天,安乐死全部裸鼠,分离移植瘤,称瘤重,抑瘤率=(对照组瘤重-治疗组瘤重)/对照组瘤重 ×100%。
1.3.2 移植瘤体积
自第8天开始治疗起,每周两次于吉西他滨给药前用游标卡尺测量各组移植瘤的长径和短径,肿瘤体积V=0.5×长径 ×短径 ×短径(mm3)。
1.3.3 裸鼠体重
自接种后第8天起,每周两次测量裸鼠的体重。
1.4 统计学方法
采用单因素方差分析进行组间差异比较,统计软件为SPSS 11.0。
2 结果
2.1 各组瘤重及抑瘤率
各组平均瘤重及抑瘤率详见表1。吉西他滨组平均瘤重明显低于对照组(P<0.05),固本抑瘤Ⅲ号联合吉西他滨治疗组抑瘤率进一步提高达68.9%,与对照组比差异有显著性(P<0.01),与吉西他滨组比差异有显著性(P<0.05),中药复方固本抑瘤Ⅲ号增加了吉西他滨抑制移植瘤生长的作用。单纯固本抑瘤Ⅲ号治疗组抑瘤率为28.0%,表现出一定的抑瘤作用,但差异无统计学意义。
2.2 体积的变化
各组体积的变化请见表2。接种后对照组腋下移植瘤体积增长迅速,其余各组移植瘤体积增长均受到了一定程度的抑制。接种时间越长,各治疗组抑制移植瘤生长作用越明显。接种后第22天,固本抑瘤Ⅲ号组、吉西他滨组以及固本抑瘤Ⅲ号联合吉西他滨组移植瘤体积明显低于对照组(P<0.05或P<0.01),接种后第27天,固本抑瘤Ⅲ号组、吉西他滨组以及固本抑瘤Ⅲ号联合吉西他滨组移植瘤体积明显低于对照组(P<0.05,P<0.01)。接种后30 d,吉西他滨组移植瘤体积明显低于对照组(P<0.001),固本抑瘤Ⅲ号联合吉西他滨组体积明显小于对照组(P<0.0001)。
表1 各组裸鼠瘤重抑瘤率的比较(±s,n=10)Tab.1 Inhibition rate of the tumor mass in the four groups
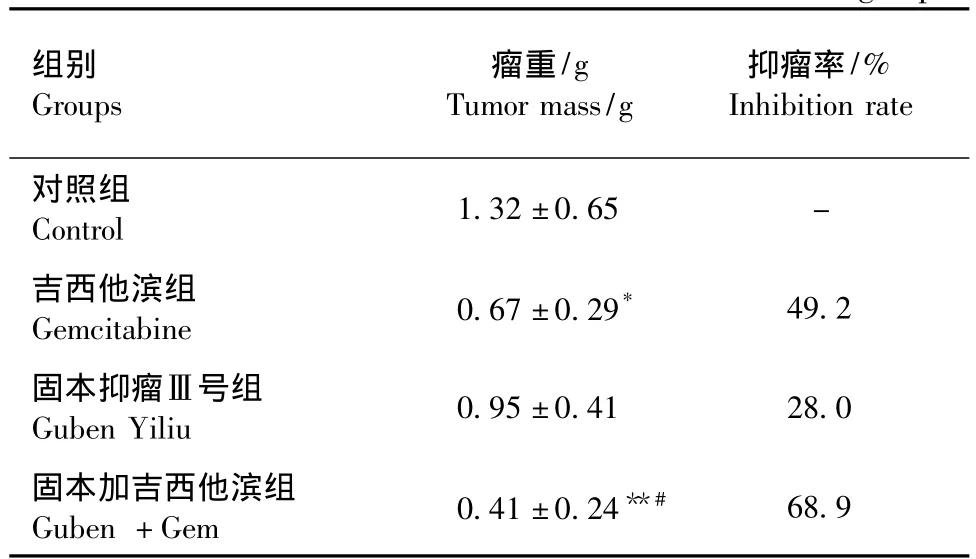
表1 各组裸鼠瘤重抑瘤率的比较(±s,n=10)Tab.1 Inhibition rate of the tumor mass in the four groups
注:*:与对照组比P<0.05,**:与对照组比P<0.01,#:与吉西他滨组比P<0.05。Note:*P <0.05,**P <0.01,vs.control group.#P <0.05,vs.gemcitabine group.
组别Groups瘤重/g Tumor mass/g抑瘤率/%Inhibition rate对照组Control 1.32±0.65 -吉西他滨组Gemcitabine 0.67±0.29* 49.2固本抑瘤Ⅲ号组Guben Yiliu 0.95±0.41 28.0 68.9固本加吉西他滨组Guben+Gem 0.41 ±0.24**#
表2 各组治疗后裸鼠移植瘤体积的比较(±s,mm3)Tab.2 The volume of transplanted tumors in the four groups after treatment
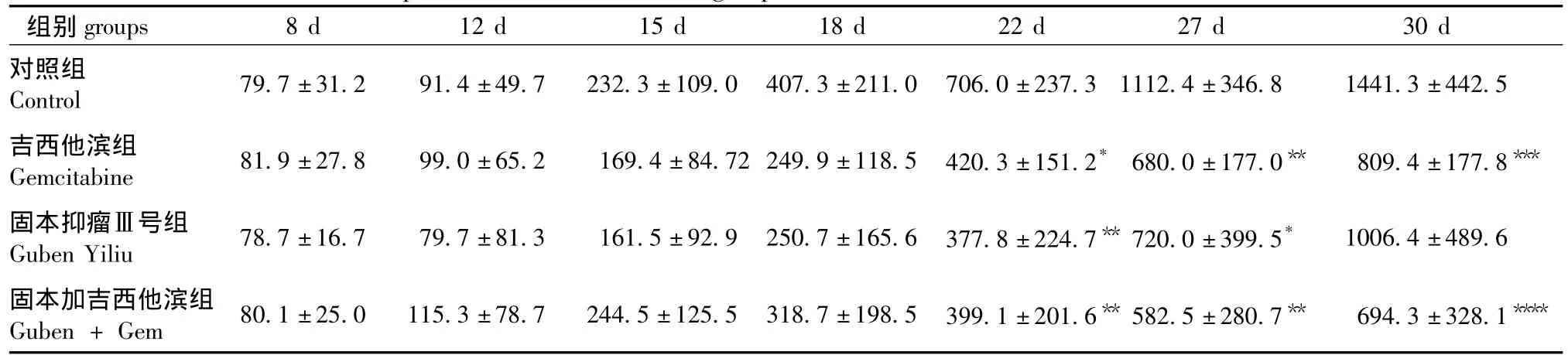
表2 各组治疗后裸鼠移植瘤体积的比较(±s,mm3)Tab.2 The volume of transplanted tumors in the four groups after treatment
注:*:与对照组比 P <0.05,**:与对照组比 P <0.01,***:与对照组比 P <0.001,****:P <0.0001。Note:*P <0.05,**P <0.01,***P <0.001,****P <0.0001,vs.control group.
组别groups 8 d 12 d 15 d 18 d 22 d 27 d 30 d对照组Control 79.7±31.2 91.4±49.7 232.3±109.0 407.3±211.0 706.0±237.3 1112.4±346.8 1441.3±442.5吉西他滨组Gemcitabine 81.9±27.8 99.0±65.2 169.4±84.72 249.9±118.5 420.3±151.2* 680.0±177.0** 809.4±177.8***固本抑瘤Ⅲ号组Guben Yiliu 78.7±16.7 79.7±81.3 161.5±92.9 250.7±165.6 377.8±224.7** 720.0±399.5* 1006.4±489.6固本加吉西他滨组Guben+Gem 80.1±25.0 115.3±78.7 244.5±125.5 318.7±198.5 399.1±201.6** 582.5±280.7** 694.3±328.1****
2.3 治疗的副作用
2.3.1 腹泻
实验期间各组裸鼠均存活,固本抑瘤Ⅲ号联合吉西他滨组、吉西他滨组均有一只裸鼠出现腹泻,2 d后恢复。
2.3.2 体重的变化
治疗前各组之间体重没有明显差别,开始治疗捒,联后治疗组在各个时间点上,体重均明显于对照组,差异有统计学意义。在接种后第15天、18天、30天,联合治疗组体重低于其他3组,差异有统计学意义。吉西他滨治疗组、固本抑瘤Ⅲ号组裸鼠体重与对照组相比差异无显著性(表3)。
表3 治疗后裸鼠体重的变化(±s,g)Tab.3 Changes of body weight of the mice in the 4 groups after treatment
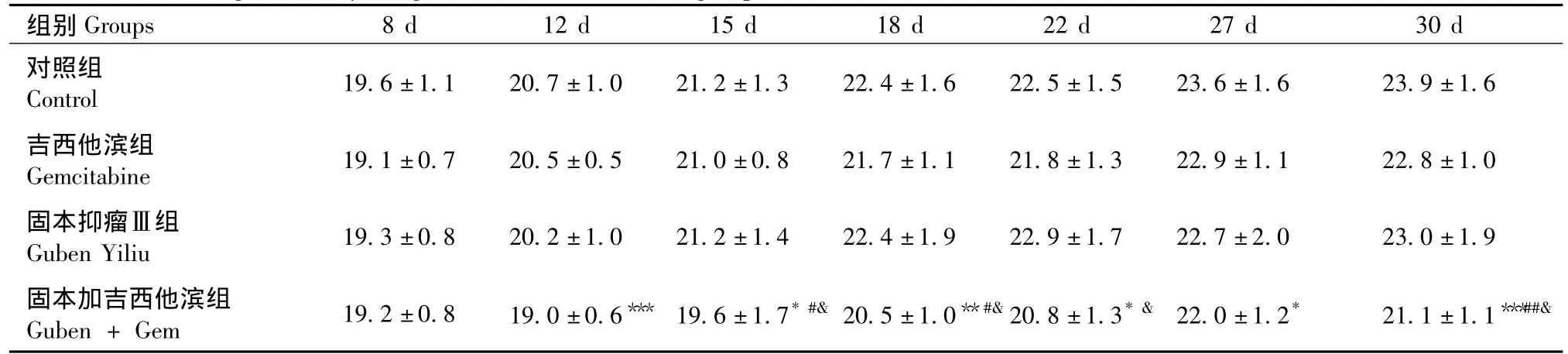
表3 治疗后裸鼠体重的变化(±s,g)Tab.3 Changes of body weight of the mice in the 4 groups after treatment
注:*:与对照组比P<0.05,**:与对照组比P<0.01,***:与对照组比P<0.0001,#:与吉西他滨组比 P<0.05,##:与吉西他滨组比 P<0.01,&:与固本抑瘤组比 P <0.05。Note:*P <0.05,**P <0.01,***P <0.0001,vs.control group.#P <0.05,##P <0.01,vs.gemcitabine group. &P <0.05,vs.Guben Yiliu group.
组别Groups 8 d 12 d 15 d 18 d 22 d 27 d 30 d对照组Control 19.6±1.1 20.7±1.0 21.2±1.3 22.4±1.6 22.5±1.5 23.6±1.6 23.9±1.6吉西他滨组Gemcitabine 19.1±0.7 20.5±0.5 21.0±0.8 21.7±1.1 21.8±1.3 22.9±1.1 22.8±1.0固本抑瘤Ⅲ组Guben Yiliu 19.3±0.8 20.2±1.0 21.2±1.4 22.4±1.9 22.9±1.7 22.7±2.0 23.0±1.9固本加吉西他滨组Guben+Gem 19.2 ±0.8 19.0 ±0.6*** 19.6 ±1.7*#& 20.5 ±1.0**#&20.8 ±1.3*& 22.0 ±1.2* 21.1 ±1.1***##&
3 讨论
本实验采用先天性免疫缺欠的实验动物裸鼠按临床应用情况设计实验组,探讨了固本抑瘤Ⅲ号方及其与吉西他滨联合应用对裸鼠人胰腺癌移植瘤的抑瘤作用。
裸鼠因为缺乏胸腺,不具备T细胞免疫力,故对异种移植不产生排斥反应。与人胰腺癌裸鼠原位移植癌相比,皮下种植的异位移植瘤模型具有移植成功率高且易于观察疗效和实施治疗的优点[5]。
在动物移植瘤抑瘤率观察上,抑瘤率是最重要的观察指标。由于移植瘤质量能够得到精确的测量,而移植瘤体积因为形状一般不规则难以得到准确的测量,所以采用移植瘤质量的抑瘤率较移植瘤体积指标能够更精确地反映药物治疗的抑瘤作用。
中药或者中药复方治疗人胰腺癌裸鼠移植瘤的研究报告较少。中药复方清胰化积方的研究采用人胰腺癌SW1990细胞移植瘤进行了研究,清胰化积中药移植瘤质量抑瘤率为21.3% ~38.2%,与固本抑瘤Ⅲ号方接近。研究认为调节癌基因及其相关的信号传导、改变肿瘤细胞蛋白合成等可能为作用机制,研究未设中药与化疗联合治疗组[6]。另一篇文章报告采用人胰腺癌SW1990细胞移植瘤模型发现中药成分大黄素与吉西他滨联合能够增强吉西他滨的抑瘤作用,机制在于促进SW1990细胞中Bax的表达和抑制Bcl-2的表达,研究采用的抑瘤率是移植瘤体积而非移植瘤质量[7]。一项采用人胰腺癌CFPAC-1细胞裸鼠移植瘤进行华蟾素的研究发现,华蟾素的抑瘤作用机制可能与IL-6、IL-8、s-VCAM-1等细胞因子表达下调有关[8]。中药合剂“振明正生”对裸鼠人胰腺癌P3移植瘤生长有一定的抑制作用,观察指标为移植瘤体积,给药时间为接种后24 h[9]。接种后开始给药时间越晚,抑瘤作用的强度要求越高。
本实验中,吉西他滨治疗组有明显的抑瘤作用,抑瘤率为49.2%,裸鼠移植瘤模型证实了吉西他滨治疗的有效性,与临床研究结果一致[10],说明裸鼠人胰腺癌移植瘤模型能够较好地反映临床上胰腺癌治疗的疗效。
研究中,固本抑瘤Ⅲ号显示了一定的抑瘤作用,抑瘤率28.0%,从移植瘤体积上看,在接种后第22天和27天,体积明显低于对照组,差异有显著意义。同时,固本抑瘤Ⅲ号联合吉西他滨组抑瘤率为68.9%,较单纯吉西他滨化疗组高。以上结果说明中药复方固本抑瘤Ⅲ号具有一定的抑制胰腺癌细胞生长的作用,且与吉西他滨的抑制胰腺癌细胞生长作用具有一定的协同作用。
体重能够反应治疗期间的副作用。从体重数据可以看出,吉西他滨组治疗后裸鼠体重的增加受到一定程度的抑制。与对照组比,固本抑瘤Ⅲ号组体重下降不明显。值得注意的是固本抑瘤Ⅲ号联合吉西他滨治疗组体重下降明显,较其他3组均有明显的下降(表3)。这一现象说明固本抑瘤Ⅲ号与吉西他滨联合应用可能有一定的协同副作用。即固本抑瘤Ⅲ号增加了吉西他滨化疗的疗效,同时也增加了吉西他滨化疗的副作用。单纯固本抑瘤Ⅲ号治疗有一定的抑瘤作用,没有明显的导致体重下降的副作用。在临床应用中,患者的化疗周期较长,化疗用药时间较短,需要根据患者的身体状况、化疗副反应的轻重、对化疗的耐受性等对固本抑瘤Ⅲ号进行加减,以充分利用固本抑瘤Ⅲ号增加疗效的作用,避免其增加吉西他滨化疗的副作用。另外,在化疗的间期以及不进行化疗期间,采用固本抑瘤Ⅲ号治疗也能够起到一定的抑制肿瘤生长的作用,这一点已通过初步的临床观察证实。
固本抑瘤Ⅲ号方是郁仁存主任医师治疗常见恶性肿瘤的经验方,体现了治疗恶性肿瘤扶正固本、袪邪的治则,方中同时也体现了益气活血、清热解毒的用药特点。应用于肺癌、乳腺癌、胰腺癌等常见的恶性肿瘤的治疗均起到了非常好的扶正、固本、抑瘤、延长生存期的作用[2,3]。在动物实验研究中也显示了较好的疗效[11]。方中主要由补气活血药,健脾补肾、清热解毒药物组成。全方攻补结合,因此在单纯固本抑瘤Ⅲ号治疗组未显示出明显的副作用但却有一定的抑制肿瘤生长的作用。在联合治疗组,由于化疗药物吉西他滨的强大的“攻”的作用,在整个治疗中固本抑瘤Ⅲ号方中补的力量明显不足,因此,出现了明显的体重下降。临床上,吉西他滨加固本抑瘤Ⅲ号治疗适合于一般情况好的患者。而对于一般情况差的患者,可以采用固本抑瘤Ⅲ号方加减治疗。
胰腺癌是目前肿瘤治疗面临的最大的难题之一,短时间内很难有重大的突破,而中医药治疗是非常值得探讨的领域。临床实践和初步的动物实验研究显示中药复方固本抑瘤Ⅲ号方治疗有一定的化疗增效作用。下一步的研究应该进行中药拆方研究以及可能有效的中药的抑瘤作用研究,从而发现更好的方剂组成原则以及更有效的中药,进一步提高中医以及中西医集合临床治疗胰腺癌的水平。
[1]Moore MJ,Goldstein D,Hamm J,et al.Erlotinib plus gemcitabine compared to gemcitabine alone in patients with advanced pancreatic cancer.A phase III trial of the National Cancer Institute of Canada Clinical Trials Group[NCIC-CTG][J].J Clin Oncol,2007,25(15):1960-1966.
[2]刘炬,郁仁存,饶燮卿,等.灸法和固本抑制瘤Ⅲ号结合化疗治疗中晚期恶性肿瘤的临床观察[J].中国中西医结合杂志,2001,21(4):262-264.
[3]刘炬,郁仁存,唐武军,等.灸法和固本抑制瘤Ⅲ号结合化疗对中晚期恶性肿瘤患者的免疫及凝血机制的影响[J].中国中西医结合杂志,2002,22(2):104-106.
[4]徐叔云,卞如濂,陈修.药理实验方法学(第三版)[M].北京:人民卫生出版社,2002.1757-1764.
[5]张波,赵玉沛,邓一伶,等.人胰腺癌荷瘤小树模型的建立及其生物学特性的研究[J].华西医学,2001,16(4):399-400.
[6]沈晔华,刘鲁明,陆燕,等.清胰消积中药对实验性胰腺癌基因表达的影响[J].中国癌症杂志,2005,15(5):454-461.
[7]魏为添,郭亚飞,陈辉,等.大黄素增强吉西他滨对裸鼠SW1990细胞移植瘤的抑瘤作用[J].中国中药杂志,2010,35(24):3348-3353.
[8]欧阳华强,谢广茹,潘战宇,等.华蟾素对人胰腺癌CFPANC-1移植瘤裸鼠血清IL-6,IL-8及sVCAM-1表达的影响[J].中国中药杂志,2011,36(19):2731-2733.
[9]应简子,贾培杰,姚蔷,等.中药合剂“振明正生”对三株人肿瘤细胞裸鼠移植瘤抑制作用的观察[J].现代肿瘤医学,2012,20(1):46-48.
[10]Kuroda T,Kumagi T,Yokota T,et al.Improvement of long-term outcomes in pancreatic cancer and its associated factors within the gemcitabine era:a collaborative retrospective multicenter clinical review of 1,082 patients[J].BMC Gastroenterol.2013,13:134-142.
[11]刘炬,郁仁存,丁瑞,等.综合疗法对小鼠肺腺癌爪垫皮下移植后的抑瘤及抗转移作用的研究[J].中国中医药信息杂志,2001,8(2):24-25.
