青藏高原伦坡拉盆地沉积岩中烷烃氢同位素与藿烷甾烷类成熟度指标的关系
2014-07-14马永嘉贾国东
马永嘉, 贾国东
(1. 中国科学院 广州地球化学研究所 边缘海地质重点实验室, 广东 广州 510640; 2. 中国科学院大学, 北京 100049)
0 引 言
正构烷烃因其来源广泛、纯化过程简单和较强的抗降解能力被作为最基本的生物标志物广泛用于各类研究中。生物所合成的烷烃中的氢主要来源于光合作用过程中所利用的水[1–2], 所以沉积物或岩石中的烷烃的氢同位素值(δD)能很好地反映生物生长时大气降水的情况, 从而被运用于古水文[3–5]和古气候[6–7], 甚至判断油气来源[8–11]的研究上。理论上讲, 正构烷烃能在地质体中非常长时间(106~108a)地保持其δD值不变[12], 但对于年代久远的样品, 通常需要考虑其δD值是否在成岩过程曾经遭受改造。对此, 目前主要有两种方法来进行验证: 一种是运用有机质成熟度指标, 如Ro和甾烷、藿烷类的一些指数等[4]; 另一种则是考察正构烷烃和类异戊二烯烷烃之间的δD值的差异情况。后者的原理是在生物体中, 由于合成方式的不同正构烷烃和类异戊二烯烷烃之间的 δD 值具有比较大的差异[13–15], 若遭受成岩改造作用, 会显著减弱上述差异。有研究表明,在甾烷和藿烷类成熟度指标显示即将达到低成熟阶段, 进入生油窗之前, 植烷(Ph)和姥鲛烷(Pr) δD 值正偏达 90‰, 与正构烷烃之间的差异迅速减小[16]。因此, 有学者在运用沉积岩中烷烃δD值解释古降水之前, 先行用藿烷和甾烷类的成熟度指标来评估烷烃的δD值是否有受到改造的可能[4]。但也有研究发现, 在由甾烷和藿烷类成熟度指标指示的未成熟到成熟阶段早期, 成熟度的变化对原始烷烃δD值似乎并无明显影响[17]。能否由甾烷和藿烷类成熟度指标简单判定烷烃 δD是否受到了热成熟作用的影响目前尚缺乏足够研究实例。本文拟分析青藏高原中部伦坡拉盆地的10个样品, 测定正构烷烃和Ph的氢同位素、甾烷和藿烷类成熟度指标等, 讨论这些成熟度指标与烷烃δD值之间的关系, 对该盆地沉积岩中烷烃氢同位素是否受成岩作用影响进行初步判别。
1 样品采集与分析
本次研究共分析样品10个, 均来自青藏高原中部的新生代沉积盆地——伦坡拉盆地中的丁青组地表露头, 样品的视深度为 43~345 m, 时代为渐新世末期到中新世早期。剖面岩性主要为泥岩夹细粉砂岩层。采样位置和年代参见文献He et al.[18].
岩石样品在实验室刮去表层风化部分, 用稀盐酸和有机试剂(正己烷)分别清洗表层 3遍, 粉碎至100目以下, 50 ℃下烘8 h。从粉碎好的样品中取出15~25 g, 加入Teflon离心管中, 依次用二氯甲烷、二氯甲烷和甲醇混合溶液(体积比为 1∶1)、甲醇溶剂超声波提取可溶有机质, 每种溶剂分别重复提取1次。提取物进一步用活化硅胶柱进行组分分离, 用正己烷与二氯甲烷混合溶液(体积比为 95∶5)洗脱出其中的烷烃组分。然后, 烷烃组分进行尿素络合处理, 分离出正构烷烃与非正构烷烃部分组分。
正构烷烃的相对含量和藿烷、甾烷等类异戊二烯烷烃的相对含量分别通过 HP 6890N气相色谱和GC-MS(TRACE2000/SSQ-7000质谱仪)进行测定,两者的色谱条件一样, 色谱柱为 HP石英毛细管柱(30 m×0.32 mm×0.25 μm), 载气为氦气, 升温程序为:始温80 , ℃恒温2 min, 以10 /min℃的速率升温至140 ,℃ 而后以4 /min℃的速率升温至290 , ℃终温恒温15 min, 进样量为1~2 μL。质谱采集的方法为单离子(m/z 71、m/z 191和m/z 217)扫描和全扫描同时进行。
正构烷烃氢同位素测定则采用DeltaPlusXL型色谱同位素比值质谱仪和 DB-5MS毛细管色谱柱(30 m ×0.32 mm×0.25 μm)。升温程序为: 始温80 , ℃恒温2 min, 以10 /min℃的速率升温至140, ℃而后以4 /min℃的速率升温至290 , ℃恒温15 min。流出物通过热转化管加热到1440 , ℃将正构烷烃中的H转化为 H2, 然后进入质谱仪进行同位素比值的测定。每天测定一次仪器的H3因子, 以确保整个分析过程中仪器的稳定性。在单体氢同位素测定过程中,用Indiana大学的混合物标样(包括nC12~nC35之间的11个正构烷烃化合物)来检验仪器状态以及分析准确性。所有的氢同位素值都是2次以上测定结果的平均值, 相对偏差在 10‰以内。其中, 类异戊二烯结构的Ph由于含量较高, 在正构烷烃组分中有部分保留, 从而也获得了该化合物的同位素值。通过标样的测试结果发现, 当化合物峰面积小于 10 vs时,δD数据变异增大, 有显著变重的趋势, 可能与仪器热裂解反应器的“视空白(apparent blank)”[4]有关。在我们的测试中数据中, Ph的峰面积大于10 Vs。
2 结果与讨论
2.1 甾烷、藿烷类成熟度指标
样品中正构烷烃碳数主要分布于C15~C34之间, >C25的部分有明显的奇偶优势, CPI值变化范围为2.6~4.0, 平均为3.3; OEP值变化范围为2.1~4.5, 平均为3.2(见表1)。Pr/Ph比值较低, 指示了相对还原的沉积环境。藿烷以C27~C32为主, 甾烷则呈现出比较一致的C29> C27> C28的分布样式。本工作中主要分析了较常用的甾烷、藿烷类成熟度指标, 包括C29甾烷的 20S/(20S+20R)比值、C27藿烷的 Ts/(Ts+Tm)比值和C31藿烷22S/(22S+22R)比值。其中, C29甾烷20S/(20S+20R)比值在 0.09~0.49之间, C27藿烷 Ts/(Ts+Tm)比值在 0.28~0.55之间, C31藿烷 22S/ (22S+22R)比值在0.41~0.57之间。

表1 岩石样品视深度、烷烃氢同位素值和成熟度参数Table 1 Apparent depth, alkane δD values and maturity parameters of samples
通常来说, 藿烷和甾烷类成熟度指标的数值随着成熟度升高会出现逐渐上升的趋势, 其中 C29甾烷20S/(20S+20R)的变化范围为0~0.5, 小于0.25为未成熟, 0.25以上则为低成熟阶段: C31藿烷22S/(22S+22R)的变化范围为0~0.6, 当比值大于0.5时, 说明有机质已经开始进入低成熟阶段: C27藿烷 Ts/(Ts+Tm)比值则会逐渐升高[19]。综合上述指标, 其中有四个样品接近或进入低成熟阶段(样品PL589, 661, 805, 829), 而其他样品基本处于未成熟阶段。当然, 上述指标之间的相关性并不太好, 因此, 也不能排除物质来源或沉积环境方面存在的差异对成熟度指示意义的干扰。
2.2 烷烃氢同位素值
10个样品正构烷烃的 δD 值在–110‰~ –220‰之间, 并且随着碳数的增加, δD 值表现出逐渐变轻的趋势(见图1), 这可能与不同链长的正构烷烃的来源不同有关。这种碳链长度和δD值之间的负相关关系在很多之前的研究中都有发现[20–22]。在长链的正构烷烃中, 出现了一种与相对含量类似的“奇偶优势”, 即奇碳数的烷烃 δD值相对于与其相邻的偶碳数烷烃明显偏负, 数值在 0‰~30‰之间。上述特征暗示烷烃的δD值未明显遭受到成岩作用的影响。
样品中Ph的δD值显较正构烷烃明显偏负, 在–267‰~ –324‰之间, 随视深度变化不明显, 与对应的 nC18正构烷烃的 δD 值相差–140‰~ –198‰(见图2)。由于Ph与正构烷烃在生物中的合成路径的不同是两者δD值之间存在较大差别的主要原因, 所以也暗示烷烃δD值未明显遭受到成岩作用的影响。
岩石或沉积物中的有机质的氢同位素值受到两种因素的影响, 其一是通常所说的原始信息, 即有机物被生物合成时所携带的源水信息; 另一种则是有机质在进入沉积成岩阶段后, 受到的生物降解和热降解作用,δD值往往会偏离原始信息。一旦遭受后期改造, δD值在古环境研究中将失去作用, 因此在将烷烃δD应用于古环境重建研究时必须考察其δD值是否遭受了改造。
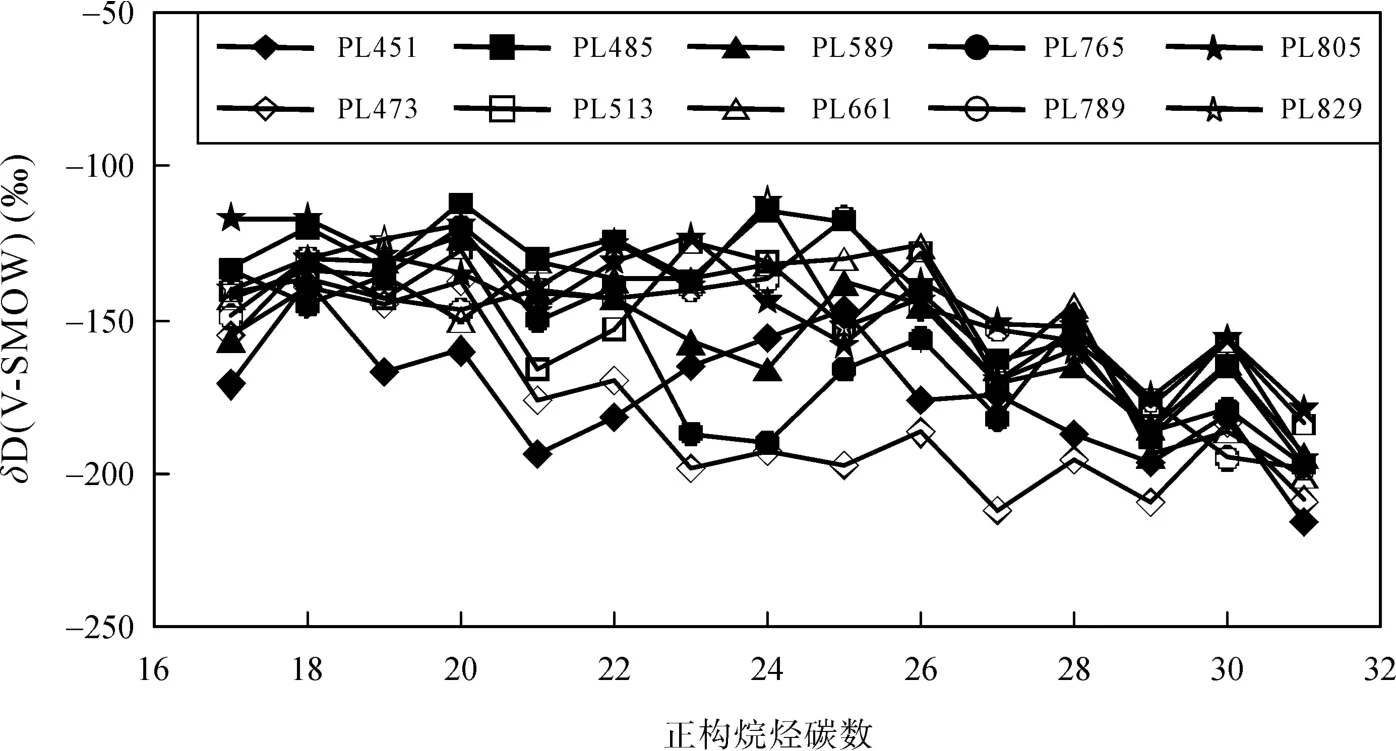
图1 正构烷烃氢同位素值分布情况Fig.1 Hydrogen isotope distribution of individual n-alkanes

图2 烷烃氢同位素值随视深度的变化Fig.2 δD values of nC18 alkane and phytane vary with the apparent depth of samples
生物降解对有机质的 δD 值影响非常小, 一般情况下可以忽略。有机质δD值变化主要发生在成岩过程和后生作用中。Sessions et al.[13]对现代植物所合成的各类化合物的δD值进行研究发现, 直链脂肪族的化合物与来源水的分馏在–150‰~ –210‰之间,非直链的类异戊二烯脂类化合物与来源水的分馏更大, 在–200‰~ –300‰之间, 而植醇的分馏最大, 可达–380‰。同样, Chikaraishi et al.[14]也发现植醇的δD值可达–345‰。Dowson et al.[23]对澳大利亚下三叠系地层中不同成熟度的有机质进行分析发现, 成熟度较低时, 正构烷烃与Ph、Pr之间存在较大的差值(–116‰)。随着成熟度的增加, 有机质中正构烷烃和 Ph、Pr等氢同位素值都呈现出逐渐上升的趋势,且Ph、Pr的偏正速度更快, 其与正构烷烃之间的差值逐渐缩小, 最终与正构烷烃齐平甚至更为偏正。Pedentchouk et al.[16]对非洲1个白垩纪的沉积柱的研究进一步证实了这一现象, 并且发现在成熟度较低的样品中, 不同链长正构烷烃的δD值的分布与现代沉积物中的相似, 特征是随着碳链长度的增加δD值逐渐偏轻。而随着采样深度的增加, 成熟度也随之增加, 正构烷烃的δD值随着碳链长度的增加而表现出逐渐偏正的趋势。出现这种现象的通常解释为:在降解过程中δD值更加偏负的甲烷气体的产生、大分子有机质的热裂解作用和有机质与 δD值偏正的孔隙水的氢交换作用等。
从我们的结果来看, Ph的δD值平均在–295‰左右, 与现代植物中的值比较接近, 而且其和对应的nC18正构烷烃之间的差值非常大, 平均在–170‰左右, 最大可达到–198‰, 两者之间如此明显的差值与现代沉积物或者 Pedentchouk et al.[16]人研究发现的未成熟有机质的特征相似, 表明样品中正构烷烃的δD值还未遭受明显改变。同时, 正构烷烃的另一个特征——δD值随着碳链长度的增加而表现出逐渐偏负的趋势, 与未经受δD值改变的烷烃特征相似。这与随成熟度升高烷烃δD值发生明显改变的情况有所不同,后者表现出的是δD值随链长逐渐升高的趋势。
2.3 成熟度指标与同位素结果间的关系
图3给出了nC18正构烷烃和Ph的δD值及其之间的差值(ΔδD(C18-Ph))与一些成熟度指标间的关系。从图上看, nC18正构烷烃δD值与各成熟度指标之间存在较弱的相关关系, R2在0.34~0.36之间, 与C29甾烷20S/(20S+20R)比值之间的R2略高; 与nC18正构烷烃相比, Ph的δD与各指标之间的关系更差,R2均在0.28左右; 而成熟度指标与ΔδD(C18-Ph)之间无相关关系, R2仅为0.1。因此尽管甾烷和藿烷成熟度指标显示样品的成熟度有了从未成熟到低成熟的变化, 烷烃的δD值却并未显示相应的改变。这一结果与 Pedentchouk et al.[16]的研究不太一致, 他们的结果表明, 在 C29甾烷 20S/(20S+20R)接近 0.4的低成熟阶段之前, Ph和Pr的δD值正偏达90‰, 与正构烷烃之间的差异迅速减小。我们的结果也与Radke et al.[24]所得出来的结果不一样。他们对波兰和德国的两个地区的上二叠统至下侏罗统海相地层进行研究发现, 正构烷烃和Ph、Pr的δD值随着成熟度的增加呈现出逐渐变重的趋势, 并且短链正构烷烃δD值与甲基菲指数(MPI1)、氢指数指标(HI)、有机质最大热解峰温度(tmax)等成熟度指标之间有良好的相关性, R2大多在 0.67~0.98之间; Ph、Pr的δD值与成熟度指标间也存在相似的关系。当然, 在Radke et al.的工作中没有使用甾烷和藿烷类成熟度指标, 我们的结果尚不能与他们的结果进行简单的对比。
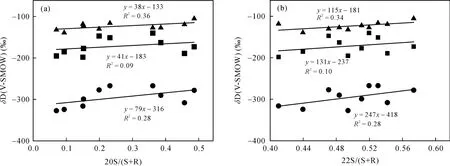
图3 烷烃氢同位素值与成熟度指标之间的相关关系Fig.3 The relationships between alkane δD values and maturity parameters
成熟度指示的是沉积有机质向油气转化和发展的趋势, 本文所采用的成熟度指标是常用的藿烷和甾烷指标, 它们是通过特定化合物的分子结构变化或者相对含量的变化来进行成熟度的判定。δD值的变化则是属于元素同位素层面的地球化学变化, 与分子结构变化处在不同层面, 后者的变化是否会引起前者的变化仍存在争议[25]。Schimmelmann et al.[26]同样也指出成熟度指标只能作为参考, 最直接的证据应该还是正构烷烃与异构的Ph等δD值之间的差值, 若两者之间具有足够大的差值(>70‰)则表明正构烷烃δD值未发生或仅发生了轻微改变, 如果两者间的差值过小, 或者异构烷烃的值更高, 则说明正构烷烃的原始 δD值已经被改变, 无法有效地用于古气候等的研究。我们的结果表明, 至少用甾烷和藿烷类指标来判断烷烃氢同位素是否受到成岩作用的影响存在一定的不确定性。当然, 成熟度指标还有很多, 本文的工作还有待进一步完善, 比如, 对更多成熟度指标进行综合分析,考察成熟度变化范围更大的一些样品等。
3 结 论
本文研究测定了青藏高原中部伦坡拉盆地丁青组沉积岩样品中正构烷烃和 Ph氢同位素组成和甾烷、藿烷类的成熟度指标。C29甾烷 20S/(20S+20R)比值、C27藿烷Ts/(Ts+Tm)比值和C31藿烷22S/ (22S+22R)比值显示成熟度变化于未成熟到低成熟阶段。其中的低成熟样品有可能出现烷烃δD发生成岩改变的情况。但烷烃 δD数据显示, 正构烷烃 δD值随着链长的增加而表现出逐渐降低的趋势, 且 nC18正构烷烃与 Ph的 δD 值之间的平均差值(ΔδD(C18-Ph))达–170‰, 与现代生物中的同位素组成相似, 表明正构烷烃δD值未发生明显改变。上述成熟度指标与烷烃δD值和ΔδD(C18-Ph)之间相关性也较差, 表明本文中的甾烷和藿烷类成熟度指标并不能很好地用来指示正构烷烃δD值的成岩改造情况。因此, 在考察岩石有机质成熟度对烷烃氢同位素的影响时, 可能还需考虑诸如Ro等其他成熟度指标来进行综合的比较分析。
感谢中国科学院地质与地球物理研究所的孙继敏研究员为本研究提供样品; 同时也感谢两位审稿人为本文章所提供的宝贵意见。
:
[1] Sachse D, Billault I, Bowen G Y, Chikaraishi Y, Dawson T E,Feakins S J, Freeman K H, Magill C R, McInerney F A, van der Meer M T J, Polissar P, Robins R J, Sachs J P, Schmidt H L, Sessions A L, White J W C, West J B, Kahmen A. Molecular paleohydrology: Interpreting the hydrogen isotopic composition of lipid biomarkers from photosynthesizing orga-nisms [J]. Ann Rev Earth Planet Sci, 2012, 40: 221–249.
[2] Luo Pan, Peng Ping’an, Gleixner G, Zheng Zhuo, Pang Zhonghe, Ding Zhongli. Empirical relationship between leaf wax n-alkane delta D and altitude in the Wuyi, Shennongjia and Tianshan Mountains, China: Implications for paleoaltimetry [J]. Earth Planet Sci Lett, 2011, 301(1/2): 285–296.
[3] Jia Guodong, Wei Kai, Chen Fajin, Peng Ping’an. Soil n- alkane delta D vs. altitude gradients along Mount Gongga, China [J].Geochim Cosmochim Acta, 2008, 72(21): 5165–5174.
[4] Polissar P J, Freeman K H, Rowley D B, McInerney F A, Currie B S. Paleoaltimetry of the Tibetan Plateau from D/H ratios of lipid biomarkers [J]. Earth Planet Sci Lett, 2009, 287(1/2): 64–76.
[5] Collins J A, Schefuss E, Mulitza S, Prange M, Werner M,Tharammal T, Paul A, Wefer G. Estimating the hydrogen isotopic composition of past precipitation using leaf-waxes from western Africa [J]. Quatern Sci Rev, 2013, 65: 88–101.
[6] Tierney J E, Russell J M, Damste J S S, Huang Y S,Verschuren D. Late Quaternary behavior of the East African monsoon and the importance of the Congo Air Boundary [J].Quatern Sci Rev, 2011, 30(7/8): 798–807.
[7] Sachs J P, Sachse D, Smittenberg R H, Zhang Z H, Battisti D S, Golubic S. Southward movement of the Pacific intertropical convergence zone AD 1400–1850 [J]. Nat Geosci, 2009,2(7): 519–525.
[8] 张明峰, 妥进才, 吴陈君, 张小军, 郭力军. 柴达木盆地北缘原油中单体正构烷烃的碳、氢同位素组成研究[J]. 沉积学报, 2012, 30(5): 983–990.Zhang Ming-feng, Tuo Jin-cai, Wu Chen-jun, Zhang Xiao-jun,Guo Li-jun. Carbon and hydrogen isotopic composition of individual n-alkanes for crude oil from north margin of Qaidam Basin [J]. Acta Sedimentol Sin. 2012, 30(5): 983–990(in Chinese with English abstract).
[9] Aboglila S, Grice K, Trinajstic K, Dawson D, Williford K H.Use of biomarker distributions and compound specific isotopes of carbon and hydrogen to delineate hydrocarbon characteristics in the East Sirte Basin (Libya) [J]. Org Geochem, 2010, 41(12): 1249–1258.
[10] 卢鸿, 李超, 肖中尧, 孙永革, 彭平安. 轮南油田代表性原油正构烷烃单体氢同位素组成、分布与母源信息[J]. 中国科学(D辑), 2004, 34(12): 1145–1150.Lu Hong, Li Chao, Xiao Zhongyao, Sun Yongge, Peng Ping’an.Hydrogen isotopic compositions, distributions and source signals of individual n-alkanes for some typical crude oils in Lunnan Oilfield,Tarim Basin, NW China [J]. Sci Chin (D), 2005, 48(8): 1220–1226.
[11] 刘金萍, 耿安松, 熊永强, 李永新, 朱桂娟, 张应心, 李宇生. 正构烷烃单体碳、氢同位素在油源对比中的应用[J]. 新疆石油地质, 2007, 28(1): 104–107.Liu Jin-ping, Geng An-song, Xiong Yong-qiang, Li Yong-xin,Zhu Gui-juan, Zhang Ying-xin, Li Yu-sheng. Application of free C and H isotopes in normal alkane to C orrelation of oil sources in Huanghua D epression [J]. Xinjiang Pet Geol, 2007,28(1): 104–107 (in Chinese with English abstract).
[12] Schimmelmann A, Lewan M D, Wintsch R P. D/H isotope ratios of kerogen, bitumen, oil, and water in hydrous pyrolysis of source rocks containing kerogen types I, II, IIS, and III [J].Geochim Cosmochim Acta, 1999, 63(22): 3751–3766.
[13] Sessions A L, Burgoyne T W, Schimmelmann A, Hayses J M.Fractionation of hydrogen isotopes in lipid biosynthesis [J].Org Geochem, 1999, 30(9): 1193–1200.
[14] Chikaraishi Y, Tanaka R, Tanaka A, Ohkouchi N. Fractionation of hydrogen isotopes during phytol biosynthesis [J].Org Geochem, 2009, 40(5): 569–573.
[15] Andersen N, Paul H A, Bernasconi S M, McKenzie J A,Behrens A, Schaeffer P, Albrecht P. Large and rapid climate variability during the Messinian salinity crisis: Evidence from deuterium concentrations of individual biomarkers [J].Geology, 2001, 29(9): 799–802.
[16] Pedentchouk N, Freeman K H, Harris N B. Different response of delta D values of n-alkanes, isoprenoids, and kerogen during thermal maturation [J]. Geochim Cosmochim Acta, 2006,70(8): 2063–2072.
[17] 王彦美, 熊永强, 王立武, 苗洪波. 松辽盆地南部上白垩统烃源岩和原油中正构烷烃的氢同位素组成研究[J]. 地球化学, 2006, 35(6): 602–608.Wang Yan-mei, Xiong Yong-qiang, Wang Li-wu, Miao Hong-bo. Hydrogen isotopic compositions of n-alkanes in crude oils and extracts of Upper Cretaceous from southern Songliao Basin [J]. Geochimica, 2006, 35(6): 602–608 (in Chinese with English abstract).
[18] He Huaiyu, Sun Jimin, Li Qiuli, Zhu Rixiang. New age determination of the Cenozoic Lunpola basin, central Tibet [J].Geol Mag, 2012, 149(1): 141–145.
[19] 彼得斯 K, 莫尔多万 J. 生物标记化合物指南[M]. 北京:石油工业出版社, 1995: 79–187.Peters K, Moldowan J. The Biomarker Guide: Interpreting Molecular Fossils in Petroleum and Ancient Sediments [M].Beijing: Petroleum Industry Press, 1995: 79–187 (in Chinese).
[20] Bi Xinhui, Sheng Guoying, Liu Xiaohong, Li Chao, Fu Jiamo.Molecular and carbon and hydrogen isotopic composition of n-alkanes in plant leaf waxes [J]. Org Geochem, 2005, 36(10):1405–1417.
[21] Tuo Jincai, Zhang Mingfeng, Wang Xianbin, Zhang Chuanlun.Hydrogen isotope ratios of aliphatic and diterpenoid hydrocarbons in coals and carbonaceous mudstones from the Liaohe Basin, China [J]. Org Geochem, 2006, 37(2): 165–176.
[22] Li Chao, Sessions A L, Kinnaman F S, Valentine D L. Hydrogenisotopic variability in lipids from Santa Barbara Basin sediments [J].Geochim Cosmochim Acta, 2009, 73(16): 4803–4823.
[23] Dawson D, Grice K, Alexander R. Effect of maturation on the indigenous delta D signatures of individual hydrocarbons in sediments and crude oils from the Perth Basin (Western Australia) [J]. Org Geochem, 2005, 36(1): 95–104.
[24] Radke J, Bechtel A, Gaupp R, Puttmann W, Schwark L,Sachse D, Gleixner G. Correlation between hydrogen isotope ratios of lipid biomarkers and sediment maturity [J]. Geochim Cosmochim Acta, 2005, 69(23): 5517–5530.
[25] Sessions A L, Sylva S P, Summons R E, Hayses J M. Isotopic exchange of carbon-bound hydrogen over geologic timescales [J].Geochim Cosmochim Acta, 2004, 68(7): 1545–1559.
[26] Schimmelmann A, Sessions A L, Mastalerz M. Hydrogen isotopic(D/H) composition of organic matter during diagenesis and thermal maturation [J]. Earth Planet Sci Lett, 2006, 34: 501–533.
