直接皂化法制备叶绿素铁钠盐
2014-06-27种亚莉曹江绒
李 祥, 种亚莉, 曹江绒
(1.陕西科技大学 化学与化工学院, 陕西 西安 710021; 2.北京弘祥隆生物科技股份有限公司, 北京 100085)
0 引言
叶绿素属于卟啉类化合物[1],是重要的天然色素,广泛存在于植物和某些动物体内,常作为着色剂或添加剂应用于医药、食品、日用化工等领域[2-4].大多数叶绿素从绿色植物中提取,但成本较高.我国养蚕历史悠久,是世界蚕业的发源地和主产国[5,6],研究表明,蚕沙中叶绿素的质量分数约为0.8%~1.0%,高于绿色植物中的含量[7].但由于叶绿素的稳定性差,故将叶绿素合成其衍生物,如叶绿素铁钠盐[8]、叶绿素锌钠盐[9]、叶绿素铜钠盐[10,11]等.目前,利用蚕沙制备叶绿素铁钠盐的研究较少,故研究蚕沙叶绿素铁钠盐的制备工艺有一定的经济效益.
叶绿素铁钠盐是一种带胺味的墨绿色结晶性粉末,在食品方面,用作食品添加剂、染色剂、脱臭剂;在医疗方面,由于叶绿素铁钠盐的结构和人体血红蛋白的结构非常相似,故在人体中的生物利用率很高,可作为缺铁性贫血治疗的辅助药品[8].近年来,发现叶绿素铁钠具有抗菌、抗病毒、抗过敏和促进组织再生等作用,是一种良好的造血细胞复合剂,对各种原因引起的白细胞减少症及各种贫血有治疗作用[12].
传统叶绿素铁钠盐的制备是先用有机溶剂提取叶绿素然后浓缩再皂化[13-15],工艺路线较长,成本高,为了克服这一缺点.本研究将叶绿素的提取与皂化合并,探讨了直接皂化法制备叶绿素铁钠盐的最优工艺条件,并且与传统的工艺进行比较说明了直接皂化法是可行的.
1 材料与方法
1.1 原料与试剂
蚕沙,购于陕西安康旬阳;95%乙醇,氢氧化钠,石油醚,硫酸,硫酸亚铁,无水乙醇均为分析纯,购于西安化学试剂有限公司.
1.2 主要仪器
FZ102型植物试样粉碎机,北京市永光明医疗仪器厂;KQ5200DE型数控超声波清洗器,昆山市超声仪器有限公司;HH-2数显恒温水浴锅,国华电器有限公司;7230G型可见分光光度计,上海精密科学仪器有限公司;DZF-6050型真空干燥箱,上海一恒科学仪器有限公司;R201L型旋转蒸发仪,上海申生科技有限公司;TDL-40B型台式离心机,上海安亭科学仪器厂;SHB-B 95型循环式多用真空泵,陕西太康生物科技有限公司.
1.3 试验方法
1.3.1 叶绿素的测定
准确移取0.5 mL萃取除杂后的皂化液,用95%乙醇定容至10 mL,分别测定649 nm和665 nm处的吸光度A.按如下公式计算叶绿素提取率[16].
叶绿素a的质量浓度
ρa=13.95A665-6.88A649.
叶绿素b的质量浓度
ρb=24.96A649-7.32A665.
叶绿素总的质量浓度
ρ总=ρa+ρb.
叶绿素提取率=ρ总×提取液体积×稀释倍数/样品质量
1.3.2 直接皂化条件的确定
(1)体系pH的确定
称取6份10 g干蚕沙粉分别于250 mL烧杯中,加入15 mL蒸馏水软化20 min,软化完后加入100 mL95%乙醇,分别用10%NaOH调节体系pH为8、9、10、11、12、13,之后将其同时放置在KQ5200DE型数控超声波清洗器中并设置超声时间为120 min,超声温度为70 ℃,待其超声结束,测定溶液中叶绿素的含量.
(2)超声时间的确定
称取6份10 g干蚕沙粉分别于250 mL烧杯中,加入15 mL蒸馏水软化20 min,软化完后加入100 mL95%乙醇,用10%NaOH调节体系pH为12,之后将其分别放置在超声时间为60、80、100、120、150、180 min,超声温度为70 ℃的KQ5200DE型数控超声波清洗器中,待其超声结束,测定溶液中叶绿素的含量.
(3)超声温度的确定
称取6份10 g干蚕沙粉分别于250 mL烧杯中,加入15 mL蒸馏水软化20 min,软化完后加入100 mL95%乙醇,用10%NaOH调解体系pH为12,之后将其分别放置在超声时间为120 min,超声温度为30 ℃、40 ℃、50 ℃、60 ℃、70 ℃、80 ℃的KQ5200DE型数控超声波清洗器中,待其超声结束,测定溶液中叶绿素的含量.
1.3.3 酸化置铁条件的确定
(1)置铁量的确定
取6份100 mL皂化液分别于250 mL的三口烧瓶中,连接搅拌装置,开启电动搅拌器,用6 mol/L H2SO4调节体系pH至2~3,酸化30 min后至皂化液完全成褐色,在此酸性条件下分别加入2、3、4、5、6、7 mL的10% FeSO4,调节水浴温度为65 ℃,反应120 min,待反应完全,静置、冷却后加等量蒸馏水,过滤得叶绿素铁酸,将所得叶绿素铁酸溶解在丙酮中,加10% NaOH-乙醇溶液调节pH在11~12,此时出现墨绿色的晶体,静置片刻用离心机常温离心,60 ℃烘干得墨绿色叶绿素铁钠盐.
(2)置铁时间的确定
取6份100 mL皂化液分别于250 mL的三口烧瓶中,连接搅拌装置,开启电动搅拌器,用6 mol/L H2SO4调节体系pH至2~3,酸化30 min后至皂化液完全成褐色,在此酸性条件下加入6 mL的10%FeSO4,调节水浴温度为65 ℃,反应时间分别为30 min、60 min、90 min、120 min、150 min、180 min,待反应完全,静置、冷却后加等量蒸馏水,过滤得叶绿素铁酸,将所得叶绿素铁酸溶解在丙酮中,加10%NaOH-乙醇溶液调节pH在11~12,此时出现墨绿色的晶体,静置片刻用离心机常温离心,60 ℃烘干得墨绿色叶绿素铁钠盐.
(3)置铁温度的确定
取6份100 mL皂化液分别于250 mL的三口烧瓶中,连接搅拌装置,开启电动搅拌器,用6 mol/L H2SO4调节体系pH至2~3,酸化30 min后至皂化液完全成褐色,在此时的酸性条件下加入6 mL的10% FeSO4,调节水浴温度分别为50 ℃、55 ℃、60 ℃、65 ℃、70 ℃、75 ℃,反应时间为120 min,待反应完全,静置、冷却后加等量蒸馏水,过滤得叶绿素铁酸,将所得叶绿素铁酸溶解在丙酮中,加10%NaOH-乙醇溶液调节pH在11~12,此时出现墨绿色的晶体,静置片刻用离心机常温离心,60 ℃烘干得墨绿色叶绿素铁钠盐.
1.3.4 正交试验设计方法
在单因素实验的基础上,采用正交法在四因素三水平上主要考察体系pH、超声温度、置铁时间、置铁量对叶绿素铁钠盐制备的影响,探索蚕沙叶绿素铁钠盐制备的最优工艺,试验安排如表1所示.

表1 因素水平
1.4 对照试验
传统制备法见参考文献[15].
直接皂化法:称取干蚕沙粉10 g,于250 mL烧杯中加入15 mL蒸馏水软化20 min,软化完后加入95%乙醇100 mL,并用10% NaOH调节使体系pH≈12,放置在KQ5200DE型数控超声波清洗器中,将其设置为超声时间120 min,超声温度70 ℃.待其超声结束后,用等量石油醚萃取三次,收集下层萃取液待用.将萃取液转入250 mL三口烧瓶中用6 mol/L H2SO4调节体系使pH≈2~3,65 ℃下酸化30 min,加入6 mL10% FeSO4溶液,置铁时间150 min,最后用10% NaOH-CH3CH2OH调节溶液使叶绿素铁酸成盐析出.
2 结果与讨论
2.1 单因素实验结果与讨论
2.1.1 直接皂化条件的确定
按1.3.2中的(1)进行试验,试验结果如图1所示.

图1 体系pH对皂化反应的影响
由图1可知,体系pH在8~12,皂化液中叶绿素含量迅速降低;体系pH在12~13,皂化液中叶绿素含量基本不变.原因可能是:此时被萃取出来的叶绿素参与皂化反应且皂化反应已经基本达到了平衡.因此,试验结果表明:体系维持在pH≈12为宜.
按1.3.2中的(2)进行试验,试验结果如图2所示.

图2 超声时间对皂化反应的影响
由图2可知,随着超声时间的延长皂化液中叶绿素含量逐渐降低,大部分叶绿素已被皂化.反应时间在60~120 min之间时,叶绿素含量降低较快,120~180 min之间时,叶绿素含量降低趋于平缓.原因可能是:①皂化反应本身就是一个可逆反应,在某一时间会达到平衡状态,在该试验中超声时间达到120 min时皂化反应即达到平衡状态,此时继续延长超声时间,对叶绿素铁钠盐的产率影响并不明显.②叶绿素不稳定,随着超声时间的延长叶绿素在碱性和温度比较高的条件下会分解.所以120~180 min之间叶绿素的缓慢降低是由于叶绿素被氧化分解变性了,因此,超声时间以120 min为宜.
按1.3.2中的(3)进行试验,试验结果如图3所示.

图3 超声温度对皂化反应的影响
由图3可知,随着超声温度的增加皂化液中的叶绿素含量逐渐降低,当超声温度超过70 ℃时,皂化液中的叶绿素降低趋于平缓,原因可能是:温度升高,动态反应平衡向右移动,而70 ℃时反应达到动态平衡,此时继续增加超声温度皂化液中叶绿素含量基本不变而且还会使叶绿素降解.因此,超声温度以70 ℃为宜.
2.1.2 酸化置铁条件的确定
按1.3.3中的(1)进行试验,试验结果如图4所示.

图4 置铁量对置铁反应的影响
由图4可知,随着10% FeSO4量的增加,叶绿素铁钠盐的含量也在增加,当10% FeSO4增加到6 mL时叶绿素铁钠盐的产量达到最大且继续增加10% FeSO4叶绿素铁钠盐的产量基本不变,这是由于能够和铁离子络合的脱镁叶绿素是有限的,当达到一定程度就不再络合,此时继续加入铁盐,铁离子只能以游离态存在于溶液中,不仅增加成本而且还对后期污水的处理增加工作量,所以加入铁盐以6 mL为最佳.
按1.3.3中的(2)进行试验,试验结果如图5所示.

图5 置铁时间对置铁反应的影响
由图5可知,随着反应时间的延长叶绿素铁钠盐的产量逐渐增加,但当超过120 min后,叶绿素铁钠盐的产量反而降低.这是由于在酸化置铁反应过程中溶液中的溶剂在慢慢蒸发,随着反应的延长蒸发的溶剂也就越多,生成的叶绿素铁酸的浓度也就变的越大,会将原本在120 min处的反应平衡打破,使酸化置铁反应逆向进行,从而导致生成的叶绿素铁酸含量降低,因此,置铁时间以120 min为宜.
按1.3.3中的(3)进行试验,试验结果如图6所示.

图6 置铁温度对置铁反应的影响
由图6可知,随着反应温度的升高,叶绿素铁钠盐的产量逐渐增加,但当超过65 ℃时,叶绿素铁钠盐的产量反而降低.原因可能是:①随着温度的升高溶剂的挥发,会使生成的叶绿素铁酸的浓度也增大,该置铁反应是一个可逆反应,产物浓度增大会使反应逆向进行,从而使已经生成的叶绿素铁酸又被分解;②叶绿素铁酸的溶解度随着温度的升高而增大,温度过高不能使叶绿素铁酸完全析出来,而是溶解在溶液里.所以,综合考虑选取65 ℃为酸化置铁最优温度.
2.2 正交试验结果与讨论
在单因素实验基础上,综合考虑主要因素对叶绿素铁钠盐产率的影响,进行L9(34)正交试验,结果如表2所示.
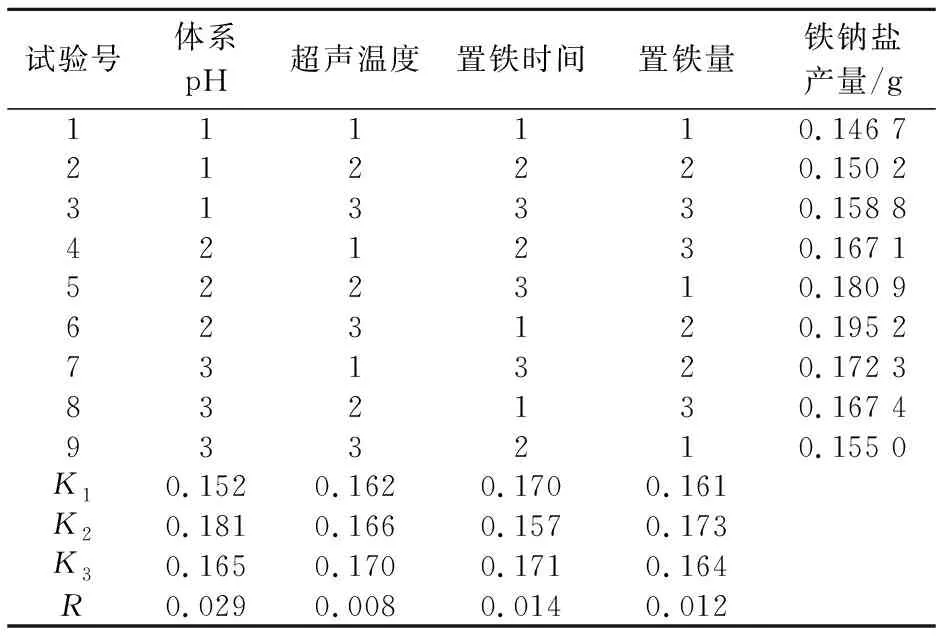
表2 正交试验方案与结果
由表2的极差分析可知,影响叶绿素铁钠盐制备诸因素的主次关系为体系pH﹥置铁时间﹥置铁量﹥超声温度.制备叶绿素铁钠盐的最优条件为加碱使皂化体系pH≈12,置铁时间为150 min,置铁量为6 mL,超声温度为80 ℃.
2.3 对照试验结果
按照1.4进行试验,试验结果如表3所示.

表3 对照试验结果
由表3可知,直接皂化法叶绿素铁钠盐的得率大于传统制备法叶绿素铁钠盐的得率,而且直接皂化法比传统制备法在制备工艺上还少一道工序,因此直接皂化法是可行的.
3 产品分析
3.1 产品性状
本法制备的叶绿素铁钠盐为墨绿色具有金属光泽的粉末,易溶于水,水溶液透明无沉淀,微溶于乙醇,氯仿,不溶于乙醚.
3.2 光谱分析
配制0.01%的叶绿素铁钠盐溶液,用7230G紫外-可见分光光度计扫描其吸收光谱,在405 nm和655 nm处有最大吸收波长,与传统制法得到的叶绿素铁钠盐的波长一致[13].结果如图7所示.
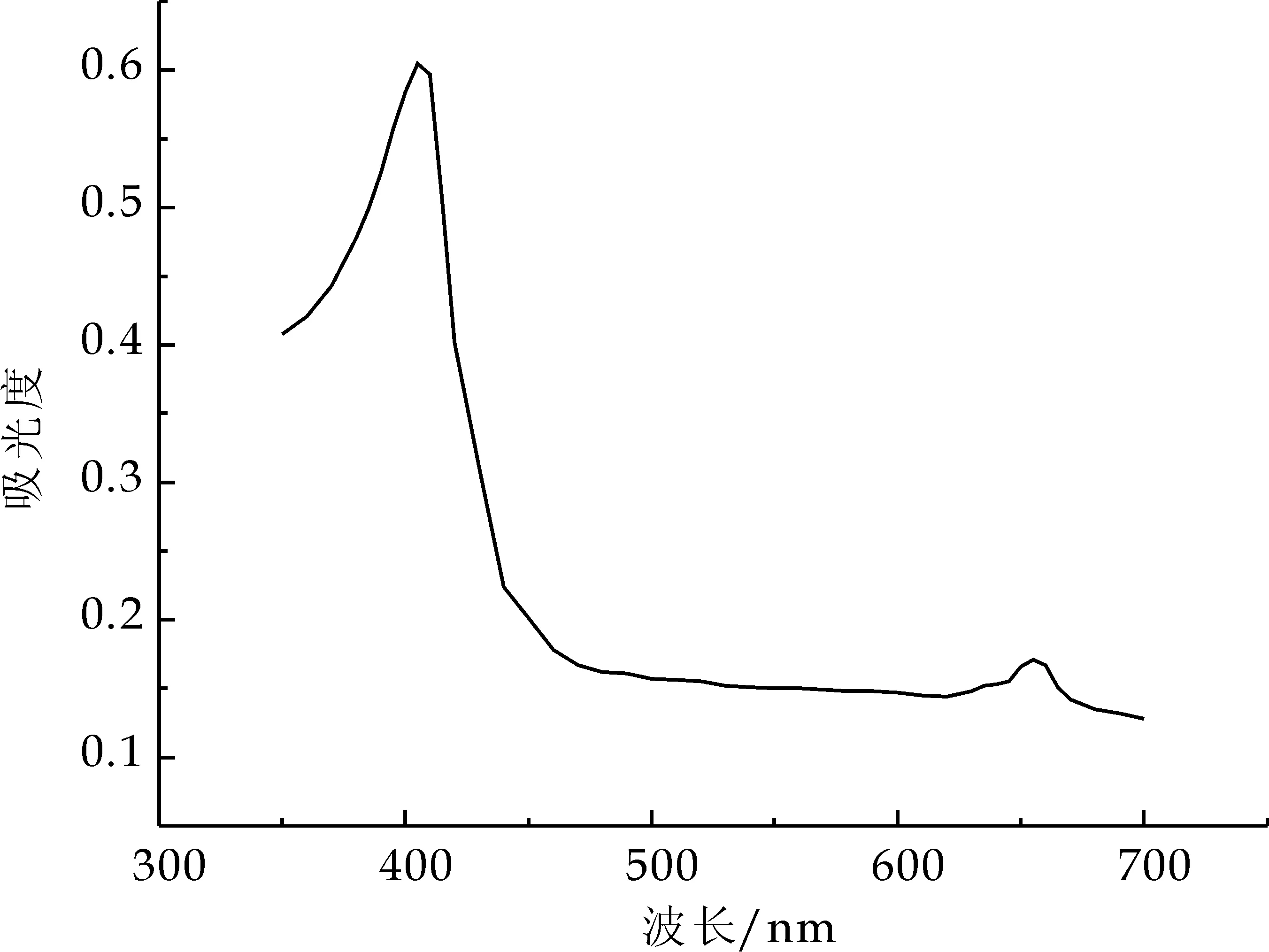
图7 叶绿素铁钠盐紫外吸收光谱图
4 结论
本文探讨了体系pH、超声时间、超声温度、置铁量、置铁时间、置铁温度对叶绿素铁钠盐产率的影响,得到直接皂化法制备叶绿素铁钠盐的最优条件.直接皂化法将叶绿素的提取与皂化合并,在提取叶绿素的溶液体系中直接加入碱,给定一定的温度、一定的时间,使萃取出来的叶绿素直接皂化,比传统的先提取叶绿素再皂化制备叶绿素铁钠盐少了一道工序,为其工业化生产节约了成本,使得叶绿素铁钠盐的制备从理论向实际又迈进了一步.
[1] 罗庆锋.叶绿素的研究进展及叶绿素铜钠盐的开发利用[J].林产化工通讯,1995(1):32-33.
[2] 王顺民,牛 彬.莴笋叶叶绿素的提取工艺研究[J].安徽工程科技学院学报,2007,22(4):14-17.
[3] 李景琳,李传欣,张 华.叶绿素铜钠盐生产工艺与产品质量关系[J].沈阳农业大学学报,1998,29(2):196-198.
[4] 汪 坤,洪 海,金文英,等.微波辅助提取蚕沙中叶绿素的工艺研究[J].食品科学,2009,30(6):76-79.
[5] Xu X Q.Research on pigment extracted from the byproduct of silkworm and applied to dye silk fabrics[D].Soochow:Soochow University,2007.
[6] Sun B,Li Y,Wu H L,et al.Progress in study of extracting process of silkworm excrement[J].Plant Physiol,2009,31(4):18-21.
[7] 胡军华,张袁松,李鸿筠,等.蚕粪中提取叶绿素铜钠盐的稳定性研究[J].蚕业科学,2005,31(3):370-373.
[8] 王立娟,钱学仁.竹叶叶绿素铁钠的制备及性质研究[J].林产化学与工业,2006,25(3):89-92.
[9] 才 红,郑炳灿.叶绿素锌钠制备的研究[J].食品研究与开发,2006,27(5):19-21.
[10] 杨国恩,陈丛瑾.毛竹叶叶绿素铜钠的制备[J].生产应用,2009,25(20):127-129.
[11] 鲍会梅.蚕沙中叶绿素铜钠盐和果胶的提取工艺[J].安徽农业科技,2012,40(2):1 047-1 049.
[12] 相纪明,王 琳,潘晓辉,等.蚕沙中叶绿酸铜钠、叶绿酸铁钠的提制及应用[J].安康师专学报,1999,11(3):40-42.
[13] 王立娟,李 坚,叶结旺.松针叶绿素铁钠的制备及稳定性的研究[J].林业科技,2004,29(2):43-45.
[14] 李 祥,文 星,房 媛,等.叶绿素铁钠盐的制备[J].食品与发酵工业,2012,38(4):77-81.
[15] 李培尊.利用蚕沙制备糊状叶绿素及叶绿素衍生物[D].南宁:广西大学,2009.
[16] 李 祥,种亚莉,曹江绒,等.微波协同超声辅助提取蚕沙叶绿素的工艺研究[J].日用化学工业,2013,43(4):285-289.
