人工色素的TLC检测
2014-06-27周冕罗敏张吉坪李晨曦
周冕,罗敏,张吉坪,李晨曦
(重庆理工大学材料科学与工程学院,重庆 400054)
人工色素的TLC检测
周冕,罗敏,张吉坪,李晨曦
(重庆理工大学材料科学与工程学院,重庆 400054)
通过氢键调节作用建立一种快速分离与鉴定人工色素的薄层色谱法。以石油醚-二氯甲烷(7:3,V/V)为基础展开体系,分别对硅胶进行接枝改性和在基础展开体系中添加氢键调节剂,再对人工色素进行薄层色谱检测分析。结果表明:相较于硅胶,改性硅胶的氢键密度明显增大,其氢键密度随着改性剂质量浓度的增加而增大;主链型改性剂和氢键调节剂的引入增加了固定相、流动相与人工色素间形成氢键的可能性,改变了人工色素的Rf值。
人工色素;薄层色谱;氢键作用
人工色素因其色彩鲜艳、着色力强、稳定性好、价格便宜而广泛应用于食品中。然而,在食品中添加的人工色素一旦超过国家规定的使用范围或使用限量,就会直接危害人民群众的身体健康[1-2]。我国《食品添加剂使用标准》[3]明确规定:婴幼儿食品禁止使用任何人工色素。此外,我国对人工色素的使用范围及标准有明确的规定。为了避免不法商家随意扩大人工色素的应用范围和使用剂量,对人工色素的检测非常重要[4]。
目前,检测人工色素的国标方法为高效液相色谱法,另外高效液相-质谱联用法用于检测结果的确证,气相-质谱联用仪也能取得较好效果[5-6]。但是上述方法的检测仪器昂贵、操作复杂、在基层不易普及。为了找到一种更适用于现场快速测定的方法,本文通过对薄层色谱法(TLC)固定相进行改性和在流动相中添加氢键调节剂来调节人工色素与流动相、固定相的氢键作用,建立一种使用薄层色谱法检测人工色素的方法。
大多数常见的人工色素如诱惑红、靛蓝、对位红、苏丹蓝Ⅱ等都含有氢键供体或氢键受体,在与TLC的固定相、流动相作用时,有可能产生氢键作用。近年来的研究成果表明:氢键作用[7-8]在现代色谱分离过程中起重要作用。基于前人[9]对硅胶改性和展开剂调节以改善人工色素分离效果的研究,本文选择主链型改性剂聚乙二醇和侧链型改性剂聚乙烯醇对硅胶进行改性处理,即在硅胶表面接枝含氢键供体或受体较多的聚合物以增加硅胶中易于形成氢键的基团,分析两类改性硅胶对人工色素的不同影响。此外,将氢键作用引入流动相,即配置含氢键调节剂的展开剂,通过调节展开剂的氢键供(受)体密度达到调节和改善展开剂吸附-解吸附作用的效果。因此,本文选择了6种人工色素(见表1)作为目标物质,并根据人工色素的氢键供、受体种类、位置及数量的不同来研究氢键作用对TLC检测人工色素的影响。

表1 目标物质的分子结构及氢键供、受体分布情况
1 材料与方法
1.1 仪器与试剂
1)仪器:SB-100D超声清洗机,宁波新芝生物科技股份有限公司;DZG-6020真空干燥箱,上海森信实验仪器有限公司。
2)试剂:硅胶GF254、聚乙烯醇(polyvinyl alcohol,PVA)、聚乙二醇(polyethylene glycol,PEG)、丙酮、正丙醇、石油醚、二氯甲烷,分析纯,均为市售。
3)目标物质(表1):邻氨基偶氮甲苯、苏丹红B、苏丹Ⅱ、苏丹红7B、苏丹蓝Ⅱ标准品,由重庆市计量质量检测研究院提供。
1.2 改性硅胶及薄层色谱板的制备
根据改性剂氢键供、受体位置的不同,将改性硅胶分为主链型改性硅胶和侧链型改性硅胶;实验选用的主链型改性剂为聚乙二醇,侧链型改性剂为聚乙烯醇。实验通过超声处理将不同质量浓度的改性剂接枝包覆于硅胶表面,以制备不同氢键密度的改性硅胶,研究分析2种改性硅胶对TLC检测人工色素的影响。
称取1.5 g硅胶置于烧杯中,加入20 mL一定质量浓度的改性剂溶液。待硅胶完全浸润后,超声处理15 min,取出烧杯静置并滤去上层清液,置于真空干燥箱中烘干,即得到所需改性硅胶。将所得改性硅胶与适量胶结剂混合至胶粘态,用涂布器涂覆于铝板上,烘干,即制得改性薄层色谱板。
1.3 氢键展开剂的选择
展开剂体系[10]一般为二元以上的流动相体系,采用极性—非极性组合,以便于调节展开剂极性。综合考虑各目标物质的溶解度参数和极性,同时为了避免基础展开剂体系对实验结果的影响,通过实验对常用展开剂体系进行筛选,最终采用的基础展开剂体系为石油醚—二氯甲烷体系,保证基础展开剂体系与人工色素无氢键作用。文中未经特别说明的基础展开剂体系均指石油醚-二氯甲烷体系(体积比为7∶3,每次用量均为10 mL)。根据氢键调节剂与基础展开剂体系的互溶性,选择丙酮、正丙醇(见表2)作为实验的氢键调节剂。

表2 氢键调节剂的分子结构及氢键供、受体分布情况
2 结果与讨论
2.1 改性硅胶对TLC检测人工色素的影响分析
2.1.1 主链型改性硅胶对TLC检测人工色素的影响
实验通过调节主链型改性剂聚乙二醇的质量浓度(0~17.5 g/L)来调节固定相的氢键受体密度,考察人工色素的Rf值随聚乙二醇质量浓度的变化情况。如图1所示,人工色素Rf值增大,可认为是由PEG/SiO2与人工色素之间的氢键作用增强引起的。
对于氢键供体数目不同、氢键供体类型相同的苏丹红7B和苏丹蓝Ⅱ,从图1可以看出随着聚乙二醇质量浓度的增大,苏丹蓝Ⅱ的Rf值增加速率高于苏丹红7B,这可能是因为苏丹蓝Ⅱ中氢键供体数目比苏丹红7B的氢键供体数目多,因此苏丹蓝Ⅱ中可与聚乙二醇氢键受体作用的氢键供体数目比苏丹红7B多,所以PEG/SiO2对苏丹蓝ⅡRf值的影响比苏丹红7B大。对于氢键供、受体数目均相同且分布位置类似的苏丹红B和苏丹红7B,如图1所示,二者的Rf值随着聚乙二醇质量浓度的增加而增大,但苏丹红B的Rf值增加速率高于苏丹红7B。原因在于苏丹红7B与聚乙二醇形成了较弱的氢键体系[11](N—H…O,键能为8 kJ/mol),而苏丹红B与聚乙二醇可形成较强的氢键体系(O—H…O,键能为21 kJ/mol)。因此,相比苏丹红B,PEG/SiO2对苏丹红7B的影响较小。在图1中,可以明显地看到:当聚乙二醇质量浓度增大到某一值后,人工色素的Rf值变化趋于稳定,原因是改性硅胶的氢键密度随着改性剂聚乙二醇的质量浓度增加而增加,当固定相的氢键密度增大到一定值后,固定相与人工色素氢键作用达到饱和状态。
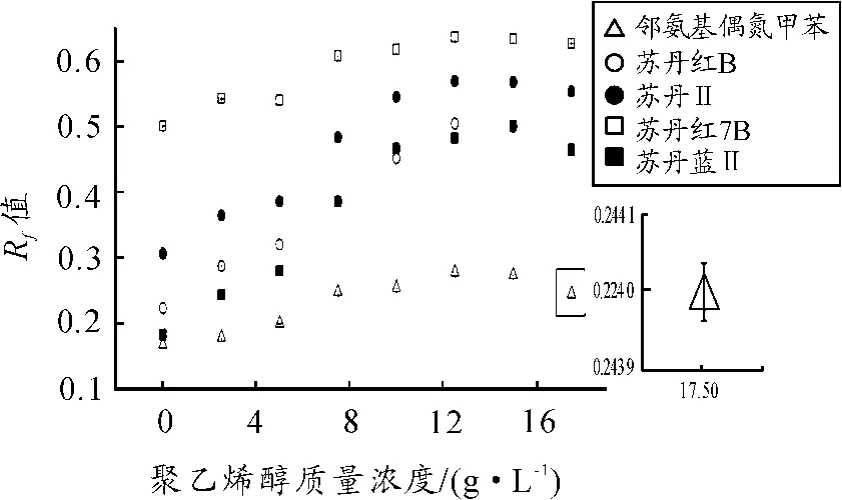
图1 PEG/SiO2对Rf值的影响
2.1.2 侧链型改性硅胶对TLC检测人工色素的影响
选用基础展开剂体系,以便于对照分析,固定相由质量浓度为0~3 g/L的侧链型改性剂聚乙烯醇超声处理得到,实验考察了人工色素Rf值随聚乙烯醇的质量浓度的变化情况,结果表明:PVA/ SiO2对人工色素的Rf值影响甚小。聚乙烯醇的侧链倾向于形成分子内氢键[12],且构成了相对稳定的五、六元环,在展开剂和人工色素的作用下不易于将其分子内氢键打开,因此人工色素与侧链型改性硅胶的氢键作用可忽略。
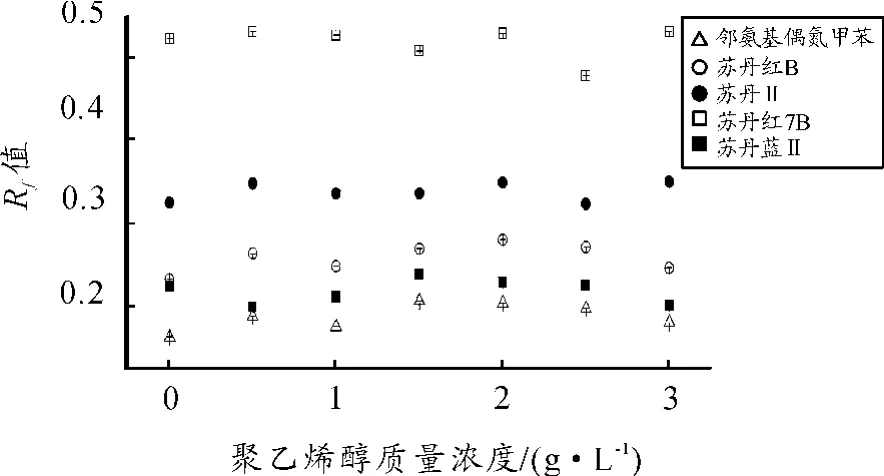
图2 PVA/SiO2对Rf值的影响
2.2 氢键调节剂对TLC检测人工色素的影响分析
选择丙酮和正丙醇作为实验的氢键调节剂加入基础展开剂体系中,通过添加少量的氢键调节剂(0~0.4 mL)来调节流动相中氢键供、受体密度,分析人工色素与流动相的氢键作用对Rf值的影响。但需注意:只有加入少量氢键调节剂时,人工色素Rf值的变化趋势才较为明显,若氢键调节剂的添加量较大,即流动相的氢键供(受)体密度较大时,流动相与人工色素的氢键作用达到饱和,此时氢键调节剂对人工色素的氢键调节作用已趋于稳定。
2.2.1 受体型氢键对TLC检测人工色素的影响
当氢键调节剂为丙酮时,注意到图3与图1的变化趋势相似,且聚乙二醇和丙酮仅提供氢键受体与人工色素产生氢键作用。由图3可知:苏丹红B和苏丹红7B随着丙酮浓度的增加,二者的Rf值也随之增大,但苏丹红7B的Rf值增加速率低于苏丹红B,这可能是由于苏丹红7B与丙酮形成了较弱的氢键体系(N—H…O,键能为8 kJ/ mol),而苏丹红B与丙酮可形成较强的氢键体系(O—H…O,键能为21 kJ/mol)。因此,丙酮对苏丹红7B的Rf值影响比苏丹红B小。对于氢键供体数目不同但类型相同的苏丹红7B和苏丹蓝Ⅱ,从图3可以看出:随着丙酮浓度的增大,苏丹蓝Ⅱ的Rf值增加速率高于苏丹红7B,这可能是由于苏丹蓝Ⅱ中氢键供体数目比苏丹红7B的氢键供体数目多。因此,苏丹蓝Ⅱ中可与丙酮氢键受体作用的氢键供体数目比苏丹红7B多,所以丙酮对苏丹蓝ⅡRf值的影响比苏丹红7B大。
2.2.2 供体型氢键调节剂对TLC检测人工色素的影响
当氢键调节剂为正丙醇时,结果如图4所示。对于氢键受体数目不同的苏丹红B、苏丹Ⅱ2种人工色素,氢键供体和受体的类型相同,此外氢键供、受体的位置分布也类似,排除了氢键体系强弱及氢键形成位置(分子内和分子间)的不同对人工色素Rf值的影响。随着正丙醇添加量的增大,二者的Rf值也增大,但苏丹红B的Rf值增大速率较大。分析其原因,可能是人工色素氢键受体越多,与氢键调节剂形成的氢键数目越多,对人工色素Rf值的影响也越大。再讨论邻氨基偶氮甲苯和苏丹Ⅱ,二者有相同的氢键供体及受体数目,但氢键供体的类型不同,若以氢键体系的强弱分析,按照上文得到的结论,氢键体系越强,对人工色素的Rf值影响越大,即苏丹Ⅱ的Rf值所受影响较大。但从图4可明显地看出:随着正丙醇添加量的增加,邻氨基偶氮甲苯Rf值的变化速率明显高于苏丹Ⅱ。分析其原因是由于苏丹Ⅱ中氢键受体和氢键供体相距较近,为分子内氢键的形成提供了条件,且分子内氢键可构成一种稳定的五、六元环结构,有利于分子内氢键的形成,抑制了正丙醇与苏丹Ⅱ的分子间氢键形成,因此正丙醇对邻氨基偶氮甲苯Rf值的影响更大。

图3 丙酮添加量对Rf值的影响(V展开剂=10 mL)
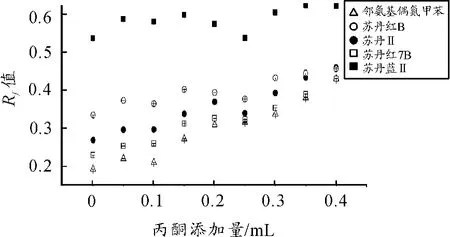
图4 正丙醇添加量对Rf值的影响关系图(V展开剂=10 mL)
3 结束语
通过在TLC的固定相和流动相中引入易于与人工色素形成氢键作用的物质,观察人工色素Rf值的变化情况。结果表明:TLC固定相采用PEG/ SiO2或在流动相中添加少量丙酮时,有利于人工色素的检测分离;PVA/SiO2易于形成分子内氢键,对人工色素Rf值的影响可忽略;而正丙醇添加剂使人工色素的Rf值趋近,不利于人工色素的检测分离。
因此,在薄层色谱法检测实验中,当人工色素难以分离时,可根据人工色素氢键体系的强弱和是否形成分子内氢键及氢键供、受体数目来选择合适的改性剂或氢键调节剂,快速分离人工色素,达到监测食品安全的目的。
[1]徐亚新,肖海波.食品添加人工色素的危害性分析[J].中外医学研究,2009,7(6):124.
[2]葛宇.食品中人工合成色素使用法规及检测标准进展[J].质量与标准化,2011(9):31-35.
[3]中华人民共和国卫生部.GB 2760—2011食品添加剂使用标准[S].北京:中国标准出版社,2011.
[4]Hajslova J,Kraska R,Michel W F.NIELEN.Recent advances in food analysis[J].Analytical and Bioanalytical Chemistry,2012,403(10):2795-2796.
[5]苏小川,黄梅,甘宾宾,等.气相色谱-质谱联用法测定调味品中苏丹红Ⅰ、Ⅱ色素[J].理化检验:化学分册. 2006,42(12):1003-1006.
[6]林晓珊,杭义萍,吴惠勤,等.气相色谱-串联质谱法测定焦糖色素中2-甲基咪唑和4-甲基咪唑[J].分析试验室,2011,30(11):85-88.
[7]Ren-qi WANG,Teng-teng ONG,Weihua TANG,et al. Cationic cyclodextrins chemically-bonded chiral stationary phases for high-performance liquid chromatography[J]. Analytica Chimica Acta,2012,718:121-129.
[8]Karthika M,Senthilkumar K,Kanakaraju R.Hydrogen bond interactions in hydrated acetylsalicylic acid[J]. Computational and Theoretical Chemistry,2011,966(1-3):167-179.
[9]张栓红,孙昌梅,曲荣君,等.几种聚合物改性硅胶对苯胺的吸附性能研究[J].离子交换与吸附,2011,27 (1):43-52.
[10]孙毓庆,胡育筑.液相色谱溶剂系统的选择与优化[M].北京:化学工业出版社,2008:112-114.
[11]Oliveira,Boaz G,Araujo,et al.Bonding topology,hydrogen bond strength,and vibrational chemical shifts on hetero-ring hydrogen-bonded complexes-Theoretical insights revisited[J].Canadian Journal of Chemistry,2012,90 (4):368-375.
[12]朱新生,戴礼兴,闻荻江.氢键与高强高模聚乙烯醇纤维[J].纺织学报,2002,23(2):7-8.
(责任编辑 何杰玲)
TLC Detection of Synthetic Pigment
ZHOU Mian,LUO Min,ZHANG Ji-ping,LI Chen-xi
(College of Materials Science and Engineering,Chongqing University of Technology,Chongqing 400054,China)
This article establishes a thin layer chromatography(TLC)for the fast separation and identification of synthetic pigment by hydrogen-bonding effects.Based on the conditions of petroleum ether -methylene chloride(7∶3,V/V),TLC detection and analysis on synthetic pigment was carried out by grafting hydrogen-bonding modifier onto silica gel and adding hydrogen bonding regulator to based system respectively.The results suggest that hydrogen-bonding density of modified silica gel is significantly higher than that of silica gel and increases with modifiers mass concentration.Main chain modifier and hydrogen-bonding eluent increases the possibility of hydrogen-bonding between synthetic pigment and stationary phase,as well as mobile phase,which changes the Rfvalue effectively.
synthetic pigment;thin layer chromatography;hydrogen-bonding effects
R155
A
1674-8425(2014)08-0055-05
10.3969/j.issn.1674-8425(z).2014.08.012
2014-04-21
重庆理工大学拔尖创新人才培养项目(BC201204)
周冕(1973—),博士,副教授,主要从事产品质量检测与功能高分子材料制备方面的研究。
周冕,罗敏,张吉坪,等.人工色素的TLC检测[J].重庆理工大学学报:自然科学版,2014(8):55-59.
format:ZHOU Mian,LUO Min,ZHANG Ji-ping,et al.TLC Detection of Synthetic Pigment[J].Journal of Chongqing University of Technology:Natural Science,2014(8):55-59.
