不同形貌纳米ZnO的光催化性能研究*
2014-06-09周小岩于建平刘彦民周鹏威任汝飞
周小岩,于建平,刘彦民,周鹏威,任汝飞
(中国石油大学 理学院,山东 青岛 266580)
随着全球化工业进程的发展,人类直接或间接地向环境排放超过其自净能力的物质或能量导致了环境污染问题,因此环境保护和可持续发展成为人们首先要考虑的问题,从而半导体光催化材料成为科学家研究的重点[1]。纳米半导体材料在光的照射下,通过把光能转换为化学能,促进化合物的合成或者使化合物分解的过程称之为光催化[2]。1972年Honda和Fujishima在Nature上发表“水的光分解现象”,发现在TiO2电极上光催化分解水的现象,开创了多相催化研究的新时代[3]。多相光催化系统中,初始的光激发发生在催化剂分子上,催化剂分子把电子转移给吸附在其上的有机物分子,导致有机物发生氧化分解,此后光催化逐渐成为世界范围内最活跃的研究领域之一。
纳米ZnO作为一种重要的光催化剂,具有无毒、经济、优异的化学和热稳定性等特点,并且在某些实验条件下具有比TiO2更高的光催化性能[4-5]。已有研究结果表明,通过形貌调控可以有效的提高纳米ZnO的光利用效率和光催化活性[6],所以研究不同形貌的ZnO对其光催化性能的影响具有重要意义。作者通过水热合成法在不添加任何表面活性剂的情况下制备出不同形貌的纳米ZnO材料,以亚甲基蓝为目标污染物研究了不同形貌纳米ZnO的光催化活性,并讨论了其生长机理及形貌对光催化性能的影响,为未来纳米ZnO光催化材料的应用提供了有价值的信息。
1 实验部分
1.1 试剂与仪器
Zn(NO3)2·6H2O:分析纯,国药集团;NaOH:分析纯,天津市巴斯夫化工厂;乙醇:分析纯,天津化工厂;亚甲基蓝:分析纯,天津市巴斯夫化工厂;去离子水。
FA2004N电子天平:上海精密仪器有限公司;L-530型离心机:湖南湘仪离心机仪器有限公司;175 W主波长为365 nm的高压汞灯:南京紫外电器有限责任公司;聚四氟乙烯内衬的水热反应釜:河南杜甫仪器厂;GZX-9023型鼓风干燥箱:上海博讯实业有限公司;85-2型恒温磁力搅拌器:上海维城仪器有限公司;X′Pert PRO MPD型X射线衍射仪:Cu靶Kα射线,波长0.154 06 nm,工作电压40 kV,工作电流28 mA,步长0.03°,荷兰帕纳科公司;S-4800冷场发射扫描电镜:日本日立公司;756PC型紫外可见分光光度计:上海光谱仪器有限公司。
1.2 催化剂的制备
首先配制100 mL不同浓度的NaOH溶液,将其缓慢滴入100 mL浓度为0.10 mol/L的Zn(NO3)2·6H2O溶液中,磁力搅拌30 min后,得到均匀的白色混浊液。然后将混浊液转移至200 mL不锈钢反应釜的聚四氟乙烯内胆中,填充度为80%,在120 ℃下恒温反应12 h,之后冷却至室温,将所得的白色沉淀物分别用去离子水和无水乙醇洗涤数次并离心,最后将分离出的样品放入60 ℃鼓风干燥箱中干燥。为了制备不同形貌的纳米ZnO,改变NaOH溶液的浓度,保持反应温度120 ℃和反应时间12 h等操作条件,得到3种不同的反应样品,其具体配比方案见表1。
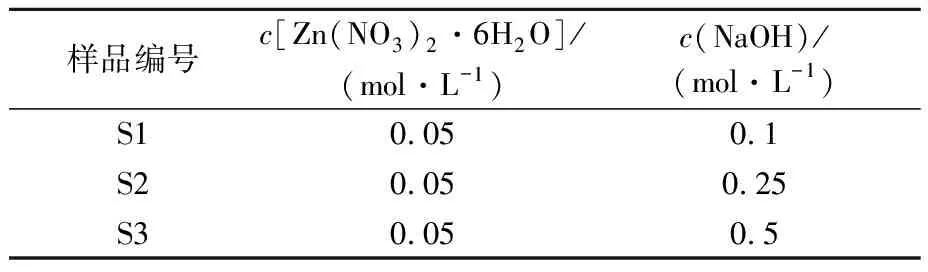
表1 反应物方案配比表
1.3 微结构表征
采用X′Pert PRO MPD型X射线衍射仪,分析催化剂的物相结构,采用S-4800冷场发射扫描电镜观察光催化剂的表面形貌。
1.4 光催化降解实验
光催化实验在自制的无色透明双层玻璃冷阱(0.40 L)中进行,通入循环自来水使反应过程中温度保持恒定,磁力搅拌器带动溶液中的搅拌子转动以保持反应过程中溶液浓度均匀。在室温下准确称取0.04 g光催化剂样品并与200 mL初始质量浓度为10 mg/L的亚甲基蓝溶液混合加入冷阱中,在磁力搅拌机上遮光搅拌0.5 h,以达到吸附-脱附平衡。然后打开175 W的高压汞灯开始照射,光源距液体22 cm,每隔15 min取样一次,直至溶液完全褪色,离心分离后,将上层清液放入石英比色皿中。采用756PC型紫外可见分光光度计测定其在亚甲基蓝最大吸收波长(λmax=664 nm) 处的吸光度A,并计算亚甲基蓝的降解率。根据朗伯-比尔定律,在整个降解过程中可用吸光度的变化表征亚甲基蓝溶液质量浓度的变化,进而表征光催化效率的高低,因此降解率D见下式[7]。
其中A0、At-分别是未光照和光照时间t时的溶液吸光度,ρ0和ρt-分别是未光照和光照时间t时的溶液质量浓度。
2 结果与讨论
2.1 光催化材料的XRD分析
样品S1、S2和S3的XRD图谱见图1。
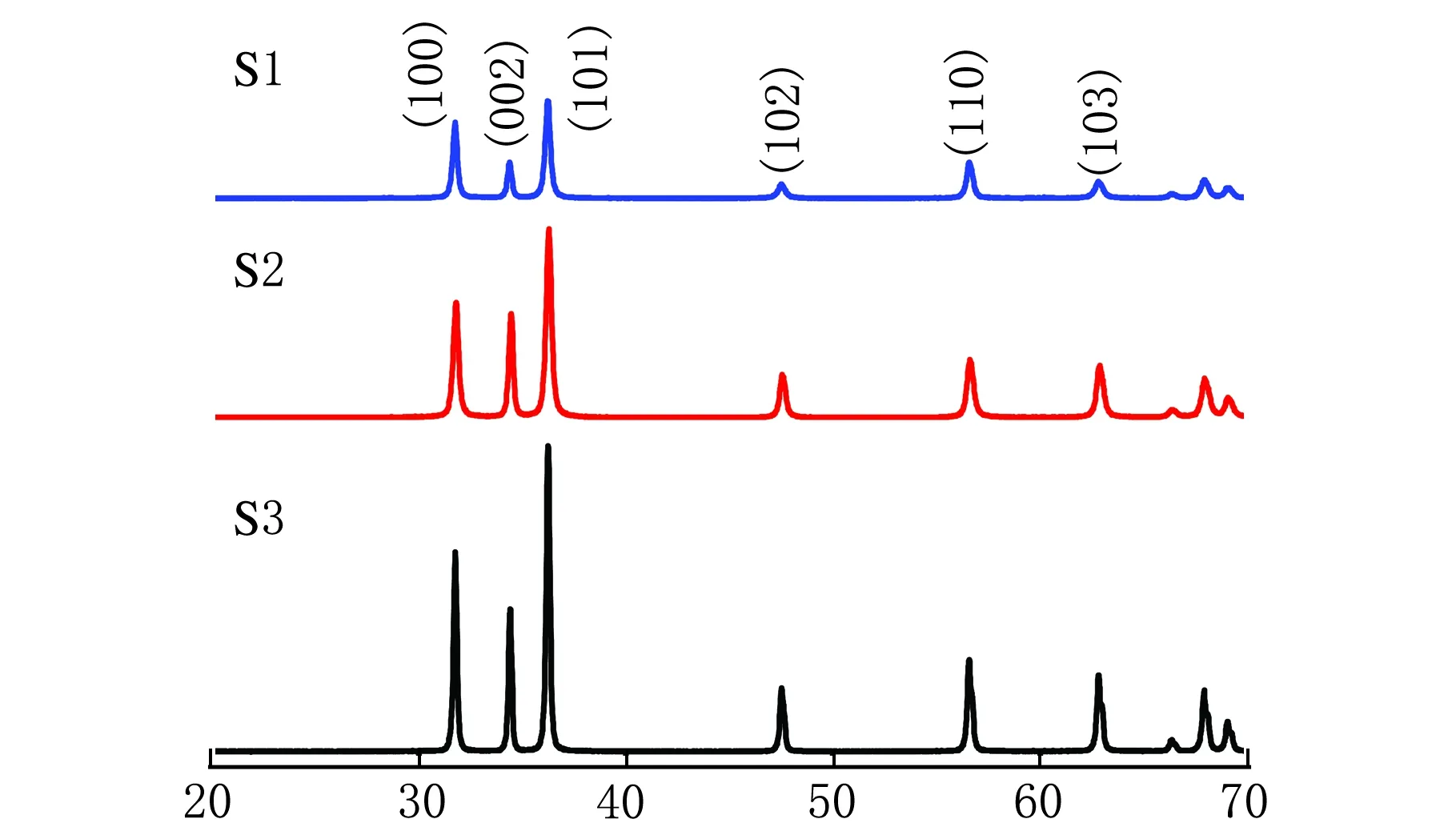
2θ/(°)图1 样品S1、S2和S3的XRD衍射图谱
衍射角范围为20°~70°,ZnO衍射峰指认结果列于图中,与JCPDS卡片上的ZnO标准谱图(00-036-1451)一致,说明制备的ZnO纳米晶均为六方晶系的纤锌矿结构。同时在XRD图谱中未发现其它衍射峰,说明制备的样品没有出现Zn(OH)2、Na等杂质,得到的样品均为纯ZnO晶体。从图1可以看出随着配比方案中NaOH溶液浓度的增大,衍射峰越尖锐,强度越大,说明结晶质量越高。
2.2 光催化材料的SEM表征
样品的SEM照片见图2,放大倍数均为3万倍。从图2可以看出,S1样品的形貌类似两端略尖中间较粗的纺锤,表面较粗糙,是由很多小的颗粒堆积而成,并且尺寸较大。S2样品呈现片状,大小不一,边界呈六角形或多边形,大的片状体是由多个纳米小片晶体通过共享边界融合生长而成的。由于c轴方向上叠合生长较慢,厚度约为40 nm。S3样品的形貌为纳米棒状,棒的末端呈六方柱状,这些纳米棒有序的自组装在一起并且由中心向外辐射成菊花状,但有少量的纳米棒散落在花状结构中,直径范围是120~200 nm,长度可达2~3 μm。可见ZnO晶体的形貌受溶液碱度的影响较大,随着碱浓度的增大,所得的产物尺寸越小形貌也越规则。



图2 样品S1、S2和S3的扫描电镜照片
2.3 光催化性能评价
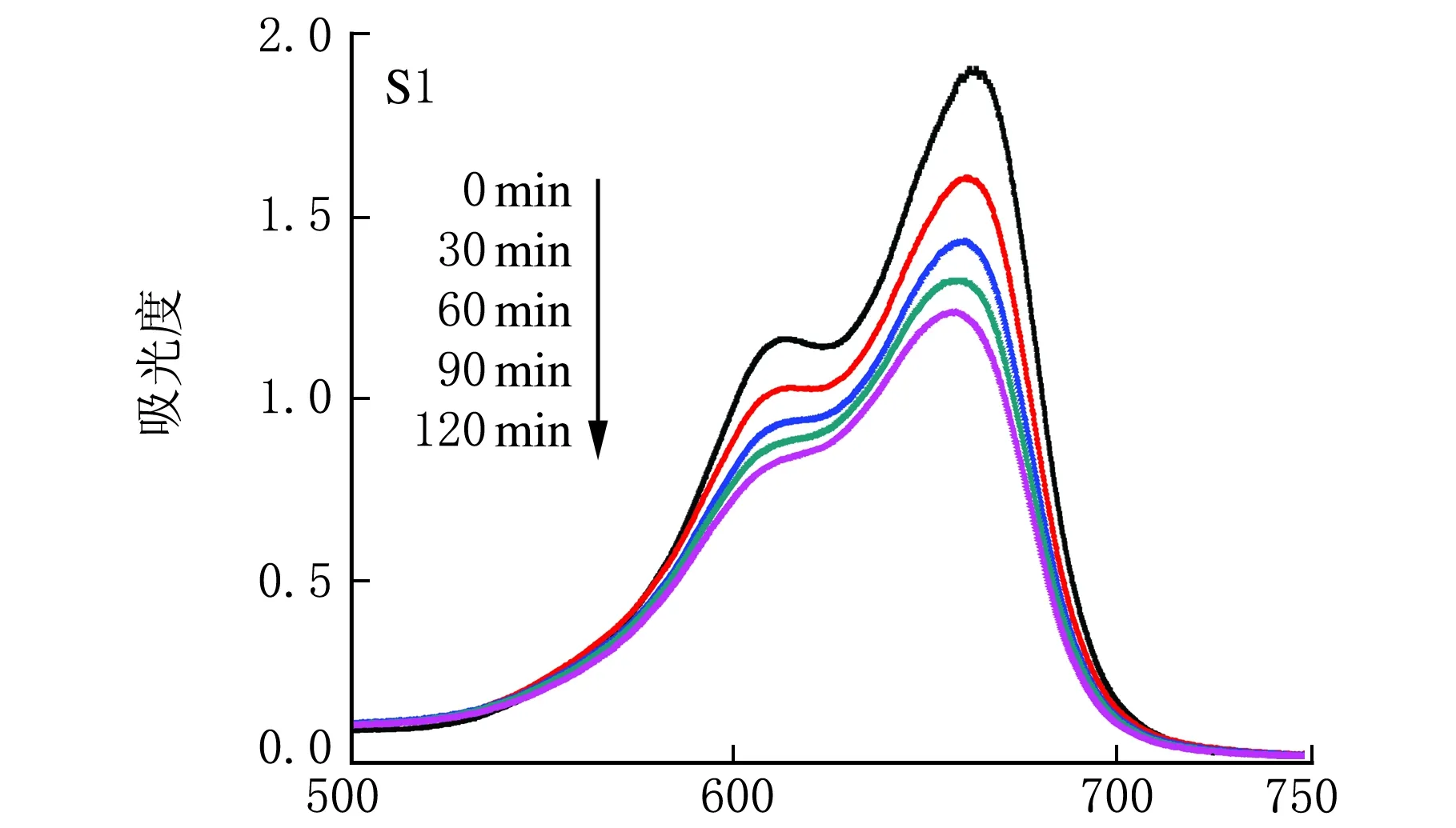
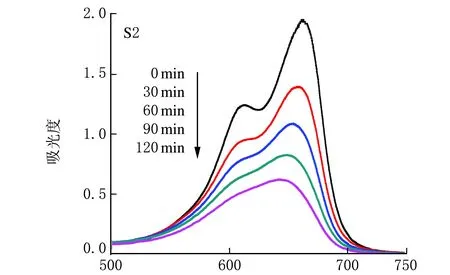
在光催化反应中,催化剂的投入量为0.04 g,亚甲基蓝溶液为0.20 L,质量浓度为10 mg/L,光照时间为120 min。样品S1、S2和S3光催化降解亚甲基蓝溶液在不同时间段的吸收光谱见图3。从图3可以看出,随着光照时间的增长,亚甲基蓝在664 nm 处的主吸收峰值明显减弱。纳米ZnO在主波长为365 nm的高压汞灯照射下,价带的电子被激发到导带,形成电子-空穴对,空穴有很强得电子能力,可夺取ZnO表面吸附的OH-、H2O或溶剂中的电子生成羟基自由基(·OH),缔合在ZnO表面的·OH为强氧化剂,既能氧化周围的有机物,也能扩散到溶液中氧化有机物,进而达到降解的目的[8]。
λ/nm
λ/nm
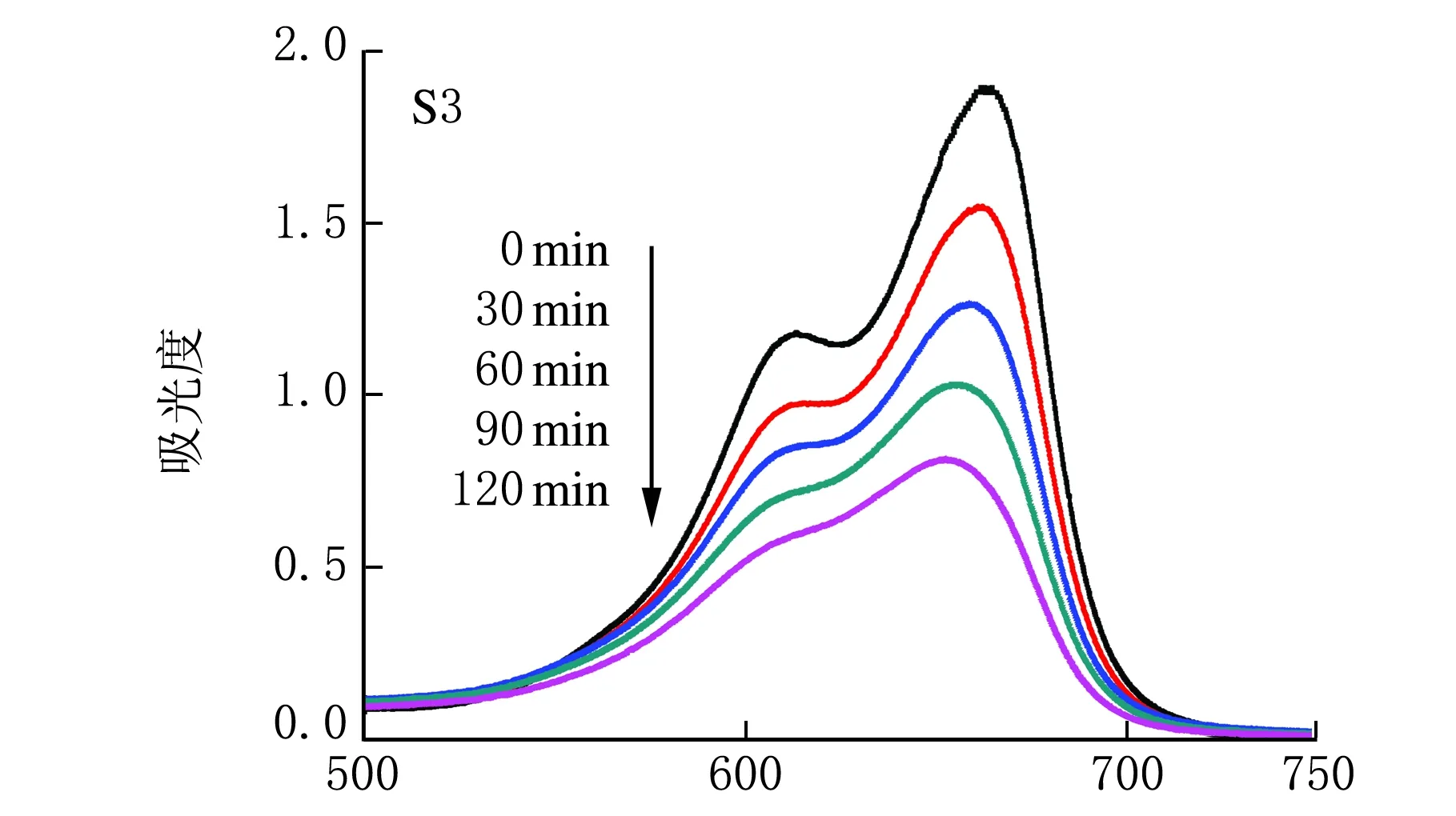
λ/nm图3 样品S1、S2和S3光催化降解亚甲基蓝溶液的吸收光谱
样品S1、S2和S3光催化亚甲基蓝溶液,其降解率随时间的变化曲线见图4。从图4可以看出,样品S2的光催化活性最高,光照120 min,降解率可达75%。在同等条件下,样品S3和S1对亚甲基蓝溶液的降解率分别为61%和37%。由此可见,以上3种不同形貌的纳米ZnO光催化剂的光催化活性顺序依次为:片状> 棒状>纺锤状。
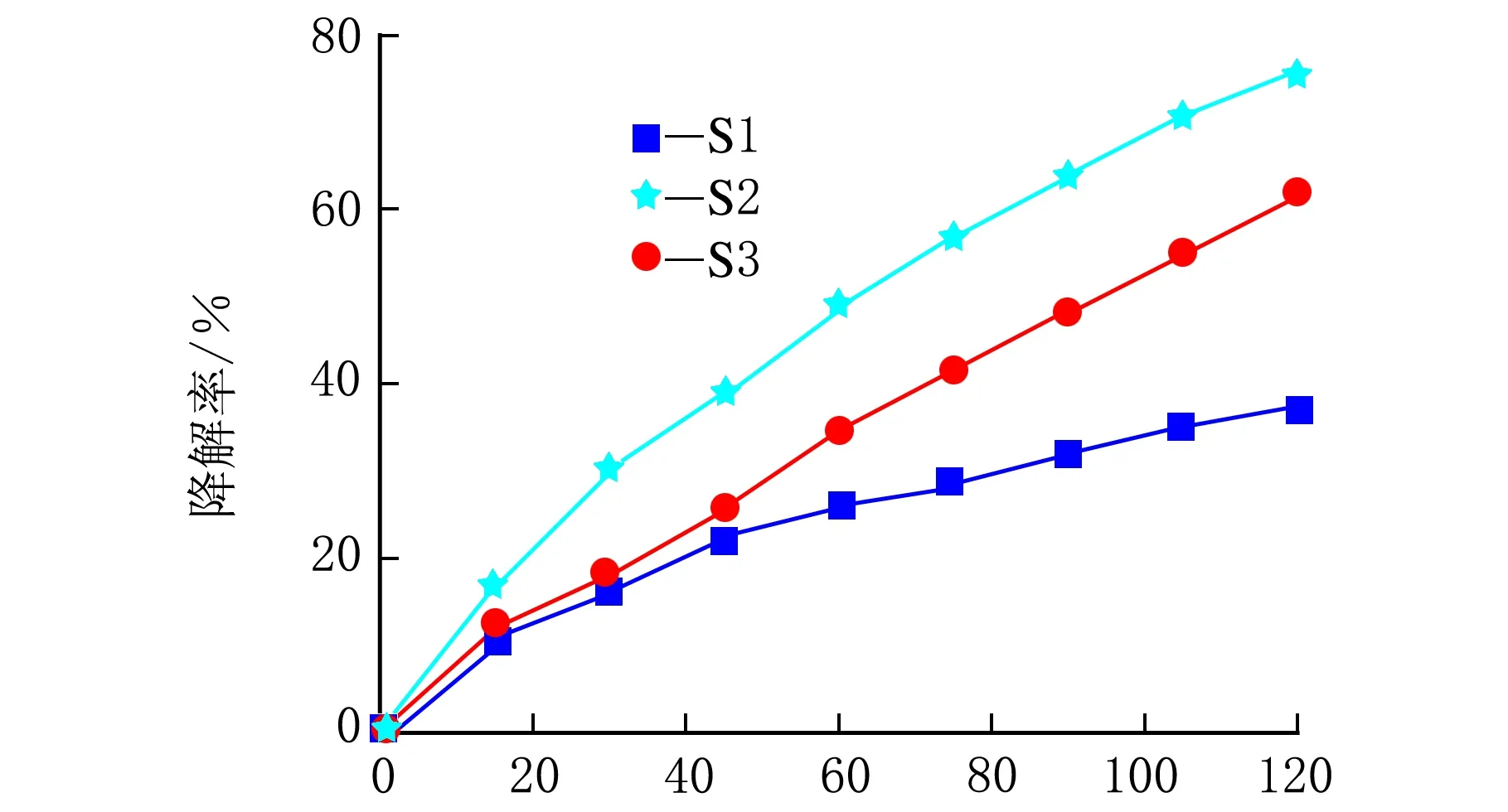
t/min图4 样品S1、S2和S3光催化性能的比较
2.4 纳米ZnO可控生长机理及光催化性能分析
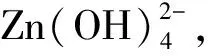

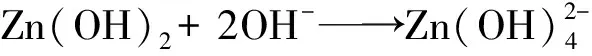
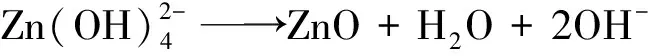
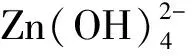
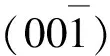
3 结 论
以Zn(NO3)2·6H2O和NaOH为主要原料,采用水热合成法制备不同形貌的纳米ZnO粉体,研究其光催化性能。与纺锤状、棒状ZnO相比,片状ZnO呈现出较高的光催化活性。片状ZnO光催化活性的增强与ZnO晶体显露极性面(001)的大小有关。ZnO晶体显露极性面的面积相对非极性面越大,其光催化活性越高。
[ 参 考 文 献 ]
[1] Pruden A L,Ollis D F.Degradation of chloroform by photoassisted heterogeneous catalysis in dilute aqueous suspensions of titanium dioxide[J].Environ Sci Technol,1983,17:628-631.
[2] 余家国,赵修建.半导体多相光催化原理及其在环境保护中的应用[J].武汉工业大学学报,2000,22:12-15.
[3] Fuijishima A,Honda K.Photolysis of water at a semiconductor electrode[J].Nature,1972,238:37-38.
[4] Khodja A A,Sehili T,Pilichowski J F,et al.Photocatalytic degradation of 2-phenylphenol on TiO2and ZnO in aqueous suspensions[J].J Photochem Photobiol A,2001,141(2/3):231-239.
[5] Daneshvar N,Salari D,Khataee A R.Photocatalytic degradation of azo dye acid red 14 in water on ZnO as an alternative catalyst to TiO2[J].J Photochem Photobiol A,2004,162(2/3):317-322.
[6] Xu F,Zhang P,Navrot sky A,et al.Hierarchically assembled porous ZnO nanoparticles:synthesis,surface energy,and photocatalytic activity[J].Chem Mater,2007,19:5680-5686.
[7] 韩冬,任湘菱,陈东,等.纳米ZnO的制备及光催化性能研究[J].感光科学与光化学,2005,23(6):414-420.
[8] 程晓丽,霍丽华,徐英明,等.氧化锌纳米粉体的制备及光催化性能研究[J].光散射学报,2006,18(4):306-308.
[9] 王步国,仲维卓,施尔畏,等.ZnO晶体的极性生长习性与双晶的形成机理[J].人工晶体学报,1997,26(2):102-108.
[10] Laudise R A,Ballman A A.Hydrothermal synthesis of zinc oxide and zinc sulfide[J].J Phys Chem,1960,64(5):688-691.
[11] Laudise R A,Kolb E D,Caporaso A J.Hydrothermal growth of large sound crystals of zinc oxide[J].Journal of the American Ceramic Society,1964,47(1):9-12.
[12] Zeng J H,Jin B B,Wang Y F.Facet enhanced photocatalytic effect with uniform single-crystalline zinc oxide nanodisks[J].Chem Phys Lett,2009,427:90-95.
[13] 郭莉,王丹军,闫龙,等.ZnO纳米晶的面催化活性特性研究[J].人工晶体学报,2011,40(4):1017-1021.
[14] Jang E S,Won J H,Hwang S J,et al.Fine tuning of the face orientation of ZnO crystals to optimize their photocatalytic activity[J].Advanced Materials,2006,18(24):3309-3312.
