电化学发光免疫分析法检测维生素D试剂盒性能验证
2014-05-25何国坚韦庆文
何国坚* 肖 庆 韦庆文
(深圳市龙岗中心医院,广东 深圳 518116)
电化学发光免疫分析法检测维生素D试剂盒性能验证
何国坚* 肖 庆 韦庆文
(深圳市龙岗中心医院,广东 深圳 518116)
目的在罗氏CS E170分析仪采用电化学发光免疫分析法检测维生素D,评价其试剂盒性能指标。方法参考美国全国临床和实验室标准化协会(NCCLS)的EP系列文件,对电化学发光免疫分析法检测维生素D试剂盒性能指标做出评估。结果电化学发光免疫分析法检测维生素D有较好的稳定性,本实验的检出限为3.0 ng/mL;两种不同浓度的定值质控血清在准确度评估中相对偏差(Bias%)均<8%;三种不同浓度的临床患者混合血清及两种不同浓度的定值质控血清评估精密度批内、批间变异系数(CV%)均<5%;在线性范围评价中均为发现离群点,线性回归方程为y=0.0181+0.988x,r=0.988。稀释变异P为0.45(P0.05=0.6841),P<0.05,稀释变异可接受,线性失拟检查G=3.22(F0.05=3.29),G< F0.05,线性良好;干扰试验以相对偏差<8%为医学决定水平,T-Bil浓度≤360 μmol/L,Hb浓度≤4.0 g/L,维生素D测定相对偏差在可接受范围;Hb浓度≥4.0 g/L,可引起维生素D测定结果升高,相对偏差尚在可接受范围;Hb浓度≥9.0 g/L,引起维生素D测定结果升高超出可接受范围。结论CS E170分析仪电化学发光免疫分析法检测维生素D试剂盒稳定性、准确度、精密度、线性范围、抗干扰能力均符合临床检验要求。
维生素D;电化学发光免疫分析法;性能验证
维生素D是一种脂溶性类固醇激素前体,主要由皮肤经光照后产生。维生素D本身无生物活性,必须在肝脏和肾脏相继接受两次羟基化才能生成具有生物活性1,25-羟基维生素D。 维生素D的两种重要形式包括维生素D3(胆钙化醇)和维生素D2(麦角钙化醇)。与维生素D3不同,人体不能合成维生素D2,只能从强化食品或食品补充剂中获取。
罗氏E170分析仪维生素D检测利用维生素D结合蛋白 (VDBP)作为捕获蛋白,结合维生素D3(25-OH)和维生素D2(25-OH)。EIecsys维生素D检测具有高灵敏度,且所受影响因素较少,能自动化批量操作。我们在罗氏CS E170分析仪采用电化学发光免疫分析法检测维生素D,参考美国全国临床和实验室标准化协会(NCCLS)的EP系列文件,对试剂盒性能指标做出评估,现分析如下。
1 材料与方法
1.1 仪器与试剂:罗氏CS 170E全自动分析仪,试剂及质控品为罗氏原厂试剂。R1为BPRu标记的维生素D结合蛋白;钌标记的维生素D结合蛋白;pH 7.5;R2为生物素标记的25-羟基维生素D;生物素化25-羟基维生素D;pH 8.6。试剂批号为174625。使用厂家提供标准品及质控品。质控1批号171270,靶值21.3 ng/mL;质控2批号170777,靶值43.6 ng/mL。
1.2 检测原理:竞争法原理,总检测时间:27 min;仪器自动通过2点校正的定标曲线计算得到检测结果。
1.3 方法:参考NCCLS的EP系列文件,对试剂盒储存稳定性、准确度、线性范围及干扰实验做出性能评估。
1.4 统计学分析:采用统计学软件SPSS12.0及EXCEL软件对数据进行分析处理。
2 结 果
2.1 稳定性:以蒸馏水代替样本监测试剂空白吸光值(Abs1)评价试剂稳定性,连续测定1个月,试剂稳定,已超过说明书开封后放置在CS 170E上稳定28 d的指标。评价样本稳定性采用选择8份在试剂盒线性范围内(3~70 ng/mL)不同浓度临床样本血清,注意排除溶血及黄疸标本,连续测定维生素D 2次取平均值,置于4 ℃保存4 d,解冻连续测定维生素D 2次取平均值,采用t检验比较各样本2次均值差异,结果各样本2次均值差异无统计学意义(P>0.05),具有较好的稳定性。
2.2 检出限:以25次试剂空白均值+3S计算检出限,本方法检出限为≤2.0 μg/mL,根据说明书,低于检出限报告维生素D≤3.0 μg/mL。
2.3 准确度:采用两种不同浓度的定值质控血清各重复测定3次,计算各浓度均值()及相对偏差(Bias%),以相对偏差<8%为医学决定水平,评价试剂盒准确度,结果见表1。
不同浓度两种定值血清相对偏差均<8%,试剂盒测试准确度评估合格。
2.4 精密度:以三种不同浓度的临床患者混合血清及两种不同浓度的定值质控血清为检测对象,每日检测2次(间隔时间>2 h),连续检测10日,评价方法的批内及批间变异系数(CV%),结果见表2。
参照美国NCCLS机构EP文件要求,批内、批间不精密度均<5%,试剂盒检测精密度符合要求。
2.5 线性范围评价:在试剂盒标定的线性范围(3.00~70 ng/mL)取高浓度血清样本(60.4 ng/mL)为5号样本及低浓度样本血清(4.12 ng/mL)为1号样本,二者3∶1混合为2号样本,等份混匀为3号,1∶3混合为4号,2~4号样本浓度计算公式:标本浓度=(C1V1+C5V5)/(V1+V5),C为浓度,V为体积。随机排列,每个标本测定4次,当天完成测定,离群点检查P0.05=0.885,本组数据均为发现离群点,采用线性回归分析,线性回归方程为y=0.0181+0.988x,r=0.988,稀释变异P为0.45(P0.05=0.6841),P<0.05,稀释变异可接受,线性失拟检查G=3.22(F0.05=3.29),G< F0.05,线性良好。
2.6 干扰试验:选取含总胆红素(T-Bil)浓度360 μmol/L,血红蛋白(Hb)浓度9 g/L的干扰物,将干扰物与临床混合血清混合制成不同浓度血清干扰物混合物,检测相对偏差,评价不同干扰物浓度对试剂盒检测影响,结果见表3。
以相对偏差<8%为医学决定水平,T-Bil浓度≤360 μmol/L,Hb浓度≤4.0 g/L,维生素D相对偏差尚在可接受范围。Hb浓度≥4.0 g/L引起维生素D测定结果升高,Hb浓度≥9.0 g/L引起维生素D测定结果升高超出可接受范围。

表1 两种不同浓度定值质控血清测定结果:(ng/L)

表2 临床混合血清、定值质控血清重复性试验标准差、变异系数结果
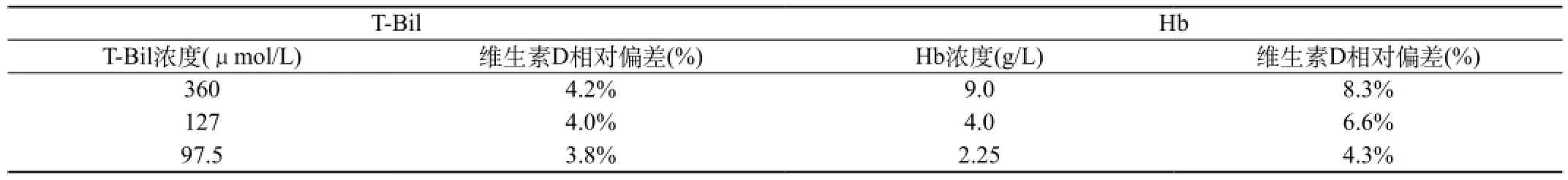
表3 干扰试剂盒实验结果
3 讨 论
维生素D是维持骨骼健康的主要元素。儿童期维生素D的严重缺乏将致骨骼畸形,即佝偻病。轻度缺乏将导致食物钙的利用度下降[1]。维生素D缺乏将导致肌肉乏力;对于中老年人,维生素D对肌肉功能的影响还将增加跌倒风险[2]。维生素D缺乏是导致继发性甲状旁腺功能亢进症的主要原因。PTH水平升高,特别是对于中老年维生素D缺乏人群,可导致骨软化症,骨转换增加,骨量减少,骨折风险增加。维生素D(25-OH)浓度降低与骨密度降低有关。 结合其他临床资料,检测结果有助于评估骨代谢情况。到目前为止,已发现维生素D可影响200多种不同基因的表达。维生素D缺乏与糖尿病、不同种类的癌症、心血管疾病、自身免疫性疾病和先天性免疫疾病有关[3]。
血清25-OHD测定是衡量VD营养状态的最佳指标,由于25-OHD的测定结果直接影响对VD营养状况的判断,测定结果准确与否、不同的测定方法之间是否一致,至关重要。现有多种方法用于临床25-OHD的测定,根据方法原理,可分为免疫分析法和色谱法。免疫分析法只能测定25-OHD总量,无法同时测定25-OHD2和25-OHD3的浓度。现有色谱法可区分并能分别定量25-OHD2和25-OHD3。免疫分析法是早期VD测定的主流方法。
目前常用方法有:①放射免疫法(RIA),灵敏度高、特异性强、精密度好,仪器设备条件要求不高,是基层单位对超微量物质测定的主要手段,但存在放射污染的潜在风险。②酶联免疫吸附法(ELISA):设备和操作简单,无污染,但敏感性和特异性较差。③化学发光免疫测定法(CLIA):具有操作简单、快速、无同位素污染等优点,容易自动化,适合在临床实验室常规开展。Leino等分析比较了罗氏E170电化学发光免疫分析仪与RIA、HPLC、LC-MS/MS检测25-OHD3结果的符合性,发现ECLIA法与LC-MS/MS、RIA检测结果的一致性较好[4-6]。
HPLC是早期应用较多的色谱法之一,灵敏度、特异性、准确性都较高,但设备较贵,标本前处理过程复杂。操作程序较复杂,需要更昂贵的特殊仪器,不适合临床常规开展。
由于检测方法学的局限,目前尚无血清25-OHD的统一标准。为保证检测方法的准确性及稳定性,我们对罗氏E170电化学发光免疫分析系统检测血清维生素D试剂盒进行评估。评估结果表明:电化学发光免疫分析法检测维生素D的检出限为3.0 ng/mL;两种不同浓度的定值质控血清在准确度评估中相对偏差(Bias%)均<8%;三种不同浓度的临床患者混合血清及两种不同浓度的定值质控血清评估精密度批内、批间变异系数(CV%)均<5%;在线性范围评价中均为发现离群点,线性回归方程为y=0.0181+0.988x,r=0.988。稀释变异P为0.45(P0.05=0.6841),P<0.05,稀释变异可接受,线性失拟检查G=3.22(F0.05=3.29),G< F0.05,线性良好;干扰试验以相对偏差<8%为医学决定水平,T-Bil浓度≤360 μmol/L,Hb浓度≤4.0 g/L,维生素D测定相对偏差在可接受范围;Hb浓度≥4.0 g/L,可引起维生素D测定结果升高,相对偏差尚在可接受范围;Hb浓度≥9.0 g/L,引起维生素D测定结果升高超出可接受范围。CS E170分析仪电化学发光免疫分析法检测维生素D试剂盒稳定性、准确度、精密度、线性范围、抗干扰能力均符合临床检验要求。
[1] Steingrimsdottir L.Relationship between serum parathyroid hormone levels,vitamin D sufficiency,and calcium intake[J].JAMA,2005, 294(18):2336-2341.
[2] Venning G.Recent deve lopments in vitamin D deficieney and muscle weakness among eldery people[J].BMJ,2005,330(7490): 524-526.
[3] Holick MF.Vitamin D deficiency[J].N Engl J Med,2007,357(3): 266-281.
[4] 杨有业,张秀明.临床检验方法学评价[M].北京:人民卫生出版社,2008.
[5] 陈益明,褚雪莲,王忠平,等.电化学发光免疫分析法检测婴幼儿血清 25-羟基维生素 D3参考区间的调查[J].现代预防医学, 2014,41(3):389-392.
[6] 李波,谭祥权,罗佳美,等.万州区儿童维生素D营养状况及其与身高发育的关系研究[J].重庆医学,2013,42(33):4070-4072.
R392
B
1671-8194(2014)23-0076-02
深圳市龙岗区科创委课题,编号LG20140519093453
*通讯作者:E-mail:583030063@qq.com
