HPLC法检查环戊丙酸雌二醇原料药的有关物质
2014-05-22杜碧莹广州市药品检验所广州510160
杜碧莹(广州市药品检验所,广州 510160)
环戊丙酸雌二醇为长效雌激素,其作用比戊酸雌二醇强而持久,维持时间在3~4周以上,临床上主要用于卵巢功能不全、闭经、更年期综合征、老年性阴道炎及前列腺癌等;其与甲羟孕酮组成复方注射用避孕药(全球通用药名Lunelle),可作为每月1次长效避孕剂,已获美国FDA认可[1-2]。环戊丙酸雌二醇质量标准仅在《美国药典》(USP)36版[3]有收载,2010年版《中国药典》以及现行版《英国药典》《欧洲药典》《日本药局方》均无收载。而目前USP 36版及国内研究并没有对环戊丙酸雌二醇的有关物质进行定性定量研究,因此难以保证药品质量。本文建立了新的有关物质检查方法,并通过测定不同浓度杂质的标准曲线计算杂质校正因子,从而提高了有关物质控制的准确性,以更好地对环戊丙酸雌二醇的质量情况进行评价。
1 材料
1.1 仪器
1200高效液相色谱(HPLC)仪系统、紫外检测器、Chem Station工作站(美国Agilent公司)。
1.2 药品与试剂
环戊丙酸雌二醇(USP对照品,批号:CAT NO.1252003,纯度:99.9%,105 ℃干燥4 h后用);杂质Ⅰ[雌甾-1,3,5(10)-三烯-3,17-二醇,(17β)-,17-环戊乙酸酯,企业工作对照品,批号:ZP034-S003,纯度:99.28%);杂质Ⅱ[雌甾-1,3,5(10),9(11)-四烯-3,17-二醇,(17β)-,17-环戊丙酸酯,企业工作对照品,批号:ZP034-S002,纯度:98.58%);环戊丙酸雌二醇原料药(北京某公司,批号:20110941、20110942、20110943,纯度:100.9%、99.9%、99.8%);乙腈为色谱纯,水为纯净水,其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件
色谱柱:Kromasil C18(以十八烷基硅烷键合硅胶为填充剂,25 cm×4.6 mm,5 μm);流动相:硝酸铵溶液(取0.8 g硝酸铵,溶解于300 ml水中)-乙腈(23∶77,V/V),流速:1.5 ml/min;柱温:35 ℃;检测波长:280 nm;进样量:50 μl。
2.2 溶液的制备
2.2.1 供试品溶液。取环戊丙酸雌二醇原料药适量,精密称定,加溶剂[乙腈-水(70∶30)]溶解并定量稀释制成每1 ml中约含1 mg的溶液,即得。
2.2.2 对照溶液。精密量取供试品溶液适量,加溶剂稀释制成每1 ml中约含1 μg的溶液,即得。
2.2.3 对照品溶液。取杂质Ⅱ对照品适量,精密称定,用溶剂溶解并定量稀释制成每1 ml中约含2 μg的溶液,作为对照品溶液。
2.3 系统适用性试验
取环戊丙酸雌二醇USP对照品、杂质Ⅰ与杂质Ⅱ对照品适量,精密称定,用溶剂溶解并定量稀释制成每1 ml中含1 mg、1.5 μg、2 μg的混合溶液。取50 μl,注入液相色谱仪,环戊丙酸雌二醇的保留时间约为20 min;环戊丙酸雌二醇峰与杂质Ⅱ的分离度应大于2.0,理论板数按环戊丙酸雌二醇峰计不低于5000。系统适用性溶液和供试品溶液(批号:20110941)色谱图见图1。

图1 高效液相色谱图A.系统适用性溶液;B.供试品溶液;1.杂质Ⅰ;2.杂质Ⅱ;3.环戊丙酸雌二醇Fig 1 HPLC chromatogramsA.system suitability solution;B.test solution;1.impurityⅠ;2.impurityⅡ;3.estradiol cypionate
2.4 不同色谱柱试验
比较了不同牌号的色谱柱对分析的影响,各指标结果见表1。
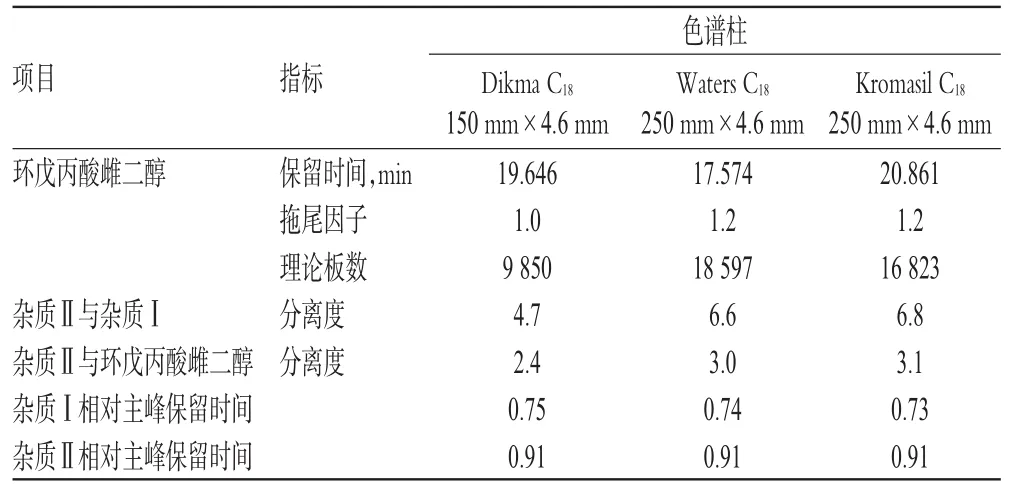
表1 不同色谱柱试验结果Tab 1 Results of tests under different columns
试验结果表明该流动相适用范围较广,选择3种不同牌号的色谱柱均可适用,杂质Ⅱ与环戊丙酸雌二醇的分离度均大于2.0。
2.5 线性关系试验
分别取环戊丙酸雌二醇、杂质Ⅰ与杂质Ⅱ对照品适量,用溶剂稀释成质量浓度分别为0.2、0.5、1.0、1.5、2.0 μg/ml,0.3、0.6、0.9、1.5、2.0 μg/ml,0.5、1.0、2.0、3.0、4.0 μg/ml的系列溶液进行测定,以峰面积(y)为纵坐标、质量浓度(x)为横坐标,计算线性回归方程,见表2。

表2 线性方程结果Tab 2 Linear equation
按最小二乘法以进样量对响应值(峰面积等)进行线性回归,求得两条标准曲线,两曲线斜率之比即为校正因子。杂质Ⅰ相对校正因子为0.970,杂质Ⅱ相对校正因子为0.368。
2.6 耐用性试验
比较了不同流动相组成比例、pH、柱温、流速、检测波长等对测定结果的影响,见表3。
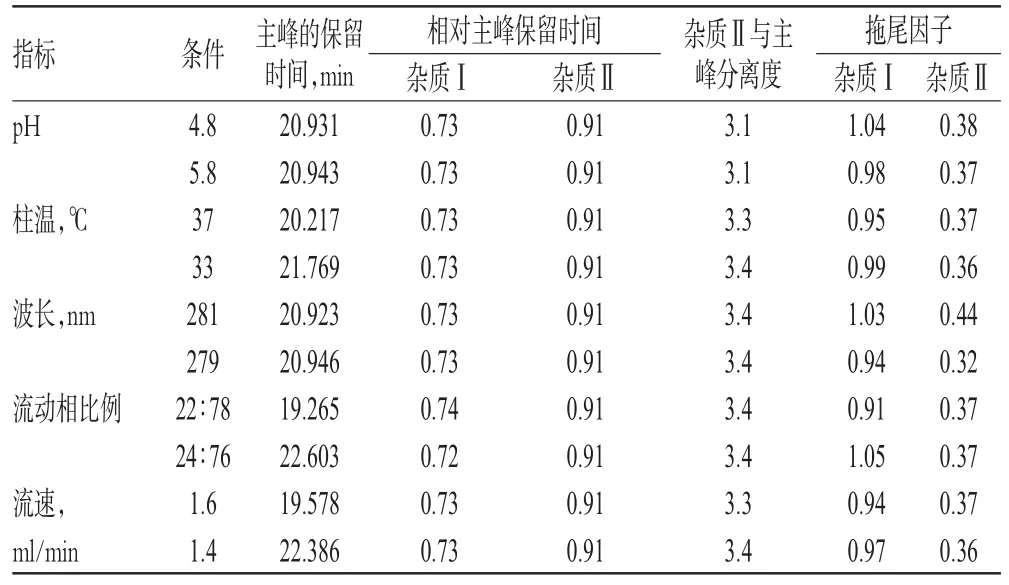
表3 耐用性试验结果Tab 3 Results of durability test
结果显示,杂质Ⅰ与杂质Ⅱ的相对保留时间比较稳定,杂质Ⅱ与环戊丙酸雌二醇的分离良好。计算得杂质Ⅰ的相对响应因子为0.9~1.0,杂质Ⅱ的相对响应因子为0.3~0.4,受参数变化影响较小。拟定标准杂质Ⅰ按不加校正因子的主成分自身对照法计算,以相对主峰的保留时间进行定性;杂质Ⅱ采用杂质对照品外标法进行定量(与加校正因子主成分自身对照法计算的结果一致,见“2.11”项)。
2.7 精密度试验
分别取“2.5”项下环戊丙酸雌二醇(1.0 μg/ml)、杂质Ⅱ(2.0 μg/ml)对照品溶液连续进样6次,环戊丙酸雌二醇、杂质Ⅱ峰面积变化的RSD分别为0.1%、0.4%(n=6)。
取供试品溶液(批号:20110941)连续进样6次,峰面积的RSD为0.2%(n=6)。
2.8 稳定性试验
取供试品溶液(批号:20110941)放置0、8、16、24 h时取样测定,峰面积的RSD为0.5%(n=4)。表明供试品溶液在24 h内稳定。
2.9 杂质Ⅱ测定的准确度试验
分别精密称取环戊丙酸雌二醇原料药(批号:20110941)9份,每份100 mg,置于100 ml量瓶中,精密加入杂质Ⅱ对照品贮备液(20 μg/ml)4、5、6 ml,加溶剂溶解并稀释至刻度,测定高、中、低3种质量浓度的回收率,结果平均值分别为98.86%、99.92%、100.07%,总平均回收率为99.62%,RSD为0.6%(n=9)。
2.10 杂质检测限与定量限试验
取“2.5”项下溶液适量,采用逐步稀释法稀释,当信噪比为3时,杂质Ⅰ、杂质Ⅱ与环戊丙酸雌二醇检测限分别为6.3、1.5、2.3 ng;当信噪比为10时,杂质Ⅰ、杂质Ⅱ与环戊丙酸雌二醇定量限分别为21.0、5.0、7.7 ng。
2.11 样品中有关物质测定结果
量取“2.2”项下供试品溶液、对照溶液、对照品溶液各50 μl,分别注入液相色谱仪,记录色谱图至主峰保留时间的3倍,供试品溶液如有与杂质Ⅱ保留时间一致的色谱峰,按外标法以峰面积计算,不得过0.2%;在相对保留时间为0.7处如有杂质峰(杂质Ⅰ),不得大于对照溶液主峰峰面积的1.5倍(0.15%);其他单个杂质不得大于对照溶液主峰峰面积(0.1%),杂质总量不得过1.0%。供试品溶液中任何小于对照溶液主峰面积0.1倍的峰可忽略不计。3批样品有关物质检查结果见表4。

表4 3批样品有关物质检查结果(%)Tab 4 Results of related substances in 3 batches of samples(%)
3 讨论
(1)本试验中取系统适用性试验溶液进样,用二极管阵列检测器(DAD)检测,环戊丙酸雌二醇、杂质Ⅰ及单个杂质的最大吸收波长为280 nm,杂质Ⅱ的最大吸收波长为263 nm。拟定标准采用280 nm作为检测波长。由于杂质Ⅰ与杂质Ⅱ的相对保留时间重现性较好,杂质Ⅰ与杂质Ⅱ的相对响应因子受参数变化影响较小,故杂质Ⅰ按不加校正因子的主成分自身对照法计算,以相对主峰的保留时间进行定性。杂质Ⅱ采用加校正因子的主成分自身对照法与外标法计算的结果一致,由于杂质Ⅱ易于获得,且经结构确证且纯度大于98.5%,故拟定标准采用杂质对照品外标法进行定量。
(2)笔者曾采用梯度洗脱的方式进行有关物质检查,由于不同的仪器间梯度准确度的差异会导致分离重现性差;而等度洗脱的方式重现性较好,各有关物质间的分离度均>2.0,有关物质的定量准确度也不受影响,因此本试验最终采用等度洗脱的方式。
(3)环戊丙酸雌二醇是以雌酚酮与环戊丙酰氯为起始原料,通过一系列酯化及水解后的终产物。环戊丙酰氯中含有微量环戊乙酰氯,与雌酚酮的反应副产物为杂质Ⅰ,杂质Ⅱ为雌酚酮脱氢物(雌酚酮及雌激素衍生物的合成中使用二氯二氰基苯醌脱氢[4])与环戊丙酰氯的反应副产物。试验发现3批样品中均检出杂质Ⅰ、杂质Ⅱ,但未检出另一已知杂质雌二醇。
[1]雷贞武.新的激素避孕方法:Lunella注射避孕针[J].国际生殖健康/计划生育杂志,2008,27(1):58.
[2]唐彦,朱珠.月用避孕药:复方甲羟孕酮[J].中国药学杂志,2001,36(11):285.
[3]The United States Pharmacopeial Convention.U.S.Pharmacopeia(36)-National Formulary(31)[S].Baltimore:United Book Press,Inc.,2013:3480.
[4]景羽.雌酚酮及雌激素衍生物的合成研究[D].上海:上海师范大学,2010:1-93.
