GP与TP方案治疗晚期老年非小细胞肺癌的临床对比研究
2014-05-18王大志郭成业
王大志 陈 娜 郭成业*
(青岛市市立医院,山东 青岛 266071)
GP与TP方案治疗晚期老年非小细胞肺癌的临床对比研究
王大志 陈 娜 郭成业*
(青岛市市立医院,山东 青岛 266071)
目的采用多中心完全随机方法,观察GP(吉西他滨和顺铂)方案和TP方案(多西他赛联合顺铂)治疗老年晚期非小细胞肺癌的疗效和毒性反应。方法144例晚期NSCLC随机分成GP组和TP组,入组的每例患者接受至少2个周期以上的GP或TP同样方案的化疗,比较两组不同化疗方案的近期疗效和毒性反应,以及1年的生存率。结果GP组CR、PR、SD、PD、总有效率、1年生存率分别为2.5%、37.5%、32.5%、27.5、40%和43.6%。TP组CR、PR、SD、PD、总有效率、1年生存率分别为3.1%、34.4%、37.5%、25%、37.5%和47.5%。二者之间无统计学差异;不良反应以粒细胞减少,消化道反应,口腔黏膜炎为主,对症处理均可恢复或耐受。结论GP和TP两种化疗方案对晚期NSCLC均有较好的临床疗效,化疗毒副反应大致相同且患者有良好的耐受性。故GP和TP两种化疗方案均可作为晚期NSCLC的一线治疗方案。
非小细胞肺癌;GP;TP;老年
近年来,化疗药物的应用范围越来越广。但化疗药物大多都有骨髓抑制作用。紫杉醇联合顺铂(TP)、吉西他滨联合顺铂(GP)两种不同治疗方案是目前应用于临床一线的化疗方案[1-2]。此次研究选取化疗方案中常见的紫杉醇+顺铂、吉西他滨+顺铂两种不同治疗方案。课题组选取青岛大学医学院附属青岛市市立医院、青岛市中心医院和解放军401医院,采用中心完全随机方法,共治疗144例老年NSCLS,现总结如下。
1 对象与方法
1.1 病例选择及一般资料
采用中心完全随机方法,144例经病理组织学及细胞学证实为初治晚期非小细胞肺癌患者,分为吉西他滨联合顺铂组和多西紫杉醇联合顺铂组。吉西他滨联合顺铂组共72例,其中39例男性患者,33例女性患者;年龄均>65岁,中位年龄77.1岁;41例ⅢB期患者,31例Ⅳ期患者。多西紫杉醇联合顺铂组共72例,其中40例男性患者,32例女性患者;年龄均>65岁,中位年龄74.3岁;39例ⅢB期患者,33例Ⅳ期患者。以上基础临床资料在两组间,不存在统计学差异。所有患者不存在化疗禁忌证。评价近期疗效的主要客观观察指标为X线或CT,患者均具备观察条件。心电图、肝肾功能及血常规在化疗前均正常。随访方式为门诊或电话。
1.2 治疗方法
吉西他滨联合顺铂方案:顺铂30 mg/m2静滴,D1~3;吉西他滨1 g/m2静滴,D1、8。多西紫杉醇联合顺铂方案:顺铂25 mg/m2,静滴,D1~3,多西紫杉醇60 mg/m2,D1,8。以上方案均21 d为1个周期,2~4周期化疗后,进行疗效评价。
1.3 疗效评价
分为完全缓解(CR),部分缓解(PR),稳定(SD)和进展(PD),依照实体瘤疗效评价(RECIST)标准进行。
1.4 统计学方法
采用SPSS12.0统计软件包进行数据分析,χ2和t检验,P<0.05具有统计学差异。
2 结 果
2.1 疗效
GP组,CR、PR、SD、PD、总有效率、1年生存率分别为2.5%、37.5%、32.5%、27.5、40%和43.6%。TP组:CR、PR、SD、PD、总有效率、1年生存率分别为3.1%、34.4%、37.5%、25%、37.5%和47.5%。二者之间无统计学差异。见表1。
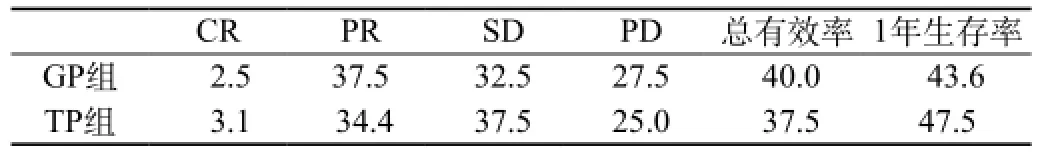
表1 两组的两组疗效的比较(%)
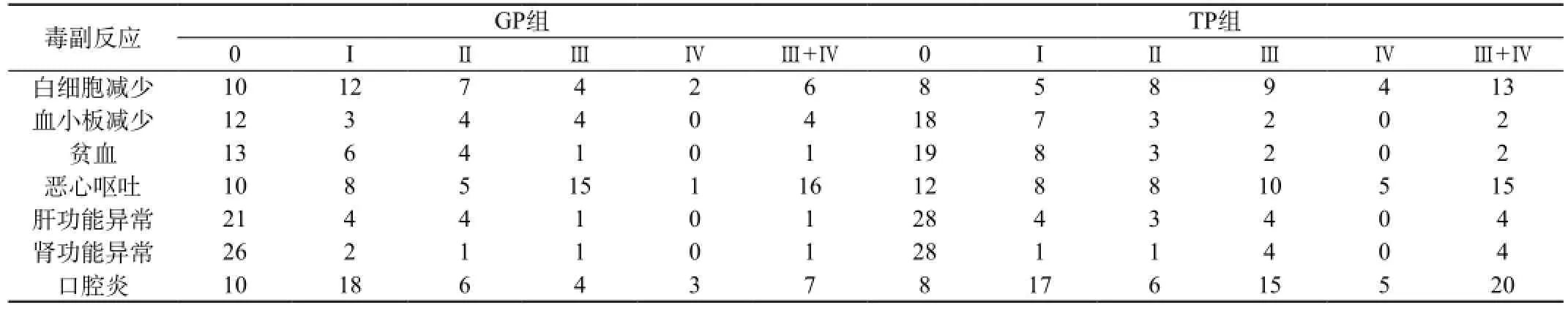
表2 两组患者不良反应比较(例)
2.2 不良反应
主要不良反应(Ⅲ~Ⅳ)度为:GP组:6例(7.5%)粒细胞减少,16例(15%)消化道反应,7例(17.5%)口腔炎,1例肾功能异常(1.4%);TP组:分别为13例 (40.6%),15例(46.9%) ,4例(5.6%),20例(62.5%),两组之间对比差异无显著性(P>0.05)。见表2。
3 讨 论
恶性肿瘤是一种严重危害人体健康的疾病,它是由于身体内细胞发生突变后不断分裂,不受身体控制,进而形成的。近年来,随着生活水平的提高、生活方式的转变和生活环境的改变,恶性肿瘤越来越成为临床的常见病和多发病。根据肿瘤的种类、性质和发展趋向,有计划、合理的综合应用现有的几种治疗手段,以期较大程度的提高治愈率,已经受到广泛的重视,使许多较晚期患者的疗效和生活治疗得到提高[3-4]。肺癌是临床最常见的恶性肿瘤。临床治疗恶性肿瘤的方式有多种,如化疗、手术、放疗等,化疗本身已经从姑息治疗向根治过度,在治疗中越来越占有重要的地位,同时由于其治疗时的方便和合理的价位成为其中最普遍和最重要的一种。
顺铂又称顺氯氨铂,作用类似于烷化剂,将氯解离后,二价的铂与DNA链上的碱基形成交叉联结。它能杀灭细胞周期中各期的细胞,抑制DNA的生物合成。顺铂抗癌普较广,对睾丸、卵巢和膀胱的疗效明显,也用于头颈部癌和其他实体癌症,常与其他抗癌药物如紫杉醇等合用。主要不良反应是恶心、呕吐,他对骨髓抑制的作用弱。
多西他赛能促进细胞微管蛋白的形成,它特异性的与微管的β-微管蛋白结合,拮抗β-微管蛋白的解聚,使细胞出现成束的微管和从微管产生的结构的畸变,最终导致有丝分裂的停止[5]。它使细胞发育停止与G2期和死状分裂期,广泛应用于治疗乳腺、肺、胃、食管、头颈部等处的癌症。其主要副作用为对骨髓的抑制、中性白细胞的减少、周围神经病变、肌肉痛等。短时间内静脉滴注也可产生过敏反应、心动过缓等不适症状[6]。
吉西他滨作为一种前药在细胞内是脱氧胸苷激酶磷酸化的良好底物,在酶的作用下转化成下列代谢物:吉西他滨一磷酸盐(dFdCMP)、吉西他滨二磷酸盐(dFdCDP)和吉西他滨三磷酸盐(dFdCTP),其中dFdCDP和dFdCTP为活性产物。dFdCDP抑制核糖核苷酸还原酶,从而减少了DNA合成和修复所需的脱氧核苷酸的量(尤其是dCTP),低水平的 dCTP逆转了脱氧胞苷激酶正常的负反馈抑制,导致 dFdCTP更多的积聚。同时dFdCDP抑制了 dCTP诱导的脱氧胞苷脱氨酶对 dFdCMP的脱氨作用,且 dFdCTP直接抑制脱氧胞苷脱氨酶,从而使更多的dFdCMP转化成活性代谢物dFdCDP、dFdCTP,而 dFdCTP则与 dCTP竞争结合进入DNA链,插入至 DNA链中脱氧胞苷的位点,并允许鸟苷与其配对,吉西他滨分子就被此鸟苷“掩蔽”,使其免受核糖核酸外切酶的移除修复,然后 DNA 链合成停止,进而DNA断裂,细胞死亡。吉西他滨主要应用于非小细胞肺癌、胰腺癌、膀胱癌、乳腺癌及其他实体肿瘤。主要不良反应是对骨髓的抑制、恶心、呕吐、肾脏毒性和过敏等[7-8]。本组应用吉西他滨联合顺铂和多西紫杉醇联合顺铂不同方案治疗144例患者,研究结果表明:两组有效率相近,统计学分析无明显差异,所以吉西他滨联合顺铂和多西紫杉醇联合顺铂不同方案治疗效果疗效相近。不良反应方面:本组Ⅲ~Ⅳ度不良反应主要表现在粒细胞减少,消化道反应和口腔黏膜炎三方面,全组无治疗相关性死亡事件发生,提示患者的耐受性良好,但吉西他滨联合顺铂组的不良反应较多西紫杉醇联合顺铂组的为轻,但两组比较无显著性差异。
[1] Stein WD.Functional implications of genetic polymorphisms in the multidrug resistance gene MDR1 (ABCB1)[J].Pharm Res, 2004,21(6):904-913.
[2] Homolya L.Multidrug resistance-associated proteins: Export pumps for conjugates with glutathione,glucuronate or sulfate[J]. Biofactors,2003,17(1/4):103-114.
[3] Sawicka M.A review of selected anti-tumour therapeutic agents and reasons for multidrug resistance occurrence[J].J Pharm Pharmacol, 2004,56(9):1067-1081.
[4] 廖子君.现代肿瘤治疗药物学[M].北京:世界图书出版社,2002.
[5] Pauli-Magnus C.Functional implications of genetic polymorphisms in the multidrug resistance gene MDR1 (ABCB1) [J].Pharm Res,2004,21(6):904-913.
[6] Klepstad P,Dale O,Kaasa S,et al.Inf l uences on serum concentrations of morphine,M6G and M3G during routine clinical drug monitoring: a prospective survey in 300 adult cancer patients[J]. Acta Anaesthesiol Scand,2003,47(6):725-731.
[7] McRee D.Protecting against cocaine,heroin,and sarin gas[J].Chem Biol,2003,10(3):295-297.
[8] Golembiewski JA.Morphine and hydromorphone for postoperative analgesia: focus on safety[J].J Perianesth Nurs,2003,18(2):120-122.
R734.2
B
1671-8194(2014)21-0134-03
*通讯作者
