利巴韦林纯度标准物质的定值及不确定度评估研究*
2014-05-15杜慧邢逞史永强杜冠华吕扬
杜慧,邢逞,史永强,杜冠华,吕扬,
(1.北京协和医学院、中国医学科学院药物研究所晶型药物北京市重点实验室,北京 100050;2.山东省晶型药物重点实验室,滕州 277500;3.北京协和医学院、中国医学科学院药物研究所药物靶点研究与新药筛选北京市重点实验室,北京 100050)
利巴韦林纯度标准物质的定值及不确定度评估研究*
杜慧1,邢逞1,史永强2,杜冠华3,吕扬1,2
(1.北京协和医学院、中国医学科学院药物研究所晶型药物北京市重点实验室,北京 100050;2.山东省晶型药物重点实验室,滕州 277500;3.北京协和医学院、中国医学科学院药物研究所药物靶点研究与新药筛选北京市重点实验室,北京 100050)
目的 以利巴韦林为研究对象,研制具有可溯源和量值传递功能的国家级计量有证标准物质,并建立有效定值分析方法。方法采用差示扫描量热法(DSC)对利巴韦林纯度标准物质进行均匀性和稳定性检验;采用DSC和高效液相色谱(HPLC)法中两种不同原理方法联合定值,建立不确定度评估的数学模型。结果利巴韦林纯度标准物质具有良好的均匀性和稳定性,纯度标准值和不确定度值为(99.5±0.4)%(k=2,P=0.95)。结论研制的利巴韦林纯度标准物质属国家一级有证计量标准物质(GBW09587),该标准物质可作为量值溯源与量值传递的计量器具,其研究结果可为我国药品质量控制提供标准物质、物质标准与标准方法,实现与国际接轨目标。
利巴韦林;纯度标准物质;量热法,差示扫描;色谱法,高效液相
利巴韦林是广谱强效的抗病毒核苷类药物,临床主要用于病毒性感冒、麻疹、带状疱疹以及与干扰素合并用于各型肝炎的治疗[1-4]。有证标准物质(certified referencematerial,CRM)是采用计量学上有效程序对其一种或多种特性定值,并附有提供特性值的不确定度和计量学溯源性描述证书的标准物质[5-7]。CRM在分析测量过程中提供测量参考标准,使得其在不同时间、不同实验室,由不同人员开展的相同内容的测量结果具有可比性[8]。目前,有证标准物质主要分布在工业材料、有色金属等领域,而在生物医药领域分布比较少,因此,研制医药领域的有证标准物质具有重大意义[9]。笔者依据我国一级标准物质研制技术规范和国家计量相关法规要求[10-11],研制利巴韦林纯度有证标准物质,并对其进行均匀性、稳定性检验、定值及不确定度评估研究,为有效实施产品质量检测提供了国家级的标准物质、物质标准及标准检测分析方法。
1 仪器与材料
1.1 仪器与条件
1.1.1 差示扫描量热法(differential scanning calorimetry,DSC)Mettler Toledo DSC-1型差示扫描量热仪。采用标准40μL氧化铝(Al2O3)坩埚;升温速率为5.0 K·min-1;升温区间为130~180℃;称样量为1.5~3.5 mg;炉内气体为静态空气。
1.1.2 高效液相色谱法(high performance liquid chromatography,HPLC)Agilent1260型高效液相色谱仪,DAD检测器。采用Agilent Eclipse XDB-C18(250 mm×4.6 mm,5μm)色谱柱;流动相为水(稀硫酸调pH2.53)100%;检测波长:207 nm;柱温:30℃;流速:1.0mL·min-1;进样量10μL。卡尔·费休滴定仪:Mettler Toledo V20型。SX2.5-10型箱式电阻炉:上海树立仪器仪表有限公司。气相色谱仪:Agilent 7890A型。
1.2 溶剂与试剂 利巴韦林原料购于山东益康药业股份有限公司(批号:090225);铟标准物质[GBW13202,国家标准物质研究中心,熔点(429.75± 0.01)K];注射用双蒸水,经Millipore制备,过孔径0.2μm微孔滤膜;甲醇、乙醇均为色谱级;卡尔·费休滴定液(J.T.Baker公司)。
1.3 利巴韦林纯度标准物质制备 取利巴韦林原料50 g,加入乙醇500 mL加热至溶解,趁热过滤,室温放置24 h,至固体析出完全后,过滤,置于60℃减压干燥24 h,即得利巴韦林高纯度样品,呈白色粉末。采用HPLC对纯化前后的利巴韦林样品进行分析,结果表明经过重结晶纯化制备工艺后,由将原来98.0%化学纯度提高到纯度>99.0%。将纯化后的利巴韦林高纯度样品经制粒、均匀混样后,采用2 mL棕色安瓿瓶密封包装,最小包装量为50 mg,共计制备获得利巴韦林纯度标准物质样品500瓶。
2 方法与结果
2.1 方法学研究
2.1.1 DSC法
2.1.1.1 线性关系考察 精密称取6份1.5~3.5 mg利巴韦林纯度标准物质,称样量分别为1.50,1.72, 2.16,2.51,3.01,3.52 mg,置于40μL的标准Al2O3坩埚中,压盖,备用。利用DSC仪进行测量,记录吸热面积值。以样品质量为横坐标,吸热面积值为纵坐标,绘制标准曲线。在1.5~3.5 mg质量范围内,回归线性方程为:Y=192.672 7X-5.993 3,相关系数R2为0.999 3(n=6),表明利用DSC法获得的利巴韦林纯度标准物质的质量与吸热面积值间呈现良好的线性关系,该法可作为其纯度定值检测分析方法。
2.1.1.2 方法精密度 随机抽取利巴韦林纯度标准物质样品6瓶,并分别精密称取2.50 mg,置于40μL的标准Al2O3坩埚中,压盖,备用。利用DSC仪进行测量,记录吸热面积值。6次测量吸热面积与称样量的比值分别为192.42,194.87,187.67,192.48,187.57, 191.88,RSD值为1.53%,表明建立的DSC法具有良好的方法精密度。
2.1.2 HPLC法
2.1.2.1 线性关系考察 随机抽取利巴韦林纯度标准物质样品1瓶,并精密称取25.01 mg,用流动相将样品完全溶解并定容至25mL量瓶中,摇匀,配制成浓度为1 000.40μg·mL-1的储备液。精密移取5份0.1, 0.5,1.0,2.0,5.0 mL储备液,用流动相定容至10 mL量瓶中,配制成系列浓度分别为10.00,50.02, 100.04,200.08,500.20,1 000.40μg·mL-1的标准溶液。分别精密移取各浓度标准溶液10μL注入液相色谱仪,重复进样3次,记录色谱峰面积。以浓度值为横坐标,以峰面积均值为纵坐标,绘制标准曲线。在10.00~1 000.40μg·mL-1浓度范围内,回归线性方程为:Y=25.43X+41.387,相关系数R2为0.999 8(n= 6),表明利用HPLC法建立的利巴韦林纯度标准物质的浓度值与吸收峰面积值之间呈现良好的线性关系,该法可作为其纯度定值检测分析方法。
2.1.2.2 仪器精密度 随机抽取利巴韦林纯度标准物质样品1瓶,并精密称取12.50 mg,用流动相将样品完全溶解定容至25 m L量瓶中,摇匀,配制成浓度为500.0μg·mL-1的溶液。精密移取10μL注入液相色谱仪,重复进样6次,记录色谱峰面积分别为13 008.9,13 007.4,13 019.6,13 020.8,12 998.2, 13 003.1,RSD值为0.07%,表明建立的HPLC法具有良好的仪器精密度。
2.1.2.3 方法精密度 随机抽取利巴韦林纯度标准物质样品6瓶,并精密称取12.50 mg,用流动相将样品完全溶解定容至25 m L量瓶中,摇匀,配制成浓度为500.0μg·mL-1的溶液。精密移取10μL注入液相色谱仪,重复进样3次,记录色谱峰面积值。6份样品峰面积均值与称样量的比值分别为1 040.3,1 041.2, 1 040.1,1 043.5,1 042.8,1 051.9,RSD值为0.42%,表明建立的HPLC法具有良好的方法精密度。
2.2 均匀性与稳定性检验
2.2.1 均匀性检验 从500瓶利巴韦林纯度标准物质中随机抽取15瓶,每瓶取样3次,采用DSC法,以样品纯度值为特性量参数进行瓶内均匀性检查。计算每一瓶3个数据的平均值,共获得15个平均值,以15个平均值为一组数据,进行瓶间均匀性检查。利巴韦林纯度标准物质均匀性的检验数据见表1。
对检测数据进行F检验,计算F值为1.44,查F检验临界值表得F0.05(14,30)=2.04,即F<F0.05(14,30)。结果表明,利巴韦林纯度标准物质具有良好的均匀性。
2.2.2 稳定性检验 采用DSC法对利巴韦林纯度标准物质进行短期与长期稳定性考察。短期稳定性包装样品经过高温(60℃)、高湿(90%±5%,25℃)、光照[照度(4 500±500)lx]分别于0,7,14 d取样考察其纯度值变化情况。每个时间点随机抽取3瓶样品,每瓶测定1次;长期稳定性将是标准物质样品放置在常温下保存,并分别于0,1,2,4,6,12个月取样进行纯度检测。每个时间点随机抽取6瓶样品,每瓶测定1次。表2与表3分别给出利巴韦林纯度标准物质短期稳定性与长期稳定性考察检测数据。

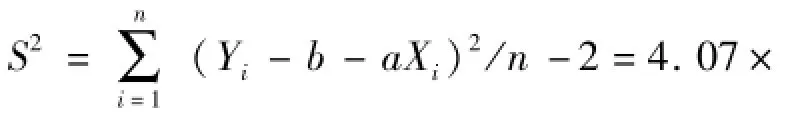

表1 利巴韦林纯度标准物质均匀性的检验数据Tab.1 Resu lts of hom ogeneity test on purity certified referencematerial of ribavirin

表2 利巴韦林纯度标准物质的短期稳定性检测数据Tab.2 Results of short-term stability test on purity cer tified referencematerial of ribavirin
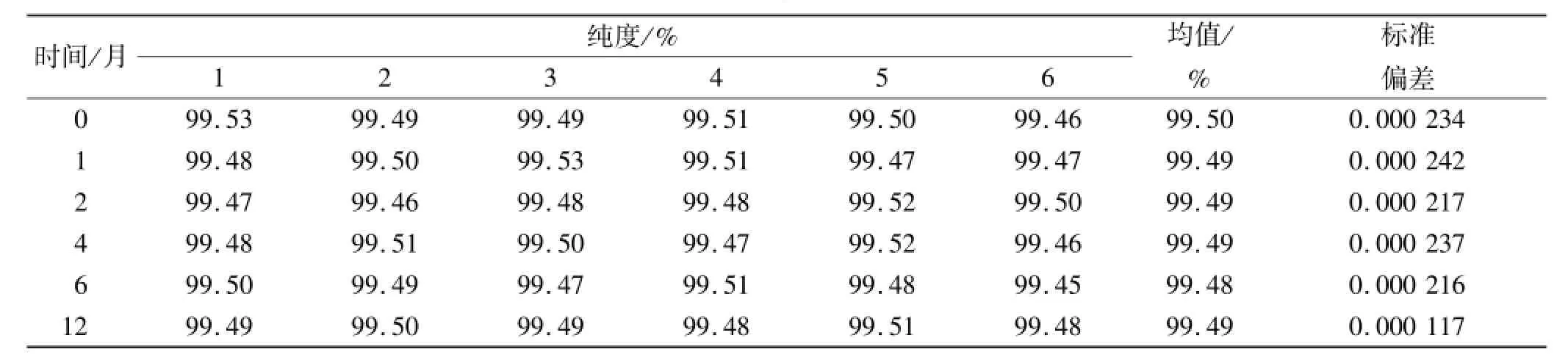
表3 利巴韦林纯度标准物质的长期稳定性检测数据Tab.3 Results of long-term stability test on purity certified referencematerial of ribavirin
2.3 纯度标准值定值
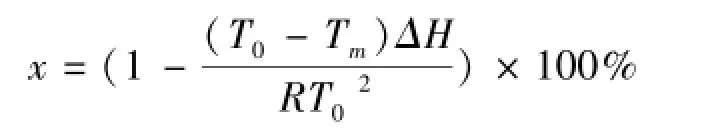
T0表示理想中的纯物质熔点值(凝固点),单位用K表示。Tm表示物质的真实熔点值(凝固点),单位用K表示。R表示气体常数,8.314 J·K-1·mol-1。χ表示纯物质的摩尔百分比。△H表示物质的摩尔熔融焓变值,单位用J·mol-1表示。T0-Tm表示物质纯度值因各种杂质成分存在而导致的熔点值下降量。
随机抽取利巴韦林纯度标准物质样品10瓶,分别精密称取样品量为1.5~3.5 mg置于40μL的标准Al2O3坩埚中,压盖,备用。记录图谱并计算纯度值,纯度定值数据见表4。
对10个数据采用格拉布斯检验以剔除可疑值,经计算G=1.631。查格拉布斯临界值表知:G0.95(10)= 2.176。因G<G0.95(10),故10个数据中无可疑值存在。将通过格拉布斯检验的10个纯度值取平均值作为其纯度标准值。故DSC法获得的利巴韦林纯度标准物质的纯度标准值为99.49%。
2.3.2 HPLC法 应用高效液相色谱面积归一化法进行标准物质的纯度测定,其原理是将特定色谱条件下,经液相分离、检测得到的所有色谱峰的峰面积视为100%,将被测化合物色谱峰所占的百分比作为该标准物质候选物的纯度值。
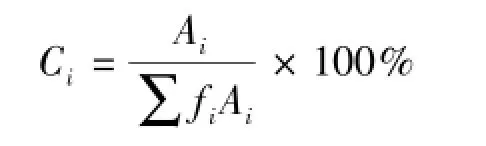
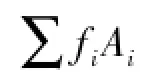
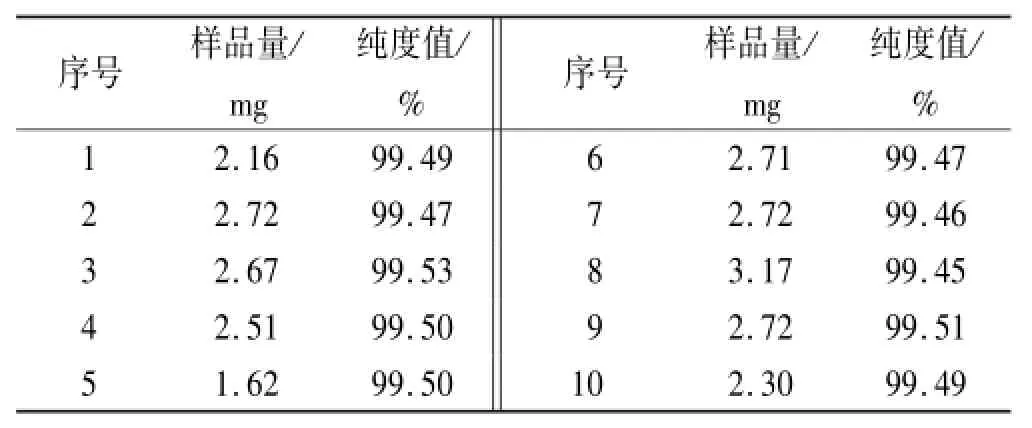
表4 DSC法利巴韦林纯度标准物质的纯度定值数据Tab.4 Determ ination results of purity certified reference material of ribavirin by DSC methods
随机抽取利巴韦林纯度标准物质样品10瓶,分别精密称取12.50 mg,用流动相将样品完全溶解定容至25 mL量瓶中,摇匀,制成浓度500μg·mL-1溶液。精密移取10μL注入液相色谱仪,每瓶测定3次,记录色谱峰面积,定值数据见表5。
对10个数据采用格拉布斯检验剔除可疑值,经计算得G=1.461。查格拉布斯临界值表知:G0.95(10)= 2.176。因G<G0.95(10),故10个数据中无可疑值存在。将通过格拉布斯检验的10个纯度值取平均值作为其纯度标准值。故HPLC法获得的利巴韦林纯度标准物质的纯度标准值为99.72%。
考虑到由于HPLC法面积归一化定量分析方法学的局限性,样品中的水分、炽灼残渣和残留溶剂在HPLC法中无法检测。笔者采用卡尔·费休法测定利巴韦林纯度标准物质中的水分值为0.188 1%,炽灼残渣采用《中华人民共和国药典》附录炽灼残渣检查法测定结果为0.037 6%,采用气相色谱法测定溶剂残留值为0.024 5%,总杂质成分含量为0.250 2%。
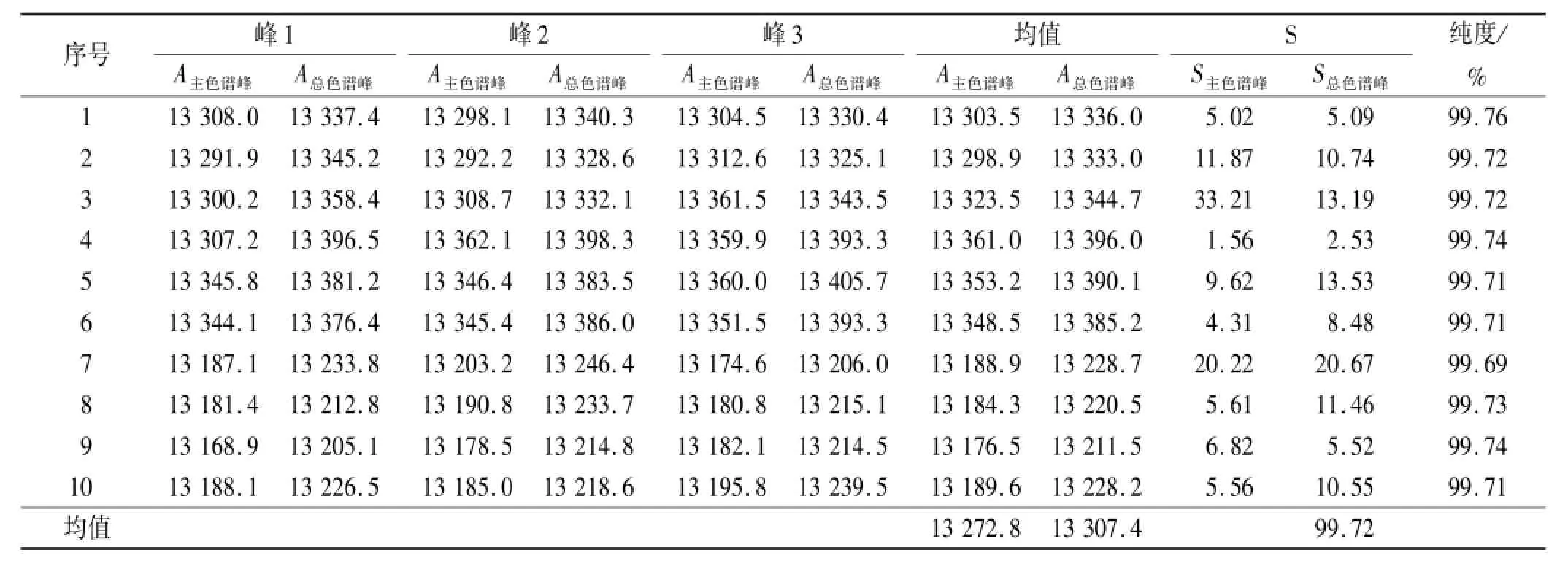
表5 HPLC法利巴韦林纯度标准物质的纯度定值数据Tab.5 Determ ination results of purity certified referencem aterial of ribavirin by HPLC methods
利巴韦林纯度标准物质的实际纯度值为99.72%× (100%-0.250 2%)=99.47%。
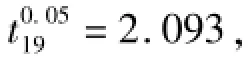
利巴韦林纯度标准物质的纯度标准值联合定值= (99.47%+99.49%)/2=99.48%。
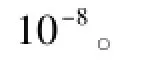

2.4.3 DSC法产生的不确定定度 DSC法的合成标准不确定度评定结果见表6。
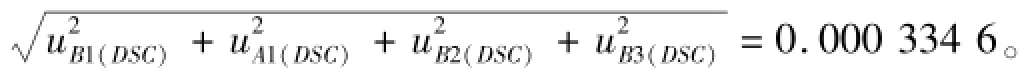
2.4.4 HPLC法产生的不确定度 HPLC法的合成不确定度由色谱峰面积不确定度、水分不确定度、炽灼残渣不确定度和残留溶剂的不确定度组成。
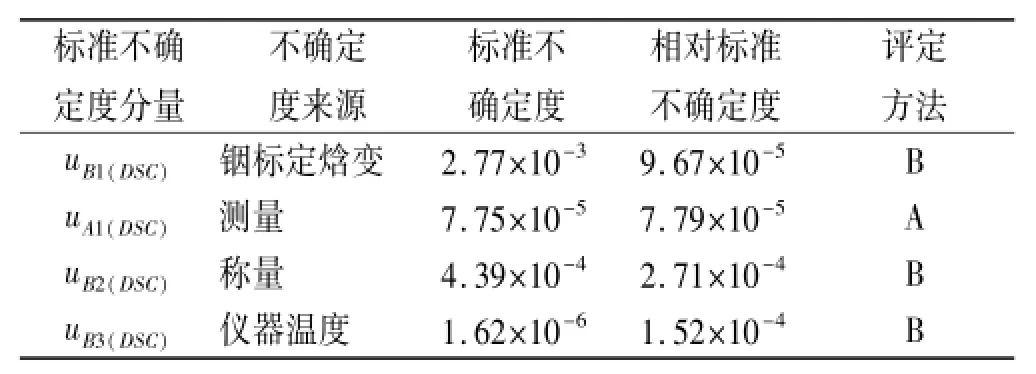
表6 DSC法的合成标准不确定度评定结果Tab.6 Combined standand uncertainty results of DSC method

HPLC法的合成不确定度;

2.4.7 扩展不确定度 当不确定度分布为均匀分布且置信概率为0.95时,包含因子k=2,其扩展不确定度U=kuc(总)=0.003 12。
2.5 利巴韦林纯度标准值及不确定度值 通过利巴韦林纯度的定值和不确定度评价,最终获得该标准物质的定值结果及不确定度值:99.5%±0.4%,k=2,P= 0.95。
3 讨论
本文研制的利巴韦林纯度标准物质尚属首次,填补我国该标准物质品种的空白,该标准物质已经获得国家标准物质管理委员会评审和国家质检总局批准,并获得国家一级标准物质(GBW 09587)证书和计量器具生产许可证。
目前文献报道利巴韦林纯度测定方法有HPLC法[12-14]、高效毛细管电泳法[15]、紫外分光光度法[16]等,尚未见关于DSC法的报道。HPLC法具有应用广泛、快速、专属性强等优点,是一种常用分析方法,但无法检测到无机物、残留溶剂、水分等物质成分,笔者在纯度标准物质定值时采用扣除法,克服因HPLC法缺陷而造成定值结果的不准确问题。DSC法具有样品量少、快速高效、检测方法准确度高以及检测结果重现性好等特点。笔者首次利用DSC法进行利巴韦林纯度测定,为高纯度化学物质的纯度检测提供了一种新的检测技术和分析方法。
笔者采用DSC和HPLC两种不同原理的检测方法联合定值,建立不确定度评估数学模型,为标准物质研制提供了技术支撑,保证了标准物质定值结果的科学性和准确性。
[1] VINCENT M,ELISABETH N,PHIIPPE S.Brief communication:case reports of ribavirin treatment for chronic hepatitis E[J].Ann Int Med,2010,153(2):85-89.
[2] REICHARD O,ANDERSON J,SCHVARCZ R,et al.Ribavirin treatment for chronic hepatitis C[J].Lancet,1991,337 (8749):1058-1061.
[3] GARNIER J L,CHEVALLIER P,DUBERNARD JM,et al. Treatment of hepatitis C virus infection with ribavirin in kidney transplant patients[J].Transplant Proc,1997,29 (1):783.
[4] FONTINE H,VALLET A,SELVES J,et al.Histopathologic efficacy of ribavirin monotherapy in kidney allograft recipients with chronic hepatitis C[J].Transplantation, 2004,78(6):853-857.
[5] 国际标准化组织.ISO Guide 34[S].2009.
[6] 国际标准化组织.ISO Guide 35[S].2006.
[7] National Institute of Standards and Technology[OL].http://www.nist.gov/srm/index.cfm.
[8] DUEWER D L,LIPPA K A,LONG SE,etal.Demonstrating the comparability of certified reference materials[J].Anal Bioanal Chem,2009,395(1):155-169.
[9] COMAR[DB].http://www.comar.bam.de/en/.
[10] 国家计量局.中华人民共和国计量法[M].北京:法律出版社,1985.
[11] 国家质量技术监督局.中华人民共和国一级标准物质研制技术规范[S].JJF,1006-1994.
[12] ARIANNA L,MARIA C S,SILVANA P.Measurement of ribavirin and evaluation of its stability in human plasma by high performance liquid chromatography with UV detection [J].J Chromatogr B,2007,856(1-2):358-364.
[13] ELISA Z,TERESA G,BARBARA L,et al.Development of a rapid LC-MS/MS method ro ribavirin determ ination in rat brain[J].J Pharm Biomed Anal,2011,54(4):889-892.
[14] LIU Y,XU C,YAN R.Sensitive and specific LC-MS/MS method for the simultaneous measurements of viramidine and ribavirin in human plasma[J].J Chromatogr B,2006, 832(1):17-23.
[15] MICHAEL C B,REGULA T.Determ iantion of ribavirin in human serum and plasma by capillary electrophoresis[J]. Electrophoresis,2004,25(10-11):1615-1622.
[16] 齐利.紫外光谱法和高效液相色谱法测定利巴韦林片含量的比较[J].医学信息,2010,23(8):195-196.
DOI 10.3870/yydb.2014.06.026
Purity Determ ination and Uncertainty Evaluation of Ribavirin Purity Reference Material
DU Hui1,XING Cheng1,SHI Yong-qiang2,DU Guan-hua3,LV Yang1,2
(1.Beijing City Key Laboratory of Pharmaceutical Polymorph,Institute of Materia Medica,Chinese Academy of Medical Sciences&Peking Union Medical College,Beijing 100050,China;2.Shandong Province Key Laboratory of Pharmaceutical Polymorph, Tengzhou 277500,China;3.Beijing City Key Laboratory of Drug Identification and Drug Screening,Institute of Materia Medica,Chinese Academy of Medical Sciences&Peking Union Medical College,Beijing 100050,China)
ObjectiveTo develop the ribavirin purity certified reference material(CRM)which has measurement traceability and high accuracy,and establish an effective method of evaluation.MethodsThe homogeneity and the stability were checked by differential scanning calorimetry(DSC).High performance liquid chromatography(HPLC)and DSC methods were used for purity determination of ribavirin.ResultsRibavirin showed satisfactory homogeneity and stability.The certified value of ribavirin was99.5%with an uncertainty of 0.4%(k=2,P=0.95).ConclusionRibavirin purity CRM obtained in this paper has been proven to be a national primary CRM with high accuracy and traceability,which can be used to validate analyticalmethods,improve the accuracy of measurement data,establishmeteorological traceability of analytical results as well as control the quality of ribavirin in the pharmaceutical industry.
Ribavirin;Purity certified reference material;Calorimetry,differential scanning;Chromatography,high performance liquid
R978.7;R927.1
A
1004-0781(2014)06-0779-06
2013-11-01
2013-12-31
*重大新药创制十二五规划项目(2012ZX09301002-001-013,2013ZX09102110);卫生部行业基金资助项目(200902008)
杜慧(1987-),女,内蒙古包头人,在读硕士,研究方向:药物分析。电话:010-63030566,E-mail:cong200767@163.com。
吕扬(1959-),女,北京人,研究员,博士生导师,从事药物分析研究。电话:010-63165212,E-mail:luy@imm.ac.cn。
杜冠华(1956-),男,山东滕州人,研究员,博士生导师,从事药物发现、高通量药物筛选、神经药理学和心脑血管药理学研究。电话:010-63165184,E-mail:dugh@imm.ac.cn。
