重复引物PCR技术在超大片段动态突变疾病基因检测中的应用
2014-05-10陈晟吴志英
陈晟,吴志英
1.福建医科大学附属第一医院神经内科,福州 350005;
2.复旦大学附属华山医院神经内科,上海 200040
动态突变疾病是指基因编码区或非编码区发生核苷酸重复序列异常扩增导致的一类遗传性疾病,根据其发生扩增的分子生物学机制不同,大致可分为三类:第一类是异常扩增引起转录过程受阻,如脆性X综合征(Fragile X syndrome, FXS)、Friedreich共济失调(Friedreich ataxia, FRDA)等;第二类是异常扩增导致病理性RNA毒性蓄积,如强直性肌营养不良症症1型(Myotonic dystrophy 1, DM1)、脊髓小脑性共济失调10型(Spinocerebellar ataxia 10, SCA10)等;以上两类均为非编码区重复序列异常扩增。第三类为编码区核苷酸重复序列异常扩增,如较为常见的脊髓小脑性共济失调3型(Spinocerebellar ataxia 3, SCA3)、亨廷顿舞蹈病(Huntington's disease, HD)和肯尼迪病(Kennedy disease, KD)等,因其为CAG三核甘酸重复序列异常扩增,所以又称为多聚谷氨酰胺疾病(Polyglutamine disease),简称polyQ疾病[1]。目前已知的PolyQ疾病共有9种,分别为HD、KD及7种SCA,这9种PolyQ疾病的CAG重复序列异常扩增一般不超过100次,可以通过普通PCR进行扩增,结合凝胶电泳或毛细管电泳片段分析进行检测。而对于第一类和第二类涉及非编码区重复序列异常扩增的动态突变疾病,其重复序列扩增次数常常超过100次,甚至达到1000次以上,对于这些超大片段动态突变疾病,普通PCR扩增无法检测出超大片段,而传统检测方法如Southern blot费时费力,且需要高质量的DNA标本,很难推广应用于临床。在此情况下,重复引物PCR技术(Repeat-primed PCR assay)应运而生,首先用于DM1的基因诊断,并陆续用于强直性肌营养不良症2型(Myotonic dystrophy 2, DM2)、FRDA、SCA10型以及C9orf72基因突变引起的额颞叶痴呆(Frontotemporal dementia,FTD)或肌萎缩侧索硬化(Amyotrophic lateral sclerosis, ALS)合并额颞叶痴呆(ALS-FTD)等疾病的基因检测。本文将简要介绍重复引物PCR技术的原理并分别阐述重复引物PCR技术在上述疾病基因检测中的应用进展。
1 重复引物PCR技术原理
重复引物 PCR技术最初称为三引物 PCR法(Triplet repeat-primed PCR, TP-PCR)。1996年,Warner等[2]发明此种方法用以诊断DM1超大片段动态突变患者。TP-PCR法有别于传统PCR,其反应中加入3个引物,分别为荧光标记的上游引物P1、与人类无同源性的21个碱基组成的通用引物P3以及由5个CAG重复加上通用引物P3(又称tail,P3尾)组成的引物 P4,3个引物以一定比例加入反应体系,具体反应过程为:引物P1与P4首先扩增出长度相差3 bp的一组PCR产物,这些产物随后被引物P1和P3再次扩增,到了循环晚期,由于加入体系的量少,引物P4首先被耗尽,保证了循环早期产生的相差3 bp的PCR产物能够充分扩增,最后采用荧光毛细管电泳检测PCR终产物,此法实际上是扩增并检测了一组相差1个CTG重复的小片段(图1)[2]。
2 重复引物 PCR技术与其他超大片段动态突变基因检测技术比较
除重复引物PCR技术外,Southern blot杂交[3]、长模板PCR扩增TM法[4]、实时荧光定量PCR联合微卫星标记连锁分析法[5]等也可用于超大片段动态突变基因检测。与重复引物PCR技术相比,这些方法各有利弊(表1)。

图1 TP-PCR技术原理示意图
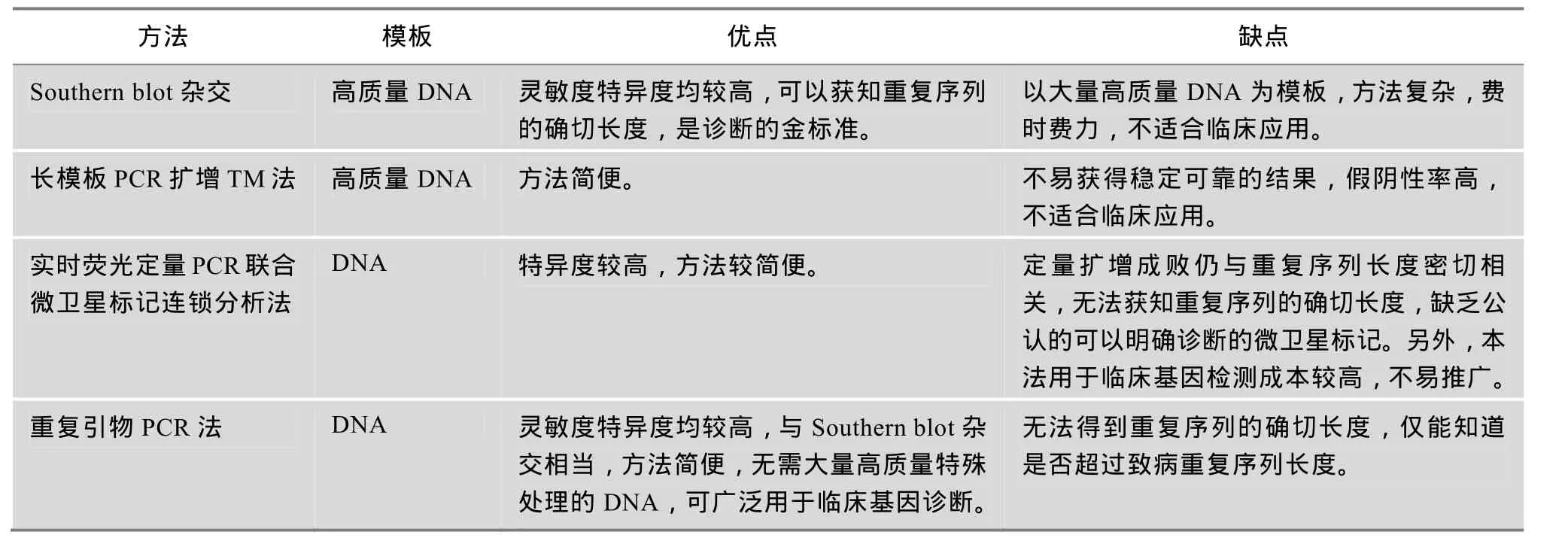
表1 几种超大片段动态突变疾病基因检测技术比较
3 重复引物PCR技术在DM1和DM2中的应用
DM 是一种累及全身多系统的常染色体显性遗传病,发病率约为 1/8000[6],根据致病基因及其临床表现,可分为两型:DM1和DM2,国内常见DM1,而芬兰、德国等国家和地区 DM2相对较为常见。DM 临床表现多种多样,除了肌无力、肌强直和彩虹样白内障为3大主要临床表现外,还可累及心脏、内分泌腺体、中枢神经系统等。
DM1为DMPK基因3′非翻译区的CTG三核甘酸重复异常扩增而致病,正常人该区域CTG重复一般为5~37次[7],重复次数38~50次为前突变,重复次数50~100次者患病,但症状轻微,重复次数100次以上患者出现明显症状[8],部分患者重复次数可多达数千次。Warner等[2]利用TP-PCR法检测出76名DM1患者,而以传统的Southern blot检测有1例患者未被检出异常扩增,其原因可能是Southern blot检测本身对样品质量要求较高,且杂交过程不稳定,因此TP-PCR法用于检测DM1灵敏度与特异度均较高。然而,该方法也并非万无一失。近年有文献报道,约5%异常扩增序列可能存在CCG、CTC和GGC等干扰序列,这些干扰序列将影响引物与序列的结合,导致假阴性结果出现[9]。针对此情况,Radvansky等[10]提出应用双向荧光标记 TP-PCR法以提高检测的灵敏度。自Warner等人发明TP-PCR以来,该方法逐渐成为DM1的常规基因诊断方法,然而国内直到2012年始才有文献针对DM1基因检测进行报道。李韵等[11]报道了以TP-PCR法确诊了19个家系共20名DM1患者以及24名健康对照,首次在中国人群中验证了该方法的可靠性和临床实用性。本中心亦对30余名临床拟诊DM1患者进行了TP-PCR检测,除 1名患者存在打断序列导致扩增失败外,其余患者均成功扩增。图2分别为某正常人A和某患者B的TP-PCR检测结果。
尽管与DM1临床表现有一定相似性,但DM2为ZNF9基因1号内含子区发生CCTG四核苷酸重复异常扩增而致病,患者四核苷酸重复异常扩增次数为75~11000次,平均重复次数可高达5000余次[7]。针对DM2的重复引物PCR法直到2003年才首次被报道[12],其引物设计思路仍然沿袭 Warner等人的TP-PCR思路,唯一区别在于将荧光标记加在了通用引物序列上,该研究结果证明,重复引物PCR技术不仅适用于三核苷酸动态突变,亦可以推广于四核苷酸,甚至是五核苷酸或六核苷酸动态突变。遗憾的是,由于亚洲人群DM2发病率较低,国内目前鲜有DM2基因确诊阳性的报道。

图2 本中心DM1 TP-PCR检测结果
4 重复引物PCR技术在FRDA、SCA10及其他共济失调中的应用
FRDA是欧美人群最常见的常染色体隐性共济失调,其发病率最高可达1/30000[13],约占欧美地区常染色体隐性共济失调的半数。FRDA主要临床特征为儿童期发病,肢体进行性共济失调,伴发音困难、深感觉消失、脊柱侧突、弓形足、心脏损害和糖尿病等。FRDA的致病基因是位于9q13的Frataxin基因(FXN),除了少数患者为点突变外,95%的患者为该基因1号内含子区发生GAA三核甘酸重复异常扩增而致病[14~16]。在正常人中,GAA重复次数小于34~36次,一般为6~12次,患者两条等位基因重复次数均大于66次,最高可达1500次,小于200次重复的患者较为罕见[17~20]。
SCA10是一种以小脑性共济失调和癫痫为主要表现的常染色体显性遗传性共济失调,由 ATXN10基因9号内含子区发生ATTCT五核苷酸重复异常扩增导致[21]。正常人该区域五核苷酸重复次数为10~22次,以13和14次最为多见,患者可出现280次以上的重复异常扩增,目前报道的最高重复次数可达4500次,其相应的区域长达22.5 kb。除此之外,作为第一个被发现的非编码区重复序列扩增所致病的亚型,SCA8是由ATXN8/ATXN8OS发生CAG/CTG双向性异常扩增致病[22,23],其临床表现主要为小脑共济失调并伴有步态痉挛和大脑半球萎缩[24,25]。SCA12则是由于PPP2R2B基因非编码区内的CAG重复序列异常扩增所致,主要临床表现为震颤、步态共济失调、辨距不良、腱反射亢进、运动活动减少、异常眼球运动及老年患者常见的痴呆。尽管目前报道SCA12的异常扩增次数为55~78次[26,27],但由于报道例数太少,不能排除存在超大片段重复异常扩增的可能。
2004年,Cagnoli等[28]首次报道应用重复引物PCR技术进行FRDA、SCA10和SCA12的基因检测。在这项研究中,共纳入43例FRDA患者、28例FRDA携带者、10例SCA10患者、6例SCA12患者以及152名健康对照,结果显示,运用重复引物PCR法对FRDA、SCA10和SCA12患者或携带者进行相应目的片段扩增均获得成功,其结果与直接PCR(仅用于 SCA12)或 Southern blot一致,FRDA和 SCA10的最大扩增片段分别达到1430次和3700次[28]。这项研究不仅将重复引物PCR技术的应用范围再次进行了扩展,证实了五核苷酸重复异常扩增亦可运用该方法进行检测,而且首次将该技术应用于常染色体隐性遗传病的基因检测中,提出了隐性遗传方式的识图方法。然而,Cagnoli等人也承认应用该方法扩增 SCA8并未取得成功,考虑其扩增失败的原因可能是局部复杂的构象限制了重复引物PCR法对目的片段的扩增效率。近年来陆续有学者成功应用重复引物PCR技术对SCA8致病基因ATXN8/ATXN8OS致病片段进行扩增[29~31],提示尽管在诊断SCA8的灵敏度上较诊断其他超大片段动态突变疾病略低,但重复引物 PCR仍不失为一种高效且低成本的SCA8基因诊断技术。
东亚地区具有FRDA典型GAA重复异常扩增的患者很罕见[32],国内对本病多是符合临床表现的个案报道,缺乏基因检测阳性结果,可能的原因有两种:一是FRDA具有种族特异性,东亚人群具有某种保护机制而不易发生FXN基因GAA重复异常扩增;二是东亚人群尤其是中国人群该病致病突变可能多为欧美人群罕见的点突变而非动态突变,但迄今为止国内尚未有针对FXN基因点突变相关研究的报道。此外,针对SCA8和SCA10的基因检测也均为阴性结果[33],可能由于这两型共济失调在中国人群中罕见,亦可能由于重复引物PCR法并未得到充分推广。
5 应用重复引物 PCR技术检测 C9orf72基因突变
新近在高加索人群中发现 C9orf72基因是家族性 ALS合并 FTD(fALS-FTD)、家族性 ALS(fALS)以及家族性 FTD(fFTD)的致病基因[34,35]。该基因 1号内含子区发生GGGGCC六核苷酸异常扩增,患者重复次数须大于30次,最高可达1600次[34]。Majounie等[36]报道,在西方人群及其后裔中,该基因突变患者可占fALS患者的39.3%及fFTD患者的24.8%,即使在散发的ALS或FTD患者中,也有4%~8%携带该突变,然而具有该基因突变的患者都携带有部分或全部的奠基者单体型(Founder haplotype),亚裔人群中,该基因突变罕见。
与其他超大片段动态突变不同,C9orf72基因突变在首次报道时就应用了重复引物PCR法进行异常或正常重复序列的扩增[34,35]。与应用于扩增 FRDA和SCA10致病基因的重复引物PCR法不同,用于扩增 C9orf72基因GGGGCC突变的重复引物PCR技术又发生了一些变化,主要发生在两个方面:一方面在于touchdown PCR技术被结合到重复引物PCR技术中。作为该突变的首次报道,DeJesus-Hernandez等[34]及 Renton等[35]在应用重复引物PCR法时都联合应用了touchdown PCR技术。Touchdown PCR技术是指 PCR反应中每个循环降低 1°C反应退火温度,直到达到目标退火温度,然后以此退火温度再进行10~25个循环普通PCR。其优点在于反应一开始先以高温扩增,从而保证了扩增的严谨性,待目的片段的丰度上升后,降低扩增的温度,这样又提高了扩增效率。另一方面是DeJesus-Hernandez等[34]在引物设计中借鉴了 Hantash等[37]的思路,在上游引物的前端加入了锚定序列(Anchor sequence),并在反应体系中加入 7-脱氮-2′脱氧 GTP(7-deaza-2-deoxy-GTP),使引物结合效率大大提高,从而增加了重复引物PCR法检测超大片段重复序列的灵敏度。然而尽管方法有所改进,但重复引物PCR法用于临床检测仍遇到了挑战。最近一项囊括了全球14个实验室针对 C9orf72基因突变检测可靠性的研究发现,参与研究的14个实验室中仅有5个实验室重复引物PCR检测结果与Southern blot检测结果完全一致,78份DNA标本仅有50份在全部14个实验室进行重复引物PCR检测得到相同结果[38]。这一结果表明,应用重复引物PCR法进行C9orf72基因突变检测可能存在一定假阳性或假阴性结果,主要问题在于各个实验室所采用的扩增反应条件不尽相同,以及部分实验室并未添加7-deaza-2-deoxyGTP而导致扩增失败[38]。
国内对于 C9orf72基因突变的检测开始较早。2012年 Zou等[39]率先对 20名 fALS患者及 324名sALS患者进行C9orf72基因筛查,未发现该基因六核苷酸动态突变。此后,Liu等[40]针对 61名 fALS患者进行的C9orf72基因筛查也未报道阳性结果。最近,唐璐等[41]报道在 401例 sALS患者中筛查到 3例 C9orf72基因突变患者。综合国内目前已报道的资料,我们认为重复引物PCR法是检测C9orf72基因六核苷酸动态突变的可靠方法,但中国人群遗传背景异于西方人群,因此中国人群sALS及fALS的分子遗传学机制很可能也与西方人群大为迥异,考虑到基因检测的经济负担,C9orf72基因突变筛查在中国ALS患者中并非首选。
6 结语与展望
自Warner等人发明三引物 PCR技术后,重复引物PCR技术因其低成本、高效率、方法简便等优点,被广泛应用于DM、FRDA、FXS以及C9orf72基因突变引起的FTD或ALS-FTD等疾病的基因检测中,随着应用经验的积累,重复引物PCR技术不断得到改良,尤其是借鉴了锚定引物设计和 touchdown PCR技术后,检测的灵敏度和特异度又有了较大的提升。但值得注意的是,即便该技术已经如此简便易行,但仍存在因反应条件不达标或实验者操作问题而导致扩增失败或扩增错误的情况。因此,应当建立一套标准化实验流程以减小假阴性或假阳性结果出现的概率,而临床医生自身也应当保持审慎态度,将基因检测结果仅作为临床诊断的依据之一。随着转化医学研究的深入,各类遗传性疾病的临床基因检测商品化试剂盒必将逐渐取代繁琐的实验室操作,从而大大降低技术的学习成本,重复引物PCR技术也必将在现有基础上继续发展,甚至可能为新的更简便的技术所取代。
[1]Nelson DL, Orr HT, Warren ST.The unstable repeats-three evolving faces of neurological disease.Neuron, 2013, 77(5):825–843.
[2]Warner JP, Barron LH, Goudie D, Kelly K, Dow D, Fitzpatrick DR, Brock DJ.A general method for the detection of large CAG repeat expansions by fluorescent PCR.J Med Genet, 1996, 33(12): 1022–1026.
[3]Buxton J, Shelbourne P, Davies J, Jones C, Van Tongeren T, Aslanidis C, de Jong P, Jansen G, Anvret M, Riley B,Williamson R, Johnson K.Detection of an unstable fragment of DNA specific to individuals with myotonic dystrophy.Nature, 1992, 355(6360): 547–548.
[4]余志良, 谢惠君, 赵晓萍, 丁素菊, 郑惠民, 邓本强, 崔毅, 张社卿.强直性肌营养不良的分子诊断技术的临床应用研究.中华神经医学杂志, 2004, 3(6): 450–452.
[5]朱宏文, 刘彦山, 杨威, 孙淼.实时定量 PCR在强直性肌营养不良1型重复突变检测中的应用.国际遗传学杂志, 2010, 33(3): 138–141.
[6]Zerylnick C, Torroni A, Sherman SL, Warren ST.Normal variation at the myotonic dystrophy locus in global human populations.Am J Hum Genet, 1995, 56(1): 123–130.
[7]Ashizawa T, Sarkar PS.Myotonic dystrophy types 1 and 2.Handb Clin Neurol, 2011, 101: 193–237.
[8]Udd B, Krahe R.The myotonic dystrophies: molecular, clinical, and therapeutic challenges.Lancet Neurol,2012, 11(10): 891–905.
[9]Musova Z, Mazanec R, Krepelova A, Ehler E, Vales J,Jaklova R, Prochazka T, Koukal P, Marikova T, Kraus J,Havlovicova M, Sedlacek Z.Highly unstable sequence interruptions of the CTG repeat in the myotonic dystrophy gene.Am J Med Genet A, 2009, 149A(7): 1365–1374.
[10]Radvansky J, Ficek A, Minarik G, Palffy R, Kadasi L.Effect of unexpected sequence interruptions to conventional PCR and repeat primed PCR in myotonic dystrophy type 1 testing.Diagn Mol Pathol, 2011, 20(1): 48–51.
[11]李韵, 笪宇威.强直性肌营养不良 1型三核苷酸重复序列的检测.中华医学遗传学杂志, 2012, 29(1): 16–18.
[12]Bachinski LL, Udd B, Meola G, Sansone V, Bassez G,Eymard B, Thornton CA, Moxley RT, Harper PS, Rogers MT, Jurkat-Rott K, Lehmann-Horn F, Wieser T, Gamez J,Navarro C, Bottani A, Kohler A, Shriver MD, Sallinen R,Wessman M, Zhang SX, Wright FA, Krahe R.Confirmation of the type 2 myotonic dystrophy (CCTG)n expansion mutation in patients with proximal myotonic myopathy/proximal myotonic dystrophy of different European origins: a single shared haplotype indicates an ancestral founder effect.Am J Hum Genet, 2003, 73(4): 835–848.
[13]Schulz JB, Boesch S, Bürk K, Dürr A, Giunti P, Mariotti C,Pousset F, Schöls L, Vankan P, Pandolfo M.Diagnosis and treatment of Friedreich ataxia: a European perspective.Nat Rev Neurol, 2009, 5(4): 222–234.
[14]Campuzano V, Montermini L, Moltò MD, Pianese L,Cossée M, Cavalcanti F, Monros E, Rodius F, Duclos F,Monticelli A, Zara F, Cañizares J, Koutnikova H, Bidichandani SI, Gellera C, Brice A, Trouillas P, De Michele G,Filla A, De Frutos R, Palau F, Patel PI, Di Donato S,Mandel JL, Cocozza S, Koenig M, Pandolfo M.Friedreich's ataxia: autosomal recessive disease caused by an intronic GAA triplet repeat expansion.Science, 1996,271(5254): 1423–1427.
[15]Cossée M, Dürr A, Schmitt M, Dahl N, Trouillas P, Allinson P, Kostrzewa M, Nivelon-Chevallier A, Gustavson KH,Kohlschütter A, Müller U, Mandel JL, Brice A, Koenig M,Cavalcanti F, Tammaro A, De Michele G, Filla A, Cocozza S, Labuda M, Montermini L, Poirier J, Pandolfo M.Friedreich's ataxia: point mutations and clinical presentation of compound heterozygotes.Ann Neurol, 1999, 45(2):200–206.
[16]Gellera C, Castellotti B, Mariotti C, Mineri R, Seveso V,Didonato S, Taroni F.Frataxin gene point mutations in Italian Friedreich ataxia patients.Neurogenetics, 2007,8(4): 289–299.
[17]Cossée M, Schmitt M, Campuzano V, Reutenauer L,Moutou C, Mandel JL, Koenig M.Evolution of the Friedreich's ataxia trinucleotide repeat expansion: founder effect and premutations.Proc Natl Acad Sci USA, 1997,94(14): 7452–7457.
[18]Epplen C, Epplen JT, Frank G, Miterski B, Santos EJM,Schöls L.Differential stability of the (GAA)n tract in the Friedreich ataxia (STM7) gene.Hum Genet, 1997, 99(6):834–836.
[19]Filla A, De Michele G, Cavalcanti F, Pianese L, Monticelli A, Campanella G, Cocozza S.The relationship between trinucleotide (GAA) repeat length and clinical features in Friedreich ataxia.Am J Hum Genet, 1996, 59(3): 554–560.
[20]Montermini L, Andermann E, Labuda M, Richter A, Pandolfo M, Cavalcanti F, Pianese L, Iodice L, Farina G,Monticelli A, Turano M, Filla A, De Michele G, Cocozza S.The Friedreich ataxia GAA triplet repeat: premutation and normal alleles.Hum Mol Genet, 1997, 6(8): 1261–1266.
[21]Matsuura T, Yamagata T, Burgess DL, Rasmussen A,Grewal RP, Watase K, Khajavi M, McCall AE, Davis CF,Zu L, Achari M, Pulst SM, Alonso E, Noebels JL, Nelson DL, Zoghbi HY, Ashizawa T.Large expansion of the ATTCT pentanucleotide repeat in spinocerebellar ataxia type 10.Nat Genet, 2000, 26(2): 191–194.
[22]Koob MD, Moseley ML, Schut LJ, Benzow KA, Bird TD,Day JW, Ranum LP.An untranslated CTG expansion causes a novel form of spinocerebellar ataxia (SCA8).Nat Genet, 1999, 21(4): 379–384.
[23]Ikeda Y, Daughters RS, Ranum LP.Bidirectional expression of the SCA8 expansion mutation: one mutation, two genes.Cerebellum, 2008, 7(2): 150–158.
[24]Day JW, Schut LJ, Moseley ML, Durand AC, Ranum LP.Spinocerebellar ataxia type 8: clinical features in a large family.Neurology, 2000, 55(5): 649–657.
[25]Ikeda Y, Shizuka M, Watanabe M, Okamoto K, Shoji M.Molecular and clinical analyses of spinocerebellar ataxia type 8 in Japan.Neurology, 2000, 54(4): 950–955.
[26]Holmes SE, O'Hearn EE, McInnis MG, Gorelick-Feldman DA, Kleiderlein JJ, Callahan C, Kwak NG, Ingersoll-Ashworth RG, Sherr M, Sumner AJ, Sharp AH,Ananth U, Seltzer WK, Boss MA, Vieria-Saecker AM,Epplen JT, Riess O, Ross CA, Margolis RL.Expansion of a novel CAG trinucleotide repeat in the 5' region of PPP2R2B is associated with SCA12.Nat Genet, 1999,23(4): 391–392.
[27]Fujigasaki H, Verma IC, Camuzat A, Margolis RL, Zander C, Lebre AS, Jamot L, Saxena R, Anand I, Holmes SE,Ross CA, Dürr A, Brice A.SCA12 is a rare locus for autosomal dominant cerebellar ataxia: a study of an Indian family.Ann Neurol, 2001, 49(1): 117–121.
[28]Cagnoli C, Michielotto C, Matsuura T, Ashizawa T, Margolis RL, Holmes SE, Gellera C, Migone N, Brusco A.Detection of large pathogenic expansions in FRDA1,SCA10, and SCA12 genes using a simple fluorescent repeat-primed PCR assay.J Mol Diagn, 2004, 6(2): 96–100.
[29]Tanaka E, Maruyama H, Morino H, Kawakami H.Detection of large expansions in SCA8 using a fluorescent repeat-primed PCR assay.Hiroshima J Med Sci, 2011, 60(3):63–66.
[30]Krysa W, Rajkiewicz M, Sułek A.Rapid detection of large expansions in progressive myoclonus epilepsy type 1,myotonic dystrophy type 2 and spinocerebellar ataxia type 8.Neurol Neurochir Pol, 2012, 46(2): 113–120.
[31]Musova Z, Sedlacek Z, Mazanec R, Klempir J, Roth J,Plevova P, Vyhnalek M, Kopeckova M, Apltova L, Krepelova A, Zumrova A.Spinocerebellar ataxias type 8, 12,and 17 and dentatorubro-pallidoluysian atrophy in Czech ataxic patients.Cerebellum, 2013, 12(2): 155–161.
[32]Labuda M, Labuda D, Miranda C, Poirier J, Soong BW,Barucha NE, Pandolfo M.Unique origin and specific ethnic distribution of the Friedreich ataxia GAA expansion.Neurology, 2000, 54(12): 2322–2324.
[33]王俊岭, 徐倩, 雷立芳, 沈璐, 江泓, 李晓辉, 周亚芳,易继平, 周洁, 严新翔, 潘乾, 夏昆, 唐北沙.中国汉族人群 SCA1、2、3、6、7、8、10、12、17亚型和齿状核-红核-苍白球-路易体萎缩亚型频率分布.中华神经科杂志, 2009, 42(10): 672–675.
[34]DeJesus-Hernandez M, Mackenzie IR, Boeve BF, Boxer AL, Baker M, Rutherford NJ, Nicholson AM, Finch NA,Flynn H, Adamson J, Kouri N, Wojtas A, Sengdy P,Hsiung GY, Karydas A, Seeley WW, Josephs KA, Coppola G, Geschwind DH, Wszolek ZK, Feldman H, Knopman DS, Petersen RC, Miller BL, Dickson DW, Boylan KB,Graff-Radford NR, Rademakers R.Expanded GGGGCC hexanucleotide repeat in noncoding region of C9ORF72 causes chromosome 9p-linked FTD and ALS.Neuron, 2011, 72(2): 245–256.
[35]Renton AE, Majounie E, Waite A, Simón-Sánchez J, Rollinson S, Gibbs JR, Schymick JC, Laaksovirta H, van Swieten JC, Myllykangas L, Kalimo H, Paetau A, Abramzon Y, Remes AM, Kaganovich A, Scholz SW, Duckworth J, Ding J, Harmer DW, Hernandez DG, Johnson JO, Mok K, Ryten M, Trabzuni D, Guerreiro RJ, Orrell RW, Neal J,Murray A, Pearson J, Jansen IE, Sondervan D, Seelaar H,Blake D, Young K, Halliwell N, Callister JB, Toulson G,Richardson A, Gerhard A, Snowden J, Mann D, Neary D,Nalls MA, Peuralinna T, Jansson L, Isoviita VM, Kaivorinne AL, Hölttä-Vuori M, Ikonen E, Sulkava R, Benatar M, Wuu J, Chiò A, Restagno G, Borghero G, Sabatelli M,Consortium I, Heckerman D, Rogaeva E, Zinman L,Rothstein JD, Sendtner M, Drepper C, Eichler EE, Alkan C, Abdullaev Z, Pack SD, Dutra A, Pak E, Hardy J, Singleton A, Williams NM, Heutink P, Pickering-Brown S,Morris HR, Tienari PJ, Traynor BJ.A hexanucleotide repeat expansion in C9ORF72 is the cause of chromosome 9p21-linked ALS-FTD.Neuron, 2011, 72(2): 257–268.
[36]Majounie E, Renton AE, Mok K, Dopper EG, Waite A,Rollinson S, Chiò A, Restagno G, Nicolaou N, Simon-Sanchez J, van Swieten JC, Abramzon Y, Johnson JO,Sendtner M, Pamphlett R, Orrell RW, Mead S, Sidle KC,Houlden H, Rohrer JD, Morrison KE, Pall H, Talbot K,Ansorge O, Chromosome 9-ALS/FTD Consortium, French research network on FTLD/FTLD/ALS, Consortium I,Hernandez DG, Arepalli S, Sabatelli M, Mora G, Corbo M,Giannini F, Calvo A, Englund E, Borghero G, Floris GL,Remes AM, Laaksovirta H, McCluskey L, Trojanowski JQ,Van Deerlin VM, Schellenberg GD, Nalls MA, Drory VE,Lu CS, Yeh TH, Ishiura H, Takahashi Y, Tsuji S, Le Ber I,Brice A, Drepper C, Williams N, Kirby J, Shaw P, Hardy J,Tienari PJ, Heutink P, Morris HR, Pickering-Brown S,Traynor BJ.Frequency of the C9orf72 hexanucleotide repeat expansion in patients with amyotrophic lateral sclerosis and frontotemporal dementia: a cross-sectional study.Lancet Neurol, 2012, 11(4): 323–330.
[37]Hantash FM, Goos DG, Tsao D, Quan F, Buller-Burckle A,Peng M, Jarvis M, Sun WM, Strom CM.Qualitative assessment of FMR1 (CGG)n triplet repeat status in normal,intermediate, premutation, full mutation, and mosaic carriers in both sexes: implications for fragile X syndrome carrier and newborn screening.Genet Med, 2010,12(3): 162–173.
[38]Akimoto C, Volk AE, van Blitterswijk M, Van den Broeck M, Leblond CS, Lumbroso S, Camu W, Neitzel B, Onodera O, van Rheenen W, Pinto S, Weber M, Smith B,Proven M, Talbot K, Keagle P, Chesi A, Ratti A, van der Zee J, Alstermark H, Birve A, Calini D, Nordin A, Tradowsky DC, Just W, Daoud H, Angerbauer S, DeJesus-Hernandez M, Konno T, Lloyd-Jani A, de Carvalho M,Mouzat K, Landers JE, Veldink JH, Silani V, Gitler AD,Shaw CE, Rouleau GA, van den Berg LH, Van Broeckhoven C, Rademakers R, Andersen PM, Kubisch C.A blinded international study on the reliability of genetic testing for GGGGCC-repeat expansions in C9orf72 reveals marked differences in results among 14 laboratories.J Med Genet, 2014, 51(6): 419–424.
[39]Zou ZY, Li XG, Liu MS, Cui LY.Screening for C9orf72 repeat expansions in Chinese amyotrophic lateral sclerosis patients.Neurobiol Aging, 2013, 34(6): 1710.e5–1710.e 6.
[40]Liu R, Tang L, Cai B, Liu X, Ye S, Ma Y, Zhang H, Fan D.C9orf72 repeat expansions are not detected in Chinese patients with familial ALS.Amyotroph Lateral Scler Frontotemporal Degener, 2013, 14(7–8): 630–631.
[41]唐璐, 刘蓉, 蔡宾, 刘晓鲁, 叶珊, 马妍, 张华纲, 崔德华, 樊东升.中国内地散发性肌萎缩侧索硬化患者9号染色体开放阅读框 72基因六核苷酸重复片段异常扩增及其临床表型.中华神经科杂志, 2013, 46(7): 443–447.
