热休克蛋白表位肽免疫对动脉粥样硬化斑块的影响
2014-04-29孙云霄张礼标王华倩张宇熊祺琰曹荣月吴洁
孙云霄 张礼标 王华倩 张宇 熊祺琰 曹荣月 吴洁
摘 要:利用BSP65 (heat shock protein 65,HSP65)中与炎症性自身免疫性疾病相关的两段功能表位EE14(176-189)、DL18 (215-232),通过戊二醛偶联法与BSA (bovine serum albumin, BSA)制备成多肽-BSA偶联蛋白,获得可用于免疫高脂膳食动物的蛋白。与PBS (phospllate buffer saline,PBS)组比较,多肽免疫组抗HSP65抗体滴度与总胆固醇(total cholesterol,TC)含量无明显区别(P<0.05),抗自身肽的抗体在两免疫组的结果不同,但两组主动脉粥样硬化斑块的面积都显著增加,两免疫组斑块面积与血管总面积百分比分别为39.61%与36.75%,为PBS组(斑块面积占血管总面积百分比为10.35 %)的3.8倍和3.6倍,有显著性差异(P<0.05) 实验结果表明HSP65相关B细胞表位肽,皮下免疫能显著促进AS (atherosclerosis,AS)斑块生成。 在后续研究中可利用以上表位,通过改变免疫方式,设计可用于抑制AS斑块生成的免疫调节剂,进一步考察HSP65功能性B细胞表位的免疫预防及治疗效果。
关键词:动脉粥样硬化(AS):热休克蛋白(HSP):免疫
中图分类号:Q789
文献标识码:A
文章编号:1007-7847(2014)06-0471-06
近年来国内外的研究表明,动脉粥样硬化(atherosclerosis. AS)是慢性自身免疫性炎症疾病,适应性免疫和天然免疫反应引起的炎症反应在AS发展的所有阶段中起着关键作用。热休克蛋白(heat shock proteins,HSPs)在进化上被认为是一类高度保守的蛋白,在AS发病过程中作为自身抗原起着重要的作用。人源的HSP60 (hHSP60)与结核分支杆菌来源的HSP65 (mHSP65)大概存在50%的同源性,高度同源,而原核微生物之间HSP同源性更是能达到97%,两者具有相似的抗原表位,因此mHSP65能通过分子模拟产生抗人自身HSP60的免疫反应.诱导自身反应性T细胞攻击自身抗原,引起人自身免疫性反应而促进AS的发生。
抗原分子在免疫反应过程中起主要作用的是T和B细胞表位。HSP65中有许多与AS相关的表位如36 -45、91-100、111 -120、160 -177、179 -190、215-232、433-450和507-516等,大部分是B细胞表位。通过对AS患者血清内获得抗体和健康人体内获得的抗体对mHSP65与hHSP60进行抗原扫描,结果发现许多抗原表位是hHSP60与mHSP65共有表位。其中HSP65(179-190)与HSP6525(215-232)就同为HSP65/60两者共有表位。HSP65(179-190)为佐剂性关节炎疾病相关重要表位,因为AS与佐剂型关节炎同为炎症性自身免疫疾病,研究选择了与 HSP65(179-190)基本相同的HSP65(176-189) (EESNT-FGLQLELTE)(EE14)B细胞表位来进行致AS研究:而HSP65(215-232)(DPYILLVSSKVSTVKDLL) (DL18)为动脉粥样硬化患者出现抗HSP65抗体频率最高的几个B细胞表位之一。选择以上两个B细胞表位,合成制备表位肽,通过皮下免疫高脂诱导的新西兰大白兔研究其对AS的皮下免疫效果,进一步研究HSP相关表位与AS之间的关系。前期研究利用HSP65中的T和B细胞表位构建的多肽疫苗经粘膜免疫后降低AS斑块形成的效果并不理想,本研究单独观察HSP65上的B细胞表位皮下免疫后致AS结果,基于此结果,进一步研究设计出可通过粘膜免疫的抗AS斑块形成的表位多肽疫苗,通过研究HSP重要功能表位与AS之问的关系,为抗AS多肽抑制剂的设计提供理论及实验基础。
将EE14与DL18合成肽通过戊二醛溶液法分别与牛血清白蛋白(bovine serum albumin, BSA)偶联制备成偶联蛋白,以提高表位抗原肽的免疫原性,并与弗氏不完全佐剂制备成乳剂,埘高脂膳食诱导的患AS新西兰大白兔进行皮内皮下联合免疫,测定动脉粥样斑块的大小,血清中总胆同醇含量变化及抗HSP65抗体产生情况及变化趋势,研究HSP65功能表位肽在弗氏不完全佐剂条件下经皮下免疫是否加重动脉粥样硬化病情。
1 材料和方法
1.1 试剂、融合蛋白与动物
EE14和DL18由上吉尔牛化(上海)有限公司合成。考虑单纯合成的多肽免疫原性很低,所以研究中将多肽与BSA通过戊二醛偶联成偶联蛋白来加以免疫,以克服单纯的合成多肽片段难以激发免疫反应的不足。
胆同醇纯度>99.9%(上海生工);弗氏不完全佐剂(Freund's adjuvant incomplete, IFA) (Sigma.USA);辣根过氧化物酶标记的羊抗兔IgG(武汉博士德生物工程有限公司);总胆固醇(total choles-terol, TC)测定试剂盒(上海荣盛生物技术有限公司);其余为常规试剂,国产AR级。
新西兰大白兔购自江苏省农业科学研究院,雄性,体重1.5—2.0 kg,置于一般室内环境单笼饲养
1.2 方法
1.2.1 多肽与BSA偶联
戊二醛作为一种双功能偶联剂,其两个醛基通过结合赖氨酸残基上的游离氨基,把不同抗原连接起来。合成表位肽EE14与BL18和BSA各5 mg溶解于PBS.混匀,边搅拌边向混合液缓慢滴加0.25% PBS稀释的戊二醛溶液,放置于低温条件下过夜反应。第2 d观察生成的偶联物,若溶液变为淡黄色,则逐滴加入l mol/L PBS稀释的甘氨酸溶液,在低温条件下终止此反应30 min后,将偶联液以1:20的比例对PBS透析,6h左右换透析液,随后再更换3次透析液(每隔12 h一次)。冷冻干燥,-20 ℃保存。
1.2.2 新西兰大白兔动脉粥样硬化模型的建立和免疫
新西兰大白兔随机分为3组,分别为PBS、EE14及DL18免疫组。其中PBS组9只,其余两组各8只。各组新西兰大白兔饲喂高胆固醇食物,每只兔每天的胆同醇摄人量为0.5 g(饲料配方为0.5%的胆固醇,5%的油脂与94.5%的基础饲料),前后高脂饲料饲喂共5个月左右,直至实验结束时PBS组新两兰大白兔腹主动脉中有明显的粥样斑块生成。各组药物均以灭菌PBS溶解,与IFA一起等量配制成0.2 mg/mL浓度,免疫剂量为每只200 μg,注射体积为每只1mL。皮内皮下多点注射的方法免疫新西兰大白兔,背部4点皮内注射,颈部l点皮下注射,自造模开始,免疫4次,前4个月每月免疫1次,第一次免疫在高脂喂养2周后。各组分别于免疫的第0、3、5、8、Il、14、18、22周耳缘静脉取全血,静置1 h左右,低温条件下4 000 t/min进行离心,取上清,放置冰箱-20 ℃储存备用。
1.2.3 觅体征变化情况
实验过程中肉眼观察新西兰大白兔的外观、行为、活动、摄食量、体重、粪便及眼、耳、皮肤等器官的情况,最后在解剖新西兰人白兔取出主动脉过程中观察心、肝、脾、肺、肾等内脏器管的变化。1.2.4 抗HSP65、抗EE14与抗DL18抗体(lgG)的ELISA检测
用不同的包被抗原包括纯化的HSP65或EE14. DL18包被酶标板,10μg/mL的抗原浓度溶于包被稀释液,每孔加入100 μL,低温条件下包被过夜:倒掉包被液,加2%BSA封闭液,低温条件下封闭过夜;倒掉封闭液,加1:200稀释的兔血清 1oo μL, 37℃进行孵育l h左右;去血清,用PBST与水交替洗涤6次后,加入1:20 000倍稀释的酶标记的羊抗兔IgG,孵育。倒去酶标二抗,PBST与水交替洗涤;加100 μL底物液,37℃反应45 min左右,加入H2S04终止反应,利用酶标仪测定OD450nm光密度值。
1.2.5 兔血清中总胆固醇含量检测
利用荣盛牛物技术有限公司(上海)的TC检测试剂盒,通过胆固醇氰化酶一过氧化物酶方法测定血清中的TC含量,利用可见分光光度仪于500 nm处测定吸光度,根据吸光度值,计算肌固醇含量(mmol/L) 。
1.2.6 兔腹主动脉粥样病斑测定
新西兰大白兔通过颈动脉放血的方法处死,从主动脉出心脏开始至髂动脉分义处分离出主动脉,将血管外面的脂肪组织小心剔除,后沿背侧顺剪开,用10%甲醛进行固定,4 d后用0.2%苏丹Ⅲ(SudanⅢ)乙醇溶液进行染色半小时左右,70%乙醇溶液进行洗涤完全,将染色后的血管内表面通过扫描仪进行扫描后,利用MarJlnfor7.0软件统计斑块而积与血管内表皮的总面积。
1.3 数据分析
将实验数据用平均值±标准差(x±s)的形式表示。所有统计分析采用Student's t test,P<0.05被认为有显著性差异。
2 结果
2.1 兔体征变化情况
实验过程中肉眼观察新西兰大白兔的外观、摄食量、体重、行为、活动、粪便及眼、耳、皮肤等器官的情况均未见异常变化。体重变化正常.逐日增加。
此外,对处死后兔的肝、脾、肺、肾等脏器,进上肉眼和显微观察,在外观上这些脏器无明显病变,无异常粘连物质。
结果表明,2组多肽注射免疫组与PBS对照组相比,对新西兰人门兔的生长并无明显影响,除主动脉外其他的脏器无明显异常。
2.2 抗HSP65、抗EE14与抗DL18抗体(IgG)的ELISA检测
以HSP65蛋白为包被抗原。检测PBD组、EE14、DL18免疫组血清中特异性抗HP65抗体的产生情况,检测结果如下(图1)。
在弗氏不完伞佐剂存在情况下,合成肽DLl8免疫组没有诱导产生姒的抗Hsp65抗体,与PBS相比,没有明显差异而合成肽EEl4在第一次免疫后的第3周抗Hsp65抗滴度与 PBS组相比有所升高,随后在第5周以后却低于PBS对照组,且与PBS组差异不大,不具有统计学意义(P<0.05),与PBS组未见有显著差异(图1)
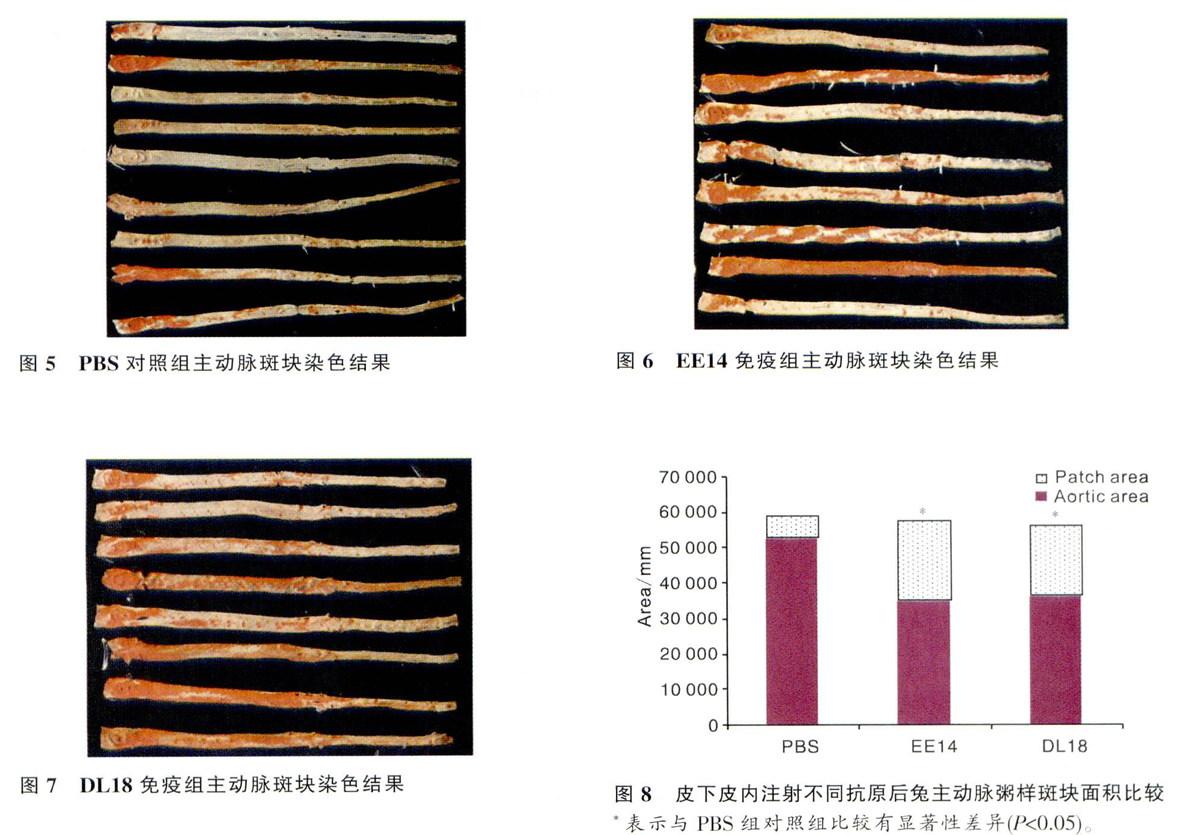
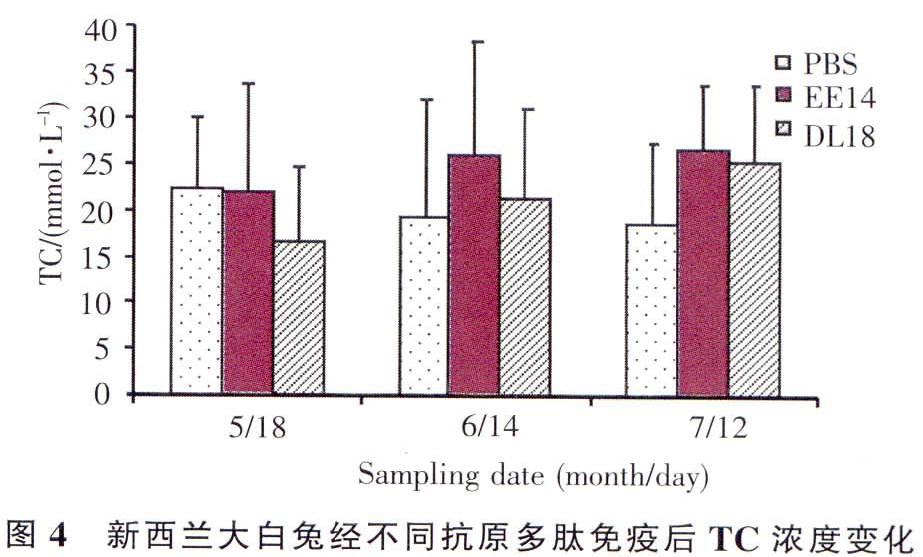
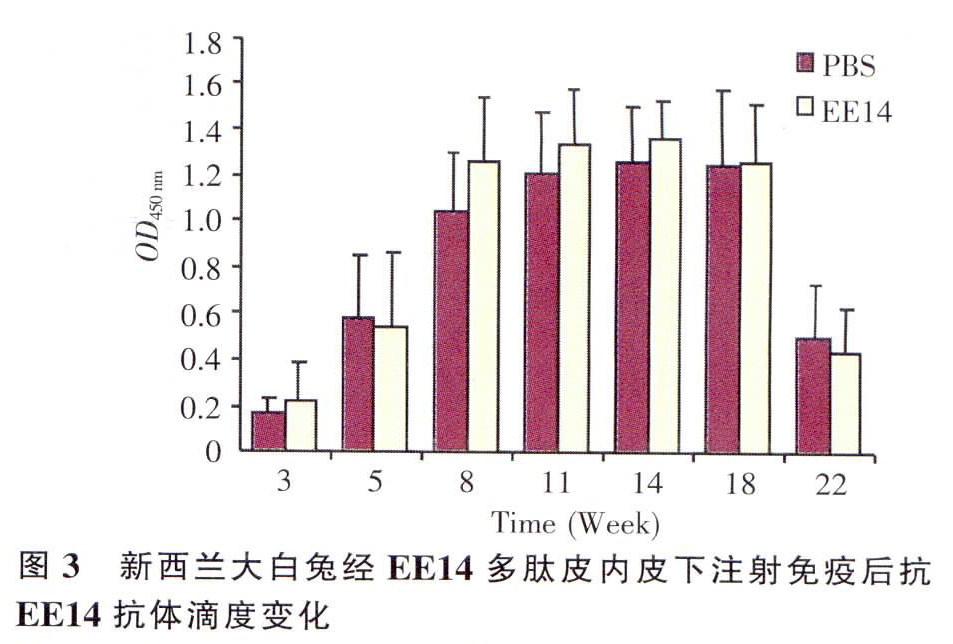
以合成肽DL18蛋白为包被抗原,检测PBS组,DLl8免疫组的血清中针对DL18合成肽抗体的的产生情况,检测结果如下。在弗氏不完余佐剂存在的情况下,以合成肽DL18皮内皮下免疫新西兰大白兔,在第一次免疫后的第3周即可测得血清中抗DL18抗体的产生,并且与对照组相比差异显著(P 以合成肽EE14蛋白为包被抗原,检测PBS组.EEI4给药组的血清中针对EE14合成肽抗体的产生情况,检测结果如下。在弗氏不完全佐剂存在的情况下,合成肽EE14皮内皮下免疫新西兰大白兔,与PBS组相比,没有诱导出针对抗EE14的抗体(图3)。 2.3 免疫后兔血清TC的含量测定 利用上海荣盛生物技术有限公司的总胆同醇测定试剂盒,测得各组兔血清的总胆固醇含量见图4。在弗氏不完全佐剂存在的条件下,EE14、DL18合成肽和PBS共同免疫新西兰大白兔,从图4可以看出,尽管后期(第22周最后一次取血测定)能影响血清中TC含量,但并无明显的差异,无统计学意义,即两组合成肽免疫组对新西兰大白兔的血脂含量(TC)不会产明显影响。从针对抗Hsp65抗体的产生情况看,与PBS组相比较两组合成肽免疫组都未能诱导出高的抗Hsp65抗体.甚至还明显低于PBS免疫组(图1),这可能与其对TC含量不会产生影响有关。 2.4 新西兰大白兔腹主动脉粥样硬化斑块测定结果 因胆固醇易被SudanⅢ染成红色,而粥样斑块中富含胆固醇,因此经染色后,斑块部分则会与斑块周围正常血管部位区别开。利用软件对粥样斑块的面积进行统计分析,PBS对照组粥样斑块面积为主动脉血管总面积的10.35%(图5);合成肽EE14和DL18与弗氏不完全佐剂免疫组主动脉粥样斑块面积分别占血管总面积的百分比分别为39.61和36.75%f图6、7)。与PBS组比较,主动脉硬化斑面积与血管总面积百分比分别约为PBS组的3.8倍和3.6倍,与PBS免疫组相比有显著性差异(P<0.05),具有统计学意义(图8)。综合以上结果,合成肽EE14与DL18在弗氏佐剂存在情况下经皮下皮内免疫新西兰大白兔均能激发加强动脉粥样硬化的斑块生成
3 讨论
许多研究发现HSP65/60是致动脉粥样硬化因子,通过用从AS患者血清内获得抗体与健康人体获得的抗体对mHSP65和hHSP60进行抗原扫描,发现两者具有许多共有表位。用从卡介苗得到的mHSP65通过皮下注射免疫高脂膳食诱导的新西兰大白兔能诱发AS,用重组的mHSP65肌注免疫后也能观察到可明显加剧AS,然而,用HSP65经鼻粘膜途径免疫高脂高胆固醇膳食新西兰大白兔,发现结核分支杆菌HSP65经粘膜免疫不仅不会加剧AS,反而能有效防止AS的发生和发展。提示在HSP65中存在AS相关的功能性表位肽段,这种表位在皮下注射免疫时会诱发AS,但通过粘膜免疫却能激发旁路抑制,起到预防AS的作用。通过研究人与微生物HSP60/65的共有表位及各自特有表位是否能诱发动脉粥样硬化,可为动脉粥样硬化的免疫治疗找到精确靶点,也能利用分栋出的表位肽段发展抗动脉粥样硬化疫苗。前期研究中选择了HSP65中的T和B细胞表位构建多肽疫苗,经粘膜免疫后降低AS斑块形成的效果不明显,原冈口JI能是免疫过程中存在T表位对B表位功能的掩盖作用,因此本研究考虑利用直接合成B细胞表位后皮下注射免疫新西兰大白兔,单独观察HSP65上的B细胞表位皮下免疫后是否能明显增加AS斑块生成,如果出现预期的结果,可利用这些B细胞表位,进一步构建设计出具有强的免疫原性的表位多肽,通过粘膜免疫方法进行免疫,进一步实验研究出有效的抗AS疫苗。选择的EE14为佐剂性关节炎疾病相关重要表位,DL18为动脉粥样硬化患者出现抗HSP65抗体频率最高的几个B细胞表位之一,本研究中将表位与BSA偶联制备成偶联蛋白加以免疫以激发显著的免疫反应,结果表明两表位确实能加剧AS粥样硬化斑块的生成。
有研究表明,HSP65抗体水平的提高与AS和冠心病及临界高血压有关,HSP65/60抗体在AS的初始阶段通过自身免疫机制发挥作用。“表位扩展”是直接致病抗体缺乏情况下,抗原特异性B淋巴细胞促进疾病发生的重要机制,B淋巴细胞能通过提高递呈的效能和多样性促进疾病发展,在持续的免疫应答过程中,免疫系统可对隐蔽抗原表位相继发生免疫应答,即个别表位免疫后能诱导出针对大分子的抗体。在弗氏不完全佐剂仔在下进行免疫,以HSP65蛋白为包被抗原,DL18和EE14两组都未检测出有明显的抗HSP65抗体的产生,可能是HSP65分子太大,上面包含了大量的T或B细胞,而我们的合成肽片段太小,上面的表位太少,而难以诱导出针对整个大分子的抗体,说明单独的小分子表位肽段免疫过程中未出现所谓的“表位扩展”,即未扩展到针对HSP65的其他表位的免疫反应。两组分别以DL18和EE14为包被抗原,结果显示DL18免疫组在第一次免疫后的第3周即可测得血清中抗DL18抗体的产生,差异显著,具统计学意义(P 在血脂方面,EE14、DL18合成肽和PBS共同免疫新西兰大白兔,两组尽管后期能影响血清中TC含量,使之稍有升高,但并无明显的差异,即两组合成肽免疫组对新西兰大白兔的血脂(TC)含量没有产生明显影响。从抗HSP65抗体的产生情况看,与PBS组相比较两组合成肽免疫组都未能诱导出高的抗HSP65抗体,无明显差别。结合项目前期研究结果,出现高的抗HSP65抗体组同时也伴随高的血清TC含量,推测抗HSP65水平可能与对TC含量的影响有关。 从粥样硬化斑块占整个主动脉血管的面积比上看,合成肽DL18和EE14两免疫组都可明显加重AS斑块生成,其斑块面积与主动脉血管总面积百分比分别为36.75%与39.61%,约为PBS组的3.6倍和3.8倍,与PBS免疫组相比有显著性差异,具有统计学意义fP<0.05),因此合成肽EE14与DL18在弗氏佐剂存在情况下经皮下皮内免疫新西兰大白兔均能激发加强动脉粥样硬化的斑块生成。和前人研究结果之HSP65及其相关表位皮下注射免疫能加重AS保持了一致,表明所选择的表位在诱导免疫反应及增加AS斑块形成过程中起着重要作用,但作用机制需进一步研究。 综上研究结果,尽管从抗体生成角度和血脂水平还不能明确其加重AS斑块形成的机制,但通过所选表位经皮下免疫确实能诱发斑块加剧生成的结果。结合前面提到在HSP65分子中存在AS相关的功能性表位肽段皮下注射免疫是诱发加重AS斑块生成,可通过粘膜免疫却能激发旁路抑制,起到预防AS的作用。在后续实验中可以考虑基于这些B细胞表位设计出通过粘膜免疫方式进行免疫的抗AS疫苗,本课题也已在开展此方面的工作。再结合粘膜免疫的结果进一步研究这些表位的功能和免疫机制及进行抗AS斑块生成的免疫调节剂的设计与开发研究。
