膜性肾病患者肾组织肥大细胞的分布及病理意义
2014-04-27郑敬民刘志红
郑敬民,尹 广,刘志红
(南京军区南京总医院全军肾脏病研究所国家肾脏疾病临床医学研究中心,南京 210002)
膜性肾病是导致成人肾病综合征的一个常见原因。在我国,膜性肾病约占原发性肾小球肾炎的10%[1]。在西方,膜性肾病的比例则高达30%[2]。但有关膜性肾病的病理机制仍不是很清楚。
近年来,有关肥大细胞在各种肾脏疾病发生发展中的可能作用引起了不少研究者的关注。包括膜性肾病在内的各种主要肾脏病患者肾组织中,均存在肥大细胞增多的现象[3−9]。但目前对肾组织肥大细胞的确切病理意义仍不了解。从已有的文献来看,针对特定肾脏疾病肾组织肥大细胞的研究仍然不多,病例数也很有限,尤其是在国内,这方面的文献更少(就我们查阅的文献来看,尚未见国内有相关报道)。就膜性肾病而言,国外文献只笼统地报道了患者肾组织肥大细胞增多的现象,尚未见对不同病理类型膜性肾病患者肾组织肥大细胞的分类比较分析。本文对包括Ⅰ~Ⅳ期在内的不同病理类型膜性肾病患者肾组织中的肥大细胞及其与某些临床病理指标的相关性进行了定量分析,以比较全面地了解我国患者(汉族人)肾组织肥大细胞的分布特点,探讨肥大细胞在膜性肾病发生发展中的可能病理意义。
1 对象与方法
1.1 病例选择及相关病理资料的获取
从南京军区南京总医院全军肾脏病研究所肾活检组织标本库中选取临床和病理资料完整的特发性膜性肾病病例55例(Ⅰ~Ⅳ期分别为5例、26例、16例和8例)。所有病例的肾活检组织均经光镜、免疫荧光和电镜分析,符合有关特发性膜性肾病的诊断标准[10]。同时选取8例移植供肾组织标本作为正常对照,所选供肾组织病理分析均显示无明显病变。所有临床相关资料(包括生化检测结果等)从有关病历资料库中获取。本文所有研究均遵守《赫尔辛基宣言》原则,并获得本单位伦理委员会的批准。
1.2 肾组织肥大细胞检测和定量计数方法
根据肾组织肥大细胞特异性高表达C3aR的特点[11,12],以免疫组化的方法标记肾组织中的肥大细胞。光镜下摄取皮质区图像,计录每张切片肾组织皮质区中的肥大细胞数;同时利用NIS Element BR软件测量每张切片皮质区的肾组织面积;得到每平方毫米肾组织(皮质区)肥大细胞平均数(肥大细胞密度)。
1.3 免疫组化染色方法
肾活检组织石蜡切片经常规脱蜡和复水处理后,于高压锅中高压进行抗原修复;以3%过氧化氢甲醇溶液灭活内源性过氧化物酶;以10%胎牛血清封阻30min;经磷酸缓冲盐溶液(phosphate buffer saline,PBS)洗3次(5min/次)后,与兔抗人C3aR多克隆抗体(Santa Cruz公司)于4℃孵育过夜;再经PBS洗涤3次(5min/次)后,加Envision试剂(Dako公司)室温孵育45min;第三次PBS洗涤后进行二氨基联苯胺显色反应,然后以苏木素复染1min,自然风干后封片观察。
1.4 小管间质相对体积测量方法
参照Okon等[13]介绍的方法,每张切片随机选取皮质区10个区域,利用NIS Element BR3.4软件(Nikon,Japan)测量每个区域中的小管间质面积和区域中不含小球的面积,计算出小管间质面积所占的比例,以平均值代表每张切片的相对小管间质体积。
1.5 统计学处理
采用SPSS10.0软件进行统计分析。由于数据的正态性不佳,采用Kruskal-Wallis检验进行组间比较,Mann-Whitney检验进行两两比较,同时采用Bonferroni法进行校正。相关性分析采用Pearson法,以P<0.05为差异有统计学意义。
2 结果
2.1 肥大细胞在膜性肾病患者肾组织中的分布定位
免疫组化分析显示(图1),肥大细胞主要分布在膜性肾病患者肾组织的皮质及皮髓交界区,与皮质区相比,髓质中肥大细胞的数量明显要少得多。在皮质区,肥大细胞主要以一种松散的方式分布于小管间质中,常出现在小管间质增宽的区域,分布于萎缩的小管和损伤小球的周围。多数情况下,肥大细胞并不与小管间质中其他炎症细胞扎堆分布(图1B-D),在有大量炎症细胞浸润的区域,肥大细胞的数量往往不多。虽然在绝大多数膜性肾病患者的肾小球中观察不到肥大细胞,但在少数病例的一些小球(在我们所分析的55例中的5例),可见肥大细胞侵入肾小球的情况(图1E-F),这与我们以前在糖尿病性肾病和IgA肾病等观察到的情况有所不同(以前在肾小球中从未观察到肥大细胞)[8,9]。在不同病理类型的膜性肾病肾组织中,没有观察到肥大细胞在分布方式上有明显差异。
2.2 不同病理类型膜性肾病患者肾组织肥大细胞数量统计分析结果
正常对照肾组织中极少发现肥大细胞。与正常对照组相比,各种病理类型膜性肾病患者肾组织肥大细胞数量(密度)均有不同程度的增加。Ⅰ期膜性肾病患者肾组织肥大细胞的数量相对较少,而其他病理类型间的差异并不显著(图2)。
2.3 膜性肾病患者肾组织肥大细胞与临床病理指标的相关性分析结果
基于双变量Person模型相关分析显示,膜性肾病患者肾组织肥大细胞数量(密度)与患者血肌酐水平(r=0.464,P<0.001)、血胱抑素C(cystatin C,Cys C,r=0.464,P<0.01)、尿视黄醇结合蛋白(retinol-binding protein,RBP,r=0.322,P=0.024)、尿N-乙酰基-β-氨基葡萄糖苷酶(N-acetyl-β-glucosaminidase,NAG,r=0.453,P<0.001)、尿α微球蛋白(r=0.351,P=0.013)、尿C3水平(r=0.334,P<0.018)、以及小管间质相对体积具有显著相关性(r=0.636,P<0.001),其中以与小管间质相对体积的相关性最高。而与24h尿蛋白、尿溶菌酶水平,以及性别等没有显著相关性。

图1 肥大细胞(黑色箭头所示)在不同病理类型膜性肾病患者肾组织中的分布情况Figure1 The distribution of mast cells (indicated by black arrows) in the renal tissue of patients with membranous nephropathy(×200)
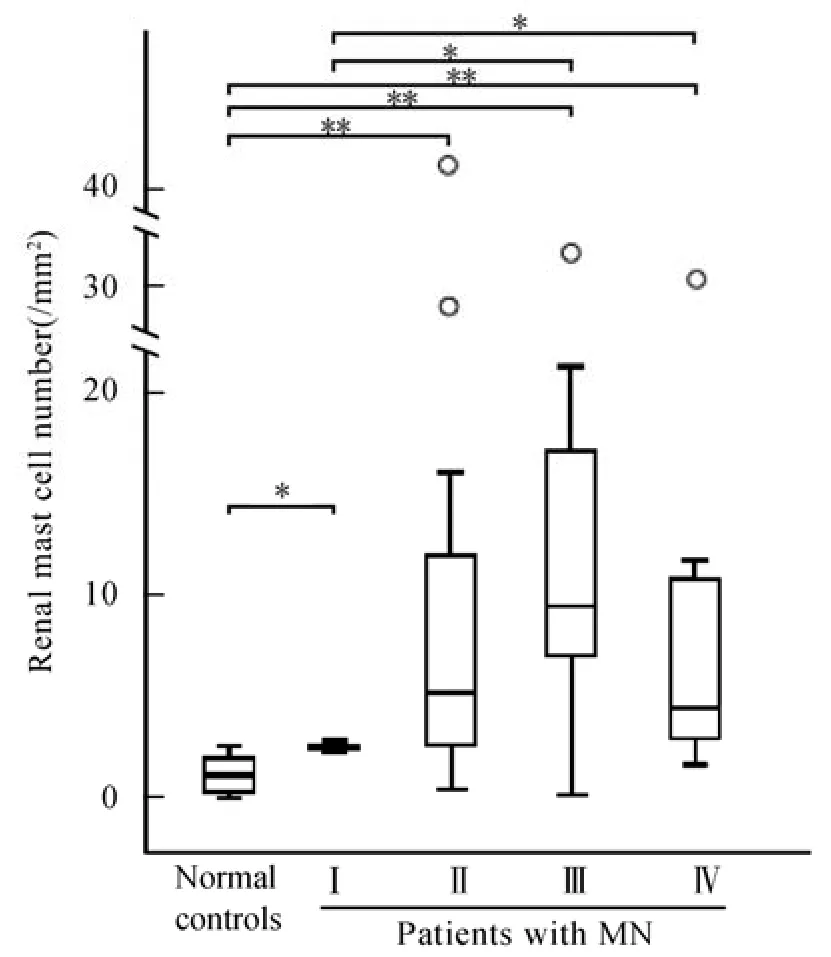
图2 不同病理类型膜性肾病患者肾组织肥大细胞数比较Figure2 Comparison of renal mast cell number in patients with different pathological types of membranous nephropathy
3 讨论
本文首次对我国(汉族人)膜性肾病患者肾组织肥大细胞进行了观察,并与国际上首次对不同病理类型膜性肾病患者肾组织肥大细胞进行了比较分析。从我们的分析结果来看,在膜性肾病患者肾组织中,肥大细胞主要是以一种松散的方式分布于肾小管间质,常出现在小管间质增宽的区域,特别是萎缩的小管和损伤小球的周围。这与肥大细胞在其他肾脏疾病中的分布相似[3−9]。但在本文,我们还在少数病例的一些肾小球中也观察到了肥大细胞的存在,特别是在硬化小球中,有时可观察到较多的肥大细胞浸润。这是我们以前对其他疾病的分析中所从未见到的[8,9]。文献上[3−7,14−16]。也未见有肥大细胞出现在肾小球中的报道。但这是否是膜性肾病特有的病理现象,以及产生这一病理现象的原因,仍有待于进一步的研究。基于膜性肾病的病理分类分析显示,不同病理类型膜性肾病的肾组织肥大细胞在分布方式上并未观察到明显的差异。与已往研究一致[3−9],在本文中,我们观察到正常肾组织中极少有肥大细胞。与正常对照相比,膜性肾病患者肾组织肥大细胞的数量显著增加。相对而言,Ⅰ期患者肾组织肥大细胞的数量较少,而其他组间的差异并不显著。相关性分析显示,膜性肾病患者肾组织肥大细胞与反映肾功能损伤程度的指标(血肌酐和Cys C)和小管间质损伤指标(包括NAG、尿视黄醇结合蛋白和小管间质相对体积)具有显著相关性。这些结果提示:(1)肥大细胞参与了膜性肾病患者肾组织损伤过程;(2)肥大细胞主要与小管和小管间质损伤有关,可能在膜性肾病慢性化病变中起重要作用;(3)在一些特定生理情况下,肥大细胞可能与膜性肾病患者肾小球的损伤有关。
需要特别指出的是,在本文的研究中,我们对不同病理类型膜性肾病患者肾组织肥大细胞进行了分类分析,虽然总的病例数并不少,但涉及到每一病理类型的病例仍很有限,因此,对于不同病理类型中的情况,仍有待于进一步扩大每组病例数进行观察,以便得出更加可靠的结论。
总之,本文的研究结果提示,肥大细胞很可能参与了膜性肾病肾组织损伤,特别是小管间质损伤的过程。肥大细胞作为一种新的致病因素以及一个潜在的膜性肾病肾组织慢性病变防治新靶标,值得我们关注。
【参考文献】
[1]Li LS, Liu ZH.Epidemiologic data of renal diseases froma single unit in China: analysis based on 13 519 renal biopsies[J].Kidney Int, 2004, 66(3): 920−923.
[2]Cattran DC.Idiopathic membranous glomerulonephritis[J].Kindney Int, 2001, 59(5): 1983−1994
[3]Papadimitriou JC, Drachenberg CB, Ramos E,et al.Mast cell quantitation in renal transplant biopsy specimens as a potential marker for the cumulative burden of tissue injury[J].Transplant Proc, 2013, 45(4): 1469−1471.
[4]Watanabe S, Miyata Y, Matsuo T,et al.High density of tryptase-positive mast cells in patients with renal cell carcinoma on hemodialysis: correlation with expression of stem cell factor and protease activated receptor-2[J].Hum Pathol, 2012, 43(6): 888−897.
[5]Welker P, Krämer S, Groneberg DA,et al.Increased mast cell number in human hypertensive nephropathy[J].Am J Physiol Renal Physiol, 2008, 295(4): F1103−F1109.
[6]Silva GE, Costa RS, Ravinal RC,et al.Mast cells,TGF-beta1 and alpha-SMA expression in IgA nephropathy[J].Dis Markers, 2008, 24(3): 181−190.
[7]Togawa H, Nakanishi K, Shima Y,et al.Increased chymase-positive mast cells in children with crescentic glomerulonephritis[J].Pediatr Nephrol, 2009, 24(5):1071−1075.
[8]Zheng JM, Yin G, Wang JP,et al.Mast cell infiltration in the renal tissue in patients with IgA nephropathy[J].J Nephol Dialy Transplant, 2011, 20(2): 114−119.[郑敬民,尹 广, 王建平, 等.IgA肾病患者肾组织肥大细胞的分布及意义[J].肾脏病与透析肾移植杂志, 2011, 20(2):114−119.]
[9]Zheng JM, Yao GH, Cheng Z,et al.Pathogenic role of mast cells in the development of diabetic nephropathy: a study of patients at different stages of the disease[J].Diabetologia, 2012, 55(3): 801−811.
[10]Li LS, Liu ZH.Chinese Nephrology[M].Beijing: People’s Military Medicine Press, 2008: 387−399.[黎磊石, 刘志红.中国肾脏病学[M].北京: 人民军医出版社, 2008:387−399.]
[11]Zheng JM, Zhu XD, Zhang MC,et al.Mast cells highly expressing C3aR were found in the kidney of diabetic nephropathy and correlated with the development of the disease[J].Prog Biochem Biophys, 2011, 38(3): 262−268.[郑敬民, 朱小东, 张明超, 等.高表达C3aR的肥大细胞在糖尿病肾病患者肾组织中的分布及病理意义分析[J].生物化学与生物物理进展, 2011, 38(3): 262−268.]
[12]Zheng JM, Zhu XD, Zhang MC,et al.C3aR: a sensitive marker for renal mast cells[J].J Nephrol Dialy Transplant,2011, 20(4): 319−324.[郑敬民, 朱小东, 张明超, 等.C3aR——检测肾组织肥大细胞的敏感标志[J].肾脏病与透析肾移植杂志, 2011, 20(4): 319−324.]
[13]Okon K, Szumera A, Kuzniewski M.Are CD34+cells found in renal interstitial fibrosis[J]? Am J Nephrol, 2003,23(6): 409−414.
[14]Silver RB.Role of mast cells in renal fibrosis[J].Kidney Int, 2013, 84(1): 214.
[15]Ehara T, Shigematsu H.Mast cells in the kidney[J].Nephrology(Carlton), 2003, 8(3): 130−138.
[16]Gilfillan AM, Austin SJ, Metcalfe DD.Mast cell biology:introduction and overview[J].Adv Exp Med Biol, 2011,716: 2−12.
