梗阻性无精子症动物不同显微外科吻合技术的实验研究
2014-04-23钱海宁李朋马猛李
钱海宁李 朋马 猛李 铮*
1. 上海市交通大学医学院附属同仁医院泌尿外科(上海 200336); 2. 上海交通大学附属仁济医院泌尿外科,上海市人类精子库
梗阻性无精子症动物不同显微外科吻合技术的实验研究
钱海宁1李 朋2马 猛2李 铮2*
1. 上海市交通大学医学院附属同仁医院泌尿外科(上海 200336); 2. 上海交通大学附属仁济医院泌尿外科,上海市人类精子库
目的研究梗阻性无精子症动物模型的制作方法,比较不同显微外科吻合技术的优缺点。方法将20只6周龄雄性SD大鼠随机分成5组,包括假手术组、对照组、双针纵向输精管附睾套叠式吻合(VE)组、单针VE组、逆向单针VE组。除了假手术组外,各组大鼠都行近附睾端双侧输精管结扎术,制作梗阻性无精子症的动物模型;2周后分别行双针VE、单针VE、逆向单针VE,对照组只行输精管结扎术,假手术组我们把睾丸移出腹腔后再移回原位。12周后处死大鼠,检测吻合口和输精管结扎处精子肉芽肿形成情况,从输精管的腹腔端向附睾注射美兰,检测吻合口的机械再通率。结果双针VE组,单针VE组,逆向单针VE组的机械再通率分别是100%、75%、87.5%,精子肉芽肿的形成率分别是12.5%、12.5%、12.5%,平均手术时间是(38.1±4.3)min、(42.3±2.9)min、(41.0±3.3)min。结论双侧近附睾端输精管结扎制作梗阻性无精子症动物模型的方法简单、可靠,适用于显微VE技术训练。单针法VE可以获得双针VE法相同的疗效,节约手术成本,在缺少双针缝线时不失为实用、有效的替代手术方法,逆向单针VE术能降低误缝输精管对侧粘膜的概率。
无精子症/外科学; 显微外科手术
Key woorrddssazoospermia/surgery; microsurgery
在男性不育症的患者中,6.1%[1]~13.6%[2]的患者诊断为梗阻性无精子症,除去输精管结扎的原因,大部分梗阻性无精子症是由双侧附睾梗阻引起。对于附睾梗阻,输精管附睾吻合术(vasoepididymostomy, VE)是解除梗阻的唯一方法,手术成功率与外科医生的显微外科经验密切相关[3,4]。本研究使用双侧近附睾端输精管结扎的方法制作梗阻性无精子症的大鼠模型,同时分析双针VE吻合法、单针VE吻合法和逆向单针VE吻合法的术后效果。
材料和方法
一、动物取材
20只6周龄雄性SD大鼠(体重240g),随机分成5组,每组4只,分别是假手术组、对照组、双针吻合组、单针吻合组、逆向单针吻合组。
二、建立附睾梗阻大鼠模型
手术时使用10%水合氯醛行腹腔麻醉。除外假手术组,所有大鼠行双侧近附睾端输精管结扎术。麻醉成功后,打开大鼠的腹腔,找到睾丸移出切口,辨认分离输精管附睾结合部位,在结合点使用4-0手术缝线结扎输精管。双侧完成后,睾丸放回原位,3-0可吸收缝线关闭腹腔。假手术组我们把睾丸移出腹腔后再移回原位。
三、VVEE
建立附睾梗阻模型2周后,行VE术。10%水合氯醛腹腔麻醉后,沿着原先腹部手术疤痕切开腹壁,睾丸移出切口。钝性游离睾丸和输精管。在4~25倍的手术显微镜下完成VE。在输精管梗阻点的腹侧切断输精管,4-0缝线结扎输精管附睾侧断端。在附睾尾部寻找并游离一根比较饱满的附睾管用于吻合。用9-0缝线将输精管腹侧断端和待吻合附睾管附近的附睾背膜缝合,减少吻合口张力。
(一)双针VE
使用两根10-0双针缝线纵向套叠式吻合输精管和附睾管。首先,沿着选定的附睾管纵向平行放置2根双针缝线的一面缝针,为了防止管腔凹陷,缝针不要抽出附睾管壁。在2根缝针之间使用显微侧切刀纵向切开附睾管,见附睾液流出,然后抽出缝针。在输精管腹侧断端管腔内均等分选定4个缝合点,缝针采用内进外出的方式穿过缝合点。2根缝线打结后,附睾管就套叠进输精管腔内。
(二)单针VE
使用两根10-0单针缝线纵向套叠式吻合输精管和附睾管。第一根缝线首先在输精管头侧断端11点位用外到内的方式穿过输精管的粘膜层,然后缝针纵向穿过附睾管管壁,不要抽出缝针以防止管壁凹陷,同样方法在输精管头侧断端1点放置第二根,第二根缝针在输精管和附睾管的位置于第一根缝针平行。在2根缝针之间使用显微侧切刀纵向切开附睾管,见到附睾液,然后抽出缝针。第一根缝针在输精管腹侧断端的7点位由内到外的方式穿过输精管粘膜层,第二根缝针在5点位同样处理。2根缝线打结后,附睾管就套叠进输精管腔内。
(三)逆向单针VE
和单针VE基本相似,主要不同点在于,先从输精管腹侧断端的7、5点位由外到内穿过输精管粘膜,同样缝合附睾管后在输精管断端11、1点位由内到外穿过输精管粘膜(图1)。
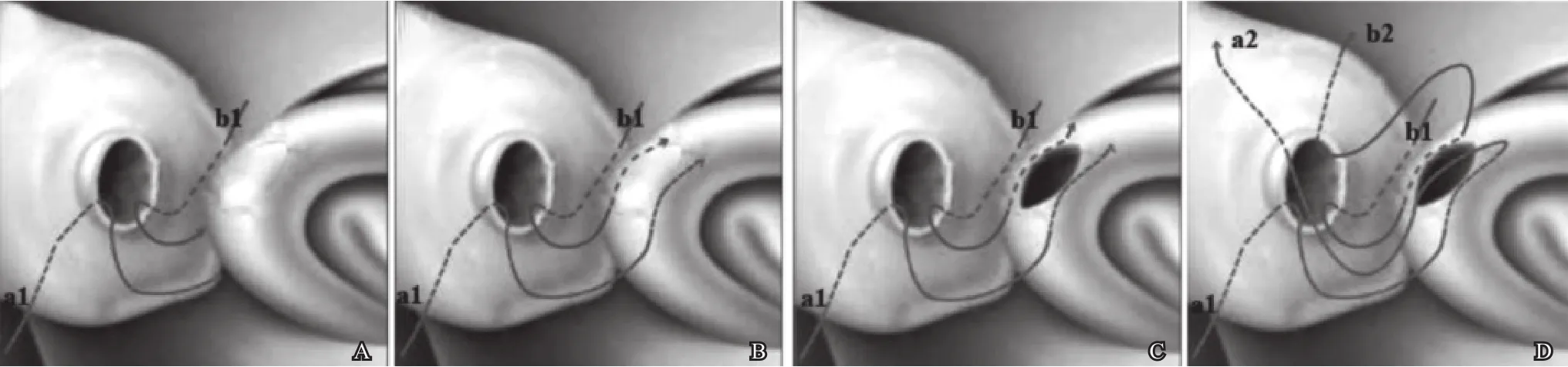
图1 逆向单针纵向套叠输精管附睾吻合术
四、术后检测
VE后12周后处死大鼠,检测精子肉芽肿形成情况。检测吻合口的机械再通率,从输精管附睾管吻合口的腹腔端向附睾注射美兰,如果美兰通过吻合口,进入附睾或睾丸组织,则认为吻合口通畅。
五、统计学分析
用费雪尔精确检验(Fisher’s exact test)方法比较各组机械再通率、精子肉芽肿发生率和手术时间,P<0.05表示差异有显著性意义。
结 果
在实验过程中没有动物死亡,也没有发生手术后的感染。三种吻合方法手术所需时间、术后机械再通率和精子肉芽肿形成率见表1。三种手术方法的机械再通率分别为,100%(双针VE)、75%(单针VE)、87.5%(逆向单针VE),无显著性统计学差异(P>0.05);3种手术方法吻合口周围精子肉芽肿形成率分别为12.5%、25%、25%,无显著性统计学差异(P>0.05)。平均手术时间单针VE(42.3±2.9)min和逆向单针VE(41.0±3.3)min之间差别不大,比双针VE(38.1±4.3)略长,无显著统计学差异。

表1 3种VE吻合术方法的手术效果
讨 论
VE的成功率和手术医生的显微外科经验、技术密切相关,选择合适的动物制作梗阻性无精子症动物模型用于手术技术培训非常重要。大鼠附睾管腔的直径大约0.25mm,梗阻后扩张至0.5mm[5],人附睾管直径0.33mm梗阻后扩张至0.5mm,两者比较接近,而且大鼠容易获得,性价比较高,所以我们选择大鼠制备附睾梗阻的动物模型,用于培训医生的显微外科技术。行输精管结扎时,应选择输精管附睾交界处结扎,这样做有利于后期吻合,同时梗阻点和附睾炎引发的附睾输精管梗阻点相似,比较符合国内梗阻性无精子症多为附睾炎引发的临床特点。结扎后不切断输精管,可以减少出血,降低术后粘连和精子肉芽肿的发生,也便于在行吻合术时寻找输精管。动物模型建立2周后,附睾和附睾管可见明显扩张,直径约为0.5mm。我们在实验时发现延长大鼠梗阻时间(4~8周)无助于附睾管腔的进一步扩张,反而因大鼠体重上升,腹腔内脂肪堆积增加VE的难度。
国外很多文献比较VE治疗和辅助生殖技术(ART)两种方法治疗梗阻性无精症效果、并发症和费用后认为:对于生精功能正常的梗阻性无精子症患者,如果配偶生育功能正常,通过VE获得下一代的性价比高于辅助生殖技术(包括IVF和ICSI)[6-9],而且避免ART的缺点,例如卵巢过度刺激综合征、多胞胎、早产和低体重新生儿等等,同时成功的吻合术满足了再次生育的要求。但是相比ART在国内发展迅猛,遍地开花,VE技术在国内只有少数地区开展,我们通过动物实验对3种VE吻合方法进行比较,希望有助于在更多地区开展这一技术。
在男性不育患者中,梗阻性无精子症是少数几种能通过手术去处病因彻底治愈的疾病。特别是引入显微外科吻合技术后,手术后精道再通率不断提高,最近报道双针纵向套叠VE的再通率达到90%~100%[11-14]。双针纵向套叠VE时,缝合输精管时全部缝针都是内进外出,手术操作相对简单,也避免了误缝输精管对侧粘膜,术后再通率高。缺点是许多医疗资源有限的地区,很难获得吻合使用的双针缝线,阻碍双针输精管附睾吻合技术的推广普及。在本次动物实验中,我们使用单针缝线行输精管附睾管吻合术,2种单针吻合方法在穿越输精管粘膜时先用显微镊子轻轻撑开输精管管腔,然后再进针,进针方向先都是外进内出,再内进外出,这样也可以避免误缝对侧粘膜,术后再通率同样令人满意[10]。单针显微缝线容易获取,大多数地区的泌尿外科医生就有机会使用单针缝线学习和实施VE,有利于这一技术的推广普及。
在本次动物实验中,双针VE的再通率达到100%,和已有文献报道再通率90%~100%[11-14]接近。2种单针吻合技术和双针吻合一样都能使附睾管套叠进输精管,这3种方法手术后输精管和附睾管的相对构型是完全相同的,只是进针方向和顺序不同。双针法针先穿过附睾管,然后所有4根针由内向外出穿过输精管粘膜。单针法针先从11、1点位由外到内穿过输精管粘膜,缝合附睾管后在7、5点位由内到外穿过输精管粘膜。逆向单针法先从输精管腹侧断端的7、5点位由外到内穿过输精管粘膜,同样缝合附睾管后在输精管断端11、1点位由内到外穿过输精管粘膜。理论上,这3种不同缝合方法得到的吻合口是相同的。
本次实验中2种单针吻合组术后再通率和双针组有差别,但是差别没有统计学意义,双针吻合的优势是所有4根针内进外出穿过输精管粘膜,避免误缝对侧粘膜。我们在本次动物实验中发现外进内出穿过输精管粘膜时,先用显微镊子轻轻撑开输精管管腔,扩张输精管内腔,可以防止误缝对侧粘膜引起吻合口梗阻,使得单针法吻合输精管附睾管获得同双针法相近的再通率。大鼠的输精管和附睾管的管径和人接近,结构相似,我们有理由相信单针缝合人的输精管和附睾管时也不会误缝对侧粘膜引起吻合口梗阻。逆向单针吻合先从输精管7、5点位由外向内进针,对侧粘膜(11、1点位)清楚暴露在手术视野下,彻底避免了误缝对侧粘膜,这是逆向单针吻合的优势所在。
3组实验动物均发现有精液肉芽肿形成,双针组1处,单针和逆向单针组各2处,组间差别无统计学意义。精液肉芽肿是由吻合口处漏出精液刺激周围组织形成炎症反应而产生[15],我们发现有精液肉芽肿形成的5例吻合口只有1例不通畅,说明精液肉芽肿的形成和VE后的机械再通率没有关系[15-17]。但是吻合口处精液漏出很有可能导致远端输精管内没有精液,造成手术失败。为了减少精液肉芽肿的形成,是否需要在吻合口的粘膜外层更多缝合或者加缝1层,需要进一步的实验研究。
单针组和逆向单针组的手术时间稍长于双针组,但差别没有统计学意义。事实上3种吻合方法缝针穿过输精管、附睾管的次数是一样的,缝线打结的数目也是相同的,我们相信通过一定时间单针吻合的训练后,3种VE手术时间差别会越来越小。2种单针吻合术的技术难度不比双针吻合术高,掌握双针吻合技术的泌尿外科医生很容易学会单针吻合技术[15]。因此,单针、逆向单针法VE是治疗梗阻性无精子症有效且容易推广的方法。
大鼠双侧近附睾端输精管结扎制作的梗阻性无精子症动物模型和临床输精管附睾梗阻的病例相似,满足显微输精管附睾吻合技术训练要求。单针法输精管附睾套叠式吻合安全、可行,可以获得双针法相同的疗效,节约手术成本,在没有双针缝线的地区也可以开展显微VE,逆向单针的优势是能降低误缝输精管对侧粘膜的概率。
1 Aziz N, Agarwal A, Nallella KP, et al. Relationship between epidemiological features and aetiology of male infertility as diagnosed by a comprehensive infertility service provider. Reprod Biomed Online 2006; 12(2)∶209-214
2 Jequier AM. Obstructive azoospermia∶ a study of 102 patients. Clin Reprod Fertil 1985; 3(1)∶ 21-36
3 Chawla A, O’Brien J, Lisi M, et al. Should all urologists performing vasectomy reversals be able to perform vasoepididymostomies if required? J Urol 2004; 172(3)∶1048-1050
4 Thomas AJ Jr. Infertility. J Urol 2004; 172(3)∶ 829-830
5 Young GPH, Li PS, Gardner TA, et al. Animal models for microsurgical training and research, in Goldstein M (Ed)∶ Surgery of Male Infertility. Philadelphia, WB Saunders, 1995, 297-320
6 Baker K, Sabanegh ES Jr. The Role of Microsurgical Reconstruction in the Era of ICSI. In∶ Sandlow JI (ed). Microsurgery for Fertility Specialists∶ A Practical Text. New York∶ Springer Science+Business Media; 2013. p.153-166
7 Pavlovich CP, Schlegel PN. Fertility options after vasectomy∶ a cost-effectiveness analysis. Fertil Steril 1997; 67(1)∶ 133-141
8 Kolettis PN, Thoas AJ Jr. Vasoepididymostomy forvasectomy reversal∶ a critical assessment in the era of intracytoplasmic sperm injection. J Urol 1997; 158(2)∶467-470
9 Donovan JF Jr, DiBaise M, Sparks AE, et al. Comparison of microscopic epididymal sperm aspiration and intracytoplasmic sperm injection/in-vitro fertilization with repeat microscopic reconstruction following vasectomy∶ is second attempt vas reversal worth the effort? Hum Reprod 1998; 13(2)∶ 387-393
10 Peng J, Yuan Y, Zhang Z, et al. Patency rates of microsurgical vasoepididymostomy for patients with idiopathic obstructive azoospermia∶ a prospective analysis of factors associated with patency-single-center experience. Urology 2012; 79(1)∶ 119-122
11 Smrkolj T, Virant-Klun I, Sinkovec J, et al. Epididymovasostomy as the first-line treatment of obstructive azoospermia in young couples with normal spermatogenesis. Reprod Biomed Online 2010; 20(5)∶ 594-601
12 Ho KL, Wong MH, Tam PC. Microsurgical vasoepididymostomy for obstructive azoospermia. Hong Kong Med J 2009; 15(6)∶ 452-457
13 Kumar R, Mukherjee S, Gupta NP. Intussusception vasoepididymostomy with longitudinal suture placement for idiopathic obstructive azoospermia. J Urol 2010; 183(4)∶ 1489-1492
14 Chan PT, Lee R, Li PS, et al. Six years of experience with microsurgical longitudinal intussusception vasoepididymostomy (LIVE)∶ a prospective analysis. Proceedings of the 2008 Annual Meeting of the American Urological Association; 17-22 May 2008; Orlando, FL, USA. Abstract.
15 Monoski MA, Schiff J, Li PS, et al. Innovative singlearmed suture technique for microsurgical vasoepididymostomy. Urology 2007; 69(4)∶ 800-804
16 Stefanovic KB, Clark SA, Buncke HJ. Microsurgical epididymovasostomy by tubule intussusception∶ a new technique in rat model. Fertil Steril 1991; 55(1)∶ 189-193
17 Goldstein M∶ Surgical management of male infertility and other scrotal disorders, in Walsh PC, Retik AB, Vaughan ED, et al (Eds)∶ Campbell’s Urology, 8th ed. New York, WB Saunders, 2002, pp 1532-1588. 804
(2013-10-13收稿)
Study on different microsurgical anastomosis in the treatment of rat model with obstructive azoospermia
Qian Haining1, Li Peng2, Ma Meng2, Li Zheng2*
1. Department of Urology, Tong Ren Hospital, Shanghai Jiaotong University School of Medicine, Shanghai 200336, China; 2. Department of Urology, Ren Ji Hospital, Shanghai Jiaotong University School of Medicine Shanghai Human Sperm Bank
ObjectiveeTo study the method of making of obstructive azoospermia(OA) animal model, and compare the advantages and disadvantages of different microsurgical anastomosis.MetthhooddssTotal of 20 male SD rats (6-week-old) were randomly divided into 5 groups, including the sham operation group, the control group, the standard double-armed longitudinal intussusception vasoepididymostomy(VE) group, the single-armed and reverse single-armed longitudinal intussusception vasoepididymostomy groups. All rats except those in the sham operation group were treated with bilateral vasectomy (closed epididymis) to make obstructive azoospermia(OA) rat model. Two weeks after vasectomy, bilateral standard double-armed longitudinal intussusception vasoepididymostomy(VE), single-armed and reverse single-armed longitudinal intussusception vasoepididymostomy were performed in the assigned rats. Rats in the control group underwent vasectomy only. In the sham operation group, the testes of rats were moved out of the scrotum and then returned. Rats were sacrificed after 12 weeks. The anastomosis and vasectomy sites were inspected for sperm granuloma. Patency was confirmed by injecting Methylene blue from the abdominal end of the vas through the anastomoses to epididymis.RessuullttssIn the standard double-armed longitudinal intussusception vasoepididymostomy(VE), the single-armed and reverse single-armed longitudinal intussusceptionvasoepididymostomy groups, the patency rates were 100%, 75%, and 87.5%, sperm granuloma rates were 12.5%, 12.5% and 12.5%, the average operation times were 38.1±4.3min, 42.3±2.9 min, and 41.0±3.3 min, respectively.ConclussiioonnBilateral vasectomy (closed epididymis) is reliable, simple method to make obstructive azoospermia(OA) animal model, suitable for performing microscopic vasoepididymostomy(VE) training. This study suggests that the single-armed suture technique for vasoepididymostomy performing is almost as effective as the double-armed technique and can save operation cost. It allows the use of single-armed sutures to perform microsurgical vasoepididymostomy, in which double-armed sutures are not available. Reverse single-armed longitudinal intussusception vasoepididymostomy can reduce the probability of back-walling the tubular lumen.
∶ Li Zheng, E-mail∶ Lizhengboshi@163.com
R 698.2; R 699.8
*通讯作者, E-mail∶ Lizhengboshi@163.com
ddooii∶10.3969/j.issn.1008-0848.2014.02.012
