艾瑞昔布治疗膝骨关节炎的Ⅲ期多中心随机双盲临床试验
2014-04-09张奉春古洁若徐建华张凤肖何培根鲍春德肖卫国
徐 东,张奉春,古洁若,徐建华,陶 怡,张凤肖, 何培根,鲍春德,肖卫国
(中国医学科学院 北京协和医学院 北京协和医院风湿免疫科,风湿免疫病学教育部重点实验室,北京 100730)
ChinJAllergyClinImmunol,2014,8(3):205- 210
艾瑞昔布为环氧化酶(cyclooxygenase,COX)-2抑制剂,是由中国医学科学院药物研究所和江苏恒瑞医药股份有限公司共同开发的具有自主知识产权的非甾体抗炎药。艾瑞昔布Ⅱ期临床试验证实该药可有效且安全治疗骨关节炎(osteoarthritis,OA),本研究为药物Ⅲ期临床试验,在Ⅱ期临床试验基础上扩大参加单位,以塞来昔布为阳性对照药,评价艾瑞昔布(100 mg,2次d)治疗膝OA的有效性和安全性。
对象和方法
研究方案
本试验为多中心、随机、双盲、阳性药物平行对照临床试验,研究方案得到北京协和医院伦理委员会批准认定并报国家药品食品监督管理局备案。
研究对象
入选标准:(1)所有病例均为2008年4月至12月间门诊入组并符合美国风湿病协会原发性膝OA的分类标准[1],关节功能Ⅰ级至Ⅲ级;(2)年龄40~70岁;(3)生育期或绝经时间少于2年的妇女,试验期间必须采取充分避孕措施,哺乳期妇女不能入选;(4)存在受累关节的受试者,其可视疼痛评分(visual analog scale, VAS)≥40 mm;(5)存在胃肠道症状者上消化道纤维镜检查合格。
排除标准:(1)继发性OA;(2)长期服用小剂量阿司匹林者;(3)筛选前6个月内有严重器官受累者;(4)已知对磺胺类和昔布类药物过敏,以及先前参加过艾瑞昔布试验者。
脱落标准:无论因何退出,未完成临床试验全程观察者均为脱落病例。
剔除标准:(1)入组后发现受试者不符合纳入标准或符合排除标准;(2)使用了方案规定的禁用药品;(3)不能按规定用药,依从性差,无法判断疗效或资料不全等影响疗效和安全性判断者。
分组和给药方案
按照3:1随机化原则分为试验组和对照组。试验组:早上口服艾瑞昔布片1片+塞来昔布胶囊模拟药1粒,晚上口服艾瑞昔布片1片;对照组:早上口服艾瑞昔布片模拟药1片+塞来昔布胶囊1粒,晚上口服艾瑞昔布片模拟药1片,疗程8周。
观察指标
临床观察指标:治疗前及治疗2、4、8周时,进行膝关节疼痛、僵硬、日常活动难度评分,同时记录受试者和医生对疾病状况的总体评价。
实验室和辅助检查:治疗前及治疗2、4、8周时,行肝肾功能、凝血功能、血常规、尿常规、便隐血检查。治疗前后各做1次心电图。育龄妇女治疗前作妊娠试验。试验前即存在或用药后出现胃肠道症状,血色素下降和大便潜血阳性并判断与试验药物有关者,需进行胃镜检查;无症状者选做胃镜检查;进行胃镜检查的病例数须占总病例14以上。
疗效及安全性评价
疗效评价:治疗2、4、8周时进行疗效评价。主要疗效指标为平地行走疼痛程度评分,根据疼痛下降指数评定疗效等级和有效率。疗效等级定义为有效和显效,有效为临床症状和体征改善≥50%但<75%,显效为疗程结束后炎性症状与体征基本消失或减轻≥75%。有效率=(显效例数+有效例数)病例总数×100%。次要疗效指标包括僵硬[骨关节炎调查量表(WOMAC VA 3.0)问题6~7]、进行日常活动的难度(WOMAC VA 3.0问题8~24)、WOMAC VA 3.0亚组总平均分、受试者及研究者对疾病状况及治疗反应的总体评价。
安全性评价:不良事件及不良反应发生情况,治疗前后实验室检查和胃镜检查结果。
统计学处理
有效性评价:对主要疗效指标的两组比较采用考虑中心效应的CMH方法;各个单个疗效指标的改善程度组内比较采用配对t检验,组间比较用成组t检验。
安全性评价:监测生命体征,组内比较采用配对t检验,改变值的组间比较采用t检验。不良事件及不良反应采用统计描述方法。
数据管理与统计分析软件:数据管理采用EPiData 3.0,采用双份独立输入。统计分析采用SAS 9.1.3软件编程分析。除主要疗效指标的非劣效性检验外,其他所有假设检验均采用双侧检验(two-side test)。取α=0.05,P≤0.05认为差异具有统计学意义。所有可信区间的可信度均取95%。
结 果
一般资料
共入组469例患者,其中试验组351例,对照组118例,入组阶段各项资料表明两组受试者可比性良好,差异均无统计学意义(P>0.05)。共脱落44例,其中试验组35例,对照组9例,总脱落率9.38%(44/469),试验组脱落率9.97%(35/351),对照组脱落率7.63%(9/118)。共剔除5例,全部为试验组患者,总剔除率1.07%(5/469),试验组剔除率1.42%(5/351)。进入全分析集(full analysis set,FAS)、符合方案集(per protocol set,PPS)和安全性分析集(safety analysis set, SAS)的总病例数分别为461例、420例和461例,试验组病例数分别为344例、311例和344例,对照组病例数分别为117例、109例和117例。治疗各阶段(0~2周、2~4周、4~8周),两组受试者平均实际用药量均在理论用药量的 80%~120%范围内,组间差异均无统计学意义(P>0.05),两组受试者整体用药依从性良好。治疗各阶段用药量比较结果示,两组受试者用药量可比性较好。
疗效评价
疗效评价分别进行FAS和PPS分析。
平地行走疼痛程度:(1)程度评分比较。试验组和对照组治疗2、4和8周评分差异均无统计学意义(均P>0.05),FAS分析见表1。(2)程度评分下降值和下降率比较。两组受试者治疗后平地行走疼痛程度评分下降值及下降率明显较治疗前降低,组内治疗前后比较差异均有统计学意义(均P<0.0001)。组间比较显示,试验组治疗下降值及下降率均高于对照组,FAS分析组间差异无统计学意义(P>0.05)(表2、3);PPS分析,下降值第4周差异有统计学意义(P<0.05),其他两个时间段组间差异无统计学意义(P>0.05),下降率组间差异无统计学意义(P>0.05)。(3)对主要疗效指标平地行走疼痛程度评分进行非劣效性检验,两组下降值的非劣效性检验,非劣效界值取δ=1分,试验组与对照组之差的95%可信下限=-0.408,t=6.043,P=0.0000,试验组非劣于对照组。
疼痛疗效:治疗2、4、8周,两组间显效率和有效率差异无统计学意义(P>0.05)(表4、5)。考虑中心分层的CMH-χ2检验及中心齐同性检验见表5。两组有效率非劣效性检验(非劣效界值取10%)显示,两组率之差的95%可信下限=-9.26%,u=1.784,P=0.0372,试验组非劣于对照组。
疼痛程度总分、下降值和下降率比较:治疗2、4及8周,试验组和对照组疼痛程度差异无统计学意义(P>0.05)。疼痛程度总分下降值和下降率组内治疗前后比较,差异均有统计学意义(P<0.000 1),组间比较差异均无统计学意义(P>0.05)。
表1试验组和对照组治疗后平地行走疼痛程度评分比较(全分析集)
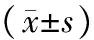

分组治疗2周治疗4周治疗8周对照组(n=117)422±175355±199301±197试验组(n=344)393±184322±183273±192t值146162137P值014410105901711

表2 试验组和对照组治疗后平地行走疼痛程度评分下降值比较(全分析集)
试验组共344例患者,对照组共117例患者

表3 试验组和对照组治疗后平地行走疼痛程度评分下降率比较(全分析集)
试验组共344例患者,对照组共117例患者

表4 试验组和对照组治疗后疼痛疗效比较(全分析集)
试验组共344例患者,对照组共117例患者
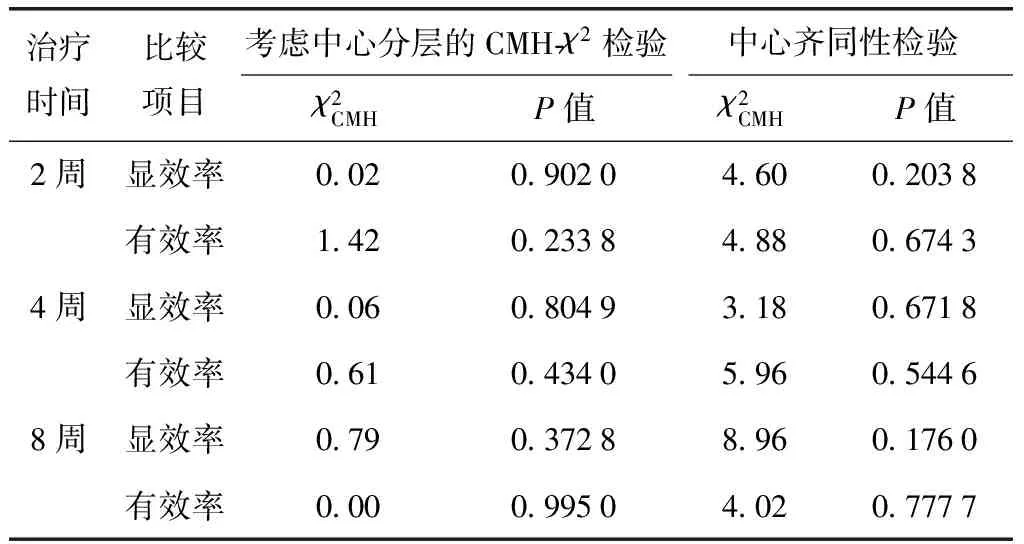
表5 试验组和对照组治疗后显效率和有效率检验
次要指标:(1)僵硬(WOMAC VA 3.0问题6~7)评分比较。两组患者治疗各时间段和治疗后评分差异均无统计学意义(P>0.05)。治疗后较治疗前评分明显下降,组内比较差异均有显著统计学意义(P<0.0001)。(2)疗后不同时段僵硬及日常活动能力总分比较,前者治疗2周、4周及8周后,两组差异均无统计学意义(P>0.05);后者治疗4周后,试验组优于对照组,差异存在统计学意义(P<0.05), 治疗2周及8周后两组差异均无统计学意义(P>0.05)。治疗后不同时段僵硬及日常生活能力总分下降值及下降率比较,治疗2周、4周及8周后明显较治疗前降低,总分下降值及下降率组内前后比较差异均有统计学意义(P<0.000 1);两组间比较差异均无统计学意义(P>0.05)。(3)进行日常生活的难度(WOMAC VA 3.0问题8~24)评分比较。治疗4周,试验组问题9、11、13、15、21~24评分低于对照组,差异有统计学意义(P<0.05),艾瑞昔布在改善上述10个日常生活难度项的效果优于对照组。其他时间点各问题评分两组间差异均无统计学意义(P>0.05)。(4)受试者和研究者对疾病状况的总体评价比较,治疗2、4及8周,疗后总体评价均好于疗前,组内治疗前后比较差异均有统计学意义(P<0.000 1),两组间比较差异均无统计学意义(P>0.05)。受试者及研究者对治疗反应的总体评价比较,治疗2周、4周及8周后,两组间差异均无统计学意义(P>0.05)。(5)关节功能分级比较。治疗2、4、8周,两组关节功能分级Ⅰ级者逐渐增加,Ⅲ级关节功能者逐渐减少,两组间级别差异无统计学意义(P>0.05)。
安全性分析
试验组和对照组临床不良反应发生率分别为7.85%和10.26%,差异无统计学意义(P=0.4430)。两组发生率>1%的不良反应为上腹部不适、消化道溃疡、胃底/胃体出血点、白细胞减少和皮疹。试验组与对照组各发生严重不良事件1例,因果关系均评价为与试验药物“肯定无关”。实验室检查显示,试验组白细胞减少、转氨酶升高各2例,尿素氮升高1例;对照组白细胞减少2例,转氨酶升高1例,无尿素氮升高者。两组均未发生心脑血管梗死病例。试验组用药前、后进行胃镜检查例数分别为137、121例,对照组为47、43例;5例[试验组3例(0.85%)、对照组2例(1.69%)]患者出现胃黏膜出血点增多和/或糜烂;5例[试验组4例(1.16%),对照组1例(0.85%)]患者出现新增溃疡,程度均不重;两组受试者胃镜检查各指标及溃疡发生率差异均无统计学意义(P>0.05)。
讨 论
OA在人群中非常常见,60岁以上人群的发病率超过50%[1]。疼痛是OA最重要的临床表现,对老年人生活质量造成严重影响。非甾体抗炎药(nonsteroidal anti-inflammatory drugs,NSAIDs)是OA治疗的主要药物之一,但传统NSAIDs的不良反应在一定程度上限制了其长期应用。美国有报道,每年因服用NSAIDs导致相关并发症而住院和死亡的患者分别高达107 000例及16 500例[2],胃肠道溃疡每年的发病率甚至达2%~4%[3]。因此,寻求一种胃肠损害小且有效的抗炎镇痛药尤为重要。但是,早在1998年全球第一个选择性COX-2抑制剂塞来昔布问世以来,关于选择性NSAIDs和非选择性NSAIDs的优势之争就一直不断[4],使用选择性抑制剂可以减少胃肠道并发症[5],但其心血管安全性也得到重视。艾瑞昔布是江苏恒瑞医药股份有限公司开发的具有自主产权的一种选择性COX-2抑制剂,临床前、Ⅰ期及Ⅱ期临床试验均显示该药具有良好的安全性和有效性,并提供了恰当的药物剂量[6-7]。本研究为Ⅲ期临床研究,选择目前已经上市并公认有效安全的塞来昔布作为对照,评价艾瑞昔布治疗膝OA的有效性和安全性。
结果显示,治疗后2、4及8周平地行走疼痛程度评分、疼痛程度总分、僵硬总分、日常生活能力总分均较治疗前显著下降,受试者和研究者对疾病状况的总体评价均较治疗前显著好转。此外,治疗2、4、8周两组间疼痛疗效显效率及有效率差异无统计学意义,两组临床有效率的比较采用考虑中心分层的CMH-χ2检验进行比较,试验组非劣于对照组。由此可见,艾瑞昔布治疗膝OA同塞来昔布疗效相当。
两种药物不良事件及不良反应发生率均较低,程度较轻,且多为一过性。严重不良事件均排除了与受试药物的相关性。胃肠道安全方面,两组各有1/4以上的患者治疗前后进行了胃镜检查,仅5例(试验组3例,对照组2例)患者出现胃粘膜的出血点增多和/或糜烂,5例(试验组4例,对照组1例)患者出现新增溃疡,程度均不重,两组受试者胃镜各指标以及溃疡发生率差异均无统计学意义。两组患者均未发生心脑血管意外。
[1]中华医学会风湿病学分会. 骨关节炎诊治指南(草案)[J].中华风湿病学杂志,2003,7:702-704.
[2]Wolfe MM,Lichtenstein DR,Singh G.Gastrointestinal toxicity of nonsteroidal antiinflammatory drugs[J].N Engl J Med,1999,340:1888-1899.
[3]Gutthann SP,García Rodríguez LA,Raiford DS. Individual nonsteroidal antiinflammatory drugs and other risk factors for upper gastrointestinal bleeding and perforation[J].Epidemiology,1997,8:18-24.
[4]American College of Rheumatology Ad Hoc Group on Use of Selective and Nonselective Nonsteroidal Antiinflammatory Drugs.Recommendations for use of selective and nonselective nonsteroidal anti-inflammatory drugs:an American College of Rheumatology white paper[J].Arthritis Rheum,2008,59:1058-1073.
[5]Mooer RA,Derry S,Mcquay HJ.Cyclo-oxygenase-2 selective inhibitors and nonsteroidal anti-inflammatory drugs:balancing gastrointestinal and cardiovascular risk[J].BMC Musculoskelet Disord,2007,8:73.
[6]黄建林,古洁若,潘云峰,等. 艾瑞昔布片治疗膝骨关节炎的Ⅱ期多中心随机双盲临床试验[J].中国药学杂志,2011,46:1740-1745.
[7]张奉春. 环氧化酶-2特异性抑制剂[J].中国药学杂志,2011,46:875-876.
