腹腔镜辅助小切口胃癌根治手术治疗进展期胃癌的技术可行性和安全性分析
2014-04-01陈涛
陈 涛
(临邑县人民医院普外科,山东 临邑 251500)
1994年日本外科医师Kitano对首例行腹腔镜辅助胃切除治疗胃癌手术进行了报道,随后应用腹腔镜治疗胃癌的数量也随着研究深入的增加而增多[1]。日本的早期胃癌的诊断率虽可达到70%以上,但由于欧美国家在医疗卫生政策的侧重点方面与日本存在一定的差异性,因此欧美的早期胃癌的诊断率仅在15%以下,75%以上为进展期胃癌[2],中国的情况与欧美国家相当,也是以进展期胃癌为主,腹腔镜手术治疗进展期胃癌仍然存在较大的争议,主要的担忧是腹腔镜手术淋巴结廓清范围以及程度不足,手术时间长以及手术费用高等[3]。本研究主要采用了腹腔镜辅助小切口胃癌根治手术治疗进展期胃癌,现报道如下。
1 资料与方法
1.1一般资料 回顾性分析2009年11月至2013年11月临邑县人民医院收治的60例进展期胃癌患者的临床资料,采取随机数字表法分为对照组与观察组各30例。两组患者在性别、年龄、肿瘤部位及术后病理分期方面的差异均无统计学意义(P>0.05),具有可比性(表1)。
1.2手术方法 对照组采用胃癌扩大根治性切除术,观察组采用腹腔镜辅助小切口胃癌根治术。
1.2.1胃癌扩大根治性切除术 具体手术方法如下[4-6]。①首先作Kocher切口,并清扫第13组淋巴结:在常规手术治疗的基础上,于十二指肠外侧作一Kocher切口,并将十二指肠充分地进行游离。②肝十二指肠韧带骨骼化,将显露的胆总管、肝固有动脉以及门静脉进行清扫,并将其周围的第12组淋巴结清扫干净。③将本组的a与b两个区的淋巴结加以清除:将胰头十二指肠向内侧进行翻起,并将左右臂动静脉、腹腔干、肠系膜上下动脉完全地进行暴露,将胰头十二指肠长a与b区的淋巴结进行清扫;④将第16组的a区淋巴结进行清扫:在清扫第7、8、9组淋巴结的同时,朝左清除第10、11组淋巴结后,沿着脾动脉向上清除腹主动脉左侧与左肾上腺之间a区的腹主动脉外侧组,并将前组、腹主动脉以及下腔静脉间的淋巴结进行清扫。根据胃上部胃癌将清除第19组,在胸腹联合切口的条件下,将对第20、110及111组的清除,若食管下端出现浸润,则将108及112组进行清除。⑤按照对b区的淋巴结较少的转移,所以胃癌b区多数患者仅限于查阅相关文献资料。手术到此结束。
表1 对照组与观察组进展期胃癌患者一般资料比较
*为t值,余为χ2;对照组:采用胃癌扩大根治性切除术;观察组:采用腹腔镜辅助小切口胃癌根治术
1.2.2腹腔镜辅助小切口胃癌根治术 具体方法如下[7-8],①术前准备:对患者进行全麻处理,嘱其取平卧位,将手术中所需仪器进行妥善安置,术者立于左下方,助手立于右侧。②于脐上小切口下进行第一站大部分淋巴结清扫:做一切口于患者脐上方,将切口长度控制在5~6 cm之间。于大网膜近横结肠无血管区域,将大网膜游离切除,同时将幽门下淋巴以及脂肪组织等清除,对第4、6组淋巴结开始清扫,后对胃右动脉切断结扎,沿着肝脏将肝胃韧带切开,对第3、5组淋巴结开始清扫。③于腹腔镜下完成第二站淋巴结的清扫。将10 mm的Trocar及腹腔镜置于脐上小切口之中,采用7号丝线建立气腹,并将压力维持在12 mm Hg水平。于左锁骨中线平脐上2 cm以及右锁骨中线平脐以上2 cm、右腋前线肋缘以下约为2 cm处分别处置一个10 mm的Trocar作为主操作孔以及5 mm的Trocar作为牵引孔。将胃窦部朝左上方进行翻转,靠近脾门于根部离断胃网膜左动静脉,于胰腺上缘显露脾动脉,沿着脾动脉向左侧清扫第11组淋巴结,向右游离脾门清扫第10组淋巴结之后,沿着脾动脉向右暴露胃左动脉以及肝总动脉。于血管鞘之中进行分离,骨骼化胃左动静脉,于胃根部上锁扣夹之后将胃左动静脉进行切断,以清扫第7、9组淋巴结。然后将肝十二指肠韧带切开,并清扫第12组淋巴结。
1.3评价标准
1.3.1疗效评价标准 新辅助化疗后的临床疗效判定,主要依据2000年美国与加拿大国立癌症研究所、欧洲癌症研究与治疗组织共同提出的“实体瘤疗效反应评价标准”,主要内容包括[9]:①CT显示肿瘤完全消失或消退为完全缓解;②可测得的肿瘤直径缩小一半以上,未出现显著的扭曲或者溃疡等为部分缓解;③可测得肿瘤直径缩小了25%~50%,溃疡程度减少,且管腔的宽度有所增大为稳定;④肿瘤直径缩小程度<25%为无效。缓解率=(完全缓解+部分缓解)/总例数×100%。
1.3.2Karnofsky评分标准 主要包括如下评价内容[10]:①100分属于正常状态,且未见任何病症的出现;②90~99分可以下床进行正常的活动,具有轻微的病症;③70~89分可以正常下地活动,但略感吃力;④50~69分为生活上可自理,但是疾病影响了患者的正常生活与工作;⑤50分以下为需经常进行帮扶或必要的护理等。
1.4观察指标 比较两组临床疗效、手术前后免疫功能指标,包括IgG、IgM及IgA,测量选用全自动特种蛋白分析仪ARRAY360(北京尚精光电技术有限公司提供)行速率散射比浊法、Karnofsky评分、手术指标变化情况,包括平均住院时间、平均手术时间、平均术中出血量及平均下地活动时间。观察术后不良反应发生率,主要包括胃出血等。
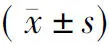
2 结 果
2.1两组临床疗效分析 观察组缓解率显著高于对照组(χ2=4.327,P<0.05),两组疗效比较差异有统计学意义(Z=5.45,P<0.05)(表2)。
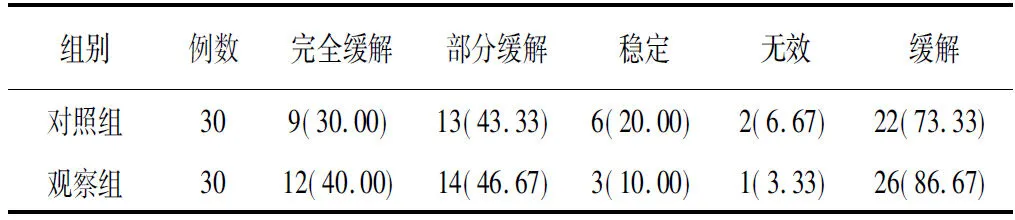
表2 两组进展期胃癌患者疗效比较 [例(%)]
对照组:采用胃癌扩大根治性切除术;观察组:采用腹腔镜辅助小切口胃癌根治术
2.3两组手术前后免疫功能指标变化对比分析 两组手术前后各免疫功能指标IgA、IgG及IgM相比,差异均具有统计学意义(P<0.05),且观察组术后免疫功能指标均显著优于对照组(P<0.05)(表3)。
2.4两组手术前后Karnofsky评分对比 两组患者手术前后Karmofsky评分相比,差异具有统计学意义(P<0.05),但两组术后Karnofsky评分差异无统计学意义(P>0.05)(表4)。
表3 两组进展期胃癌患者手术前后免疫功能指标变化情况比较 (g/L)
对照组:采用胃癌扩大根治性切除术;观察组:采用腹腔镜辅助小切口胃癌根治术
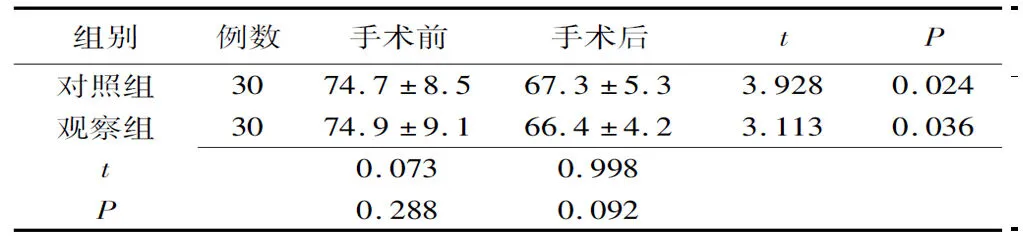
表4 两组进展期胃癌患者手术前后Karnofsky评分比较 (分)
对照组:采用胃癌扩大根治性切除术;观察组:采用腹腔镜辅助小切口胃癌根治术
2.5两组各手术指标对比分析 两组患者在平均住院时间、平均手术时间、平均术中出血量及平均下地活动时间方面,差异均无统计学意义(P>0.05)(表5)。
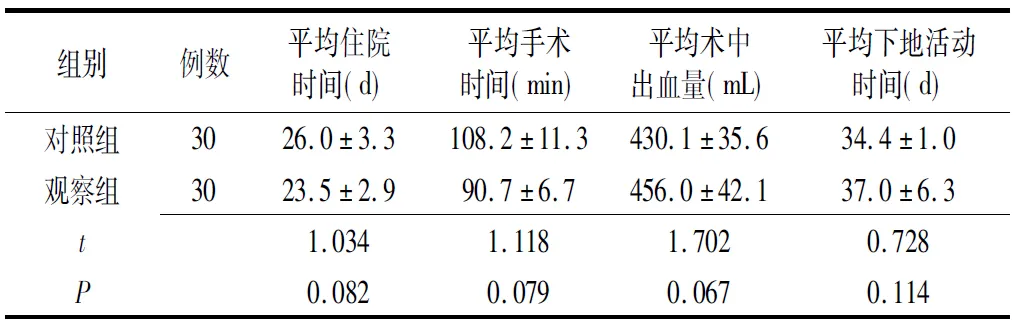
表5 两组进展期胃癌患者手术指标比较
对照组:采用胃癌扩大根治性切除术;观察组:采用腹腔镜辅助小切口胃癌根治术
2.5两组术后不良反应发生情况 对照组术后2例出现胃出血症状,占6.67%,观察组术后1例出现胃出血症状,占3.33%,两组并未出现手术中转情况。两组术后不良反应发生率差异无统计学意义(χ2=2.76,P>0.05)。
3 讨 论
随着人们生活水平的不断提高以及人们的生活方式的逐渐转变,胃癌患者呈现逐年上升的变化趋势。胃癌发病迅速,对患者的正常生活及工作造成了极大的影响[11]。因此,应该注重加强对胃癌患者的临床治疗,尤其是对于进展期胃癌,则更应注意其临床治疗。
由于区域淋巴结清扫的范围方面存在的差异性,可分为不同的几种根治术。未将第一站淋巴结完全清除的则可称为“清除术”。将第一站淋巴结完全清除称之为“根治术”[12]。采用相同的方法,对第二站以及第三站淋巴的清除,则可称之为“清除术”。此外,还可以按照淋巴结转移程度与淋巴结清除范围之间存在的相关关系,区分为绝对根治以及相对根治这两种概念,前者指的就是淋巴结清扫超越转移淋巴结的第一站上面,若第一站淋巴结出现了转移,施行根治。一般而言,根治性胃大部切除术的范围,主要包括原发性病灶在内的胃近侧或者远侧的2/3、全部大小网膜以及胃的区域性淋巴结。有时胃体癌为了能够将贲门一侧、脾门以及脾动脉周围淋巴结加以清扫完全,必须行全胃以及腺体、胃与脾脏一起切除的扩大根治性切除术。癌肿累及横结肠或肝脏左叶等邻近脏器时,也可做连同该受累脏器的根治性联合切除术[13]。
然而进展期胃癌,腹腔镜手术根治性切除的难度较大,长期效果的大样本临床研究较少。因此对于进展期胃癌.腹腔镜根治术能否成为开腹手术外的另一选择仍存有争议。本研究中,观察组手术时间显著长于对照组,这与国外文献报道一致[14]。本研究结果显示观察组临床总缓解率显著高于胃癌扩大根治性切除术组,提示腹腔镜辅助小切口胃癌根治手术的临床效果更加显著。对于进展期胃癌而言,当外界的刺激,如放、化疗、手术等,会使得机体免疫功能受到一定程度的影响,本研究主要选择了三个常见的表征免疫功能的指标:IgA、IgM及IgG作为研究对象,结果显示:两组手术切口上述指标差异均具有统计学意义。该结果与相关文献资料报道结果基本一致[15]。观察组术后Karnofsky评分与对照组比较,差异无统计学意义,提示两种手术下,术后患者生活质量无明显差异。两组不良反应发生率差异也无统计学意义。
综上所述,腹腔镜辅助小切口胃癌根治手术治疗进展期胃癌技术可行,安全性较高,值得在临床上加以推广及普及。
[1] 孙少川,周鑫,郑春宁,等.腹腔镜辅助胃癌根治术的可行性探讨[J].腹腔镜外科杂志,2012,17(5):342-344.
[2] 宋鹏,吴蕾.胃癌的淋巴结转移与清扫研究进展[J].中国普外基础与临床杂志,2012,19(1):116-121.
[3] Fujii M,Kim YH,Satoh T,etal.Randomized phase Ⅲ study of S-1 alone versus S-1 plus docetaxel(DOC) inthetreatment for advanced gastric cancer(AGC):the START trial update[J].J Clin Oncol,2011,29(15):4016.
[4] 曹攀镜,吴欣爱.替吉奥联合多西他赛治疗进展期胃癌24例临床观察[J].临床荟萃,2012,27(12):1070-1072.
[5] 吴普照.低张水充盈螺旋CT增强扫描对进展期胃肿瘤诊断的价值[J].中国现代医学,2009,47(7):126-127.
[6] 蒋志龙,周斌,徐建峰,等.腹腔镜、胃镜联合治疗早期胃癌的临床体会[J].腹腔镜外科杂志,2011,16(2):916-918.
[7] 曾毅克,刘衍民,雷建,等.腹腔镜辅助胃癌根治手术治疗进展期胃癌的短期疗效评价[J].暨南大学学报:医学版,2012,33(2):172-174.
[8] RosatiG,Ferrara D,Manzione L.New perspective sin the treatment of advanced or metastatic gastric cancer[J].World J Gastroenterol,2009,15(22):2689.
[9] 刘险峰,华云旗,杨永岩,等.多西他赛联合替吉奥治疗晚期胃癌的回顾性评价[J].临床荟萃,2013,28(9):963-965.
[10] 傅炯.奥沙利铂联合卡培他滨行新辅助化疗治疗进展期胃癌猿园例疗效观察[J].中国现代医生,2012,49(21):61-62.
[11] 倪志强.奥沙利铂联合卡培他滨行新辅助化疗治疗进展期胃癌临床疗效观察[J].中国现代药物应用,2013,7(23):154-155.
[12] 景元明,叶民峰,徐关根,等.参一胶囊联合FOLFOX4方案治疗晚期胃癌的临床研究[J].浙江临床医学,2010,12(9):940-941
[13] 任闽山,邵光军.中晚期胃癌FOLFOX4方案新辅助化疗效果观察[J].山东医药,2009,49(15):80-81.
[14] Koizumi W,Takiuchi H,Yamada Y,etal.Phase Ⅱ study of oxaliplatin plus S-1 as first treatment for advanced gastric cancer(G-SOX study)[J].Ann Oncol,2010,21:1001-1005.
[15] Kunisaki C,Takahashi M,Makino H,etal.Phase Ⅱ study of biweekly docetaxel and S-1 combination chemotherapy as first-line treatment for advanced gastric cancer[J].Cancer Chemother Pharmacol,2011,67(6):1363-1368.
