射频消融治疗合并重度肝硬化的小肝癌疗效分析
2014-03-29钱瑞坤刘建刚
钱瑞坤 乔 森 刘建刚
(1山东省医学科学院,山东济南250062;2济南大学山东省医学科学院医学与生命科学学院,济南250062;3济宁医学院附属济宁市第一人民医院,山东济宁272011;4济宁医学院临床学院,济宁272067)
肝癌是中国最常见的恶性肿瘤之一,手术切除被认为是肝癌治疗的首选方式。肝功能差、凝血机制欠佳等原因导致手术切除后易出现多种并发症。近年来,微创技术的迅猛发展,使射频消融术(radiofrequency ablation,RFA)越来越受到术者的青睐,因其创伤小、并发症少、恢复快等优点成为治疗合并有肝硬化、手术风险较大的小肝癌患者的新手段。本文旨在对比合并重度肝硬化的小肝癌手术切除与射频消融治疗的疗效。
1 资料与方法
1.1 一般资料
回顾性分析济宁医学院附属济宁市第一人民医院2010年至2013年合并重度肝硬化的小肝癌患者64例,所有的入组患者术前均行强化CT、AFP等肿瘤标志物检查,肿瘤直径1~3cm,单发,术后病理结果确诊为肝细胞肝癌。根据肝癌的治疗方法不同分为2组:射频组和手术切除组。两组的年龄,性别,肿瘤大小,术前肝功能等相比较无显著性差异,见表1。
1.2 试验方法
1.2.1 射频消融组 采用美国COVIDIEN公司冷循环射频肿瘤治疗系统。为更好明确肿瘤的部位、大小以及与肝内胆管、门静脉的关系,患者均于术前行B超检查制定好进针位点及路线。根据肿瘤位置的不同,确定病人的体位,B超定位、再次确定进针位点、路线后,常规消毒,铺巾,局部麻醉至肝包膜或静脉全麻,皮肤切口约3mm,射频针准确沿着路线进入肿瘤中心内,利用高频振荡电流使组织电子随电流变化而产生震动,迅速形成70℃以上的高温区,从而导致肿瘤细胞发生凝固性坏死。然后超声检查消融效果,若未达到完全消融,可重复进行射频,直至完全消融。
1.2.2 手术切除组 右侧肋缘下切口进腹,首先探查周围脏器有无转移,及肿瘤侵犯浸润情况,游离肝周韧带,游离韧带的部位根据肿瘤的位置而异,选择合理的肝脏血管控制方式,行肝肿瘤切除术。
1.3 观察指标及随访
观察两组患者的手术时间、出血量、平均住院日、术后镇痛剂使用率及并发症情况。64例患者术后均行定期随访,复查肝功能、血清肿瘤标记物及强化CT,观察比较两组的复发转移率和生存率。随访12个月,随访频率是术后前3个月每个月复查1次肝功能、血清肿瘤标记物及强化CT,后9个月内每3个月复查1次。
1.4 统计学方法
采用SPSS 18.0进行统计学分析。
2 结 果
2.1 两组患者一般资料比较
两组间年龄,性别,肿瘤大小,术前肝功能相比较均无统计学意义。见表1。
表1 两组病例一般资料比较(±s)

表1 两组病例一般资料比较(±s)
组别 n 性别(男/女)年龄(岁)肿瘤直径(cm)术前肝功能分级(A/B)射频消融组34(20/14)48.2±10.7 1.9±0.4 11/23手术切除组30(18/12)50.2±10.2 2.0±0.4 10/20 t/χ20.009 1.792 1.424 0.007 P 0.924 0.084 0.165 0.934
2.2 两组术中及术后资料的比较
射频消融组手术时间、出血量、平均住院日、术后镇痛使用率、并发症发生率和手术切除组相比较有显著性差异(P<0.05)。随访1a后,59例患者上腹部强化CT未发现新的病灶。手术切除组有3例肝内转移,射频消融组2例肝内转移,转移灶均给予射频消融治疗。术后1a瘤复发转移率、生存率,两组无统计学差异(P>0.05)见表2。
表2 两组患者术中及术后资料的比较(±s)
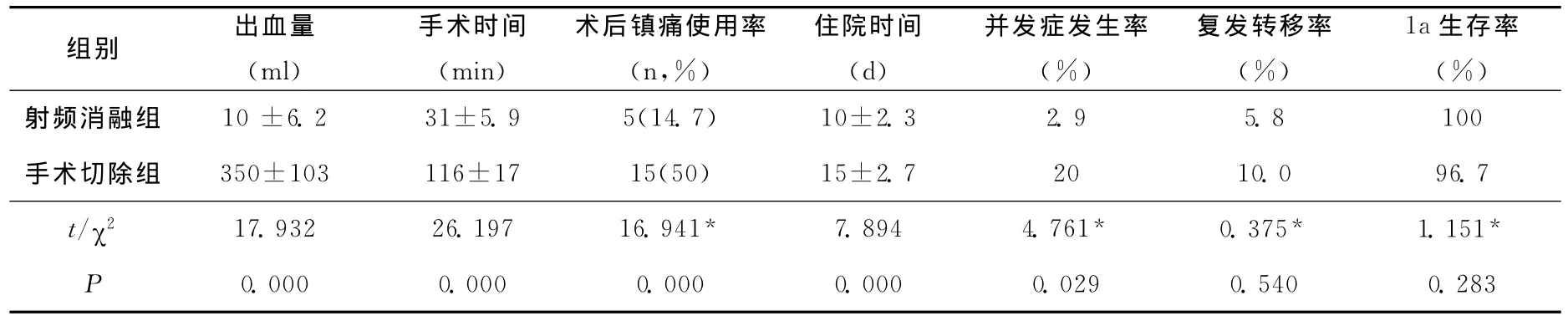
表2 两组患者术中及术后资料的比较(±s)
*为χ2值。
组别 出血量(ml)手术时间(min)术后镇痛使用率(n,%)住院时间(d)并发症发生率(%)复发转移率(%)1a生存率(%)射频消融组 10±6.2 31±5.9 5(14.7)10±2.3 2.9 5.8 100手术切除组 350±103 116±17 15(50) 15±2.7 20 10.0 96.7 t/χ2 17.932 26.197 16.941* 7.894 4.761* 0.375* 1.151*0.000 0.000 0.000 0.000 0.029 0.540 0.283 P
2.3 两组术后并发症比较
射频消融组:34例患者,1例术后并发胆漏。手术切除组:30例患者,6例术后并发症:顽固性腹水2例;肝功能衰竭1例;胆漏1例;术后早期出血2例。
3 讨 论
原发性肝癌发病率高,预后差,手术切除术后并发症多,而RFA可以直接快速地杀死肿瘤,对肝脏损伤范围局限,对机体影响小。Livraghi等[1]认为对于直径≤2.0cm的肝癌,RFA可替代手术切除治疗。他们曾对能行手术切除且直径≤2.0 cm的小肝癌行RFA治疗,术后并发症较手术切除组明显减少,只有1.8%。而5a生存率达到68.5%,与手术切除组无明显差异。本文结果显示,手术组术后1a生存率为96.7%,复发转移率为10%;射频组术后1a生存率为100%,复发转移率为5.8%。二者无统计学意义。我们的研究结果初步显示RFA的方法特别适合伴有严重肝硬化的小肝癌患者能明显改善病人的生存质量,延长生存期而无明显的不良反应。Lau等[2]同样认为RFA治疗直径≤3.0cm肝癌的疗效与手术切除类似,是最有效的小肝癌治疗手段。
RFA是使电极周围肿瘤细胞的温度在尽可能短的时间内均匀性增加,最终出现细胞坏死,从而达到临床治愈的目的[3]。治疗反应的准确评估,对确保成功的射频消融治疗非常重要。足够安全边际可以防止肿瘤的局部复发[4]。RFA虽是微创技术,但仍是一种有创性的操作,存在一定的风险及其并发症。最常见的并发症包括发热、肝区疼痛、针道出血、皮肤灼伤等[5]。这些并发症给病人带来的痛苦相对比较轻微,通过对症处理后均明显缓解、好转[6]。
本文RFA在超声实时监控下可以准确达到安全边缘,使肿瘤完全消融,小肝癌病灶完全坏死率可达到90%以上,而且术中出血量、术后并发症、住院时间等均较肝癌切除组少。我们的结果支持对于合并重度肝硬化的单发小肝癌,RFA与外科切除术疗效相当,且RFA具有创伤小、痛苦少、并发症少、恢复快、住院周期短等优势。我们下一步的研究目标是3~5cm肝癌,相信随着医疗技术的进步,RFA治疗肝癌的适应征亦会越来越宽,能够使肿瘤得到更好控制,提高患者生存期,改善其生活质量。
[1]Livraghi T,Meloni F,Di Stasi M,et al.Sustained complete response and complications rates after radiofrequency ablation of very early hepato-cellular carcinoma in cirrhosis:Is resection still the treatment of choice?[J].Hepatology,2008,47(1):82-89.
[2]Lau WY,Lai EC.The current role of radiofrequency ablation in the management of hepatocellular carcinoma:a systematic review[J].Ann Surg,2009,249(1):20-25.
[3]Yin XY,Xie XY,Lu MD,et al.Percutaneous ablative therapies of recurrent hepatocellular carcinoma after hepatectomy:proposal of a prognostic model[J].Annals of surgical oncology,2012,19(13):4300-4306.
[4]Liu L,Fang Y,Wang K,et al.Clinical investigation of CT-guided radiofrequency ablation for liver cancer in hepatic dome area[J].Tumor,2014,34(1):60-66.
[5]Kang MG,Lee TH,Na WT,et al.Hepatocolic fistula after radiofrequency ablation for hepatocellular carcinoma[J].Korean Journal of Medicine,2012,83(4):480-484.
[6]中国抗癌协会肝癌专业委员会、中国抗癌协会临床肿瘤学协作委员会、中华医学会肝病学分会肝癌学组.肝癌射频消融治疗规范的专家共识[J].临床肝胆病杂志,2011,27(3):236-238,244.
