离子交换色谱法分离氨基酸实验方法的改进
2014-03-26张宝珠赵玉红蔺宝珠李登文赵立青张金红
李 欣,张宝珠,赵玉红,蔺宝珠,李登文,赵立青,张金红
(南开大学 生命科学学院,天津 300071)
基础生物化学实验是南开大学生命科学学院面向本校药学、医学、环境科学和物理专业低年级本科生开设的基础实验课程。该课程涉及到滴定技术、生物大分子的提取和分离技术等多项生物化学基本实验技能,每学期54学时,共11个实验项目,学生人数150~200人。与生命科学学院本专业的生物化学实验课不同的是:学生所学专业不一、理论基础和实验操作能力参差不齐,导致该课程形成时间紧、任务重的特点。
离子交换色谱法是分离和纯化生物分子的常用方法之一。由于其应用的重要性和广泛性,该方法也被引入本科生基础生物化学实验“离子交换色谱法分离氨基酸”实验中。氨基酸分离效果的优劣,一方面决定于待分离氨基酸等电点的差异,差异越大,分离效果越好[1-2];另一方面,树脂的型号、缓冲液和洗脱液的种类及pH值、洗脱速度等因素都会影响分离效果[3-4]。由于天门冬氨酸(等电点为2.77)和精氨酸(等电点为10.76)的等电点相差较大,本实验依然沿用之前的实验选择,对它们的混合溶液进行分离。所不同的是,在之前的实验中,采用型号为001×7的离子交换树脂,NaCl作为洗脱溶液,出现洗脱难,耗时长的现象;而经过改进,选用具有“易洗脱”特点的D61树脂,并将洗脱液改为NaOH,大幅度地改变了氨基酸所处的pH环境。改进后的实验方法,不但使洗脱效果得以优化,还可以保证学生在规定时间内完成实验任务,保障了基础生物化学实验课程的进度安排,有利于在本科生实验教学中普及开展。
1 试剂和器材
试剂:盐酸、氢氧化钠、柠檬酸、柠檬酸钠、天门冬氨酸、精氨酸、茚三酮、95%乙醇、α-萘酚、碱性次溴酸钠溶液(把1.2 g溴溶于150 mL、5%的NaOH中)、氯化钠、氢氧化钠等。
器材:强酸性离子交换树脂001×7和D61 (天津南开和成科技有限公司)、内径为1.9 cm的下阀有导管联通的色谱柱、铁架台、蠕动泵、分部收集器、广泛pH试纸、恒温水浴锅、分光光度计等。
2 实验方法
2.1 离子交换树脂的处理
新树脂先在蒸馏水中浸泡,洗去杂质和细小颗粒,再用2 mol/L的HCl浸泡4 h左右,除去可能含有的重金属离子;用蒸馏水洗至中性后,用2 mol/L的NaOH浸泡4 h左右,用蒸馏水洗至中性,树脂即转变为Na+型。装柱前,用0.05mol/L、pH6.0的柠檬酸缓冲液和树脂搅拌,达到平衡[5]。
2.2 装柱
将平衡好的阳离子交换树脂搅拌后装柱,使树脂悬浮液慢慢沉析,直到柱子的1/2左右,此时色谱柱中装树脂的高度约为9 cm,树脂体积约为25 mL。
2.3 加样
放出过量的缓冲液,当溶液的液面与柱床表面高度相同时,加入氨基酸混合液样品(天门冬氨酸和精氨酸,10g/L)1 mL,打开蠕动泵(流速0.6 mL/min),使氨基酸混合液进入树脂,待液面与柱床表面接近相平时,吸取2~3 mL缓冲液洗涤树脂柱内壁,并重复2~3次,确保样品进柱[5]。
2.4 洗脱和收集
首先用0.05 mol/L、pH6.0的柠檬酸缓冲液以0.6 mL/min的流速洗脱,用试管进行收集,每3 mL收集1管,用茚三酮显色法进行检测。当第1种氨基酸被洗脱下来后,将洗脱液换成NaCl或NaOH,流速增加为1 mL/min,同样是每3 mL收集1管,直到第2种氨基酸被完全洗脱下来。
2.5 氨基酸的检查
从每支收集管中分别取350 μL收集液放入相应的1.5 mL炮弹管中,用试纸检测收集液的pH值并调节,使各管pH为6,再分别加入等体积的0.5%的茚三酮乙醇溶液,混匀后于沸水浴中加热10 min,如有氨基酸存在,溶液变成蓝色[5]。
2.6 精氨酸的检测
将500 μL收集液与500 μL、20%的NaOH混合,加入2滴α-萘酚,混合后加入1~2滴次溴酸钠,观察颜色变化,如果混合液变红,则说明有精氨酸存在[5]。
3 实验结果
树脂在先后两种不同洗脱液的作用下,使混合氨基酸得以分离。天门冬氨酸是酸性氨基酸,等电点为2.77;精氨酸为碱性氨基酸,等电点为10.76。实验中首先以0.05 mol/L、pH6.0的柠檬酸缓冲液作为洗脱液,此时,天门冬氨酸带负电,无法与阳离子交换树脂上的Na+进行交换,而此时带正电的精氨酸却可以和树脂结合,因此,在用0.05 mol/L、pH6.0的柠檬酸缓冲液来洗脱时,天门冬氨酸先被洗脱下来;随后,换用2 mol/L的NaCl 或1 mol/L的NaOH进行洗脱,使得盐浓度或pH大幅提高,精氨酸则与树脂脱离而被洗脱下来[6-11]。
选择001×7树脂分离两种氨基酸,以2 mol/L的NaCl作为洗脱液,洗脱结果如图1所示。

图1 001×7树脂以0.05 mol/L柠檬酸缓冲液和2 mol/L的NaCl为洗脱液的洗脱结果
从图1中可以看出,两种氨基酸均被洗脱下来。坂口反应是精氨酸的特征反应,用来检测精氨酸的存在。第1种被柠檬酸缓冲液洗脱下来的氨基酸坂口反应呈阴性,是天门冬氨酸,被收集在第3至7管中;第2种被2mol/L的NaCl洗脱下来的氨基酸坂口反应成阳性,是精氨酸,被收集在第19至42管中。
选择D61树脂分离两种氨基酸,以1 mol/L的NaOH作为洗脱液,洗脱结果如图2所示。
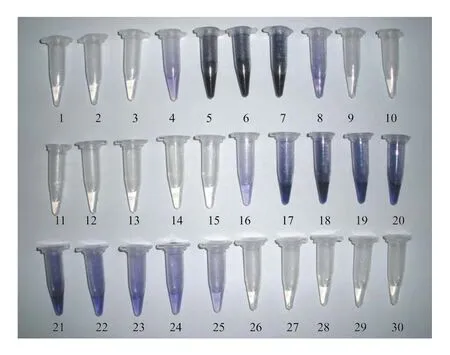
图2 D61树脂以0.05mol/L柠檬酸缓冲液和1mol/L的NaOH为洗脱液的洗脱结果
从图2 中可以看出,两种氨基酸同样被洗脱下来。第1种被柠檬酸缓冲液洗脱下来的氨基酸坂口反应呈阴性,是天门冬氨酸,被收集在第4至8管中;第2种被1mol/L的NaOH洗脱下来的氨基酸坂口反应成阳性,是精氨酸,被收集在第16至25管中。
比较两种实验方法得到的结果,选择001×7树脂以2 mol/L的NaCl作为洗脱液,分离得到的精氨酸被集中于24个管中,洗脱不集中,说明此时精氨酸不易被洗脱下来,耗费洗脱液体积较大,时间较长,严重影响到该实验的进度。而选择D61树脂以1 mol/L的NaOH作为洗脱液,分离得到的精氨酸被集中于仅仅10管中,洗脱集中,节省了洗脱液和洗脱时间,取得了良好的洗脱和分离效果,也大大提高了课堂实验教学效率。
4 讨论
(1) 实验所选用的D61树脂,是一种大孔的离子交换树脂,相比001×7树脂,具有容易洗脱的特点,改善了过去氨基酸分离效果差、难洗脱的现象,且价格便宜,实验成本低,有利于在实验教学中广泛使用。
(2) 实验中若使用001×7树脂,需要收集45管左右才能完成实验,而使用D61树脂,只需要收集30管左右即可。节省了实验时间,保证学生可以在规定时间内按时完成实验,保障了教学进度,提高了教学效率,符合基础生物化学实验的学时特点。
(3) 本实验中选择D61树脂并用NaOH作为精氨酸的洗脱液,虽然优于001×7树脂用2 mol/L的NaCl洗脱的效果,但也会带来新的问题。茚三酮反应的最适pH值为5~7,NaOH会使收集液pH大幅升高,影响到茚三酮显色。因此,在将收集液和茚三酮乙醇溶液混匀前,先要测定收集液的pH值,并将pH值调至6,和0.05 mol/L柠檬酸缓冲液的pH值一致,这样,既保证了显色条件和实验的平行性,同时也加深了学生对于茚三酮反应最适条件的理解。
5 结束语
通过本实验的改进,学生可以认识到对于离子交换色谱分离氨基酸的效果而言,装柱和加样技术的优劣、洗脱液的选择、洗脱速度的改变、pH值等因素都是至关重要的[12]。与此同时,让学生体会到实验方法并不是一成不变的,可以通过理论联系实际的逐渐摸索将方法不断优化,最终得到满意的实验结果。此过程中,不但调动了学生学习的积极性,激发了学生的学习兴趣,还为创新型人才的培养做出了新的尝试[13]。
[1] 白云峰,丁玉,张海燕.氨基酸分离纯化的研究进展[J].食品研究与发,2007,28(2):175-178.
[2] 于泓,牟世芬.氨基酸分析方法的研究进展[J].分析化学评述与进展,2005,33(3):398-404.
[3] 刘艳梅,周美华.氨基酸的分离与提纯[J].浙江化工,2004,35(7):14-17.
[4] 陈昌国,李雷光,范玉静.离子色谱、毛细管电泳及毛细管电泳离子色谱发展概况[J].分析仪器,2009(3):1-7.
[5] 于自然,黄熙泰,李翠凤.生物化学习题及实验技术[M].北京:化学工业出版社,2003.
[6] 张义萍,张伟国,郝刚.离子交换法从发酵液中提取L-精氨酸[J].食品与发酵工业,2005,31(9):63-65.
[7] 刘红,刘华.用离子交换树脂法纯化从蚯蚓体中提取的复合氨基酸[J].贵阳医学院学报,2005,30(3):289-290.
[8] 金燕,金鑫荣,施超欧.用离子交换树脂法从毛发水解氨基酸母液中提取碱性氨基酸[J].化学世界,1996,37(4):199-202.
[9] 甘林火,翁连进.胱氨酸母液中L-精氨酸提取工艺研究[J].食品工业科技,2005,26(3):157-159.
[10] 翁连进,邹建辉,甘林火,等.732离子交换树脂从胱氨酸母液提取L-精氨酸的研究[J].化工进展,2004,23(5):514-518.
[11] 李爽,迟莉丽.L-谷氨酰胺在强酸性离子交换树脂上的稳定性[J].工业微生物,2000,30(1):1-4.
[12] 董文智,程全义.离子交换分离法的发展与应用[J].中国科技博览,2012(36):320.
[13] 张红梅,盂新云,官守涛.氨基酸离子交换色谱实验方法改进[J].郧阳医学院学报,2006,25(1):42.
