钴(Ⅱ)-4,4-联吡啶-4,2′,3′-二苯醚三甲酸的合成、结构及生物活性研究
2014-03-26闫合立李迎迎高恩军
闫合立,马 驰,李迎迎,高恩军
(1.沈阳化工大学 应用化学学院, 辽宁 沈阳 110142;2.沈阳市无机分子基材料化学(国际)重点实验室, 辽宁 沈阳 110142)
近年来在药物化学领域进行研究的人们把更多的目光投向金属配合物的结构及其生物活性方面[1-6].药物化学家们的研究热点一直是一些酶和维生素B12的组成成分、钴的配合物及其聚合物,其主要原因是钴具有较强的配位能力及可变的价态,所以钴的配合物在众多领域都有非常广泛的应用[7-8].4,4-联吡啶是有机合成的重要中间体,是一种线状双基刚性配体,空间位阻少,无支链,有较好的侨联作用,主要用于医药中间体,有机合成,有机溶剂,也可应用于染料生产、农药生产及香料等方面[9-10].芳香族三元羧酸4,2′,3′-二苯醚三甲酸是一种可以作为医药中间体的重要高分子单体.所以本文采用4,4-联吡啶和4,2′,3′-二苯醚三甲酸为配体,合成配合物[Co(4,4-bipy)2(L)]·3H2O.近几年,国际生物无机化学领域研究十分活跃课题之一就有对金属配合物与DNA作用所测定的生物活性的研究[11].
1 实验部分
1.1 实验试剂及仪器
4,4-联吡啶、4,2′,3′-二苯醚三甲酸、六水合硝酸钴,均为分析纯;小牛胸腺DNA、Pbr322-DNA,均为生化试剂.
X-射线单晶衍射仪,Bruker smart 1000 CCD;红外光谱仪,Nicolet FT-IR 470(KBr压片);元素分析仪,Finniggan EA 1112;磁力搅拌器,D-MS-I;精密酸度计,PHS-3C;电子分析天平,AR2140;日立23010荧光光谱仪;上海JS380A自动凝胶图像分析仪.
1.2 配合物的合成
将10 mL浓度为15 mmol/L的六水合硝酸钴水溶液与10 mL浓度为15 mmol/L的4,4-联吡啶水溶液混合,在连续搅拌下,用0.5 mol/L的KOH调节混合溶液pH值为6.7,搅拌8 h加入10 mL浓度为15 mmol/L的4,2′,3′-二苯醚三甲酸溶液,继续搅拌8 h后pH值相对稳定为5.3.将该溶液过滤至烧杯中,在室温下放置20 d后有淡粉色晶体析出.
红外谱图,σ/cm-1:3 420(m);2 426(w);1 689(m);1 606(m);1 491(w);1 384(s);1 246(m);1 222(w);1 164(w);809(w);769(w);634(w);489(w).
元素分析实测值(C25O10N4H30Co计算值)/%:C 49.62(49.59);N 9.25(9.26);H 4.95(4.96).
2 配合物的晶体测定分析及结构
取0.2 mm×0.2 mm×0.2 mm的配合物晶体,在Bruker smart 1000 CCD型X-射线单晶衍射仪上,用经过石墨单色器的Mo-Kalpha(λ=0.710 73 nm)为辐射光源,在2.84°<2θ<26.02°范围内收集衍射数据.在566(2) K下,以ω/2θ扫描方式共收集到衍射数据17 600个,其中独立数据7 846个.晶体结构用直接法解出,对全部的非氢原子的坐标及各面异性参数进行修正,其晶体学数据为:三斜晶系,P-1空间群.晶胞参数:a=1.083 1(15) nm,b=1.180 3(15) nm,c=1.454(2) nm,α=110.72(3)°,β=93.93(8)°,γ=95.10(6)°,Z=2,V=1.722(4) nm3,Dc=1.461 Mg/m3,μ=0.567 mm-1,F(000)=786,Rint=0.084 8,-14≤h≤14,-15≤k≤15,-18≤l≤18,R1=0.067 1,wR2=0.182 0(I>2δ(I)).差值电子密度最高和最低峰为1 321 和-862 e/nm3.
配合物的非氢原子坐标和等效全向位移参数见表1,主要键长见表2,主要键角见表3.配合物晶体结构见图1.由图1 可看出:在配合物中每个钴离子分别同2个4,4-联吡啶中的1个氮原子、4,2′,3′-二苯醚三甲酸中2′位的羧酸中的1个氧原子、3个水分子中的氧原子配位,形成一个六配位的八面体结构.以Co(1)中心原子来分析N(1)、N(2)、O(8)和O(9)处于赤道位置,O(1)和O(7)处于轴向位置.其中,O9—Co1—N1,O8—Co1—N2,O8—Co1—O9和N1—Co1—N2键角分别为 87.48(12)°,92.06(13)°,93.39(12)° 和87.08(12)°,总键角和为360.01°,比预期360°值偏离0.01°,所以说明N(1)、N(2)、O(8)和O(9)几乎完全共平面,O7—Co1—O1键角为172.62(9)°,比预期的180°偏离7.37°.说明这个八面体未发生很大扭曲.

表1 配合物的原子坐标参数和等效全向位移参数

表2 配合物的主要键长
注 #1:-x+1,-y+1,-z+1; #2:-x+1,-y+2,-z+2.

图1 配合物的分子结构
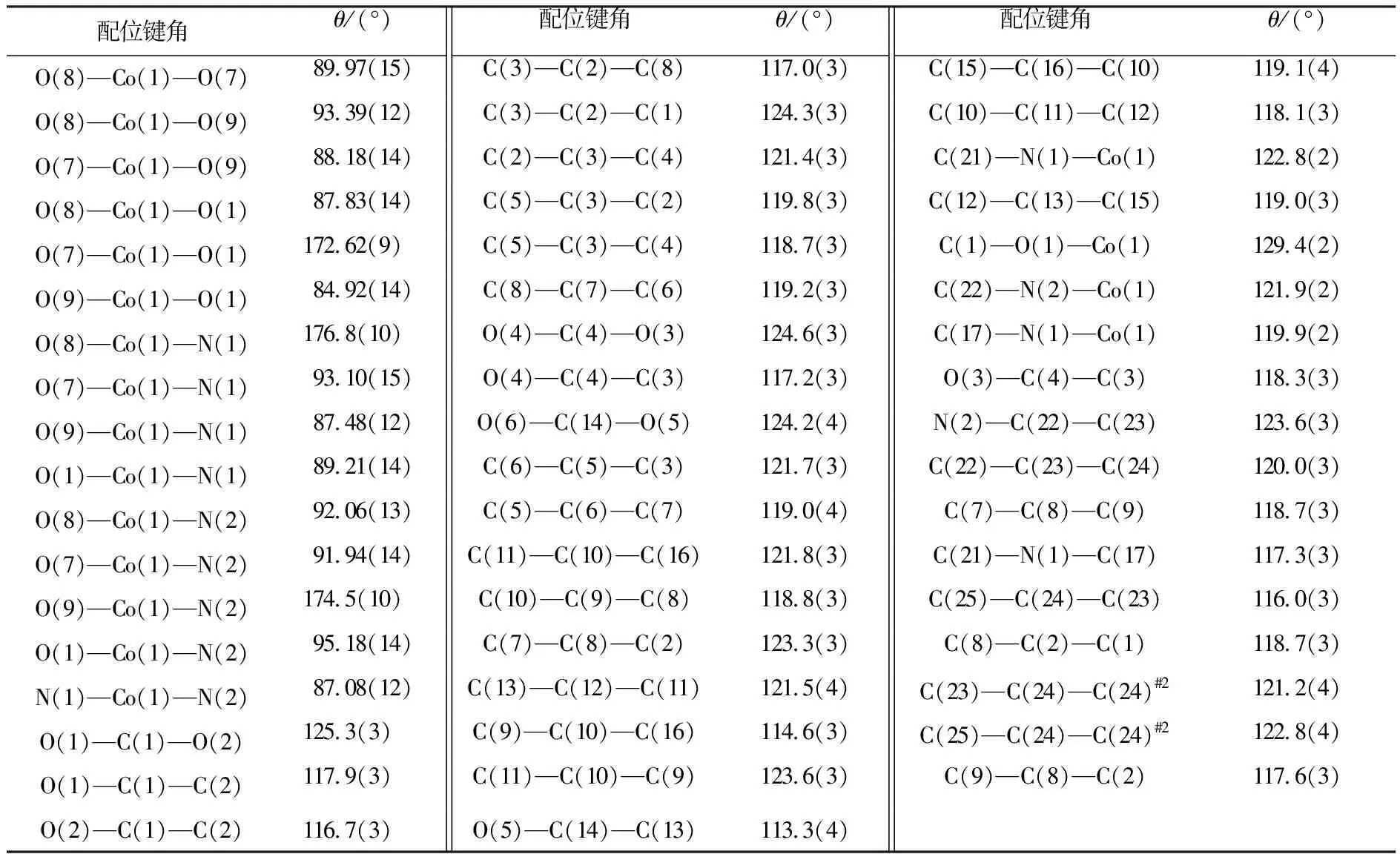
配位键角θ/(°)配位键角θ/(°)配位键角θ/(°)O(8)—Co(1)—O(7)89.97(15)C(3)—C(2)—C(8)117.0(3)C(15)—C(16)—C(10)119.1(4)O(8)—Co(1)—O(9)93.39(12)C(3)—C(2)—C(1)124.3(3)C(10)—C(11)—C(12)118.1(3)O(7)—Co(1)—O(9)88.18(14)C(2)—C(3)—C(4)121.4(3)C(21)—N(1)—Co(1)122.8(2)O(8)—Co(1)—O(1)87.83(14)C(5)—C(3)—C(2)119.8(3)C(12)—C(13)—C(15)119.0(3)O(7)—Co(1)—O(1)172.62(9)C(5)—C(3)—C(4)118.7(3)C(1)—O(1)—Co(1)129.4(2)O(9)—Co(1)—O(1)84.92(14)C(8)—C(7)—C(6)119.2(3)C(22)—N(2)—Co(1)121.9(2)O(8)—Co(1)—N(1)176.8(10)O(4)—C(4)—O(3)124.6(3)C(17)—N(1)—Co(1)119.9(2)O(7)—Co(1)—N(1)93.10(15)O(4)—C(4)—C(3)117.2(3)O(3)—C(4)—C(3)118.3(3)O(9)—Co(1)—N(1)87.48(12)O(6)—C(14)—O(5)124.2(4)N(2)—C(22)—C(23)123.6(3)O(1)—Co(1)—N(1)89.21(14)C(6)—C(5)—C(3)121.7(3)C(22)—C(23)—C(24)120.0(3)O(8)—Co(1)—N(2)92.06(13)C(5)—C(6)—C(7)119.0(4)C(7)—C(8)—C(9)118.7(3)O(7)—Co(1)—N(2)91.94(14)C(11)—C(10)—C(16)121.8(3)C(21)—N(1)—C(17)117.3(3)O(9)—Co(1)—N(2)174.5(10)C(10)—C(9)—C(8)118.8(3)C(25)—C(24)—C(23)116.0(3)O(1)—Co(1)—N(2)95.18(14)C(7)—C(8)—C(2)123.3(3)C(8)—C(2)—C(1)118.7(3)N(1)—Co(1)—N(2)87.08(12)C(13)—C(12)—C(11)121.5(4)C(23)—C(24)—C(24)#2121.2(4)O(1)—C(1)—O(2)125.3(3)C(9)—C(10)—C(16)114.6(3)C(25)—C(24)—C(24)#2122.8(4)O(1)—C(1)—C(2)117.9(3)C(11)—C(10)—C(9)123.6(3)C(9)—C(8)—C(2)117.6(3)O(2)—C(1)—C(2)116.7(3)O(5)—C(14)—C(13)113.3(4)
注 #2:-x+1,-y+2,-z+2.
配合物中心原子钴分别与1个4,4-联吡啶中的两个氮原子相连,所以依靠4,4-联吡啶连接成链状聚合物,如图2所示.链与链之间依靠4,4-联吡啶和氢键连接成二维结构,如图3所示.
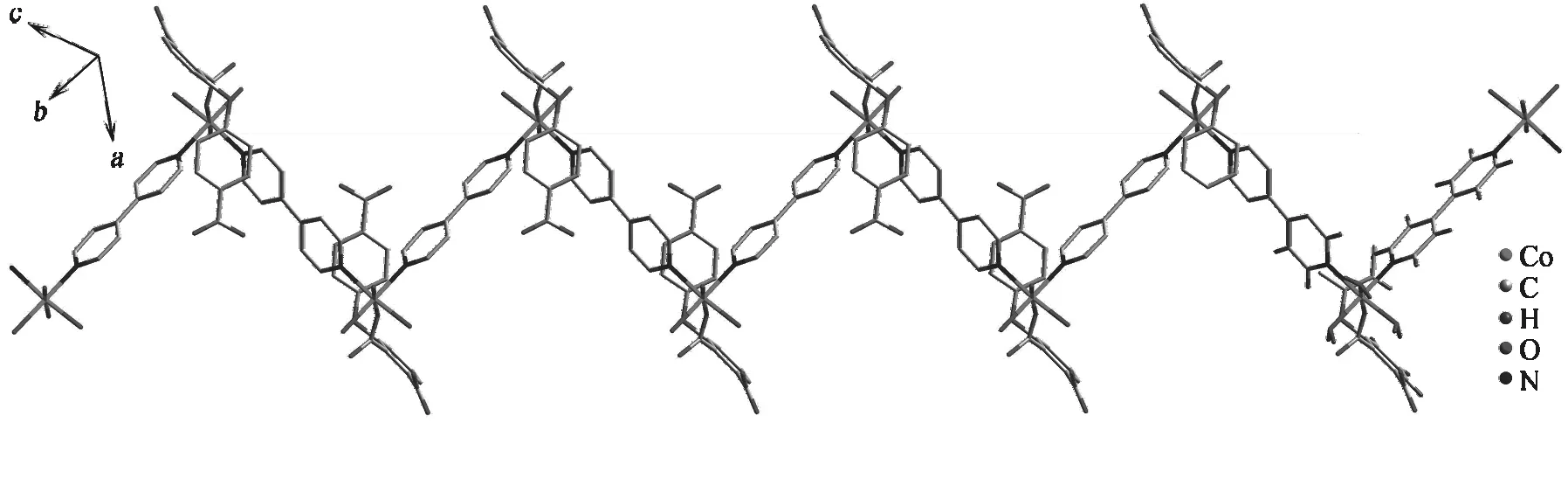
图2 配合物的一维结构
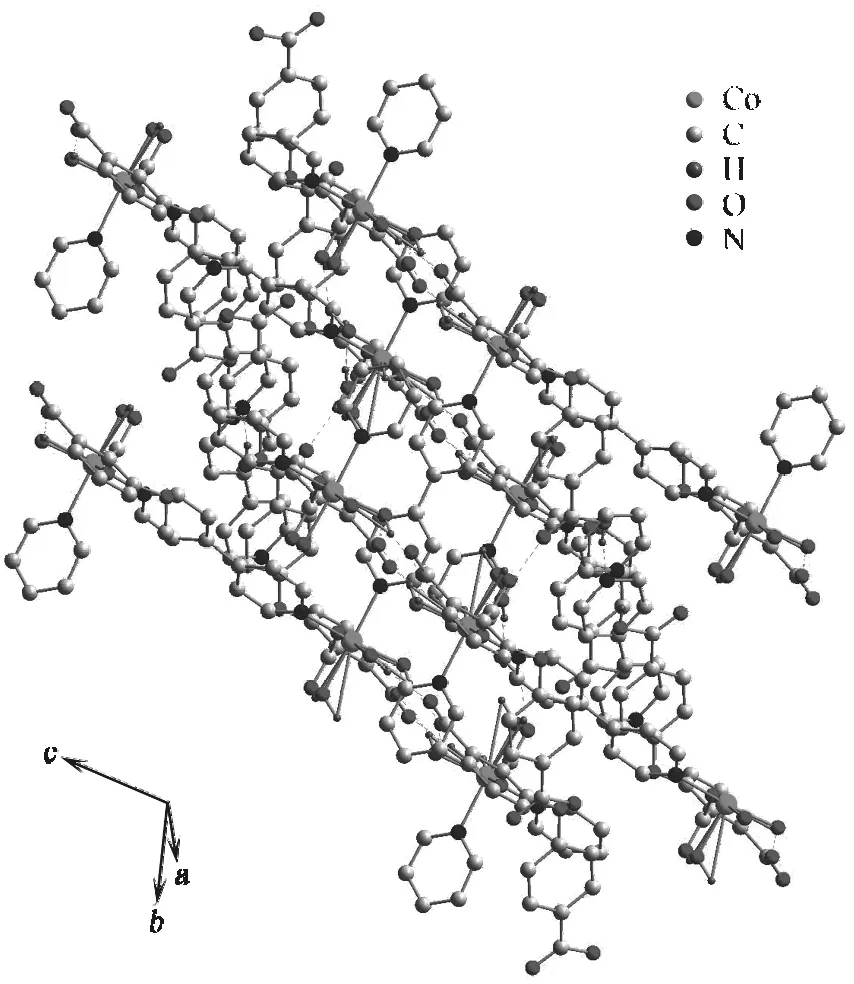
图3 配合物的二维结构
3 配合物与TC-DNA作用的荧光光谱测定
以溴化乙锭(EB)为DNA荧光探针.溴化乙锭含有一个可以嵌入DNA堆积碱基之间的三环平面基团,它与DNA的结合几乎没有碱基序列特异性.溴化乙锭(EB)为一共轭平面分子,本身荧光很弱,但能专一性地插入DNA双螺旋或三螺旋内部的碱基对之间使荧光显著增强,当
EB从DNA中出来或DNA双螺旋减少时,荧光发生淬灭[12].根据经典Stem-Volmer方程[13]:I0/I=1+Ksqr,其中:I,I0分别代表存在淬灭剂和不存在淬灭剂时的荧光强度;Ksq是Stem-Volmer淬灭常数;r是淬灭剂浓度.配合物与CT-DNA作用的荧光光谱如图4所示.由图4 可以看出:随着配合物浓度的增加,DNA-EB体系荧光逐渐减弱,并且浓度越大,荧光淬灭现象越明显.从图5可以计算出配合物的淬灭常数Ksp=0.178,对CT-DNA具有一定的插入能力.

c(DNA)=5×10-6 mol/L

图5 配合物的淬灭常数
4 结 论
采用常温法合成了钴(Ⅱ)与4,4-联吡啶和4,2′,3′-二苯醚三甲酸的配合物.其分子形式为[Co(4,4-bipy)2(L)]·3H2O(L=4,2′,3′-二苯醚三甲酸).通过元素分析、红外光谱两种手段对配合物进行了表征,表明合成的配合物为预期目标产品.用X-射线单晶衍射技术测定配合物单晶的晶体结构.在配合物晶体中,中心原子Co(Ⅱ)采取六配位模式,与2个N原子(分别来自2个4,4-联吡啶)和4个氧原子(1个来自4,2′,3′-二苯醚三甲酸、3个来自结晶水)配位,形成八面体结构.配合物依靠4,4-联吡啶连接成一维链状结构和二维结构,这使其结构更加新颖.配合物与DNA作用的荧光光谱研究表明复合物中加入配合物后,会发生淬灭现象,且浓度越大淬灭现象越明显.
参考文献:
[1] Ma L F,Wang L Y,Lu D H,et al.Structural Variation from 1D to 3D:Effects of Temperature and pH Value on the Construction of Co(Ⅱ)-H2tbip/bpp Mixed Ligands System[J].Cryst.Growth Des.,2009,9(4):1741-1749.
[2] Jia H P,Li W,Ju Z F,et al.A Novel Three-dimensional Coordination Polymer Containing Tetranuclear[Co4(μ3-OH)2] Building Blocks:Synthesis,Crystal Structure and Magnetic Behavior of {[Co2(btc)(μ3-OH)(H2O)2]· H2O}n[J].Inorg.Chem.Com-mun.,2007,10(3):265-268.
[4] Wang R,Zhang J,Li L.Conformation Preference of a Flexible Cyclohexanetetracarboxylate Ligand in Three New Metal-organic Frameworks:Structures,Magnetic and Luminescent Properties[J].Inorg.Chem.,2009,48(15):7194-7200.
[5] Shandhya Rani D,Anantha Lakshmi P V,Kamala Prasad V,et al.VO(Ⅱ),Fe(Ⅱ),Co(Ⅱ),Ni(Ⅱ)和Cu(Ⅱ)的2,3-二(3,5-二甲基-1H-吡唑基)喹啉配合物的合成与表征[J].无机化学学报,2012,28(6):1245-1250.
[6] 唐云志,杨燕明,曹赞,等.2,2′-联喹啉-4,4′-二羧酸构筑的一维钴(Ⅱ)配位聚合物[J].无机化学学报,2012,28(6):1265-1270.
[7] 计亮年,黄锦汪,莫庭焕.等.生物无机化学导论[M].广州:中山大学出版社,2001:259.
[8] 玉占君,赵君,金晶.两个Co(Ⅱ)配位超分子的合成、晶体结构及光谱[J].辽宁师范大学学报:自然科学版,2007,30(3):332-335.
[9] Lou B Y,Yuan D Q,Gao S Y,et al.A Chiral Supramolecular Architecture[Cu2(4,4′-bipyridine)2(sala)2]n·4.5nH2O(sala=N-(2-hydroxybenzyl)-l-alanine anion)[J].Journal of Molecular Structure,2004,707(1/3):231-234.
[10] 胡久荣,梁福沛,陈自卢.Cu(Ⅱ)与N-(2-羟苄基)-DL-丙氨酸、4,4′-联吡啶三元配合物的合成与晶体结构[J].无机化学学报,2007,23(7):1291-1294.
[11] 王树玲,于俊生.表面增强拉曼光谱研究小檗碱与DNA的相互作用[J].高等学校化学学报,2002,23(9):1676-1679.
[12] Chao H,Mei W J,Huang Q W,et al.DNA Binding Studies of Ruthenium(Ⅱ) Complexes Containing Asymmetric Tridentate Ligands[J].Journal of Inorganic Biochemistry,2002,92(3/4):165-170.
[13] Lakowicz J R,Weber G.Quenching of Fluorescence by Oxygen.A Probe for Structural Fluctuations in Macromolecules[J].Biochemistry,1973,12(21):4161-4170.
