下瘀血汤对肝硬化大鼠肝组织CD68和CD163蛋白表达的影响
2014-03-23刘乐平王晓斌谢洁雅丁赛丹
刘乐平,陆 芩,王晓斌,谢洁雅,丁赛丹
(温州医科大学附属第一医院1.外科实验室,2.神经外科,浙江温州 325000)
下瘀血汤对肝硬化大鼠肝组织CD68和CD163蛋白表达的影响
刘乐平1,陆 芩2,王晓斌2,谢洁雅1,丁赛丹1
(温州医科大学附属第一医院1.外科实验室,2.神经外科,浙江温州 325000)
目的探讨下瘀血汤抗肝硬化的作用机制。方法SD雄性大鼠ip给予硫代乙酰胺200 mg·kg-1每周2次,连续8周,制备大鼠肝硬化模型。造模成功后,模型大鼠于第9周首日ig给药下瘀血汤0.313,0.626和1.252 g·kg-1,每天1次,连续3周。于第11周末处死大鼠,取肝组织,用W estern蛋白质印迹法和免疫组化法测定肝组织CD68和CD163蛋白表达;用激光共聚焦方法检测肝组织CD68+TUNEL+和CD163+TUNEL+双阳性细胞,观察ED1和ED2肝巨噬细胞凋亡。结果与正常对照组比较,模型组大鼠血清谷丙转氨酶(GPT)和谷草转氨酶(GOT)活性增强(P<0.01),血清总胆红素(TBil)水平升高(P<0.01),血清白蛋白(Alb)水平显著降低(P<0.01)。与模型组比较,下瘀血汤0.626和1.252 g·kg-1组大鼠血清GPT和GOT活性以及Tbil水平均显著降低(P<0.05,P<0.01),Alb水平显著升高(P<0.01)。Western蛋白质印迹和免疫组化实验结果显示,与正常对照组比较,模型组CD68表达升高(P<0.01),CD163表达明显降低(P<0.01);与模型组相比,下瘀血汤0.626和1.252 g·kg-1组CD68表达明显降低(P<0.01),CD163表达显著升高(P<0.01)。激光共聚焦实验结果表明,与正常对照组比较,模型组大鼠CD68+TUNEL+双阳性细胞显著增加(P<0.05);与模型组比较,下瘀血汤0.626和1.252 g·kg-1组CD68+TUNEL+双阳性细胞进一步增加(P<0.05,P<0.01);所有组别均未检测到CD163+TUNEL+双阳性细胞。结论下瘀血汤对肝硬化大鼠肝功能具有改善作用,可抑制肝硬化大鼠肝组织CD68表达,促进CD163表达。
下瘀血汤;肝硬化;CD68;CD163;肝巨噬细胞
DO l:10.3867/j.issn.1000-3002.2014.01.006
肝硬化是由一种或多种病因长期或反复作用形成的弥漫性肝损害,组织病理学上有广泛的肝细胞坏死、残存肝细胞结节性再生、结缔组织增生和纤维隔形成,导致肝小叶结构破坏和假小叶形成,肝逐渐变形、变硬而发展为肝硬化。肝巨噬细胞(Kupffer cells,KC)是肝细胞的重要组成,在肝硬化形成过程中起着非常关键的作用[1]。肝硬化时肝内巨噬细胞增加,活性下降。Orfila等[2]用免疫组化法研究CCl4所致肝硬化,发现局部KC增生导致肝内巨噬细胞增多,与肝损伤和纤维化相关。正常肝脏组织中KC有2种亚型,一种是ED1 KC,CD68是ED1 KC的标志物[3],主要位于门脉血管和中央静脉周围,主要为外来细胞,几乎无吞噬能力,主要发挥促炎作用;另一种是ED2 KC,CD163是CD2 KC的标志物[4-6],沿着血窦分布,主要为局部增生的细胞,有吞噬能力,主要发挥吞噬和清除作用[7-9]。
近年来,中医药治疗肝硬化已显示明显的优势。中医认为,肝硬化的基本病机为气阴虚损、瘀血阻络和湿热内蕴等,益气、养阴、化瘀及清热利湿是常用的基本治法。下瘀血汤出自《金匮要略》,由大黄、桃仁和土鳖虫组成,具有活血逐瘀、攻坚破积之长,故凡瘀血内行、瘀阻经络之证均可因证施治,适用于肝硬化的肝血瘀阻症。下瘀血汤对实验性肝硬化的形成具有干预作用,能抗肝纤维化、防治肝硬化[10]。本研究观察下瘀血汤对肝硬化大鼠肝组织CD68和CD163蛋白表达的影响,试图从ED1和ED2 KC增殖和凋亡的途径探讨其抗肝硬化的作用机制。
1 材料与方法
1.1 动物、主要试剂和仪器
SD雄性大鼠,清洁级,购于中国科学院上海实验动物中心,实验动物许可证号为SCXK(沪)2003-0002。
硫代乙酰胺(thioacetamide,TAA),分析纯,上海凌峰化学试剂有限公司;血清谷丙转氨酶(glutamic-pyruvic transaminase,GPT)、谷草转氨酶(glutamic-oxalacetic transaminase,GOT)、白蛋白(albumin,Alb)和总胆红素(total bilirubin,TBil)测定试剂盒,均购自上海生物制品研究所;丙酮,分析纯,衢州巨化试剂有限公司;小牛血清和辣根过氧化物酶-羊抗小鼠IgG抗体,武汉博士德公司;DAB试剂盒,北京中杉金桥生物技术公司;小鼠CD68和CD163单克隆抗体,Serotic公司;CY3-羊抗小鼠IgG抗体,Jackson公司;TUNEL测定试剂盒,罗氏公司;天狼猩红(sirus red),Sigma公司产品;大黄(Radix et Rhizoma Rhei,产地:甘肃)和桃仁(Semen Persicae,产地:河北)均购自南宁医药股份有限责任公司,土鳖虫(Eupolyphaga seu Steleophaga,产地:山东)购自上海华浦中药饮片厂,由温州医科大学药学院王学宝实验师鉴定。取大黄2.0 kg,桃仁2.0 kg和地鳖虫1.2 kg制成粗粉末;加8倍体积20%乙醇(原方用黄酒,含乙醇为16.5%)浸泡1 h,回流提取2次,第1次加20%乙醇回流提取30 m in,滤过取汁;药渣再加6倍体积20%乙醇回流提取1 h,滤过取汁,合并2次提取液。回收乙醇,留浸膏备用。真空干燥后为0.585 kg,每克含生药8.889 g,冷藏保存。
纯水系统(HPLC/UP),美国Labconco公司;ASP300型自动脱水机、EG1160型石蜡包埋机、RM2035轮转切片机、HI1220烤片机和HI1210捞片机,均为德国Leica公司;20RS型高速低温离心机,德国Heraus公司;UV2102C型紫外可见光分光光度计,上海UNICO仪器有限公司;超低温冰箱(-80℃),美国Forma Scientific公司;AA-200A型分析天平,美国Denver公司;电热恒温水浴箱(37~65℃),上海医疗器械七厂;BX40型光学显微镜、IX70型倒置光学显微镜和PM-30型曝光控制系统,均为日本Olympus公司;TY-B型多用脱色摇床,上海市新波无线电厂;Power Pac Basic电泳系统,Bio-Rad公司;XJX-Ⅱ型X射线摄影暗匣:上海跃进医用光学器械厂;复日科技FR-200紫外与可见分析装置和复日FR-980生物电泳图像分析系统,上海复日科技有限公司;共聚焦图片采用Leica TCS2SP采集分析。
1.2 肝硬化模型制备
50只SD雄性大鼠,根据随机排列表完全随机选取10只作为正常对照组,其余40只ip给予TAA(40 g·L-1,水溶液)200 m g·kg-1,每周2次,连续8周,制备大鼠肝硬化模型[11]。8周末,随机选取正常大鼠、模型大鼠各4只作为药前观察,其余模型大鼠于第9周首日随机分为4组,每组9只,即模型组和下瘀血汤0.313,0.626和1.252 g·kg-1组,下瘀血汤组分别ig给予下瘀血汤0.313(相当于生药1.6 g·kg-1,为65 kg体质量成人临床用量的4倍),0.626和1.252 g·kg-1[12],给药体积10 m L·kg-1(用蒸馏水10 m L稀释),正常对照组和模型组大鼠ig给予等体积生理盐水,每天1次,连续3周。
1.3 标本采集
正常对照组和造模大鼠于造模8周末随机抽取4只,用戊巴比妥钠50 m g·kg-1麻醉后打开腹腔,观察肝的大体形态,取新鲜肝方叶小块组织,4%甲醛固定,24 h内石蜡包埋,切片。11周末,所有大鼠均用戊巴比妥钠麻醉后打开腹腔,观察肝的大体形态,经下腔静脉采血,取新鲜肝方叶小块组织,一部分制备冰冻切片,另一部分制备石蜡切片。剩余肝组织分装,-80℃保存。血液4℃静置3 h后,1000×g离心30 m in,分离血清,-80℃保存备用。
1.4 肝组织病理变化观察
肝组织石蜡切片按常规方法进行HE染色和天狼星红染色,光学显微镜下观察肝组织的病理变化。
1.5 血清肝功能检测
血清GPT活性,赖氏法;血清GOT活性,赖氏法;血清TBil含量,重氮法;血清Alb含量,溴甲酚绿法;均按照试剂盒说明书方法测定。
1.6 Western蛋白质印迹法测定肝组织CD68和CD163表达
大鼠肝组织裂解,匀浆,离心后取上清液(即肝组织总蛋白)变性10 m in,以15%SDS-聚丙烯酰胺凝胶电泳,将分离的蛋白转移至硝酸纤维素膜,5%脱脂奶粉封闭1 h,加小鼠CD68和CD163抗体,4℃孵育过夜,用TBST充分洗涤后,加入辣根过氧化物酶标记羊抗小鼠IgG抗体(二抗)37℃孵育1 h,TBST充分洗涤,ECL显影,曝光,扫描曝光后,应用复日FR-200生物电泳图像分析系统分析底片中的目的条带,计算机自动读取并记录每条条带的积分吸光度值。GAPDH作为内参照。
1.7 免疫组化测定肝组织CD68和CD163表达
肝组织石蜡切片按SP法进行免疫组化染色,脱蜡至水,柠檬酸缓冲液微波修复抗原,PBS冲洗3次,0.3%过氧化氢去除内源性过氧化物酶10 m in,PBS冲洗3次,加入小鼠CD68或CD 163单抗4℃孵育过夜,PBS冲洗3次,加入辣根过氧化物酶标记的二抗37℃孵育30 m in,PBS冲洗3次,DAB显色,苏木素复染,脱水,透明,封片,显微镜下观察。PBS代替一抗作为阴性对照。
1.8 激光共聚焦显微镜测定ED1和ED2 KC凋亡
用TUNEL分别与CD68和CD163共定位观察KC凋亡。首先用TUNEL检测试剂盒将TUNEL标记上FITC绿色荧光,随后血清封闭30 m in,加小鼠CD68或CD163单抗,37℃孵育1 h,PBS冲洗3次,加CY3-羊抗小鼠IgG抗体37℃孵育1 h,PBS冲洗3次,DAPI染核,封片,激光共聚焦显微镜观察CD68+TUNEL+和CD163+TUNEL+双阳性细胞。
1.9 统计学分析
2 结果
2.1 下瘀血汤对肝硬化模型大鼠肝功能的影响
与正常对照组比较,模型组大鼠血清GPT和GOT活性显著增强(P<0.01),Tbil水平显著升高(P<0.01),Alb水平显著降低(P<0.01)。与模型组比较,下瘀血汤0.626和1.252 g·kg-1组大鼠血清GPT和GOT活性以及Tbil水平均显著降低(P<0.05,P<0.01),Alb水平显著升高(P<0.01);下瘀血汤0.313 g·kg-1组大鼠血清GPT活性以及Tbil和Alb水平无显著差异,GOT活性显著降低(P<0.05)(表1)。
2.2 下瘀血汤对大鼠肝硬化组织病理变化的影响
正常大鼠肝小叶结构清晰,肝细胞索由中央静脉向四周呈放射状排列,中央静脉、汇管区动、静脉和胆管结构正常,肝窦不扩张,肝窦内和汇管区周围可见少量的间质细胞(图1A1和B1)。造模8周后,模型大鼠肝内可见肝细胞脂肪变性,且累及整个肝小叶,正常肝细胞减少,可见很薄的胶原纤维间隔形成,极少见紧密包绕的完整假小叶结构。肝窦扩张,窦内和汇管区可见较多的间质细胞,以活化的星状细胞为主,可见新生的纤维呈尾展状与星状细胞存在结构上的联系,少量炎症细胞浸润,大胆管损害明显,有少量小胆管增生(图1A2和B2)。表明肝硬化大鼠造模成功。给药结束后,与模型组(图1A3和B3)比较,下瘀血汤0.313 g·kg-1组大鼠见少量肝细胞肿胀,汇管区和中央静脉周围有少量浸润的炎症细胞,胆小管增生程度低,少量增生纤维间隔(图1A4和B4);下瘀血汤0.626 g·kg-1组大鼠胶原纤维增生明显减轻,少见完整包绕假小叶结构(图1A5和B5);下瘀血汤1.252 g·kg-1组纤维间隔较窄、疏松而不连续(图1A6和B6)。表明下瘀血汤可改善模型大鼠肝硬化症状。
2.3 下瘀血汤对大鼠肝硬化组织CD68和CD163蛋白表达的影响
Western蛋白质印迹实验结果表明,正常对照组大鼠有少量CD68蛋白表达,模型组大鼠CD68蛋白表达显著升高(P<0.01);与模型组比较,下瘀血汤0.626和1.252 g·kg-1可以显著降低CD68蛋白表达(P<0.01),下瘀血汤0.313 g·kg-1组无明显变化(图2A)。由图2B结果显示,正常对照组CD163蛋白表达较高,模型组CD163蛋白表达显著降低(P<0.01);与模型组相比,下瘀血汤0.626和1.252 g·kg-1可以显著升高CD163蛋白表达(P<0.01),下瘀血汤0.313 g·kg-1组无明显变化。
免疫组化实验结果表明,正常对照组大鼠肝组织CD68表达水平较低,主要分布在肝窦;模型组CD68表达升高,除了分布肝窦外,还有一部分在汇管区和纤维间隔内;下瘀血汤0.313 g·kg-1组较模型组无明显差异,0.626和1.252 g·kg-1组CD68表达显著降低(图3A)。图3B结果显示,正常对照组大鼠CD163分布在肝窦和汇管区,呈小棒状;模型组CD163表达减少,肝窦的CD163大部分消失,主要在汇管区分布;下瘀血汤0.313 g·kg-1组较模型组无明显变化,下瘀血汤0.626和1.252 g·kg-1组CD163表达较模型组明显升高,并且CD163表达分布在肝窦。

Tab.1 Effects of Xiayuxue decoction(XYXD)on liver function of rats with liver cirrhosis
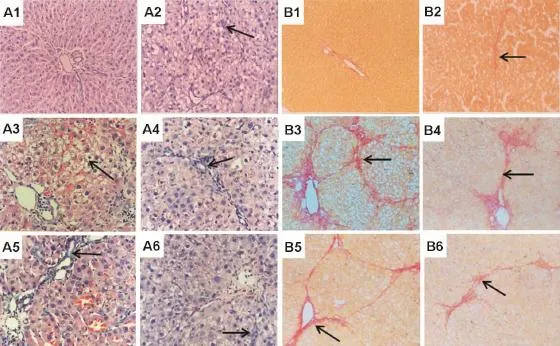
Fig.1 Effect of XYXD on liver histo pathological changes in liver cirrhotic rats(A.HE×200,B.Sirius red×100).See Tab.1 for the rat treatment.1:normal control;2:m odel,8 week;3:model,11 week;4,5 and 6:XYXD 0.313,0.626 and 1.252 g·kg-1group,respectively.Arrows show inflammatory cells and fiber spacing.
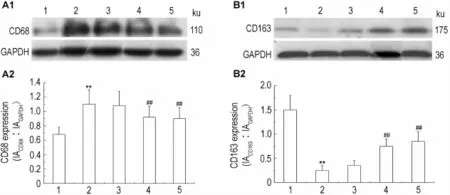
Fig.2 Effect of XYXD on CD68(A)and CD163(B)protein expression in liver tissue of rats with liver cirrhosis detected with Western blotting.See Tab.1 for rat treatment.1:normal control;2:model;3,4 and 5:XYXD 0.313,0.626 and 1.252 g·kg-1group,respectively.A2 and B2 was the semiquantitative result of A1 and B1,respectively.IA:integrated absorbance.,n=6-9.**P<0.01,com pared with normal control group;##P<0.01,com pared with model group.
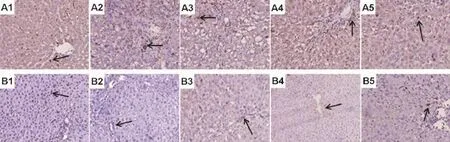
Fig.3 Effect of XYXD on CD68(A)and CD163(B)protein expression in liver tissue of rats with liver cirrhosis(Immunohistochemistry×200).See Tab.1 for the rat treatment.1:normal control;2:model;3,4 and 5:XYXD 0.313,0.626 and 1.252 g·kg-1group,respectively.Arrows show positive cells.
2.4 下瘀血汤对大鼠肝硬化组织ED1和ED2 KC凋亡的影响
如图4所示,CD68和TUNEL激光共聚焦实验结果表明,正常对照组大鼠肝组织中CD68+TUNEL+双阳性细胞较少,在TUNEL+细胞中占(10±4)%;模型大鼠双阳性细胞显著增加,在TUNEL+细胞中占(20±7)%(P<0.05);与模型组比较,下瘀血汤0.313 g·kg-1组双阳性细胞数量无明显变化,为(15±5)%,0.626 g·kg-1组双阳性细胞增加至(25±9)%(P<0.05),1.252 g·kg-1组进一步增加,为(45±10)%(P<0.01)。表明正常大鼠的ED1KC凋亡很少,模型组大鼠出现ED1 KC凋亡,下瘀血汤可增加模型大鼠ED1 KC凋亡,且随着浓度的增加凋亡细胞增多。
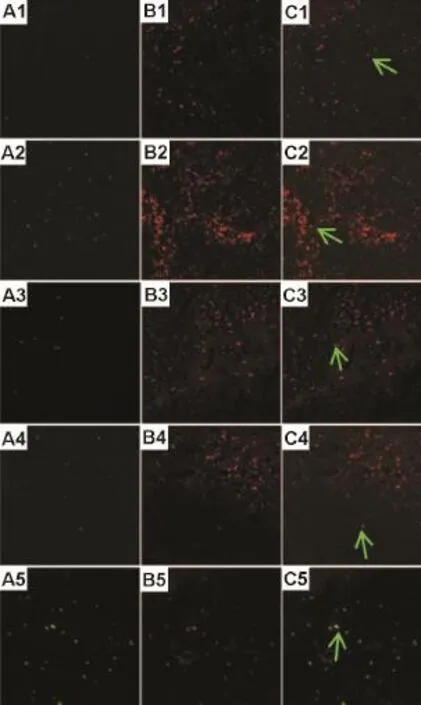
Fig.4 Effect of XYXD on apoptosis of ED1 KC in liver tissue of rats with liver cirrhosis(×200,TUNEL,green;CD68,red).See Tab.1 for rat treatment.A:TUNEL;B:CD68-CY3;C:confocal.1:normal control;2:model;3,4 and 5:XYXD 0.313,0.626 and 1.252 g·kg-1group,respectively.Arrows show double positive cells.
CD163和TUNEL激光共聚焦实验结果显示,各组均未检测到CD163+TUNEL+双阳性细胞,表明在正常对照、模型和下瘀血汤组大鼠肝组织内均无ED2 KC凋亡(图5)。
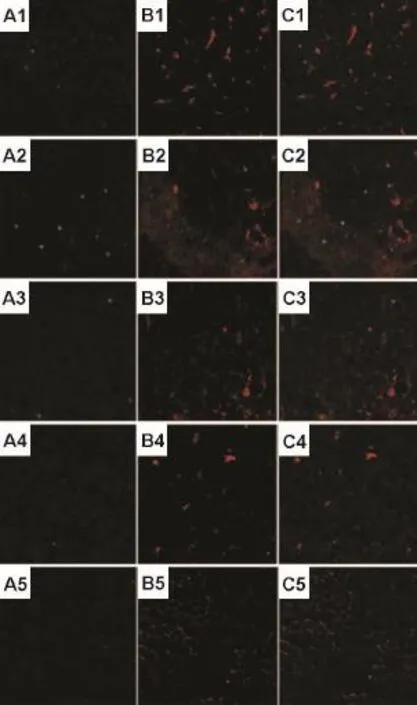
Fig.5 Effect of XYXD on apoptosis of ED2 KC in liver tissue of rats with liver cirrhosis(×200,TUNEL,green;CD163,red).See Tab.1 for rat treatment.A:TUNEL;B:CD163-CY3;C:confocal.1:normal control;2:model group;3,4 and 5:XYXD 0.313,0.626 and 1.252 g·kg-1group,respectively.
3 讨论
本研究采用大鼠ip给予TAA水溶液的方法制备肝硬化模型,连续注射8周,肝组织病理学观察确定模型成功后,ig给予下瘀血汤,观察下瘀血汤对肝硬化大鼠肝脏组织CD68和CD163蛋白表达的影响。
本研究Western蛋白质印迹和免疫组化实验结果表明,正常对照组大鼠肝组织低表达CD68,高表达CD163;模型组大鼠CD68表达显著升高,CD163表达显著降低;下瘀血汤0.626和1.252 g·kg-1可明显降低CD68表达,增强CD163表达。由此提示,下瘀血汤对肝硬化的治疗作用可能与其降低CD68表达并增加CD163表达有关。
KC在肝硬化形成过程中起重要作用。CD68是ED1 KC的特异性标志物,CD163是ED2 KC的特异性标志物。上述结果提示,下瘀血汤降低肝硬化组织CD68蛋白表达、增强CD163蛋白表达是否是其促进ED1 KC凋亡和ED2 KC增殖,使得ED1 KC数量减少和ED2 KC数量增加引起的,为此,本研究分别用CD68和TUNEL以及CD163和TUNEL激光共聚焦的方法进一步观察了下瘀血汤对肝硬化组织CD68+TUNEL+和CD163+TUNEL+双阳性细胞数量的变化。TUNEL+阳性细胞为凋亡细胞。实验结果表明,模型组肝硬化组织CD68+TUNEL+双阳性细胞在TUNEL+阳性细胞中的百分比明显增加,下瘀血汤0.626和1.252 g·kg-1可使CD68+TUNEL+双阳性细胞进一步增多,提示下瘀血汤可能促进ED1 KC凋亡,这一结果与其降低肝硬化组织CD68蛋白表达一致。但模型组CD68+TUNEL+双阳性细胞较正常对照组增多,这与模型组CD68蛋白表达升高不符,原因尚不清楚。
另外,激光共聚焦实验在各组中均未检测到CD163+TUNEL+双阳性细胞,提示肝硬化组织无ED2 KC凋亡。但Western蛋白质印迹法和免疫组化实验结果表明,模型组肝硬化组织CD163蛋白表达降低,下瘀血汤0.626和1.252 g·kg-1组CD163蛋白表达升高。由此提示,下瘀血汤对肝硬化组织ED2 KC凋亡无影响,可能是促进了ED2 KC增殖。
综上所述,下瘀血汤可降低大鼠肝硬化组织CD68蛋白表达,促进CD163蛋白表达。下瘀血汤抗肝硬化的作用机制有可能与促进ED1 KC凋亡有关。至于其是否可促进ED1 KC增殖尚需深入研究。
[1] Huang CY.Liver cirrhosis and liver immune system[J].Foreign Medl Sci Surg(国外医学外科学分册),2004,31(2):102-105.
[2] Orfila C,Lepert JC,Alric L,Carrera G,Beraud M,Vinel JP,et al.Expression of TNF-alpha and immunohistochemical distribution of hepatic macrophage surface markers in carbon tetrachloride-induced chronic liver injury in rats[J].Histochem J,1999,31(10):677-685.
[3] Damoiseaux JG,Döpp EA,Calame W,Chao D,MacPherson GG,Dijkstra CD.Rat macrophage lysosomal membrane antigen recognized by monoclonal antibody ED1[J].Immunology,1994,83(1):140-147.
[4] Kumagai K,Kiyosawa N,Ito K,Yamoto T,Teranishi M,Nakayama H,et a l.Influence of Kupffer cell inactivation on cycloheximide-induced hepatic injury[J].Toxicology,2007,241(3):106-118.
[5] Polfliet MM,Fabriek BO,Daniëls WP,Dijkstra CD,van den Berg TK.The rat macrophage scavenger receptor CD163:expression,regulation and role in inflammatory mediator production[J].Immunobiology,2006,211(6-8):419-425.
[6] Zwad lo G,Voege liR,Schulze Osthoff K,Sorg C.A monoclonal antibody to a novel differentiation antigen on human macrophages associated with the down-regulatory phase of the inflammatory process[J].Exp Cell Biol,1987,55(6):295-304.
[7] Gomes LF,Lorente S,Simon-Giavarotti KA,Areco KN,Araújo-Peres C,Vide la LA.Tri-iodothyronine differentially induces Kupffer cell ED1/ED2 subpopulations[J].Mol Aspects Med,2004,25(1-2):183-190.
[8] Kono H,FujiiH,Asakawa M,Yamamoto M,Maki A,Matsuda M,et al.Functional heterogeneity of the Kupffer cell population is involved in the mechanism of gadolinium chloride in rats administered endotoxin[J].J Surg Res,2002,106(1):179-187.
[9] Luckey SW,Petersen DR.Activation of Kupffer cells during the course of carbon tetrachloride-induced liver injury and fibrosis in rats[J].Exp Mol Pathol,2001,71(3):226-240.
[10] Qin DP,Jiang TY,Ren YB,Han JX,Xu ZL,Zheng SC.Interventional study of decoction for removing blood stasis(Xiayuxue Tang)on experimental hepatic cirrhosis and lipid peroxidation[J].Chin J Inf TCM(中国中医药信息杂志),2003,10(3):25-27.
[11] Fitzhugh OG,Nelson AA.Liver tumors in rats fed thiourea or thioacetamide[J].Science,1948,108(2814):626-628.
[12] Ding SD,Chen BC,Liu Y,Dong QT,Li ZP,Yu Z.Proteomic study of Xiayuxue Decoction on liver cirrhosis of rats[J].Chin Tradit Herb Drugs(中草药),2012,43(1):131-138.
Effect of Xiayuxue decoction on CD68 and CD163 protein expression in liver tissue of rats with liver cirrhosis
LIU Le-ping1,LU Qin2,WANG Xiao-bin2,XIE Jie-ya1,DING Sai-dan1
(1.Key Laboratory of Surgery,2.Neurosurgery Department,the First Affiliated Hospital of Wenzhou Medical University,Wenzhou 325000,China)
OBJECTlVETo investigate the mechanism of anti-liver cirrhosis of Xiayuxue decoction.METHODSTen male SD rats were randomly chosen as the normal control group,and the remaining 40 rats were ip given thioacetamide 200 m g·kg-1,twice each week for 8 weeks,to prepare the rat model with liver cirrhosis.At the 9 th week,the model rats were randomly assigned to model,Xiayuxue decoction 0.313,0.626 and 1.252 g·kg-1groups.The rats were ig given Xiayuxue decoction once daily for3 weeks.At the 11th week,CD68 and CD163 protein expression in liver tissue was detected with Western blotting and immunolistochemistry method.CD68+TUNEL+and CD163+TUNEL+double positive cells in liver tissues were analyzed under a laser confocal microscope.RESULTSCompared with normal control group,the activity of serum glutamic-pyruvic transaminase(GPT)and glutamic-oxalacetic transaminase(GOT)was enhanced(P<0.01),the level of total bilirubin(Tbil)was elevated(P<0.01),while the level of albumin(Alb)was decreased in model group(P<0.01).Compared with model group,the activity of serum GPT and GOT and the level of Tbil were decreased(P<0.05,P<0.01),while the level of Alb was increased in Xiayuxue decoction group.Western blotting and immunohistochemistry results showed that the expression of CD68 was increased(P<0.01)and that of CD163 was significantly reduced(P<0.01)in the model group.Compared with model group,the expression of CD68 was reduced(P<0.01)and the expression of CD163 was significantly increased(P<0.01)in Xiayuxue decoction 0.626 and 1.252 g·kg-1groups.Laser confocal results showed that CD68+TUNEL+double-positive cells were significantly increased(P<0.05)in mode l group com pared with the normal group.Compared with the m odel group,the CD68+TUNEL+double-positive cells were significantly increased(P<0.05 or P<0.01)in Xiayuxue decoction 0.626 and 1.252 g·kg-1groups.CD163+TUNEL+double-positive cells were not detected in any group.CONCLUSlONXiayuxue decoction improves liver functions of rats with liver cirrhosis,inhibits CD68 expression and promotes CD163 expression in tissues of liver cirrhosis.
Xiayuxue decoction;liver cirrhosis;CD68;CD163;Kupffer cells
DING Sai-dan,E-mail:firstdsdan@hotmail.com,Tel:(0577)88069338
R285,R975
A
1000-3002(2014)01-0035-07
Foundation item:The project supported by Science and Technology Project of Wenzhou City(Y20110155)
2013-07-22 接受日期:2013-12-03)
(本文编辑:齐春会)
温州市科技计划项目(Y20110155)
刘乐平(1986-),女,理学学士,助理实验员,主要从事中医药治疗肝硬化药理作用机制研究。
丁赛丹,E-mail:firstdsdan@hotmail.com,Tel:(0577)88069338
