苯胺对水中挥发酚测定干扰规律的研究
2014-03-22
(山西省环境监测中心站,山西 太原030027)
酚类物质是水中的高毒物质,是细胞的原浆毒物,低浓度的酚类物质能使蛋白质变性,高浓度的酚类能使蛋白质沉淀,对一切生活个体都有毒杀作用,对皮肤及粘膜具有强烈的腐蚀作用,也可抑制中枢神经系统或损害肝、肾功能。长期饮用被酚类物质污染的水,可引起头昏、出疹、瘙痒、贫血、恶心、呕吐及各种神经系统症状。水中酚类的主要来源有煤气洗涤、炼焦、合成氨、造纸、木材防腐以及化工行业的工业废水。根据酚类能否与水蒸气一起蒸出,分为挥发酚和不挥发酚,通常认为沸点在230℃以下的为挥发酚,一般为一元酚;沸点在230℃以上的为不挥发酚[1]。水质中挥发酚的测定方法有很多,如:高效液相色谱法、气相色谱法[2]、流动注射法[3,4]、4-氨基安替比林分光光度法[5]等,其中最经典且最常用的方法是4-氨基安替比林分光光度法,国际标准化颁布的方法同样如此,很多文献从实验室用水、4-氨基安替比林的纯化及存放时间等方面[6-8]对挥发酚测定的影响进行了大量的报道,然而对于该方法中苯胺干扰规律及消除方法鲜有报道,笔者对苯胺如何干扰挥发酚的测定及如何消除苯胺的干扰进行探讨。
1 实验方法
1.1 实验原理
酚类化合物在pH 10±0.2介质中,在铁氰化钾的存在下,与4-氨基安替比林反应生成的橙红色安替比林染料可被三氯甲烷萃取,并在460 nm波长处有最大吸收。
1.2 实验仪器及主要试剂
721分光光度计,500 ml全玻璃蒸馏器,500 ml分液漏斗;
500 mg/L苯酚标准储备液(环保部国家标准样品研究中心配制),1.00 mg/L苯酚标准使用液,100 mg/L苯胺标准储备液(环保部国家标准样品研究中心配制),10.00 mg/L苯胺标准使用液,氯化铵(分析纯),4-氨基安替比林(分析纯),铁氰化钾(分析纯),盐酸(优级纯)、磷酸(优级纯),氢氧化钠(分析纯)二氯甲烷(农残级),实验用水为无酚用水。
2 挥发酚标准曲线的绘制实验
分别在7个分液漏斗中加入100 ml水,依次加入0 ml、0.50 ml、1.00 ml、3.00 ml、5.00 ml、7.00 ml、10.00 ml苯酚标准使用液,再分别加水至250 ml,加2.0 ml缓冲溶液混匀,再加入1.5 ml的2%的4-氨基安替比林溶液,混匀,再加1.5 ml的8%铁氰化钾溶液混匀,充分混匀后,放置10 min。经三氯甲烷萃取后,放入30 mm的比色皿中,以三氯甲烷为参比,测得吸光度,经空白校正后,绘制工作曲线。
苯酚标准曲线及标样测试结果见表1。由下表可知,本次实验工作曲线空白吸光度小于0.1,相关系数r≥0.999 5,标样测定值准确,表明该曲线可以满足工作需要。
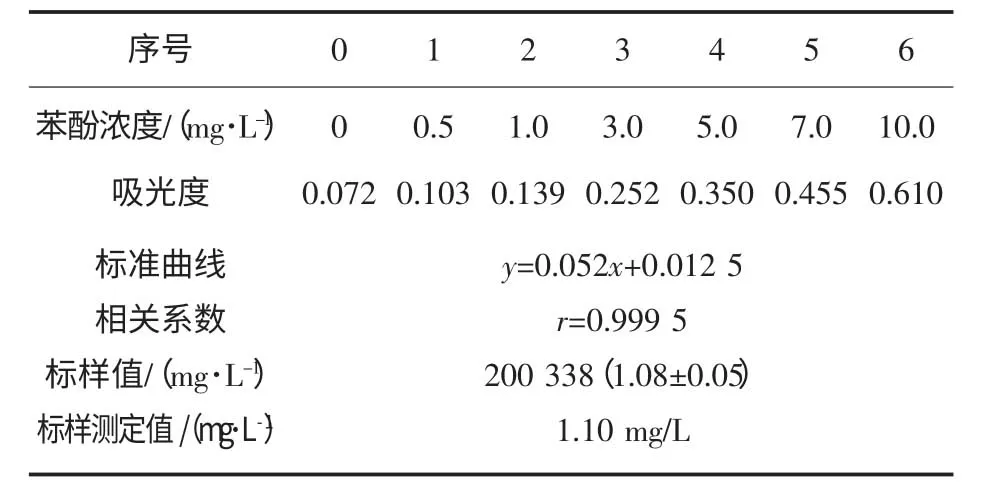
表1 苯酚的标准曲线
3 苯胺对挥发酚测定的干扰及消除实验
不同浓度的苯胺对挥发酚的测定干扰。
在一组10个500 ml蒸馏瓶中,分别加入100 ml水及5 ml 1 mg/L苯酚标准使用液,再依次分别加 入0 ml、0.50 ml、1.00 ml、1.50 ml、2.00 ml、2.50 ml、12.50 ml、17.50 ml、25.00 ml和37.50 ml 100 mg/L苯胺标准溶液,再分别加水至250 ml,使得溶液中苯酚的浓度为0.02 mg/L,苯胺的浓度分别为0.0 mg/L、0.2 mg/L、0.4 mg/L、0.6 mg/L、0.8 mg/L、1.0 mg/L、5.0 mg/L、7.0 mg/L、10.0 mg/L、15.0 mg/L,蒸馏冷却至室温后转移至500 ml的分液漏斗中,以下步骤同挥发酚标准曲线的绘制。
实验结果见表2。结果表明,当体系中苯胺的浓度小于或等于1 mg/L时,对挥发酚的测定没有干扰;当体系中苯胺的浓度大于1 mg/L小于10 mg/L时,在pH 10±0.2介质中,铁氰化钾的存在下,苯胺与4-氨基安替比林反应生成的橙红色安替比林染料也可被三氯甲烷萃取,对挥发酚的测定产生微弱的正干扰;当体系中苯胺的浓度大于或等于10 mg/L时,苯胺对挥发酚的测定产生显著的正干扰,而且随着苯胺浓度的增大,吸光度逐渐增大,正干扰逐渐增强。
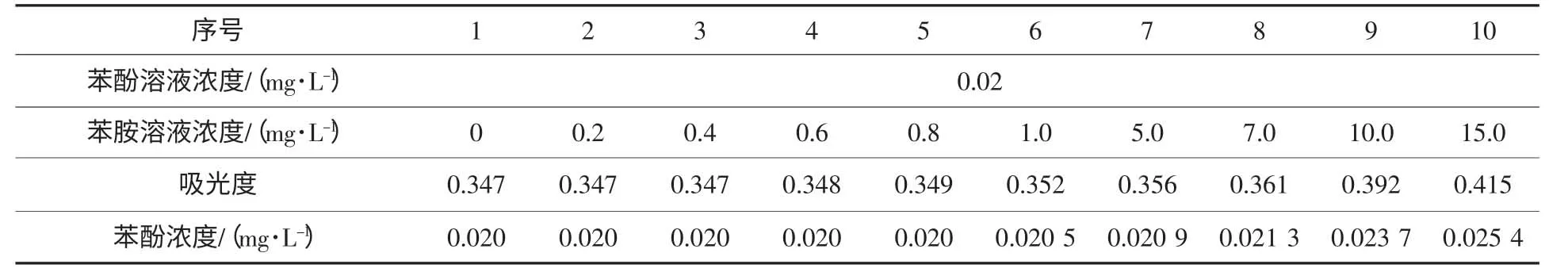
表2 不同浓度的苯胺对挥发酚的测定干扰
4 干扰的消除
4.1 盐酸消除苯胺干扰的实验
于一组9个蒸馏瓶中,分别加入100 ml水及5 ml苯酚标准使用液,再依次加入0 ml、5.00 ml、5.00 ml、10.00 ml、10.00 ml、25.00 ml、25.00 ml、30.00 ml、30.00 ml苯胺标准溶液,再分别加水至250 ml使得溶液中苯酚的浓度为0.02 mg/L,苯胺的浓度分别为0 mg/L、2.0 mg/L、2.0 mg/L、4.0 mg/L、4.0 mg/L、10.0 mg/L、10.0 mg/L、12.00 mg/L、12.00 mg/L,盐酸调节pH值至0.5,蒸馏冷却至室温后转移至500 ml的分液漏斗中,以下步骤同挥发酚标准曲线的绘制。
标准HJ 503-2009中指出“苯胺类物质可与4-氨基安替比林发生显色反应而干扰酚的测定,一般在酸性(pH<0.5)条件下,可以通过预蒸馏分离。”然而,根据磷酸的电离常数,即使是优级纯的磷酸,其本身的pH值也只有0.48左右[9],不可能再将试样pH值调节到0.5以下,因此在实验分析过程中不能用磷酸来调节试样的pH值以消除苯胺对挥发酚的测定干扰。鉴于苯酚是弱酸,苯胺是弱碱的性质[10],采用盐酸调节试样的pH值,来消除苯胺对挥发酚测定的干扰,实验结果见表3。当苯胺的浓度大于等于10 mg/L时,单纯使用盐酸调节pH值不能达到消除苯胺的目的,不适宜采用光度法进行挥发酚的测定,建议采用气相色谱-质谱方法或液相色谱方法进行仪器分析,以获取挥发酚的测定值。
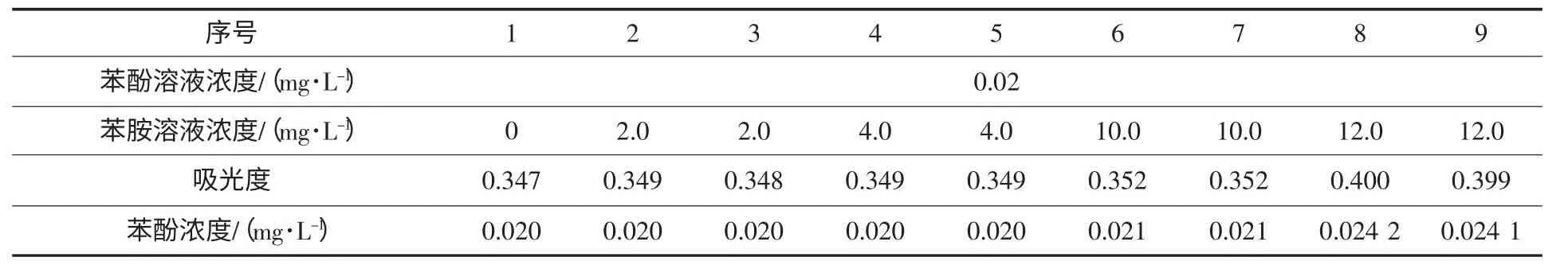
表3 盐酸消除苯胺对挥发酚测定干扰的实验结果
4.2 萃取法消除苯胺干扰实验
9个分液漏斗中分别加入100 ml水及5 ml苯酚标准使用液,再依次加入0 ml、2.50 ml、2.50 ml、7.50 ml、7.50 ml、12.50 ml、12.50 ml、17.50 ml、17.50 ml苯胺标准溶液,再分别加水至250 ml使得溶液中苯酚的浓度为0.02 mg/L,苯胺的浓度分别为0 mg/L、1.0 mg/L、1.0 mg/L、3.0 mg/L、3.0 mg/L、5.0 mg/L、5.0 mg/L、7.00 mg/L、7.00 mg/L,氢氧化钠溶液调节pH值至12,用二氯甲烷萃取后,将水相转移至500 ml蒸馏瓶中,再用磷酸调节pH值至4左右,蒸馏冷却至室温后转移至500 ml的分液漏斗中,以下步骤同挥发酚标准曲线的绘制。
利用苯酚及苯胺的性质,首先使用氢氧化钠将试样的pH值调至12左右,苯酚与氢氧化钠发生酸碱中和反应生成苯酚钠,极好地将苯酚固定在了水相;而苯胺本身是弱碱,不与氢氧化钠反应,故在试样中加入二氯甲烷萃取剂后,充分振荡,可以将苯胺转移至有机相,以达到苯酚与苯胺分离的目的,弃去有机相。此时将水相转移至烧杯中,在通风柜中水浴上加热以除去水相中残留的二氯甲烷[11],用磷酸调节pH值至4左右,蒸馏后进行测定,结果见表4。

表4 萃取法消除苯胺对挥发酚测定干扰的实验结果
5 实验结论
通过研究发现只有当水样中的苯胺达到一定浓度时,才对4-氨基安替比林萃取光度法测定水中的挥发酚产生正干扰;在我们日常分析工作中,当水样中苯胺类物质浓度小于1 mg/L时,依据HJ 503-2009进行测定即可。实际工作中有些情况较为复杂,水体中可能同时存在较高浓度的苯胺,当水样中苯胺类物质浓度大于1 mg/L小于10 mg/L时,可以使用盐酸调节水样的pH值,蒸馏后进行测定,也可以将水样的pH值调至碱性,萃取出苯胺,再将水相的pH值调至酸性,蒸馏后进行测定;当水样中苯胺类物质浓度大于10 mg/L时,建议萃取后使用气相色谱-质谱或液相色谱仪进行测定。
[1]国家环境保护总局《水和废水监测分析方法》编委会.水和废水监测分析方法[M].4版(增补版).北京:中国环境出版社,2002:29,508-514.
[2]赵艳红,王立国.气相色谱法测定生活饮用水中多种微量挥发酚[J].新疆化工,2005(3):26-27.
[3]曲海琳.连续流动注射分光光度法检测水中挥发酚含量[J].山西科技,2009(4):129-130.
[4]李勇,陈斌生,魏建荣.流动注射测定饮用水中挥发酚类化合物方法的研究[J].中国卫生检验杂志,2004,14(3):300-301.
[5]大连市环境监测中心.HJ 503-2009 水质挥发酚的测定4-氨基安替比林分光光度法[S].北京:中国环境科学出版社,2009.
[6]杨功勇.4-氨基安替比林法测定挥发酚常见问题的探讨[J].滁州学院学报,2004,6(4):118-119.
[7]李志亮,张蕙兰.挥发酚测定中影响空白值大小因素的探讨[J].环境研究与监测,2007,20(3):22-24.
[8]夏冬前,徐波.用氯仿降低挥发酚空白值的方法探讨[J].现代测量与实验室管理,2005(1):28-29.
[9]华中师范大学,东北师范大学,陕西师范大学.分析化学[M].2版.北京:高等教育出版社,2001:198-204.
[10]胡宏文.有机化学[M].2版.北京:高等教育出版社,1990:512-515.
[11]姚运先.环境监测技术[M].2版.北京:化学工业出版社,2008:72-73.
