日落黄在聚结晶紫膜修饰电极上的 电化学行为及其测定
2014-03-22,
,
(菏泽学院化学与化工系,山东菏泽 274015)
食品添加剂是为改善食品品质和色、香、味,以及为防腐、保鲜和加工工艺的需要而加入食品中的人工合成或者天然物质。日落黄是一种人工合成的偶氮类色素(结构式见图1),是我国允许使用的食品添加剂。由于其能够保持和改善食品的色、香、味,一般有色泽鲜艳、着色力强、坚牢度大、性质稳定、价格低廉等优点[1],受到商家和消费者的青睐,常用于糖果、饮料等食品和药物的着色。由于含有R-N=N-R键、苯环结构,且多以苯、萘等化工产品为原料,经过磺化、偶氮化等一系列有机反应合成。因此它对人体存在一定的不安全性,有慢性毒性和致癌性[2],所以对其含量的测定显得尤为重要。根据中国食品添加剂使用卫生标准规定日落黄在各类食品中的最大用量为0.02~0.6g/kg[3]。
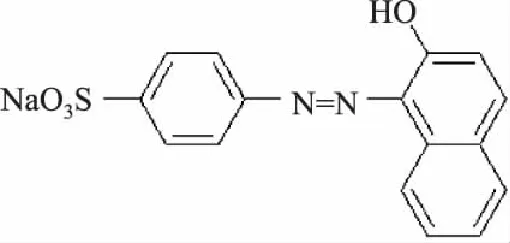
图1 日落黄的化学结构式 Fig.1 Chemical structure of sunset yellow
目前报道的对食品中日落黄的检测方法主要有光谱法[4-8]与色谱法[9-11]等。色谱应用更为广泛,但是仪器条件和方法检测要求比较高,需要复杂的预处理过程与大量的有机溶剂,专门的操作人员,为克服色谱方法的不足,本工作探讨了测定日落黄的电化学新方法。由于日落黄结构中含有电化学活性的官能团,因此建立了电化学修饰电极测定日落黄。电化学修饰电极对日落黄的测定已有报道[12-13],但是聚结晶紫修饰膜电极测定日落黄还未见报道。
结晶紫是一种三苯甲烷类阳离子染料,它在弱酸性条件下可以在玻碳电极表面电氧化聚合成膜[14],该聚结晶紫膜呈现紫色且附着力好,膜结构紧密均匀,该修饰电极已用于尿酸的测定[15]。本工作建立了测定日落黄的简便、快速、灵敏的新方法。将该方法用于样品中日落黄的测定,结果令人满意。
1 材料与方法
1.1 材料与仪器
结晶紫 广州化学试剂厂;日落黄 阿拉丁试剂(上海)有限公司;柠檬酸-磷酸氢二钠缓冲溶液 不同比例的0.1mol/L柠檬酸水溶液和0.2mol/L磷酸氢二钠水溶液混合配制;果汁,糖果 市售。
CHI-660C电化学分析系统 上海辰华仪器有限公司;KQ-100超声波清洗器 昆山超声波仪器有限公司。
1.2 样品制备
取20.0g糖果样品研碎,加入80mL柠檬酸-磷酸氢二钠缓冲溶液(pH3.0),超声1h,减压抽滤,用pH3.0的柠檬酸-磷酸氢二钠缓冲溶液定容至100mL;果汁加热至微沸赶去二氧化碳,量取20mL用pH3.0的柠檬酸-磷酸氢二钠缓冲溶液定容至100mL,5℃下保存备用。
1.3 聚结晶紫修饰电极的制备
将玻碳电极(Φ=3mm)在湿润的金相砂纸上磨光,然后用中性氧化铝(0.05μm)悬乳液在鹿皮上抛光成镜面,依次用硝酸(1∶1,V/V)、乙醇、二次水超声清洗(3min/次),每次均用蒸馏水冲洗,放入含12mL pH5.0的0.2mol/L的柠檬酸-磷酸氢二钠缓冲溶液,6mL 0.1mol/L的硝酸钾溶液,2mL 2×10-4mol/L结晶紫水溶液的修饰液中,以玻碳电极为工作电极,Ag/AgCl电极为参比电极,铂丝电极为对电极,在-1.2~2.4V电位范围内静止状态下,以80mV/s循环扫描10周后取出,用二次水淋洗,将修饰电极置于20mL的磷酸氢二钠-柠檬酸缓冲溶液(pH3.0)中循环扫描至稳定,即制得聚结晶紫修饰电极。
1.4 实验方法
1.4.1 重现性、稳定性的实验方法 利用上述方法制备的同一支聚结晶紫修饰电极为工作电极,Ag/AgCl电极为参比电极,铂丝电极为对电极,搅拌富集60s后,在0.4~1.2V电位范围内,扫描速率为100mV/s,用循环伏安法对电解池中8.0×10-6mol/L的日落黄重复测定10次,记录循环伏安曲线。对于测定结束后,将修饰电极置于20mL的磷酸氢二钠-柠檬酸缓冲溶液(pH3.0)中循环扫描至无峰,置于空白混合液中10d,同样条件下,对于日落黄进行再次测定,记录循环伏安曲线。
1.4.2 干扰实验的测定方法 利用上述方法制备的聚结晶紫修饰电极为工作电极,Ag/AgCl电极为参比电极,铂丝电极为对电极,搅拌富集60s后,在0.4~1.2V电位范围内,扫描速率为100mV/s,用循环伏安法对电解池中8.0×10-6mol/L的日落黄测定,记录循环伏安曲线。然后分别加入可能存在的干扰物质分别测定,记录循环伏安曲线。
1.4.3 标准曲线、检测限的测定方法 在电解池中加入20mL pH3.0的柠檬酸-磷酸氢二钠缓冲溶液,依次加入所需浓度的日落黄标准溶液,以聚结晶紫烯修饰电极为工作电极,Ag/AgCl电极为参比电极,铂丝电极为对电极,搅拌富集60s后,在0.6~0.9V电位范围内,用差分脉冲伏安法,分别进行扫描测定,记录差分脉冲曲线。根据3N/S计算检测限。
1.4.4 回收率的实验方法 利用测定工作曲线的方法,测定结束后,将修饰电极置于20mL的磷酸氢二钠-柠檬酸缓冲溶液(pH3.0)中循环扫描至无峰,进行加标回收实验。
每个样品取三个不同体积分别置于电解池中,分别按照标准曲线的测定方法进行测定,记录曲线,每个样品测定六次,然后加入已知浓度的标准日落黄溶液,进行测定,记录曲线。由氧化峰电流根据工作曲线线性方程,计算出测定样品中以及加入的标准日落黄溶液后的浓度总值,进而计算出标准日落黄溶液的测定值,再与已知加入浓度进行比较,计算出回收率。
2 结果与讨论
2.1 日落黄在聚结晶紫膜修饰电极上的电化学特性
图2是结晶紫在玻碳电极上聚合过程的循环伏安图。从图上可以看出,结晶紫在玻碳电极上进行了明显的氧化还原反应,在1.8V和-0.3V左右分别出现了氧化还原峰电流,随扫描次数的增加,峰电位不变,峰电流增加,但增加的幅度减小,证明随着聚合反应的进行,电极表面的聚合物膜趋于完整,聚合与沉积速率减缓。图3是聚结晶紫修饰电极的扫描电镜图。由图可见结晶紫通过电化学聚合到了玻碳电极上,成功制备了结晶紫膜修饰电极。
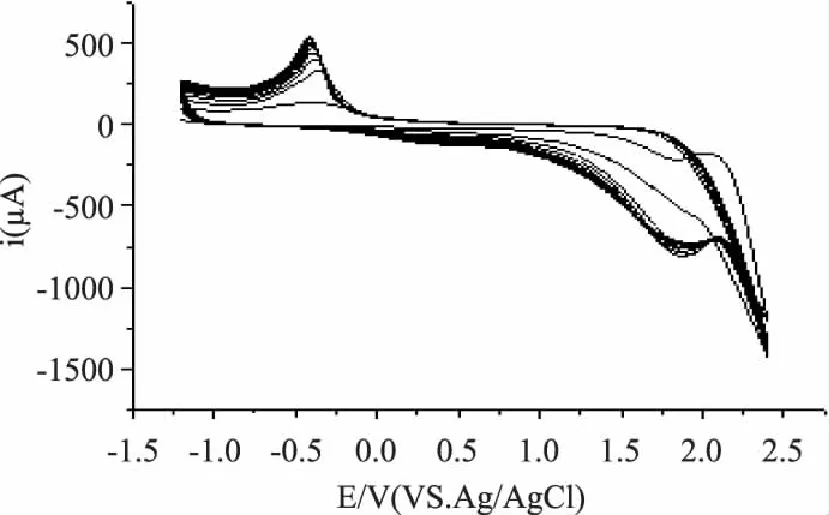
图2 结晶紫在玻碳电极上的聚合循环伏安曲线 Fig.2 Cyclic voltammograms of methyl violet on the glass carbon electrode

图3 结晶紫修饰电极的扫描电镜图 Fig.3 SEM of poly(methyl violet)electrode
2.2 聚合条件的选择
为了使制备的结晶紫修饰电极更好的催化日落黄的电化学氧化还原,实验对其聚合条件进行了讨论。固定低电位为-2.0V,改变高终止电位进行实验,结果表明:高电位等于2.4V时,日落黄的电化学信号最强,所以选用聚合高电位为2.4V。固定高电位为2.4V,改变低电位进行实验。结果表明:低电位在-1.2V时,日落黄的电化学信号最强,故实验选用聚合电位范围为-1.2~2.4V。当扫描速率为80mV/s时,所制备的修饰电极对日落黄的响应峰电流最大。随着扫描周数增加,峰电流增大,当聚合10周后,基本不变,故选择聚合扫描次数为10周。同时聚合底液的pH也会影响到对于日落黄的电化学测定,实验证明pH5.0柠檬酸-磷酸氢二钠缓冲溶液作为聚合底液得到的聚结晶紫修饰电极对日落黄的响应最大。此外结晶紫的用量对聚合过程有较大的影响,实验中改变结晶紫的用量,发现当2mL的2×10-4mol/L的结晶紫时,制备的修饰电极对日落黄的响应最好,所以结晶紫取2mL的2×10-4mol/L的水溶液时最佳。
2.3 日落黄在聚结晶紫修饰电极上的电化学行为
图4为8.0×10-6mol/L日落黄,在柠檬酸-磷酸氢二钠缓冲溶液中(pH3.0),在裸电极(1)与聚结晶紫修饰电极(2)上的循环伏安曲线。由图4可见:在聚结晶紫修饰电极上氧化峰电流明显增大,说明结晶紫能很好地催化日落黄的氧化反应。
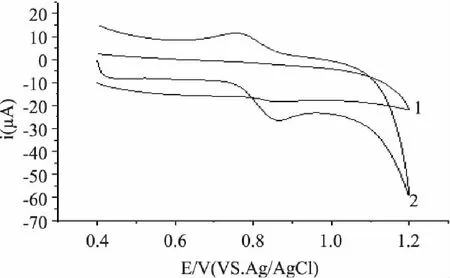
图4 日落黄在裸电极和聚结晶紫修饰电极上的 循环伏安曲线 Fig.4 Cyclic voltammograms of sunset yellow at the bare electrode and the methyl violet modified electrode
2.4 介质的影响
考察了介质对日落黄在聚结晶紫膜修饰电极上电化学响应的影响。首先改变不同类型的介质,如柠檬酸-磷酸氢二钠缓冲溶液(2.2~8.0),如图5,氧化峰电流在pH3.0时达到最大;BR缓冲溶液(2.56~7.54),如图6,氧化峰电流在pH3.29时达到最大;乙酸-乙酸钠缓冲溶液(pH3.6~5.6),如图7氧化峰电流在pH4.4时达到最大。对比发现pH3.0柠檬酸-磷酸二氢钠缓冲溶液对日落黄在聚结晶紫修饰电极上电化学响应最大,如图8,因此选定pH3.0柠檬酸-磷酸氢二钠缓冲溶液作为测定日落黄的介质。改变pH分别进行实验发现随着pH增大,氧化峰电位负移说明有质子参与日落黄的氧化反应,并且氧化峰峰电位与pH(2.2~8.0)呈线性关系,线性方程为:Epa=0.97-0.039pH,R=0.9963(图5插图)。
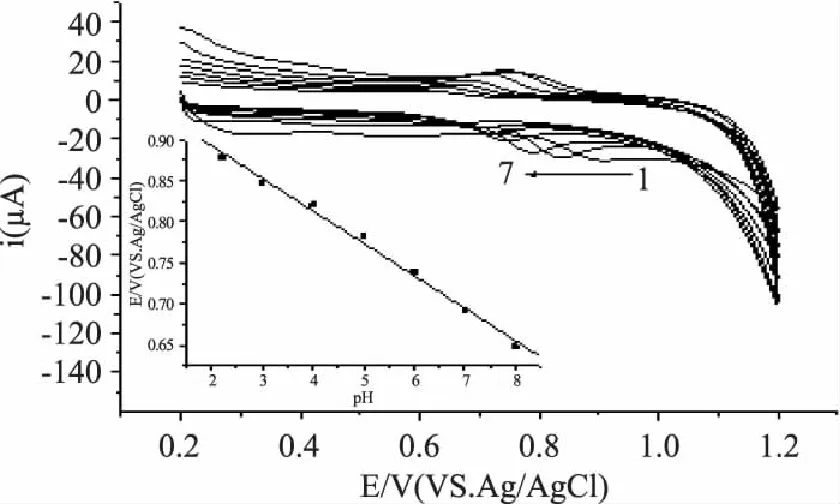
图5 日落黄在不同pH的柠檬酸-磷酸氢二钠缓冲溶液 (pH2.2~8.0)的循环伏安曲线 Fig.5 Cyclic voltammograms of sunset yellow in the citric acid-phosphate buffer(pH2.2~8.0)
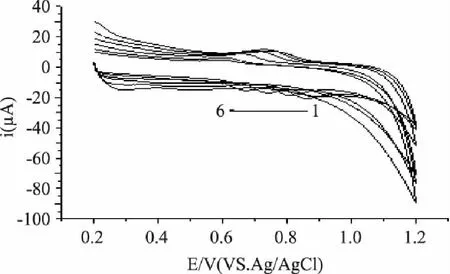
图6 日落黄在不同pH的B-R缓冲溶液 (pH2.56~7.54)的循环伏安曲线 Fig.6 Cyclic voltammograms of sunset yellow in the B-R buffer(pH2.56~7.54)
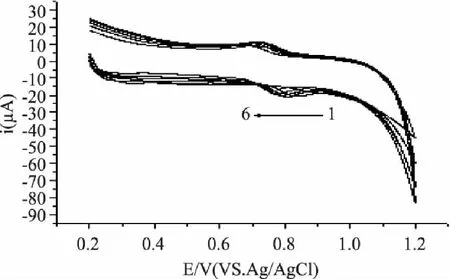
图7 日落黄在不同pH的乙酸-乙酸钠缓冲溶液 (pH3.6~5.6)的循环伏安曲线 Fig.7 Cyclic voltammograms of sunset yellow in the HAc-NaAc buffer(pH3.6~5.6)
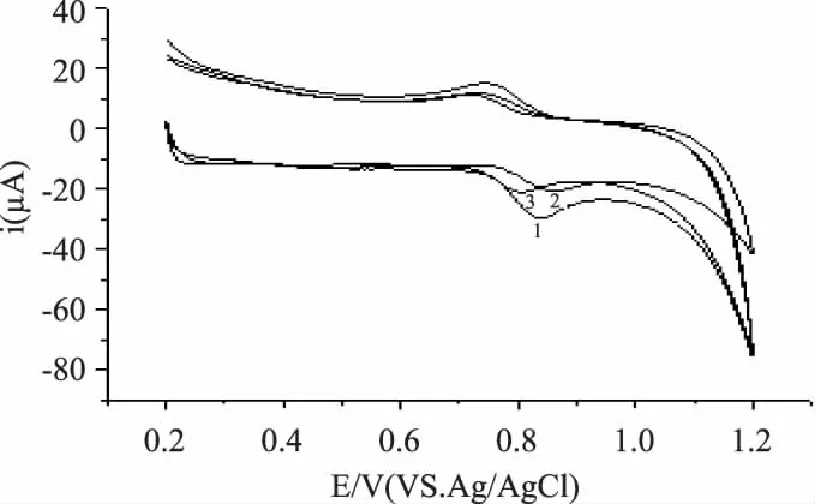
图8 日落黄在不同介质响应最大的循环伏安对比图 Fig.8 Cyclic voltammograms of sunset yellow in the citric acid-phosphate buffer
2.5 扫描速率与搅拌时间的影响
图9为日落黄在不同扫描速率的循环伏安曲线。可以看出,随着扫描速率的增加,还原峰电位略微向负方向移动而氧化峰电位略微向正方向移动;扫描速率在20~340mV/s之间,氧化峰峰电流随着扫描速率的增加线性增大(图9插图),线性方程分别为:ipa(A)=-1.43×10-7+1.26×10-8v(mV/s),R=0.9992,表明日落黄在聚结晶紫修饰电极上的电极过程为吸附过程。随着扫描速率的增大,峰形变差,且检测的灵敏度会降低,因此选择测定日落黄扫描速率为100mV/s。
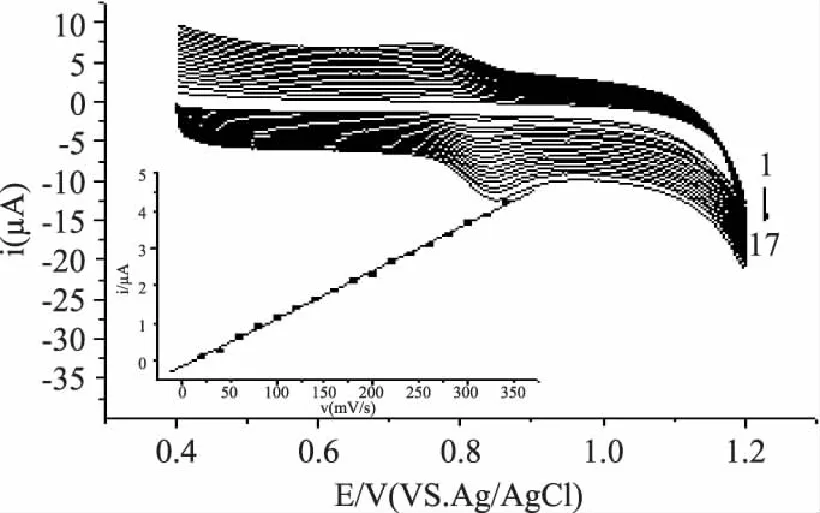
图9 日落黄在不同扫速下的循环伏安曲线 Fig.9 Cyclic voltammograms of sunset yellow at different scanning rates
改变搅拌富集时间,即从30s逐渐增大至80s时,每10s记录扫描循环伏安图,结果发现当富集时间从30s逐渐增加,峰电流逐渐增加,当富集时间继续增加到60s趋于稳定,因此选择搅拌富集时间为60s。
2.6 干扰实验
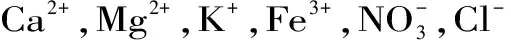
2.7 重现性与稳定性
对聚结晶紫修饰电极测定日落黄的重复性与稳定性进行了实验。利用同一支电极,对8.0×10-6mol/L日落黄重复测定10次,测定值间的相对标准偏差为4.12%,表明修饰电极重现性较好。测定结束后,将修饰电极置于20mL的磷酸氢二钠-柠檬酸缓冲溶液(pH3.0)中循环扫描至无峰,置于空白混合液中10d,对于日落黄进行再次测定,测定值为第一次测定值的97.9%,表明修饰电极稳定性较好。
2.8 标准曲线、检测限与回收率
在pH3.0的柠檬酸-磷酸二氢钠缓冲溶液的介质中,对日落黄标准溶液系列进行测定,结果表明:日落黄在聚结晶紫修饰电极上的氧化峰电流与其浓度在8.0×10-8~2.0×10-5mol/L范围内呈良好线性关系,其回归方程分别为:ipa(A)=0.46c+8.68×10-6,相关系数为0.9951,检出限为2.0×10-8mol/L(3N/S)。
按照“1.4.4”所述的回收率的实验方法,对实际样品进行回收率实验,测定值及回收率见表1。

表1 样品分析结果Table 1 Determination of sunset yellow in food
3 结论
制备了聚结晶紫修饰电极,该修饰电极对日落黄的电化学氧化具有明显的催化作用,在聚结晶紫修饰电极上的氧化峰电流与其浓度在8.0×10-8~2.0×10-5mol/L范围内呈良好线性关系,检出限为2.0×10-8mol/L。可用于实际样品分析,并建立了测定日落黄的新方法。
[1]Alves S P,Brum D M,Branco de Andrade E C,etal. Determination of synthetic dyes in selected foodstuffs by high performance liquid chromatog-raphy with UV-DAD detection[J]. Food Chemistry,2008,107(1):489-496.
[2]Fuh M R,Chia K J. Determination of sulphonated azo dyes in food by ion-pair liquid chromatography with photodiode array and electrospray mass spectrometry detection[J]. Talanta,2002,56(4):663-671.
[3]GB2760-2011.食品安全国家标准食品添加剂使用标准[S].
[4]刘冷,李建晴,郭芬,等.紫外分光光度法同时测定柠檬黄和日落黄[J].光谱实验室,2007,24(3):423-427.
[5]刘慧,胡仰栋,孙小云.连续波长紫外分光光度法对合成食用色素混合体系的同时定量测定[J].食品工业科技,2006,27(9):164-166.
[6]杜建中,李青梅,卢冬梅,等.分光光度法测定食品色素含量的研究[J].食品工业科技,2011,32(1):300-303.
[7]Capitan-vallvey L F,Fernandez M D,de Orbe I,etal. Simultaneous determination of the colorants Sunset yellow FCF and Quinoline yellow by solid-phase spectrophotometry using partial least squares multivariate calibration[J]. Analyst,1997,122:351-354.
[8]Lopez-de-alba P L,Lopez-martinez L,Cerda V,etal. Simultaneous determination of Tartrazine,Sunset yellow and Allura red in commercial soft drinks by multivariate spectral analysis[J]. Quimica Analitica,2001,20:63-72.
[9]孙娅娜,朱蕾,崔芳.高效液相色谱法测定糕点中的柠檬黄、日落黄和亮蓝[J].食品科技,2011,36(12):310-312.
[10]卢丽明,黄诚. HPLC法测定碳酸饮料中日落黄含量的不确定度分析[J].中国热带医学,2008,8(8):1448-1449.
[11]鄢兵,龙州雄,万春花,等.HPLC法同时测定饮料中柠檬黄和日落黄[J].现代测量与实验室管理,2007(4):14-15.
[12]Lopez-de-alba P L,Lopez-martinez L,De-Leon-rodriguez L M. Simultaneous Determination of Synthetic Dyes Tartrazine,Allura Red and Sunset Yellow by Differential Pulse Polarography and Partial Least Squares. A Multivariate Calibration Method[J]. Electroanalysis,2002,14(3):197-205.
[13]Zhang W,Liu T,Zheng X,etal. Surface-enhanced oxidation and detection of Sunset yellow and Tartrazine using multi-walled carbon nanotubes film-modified electrode[J]. Colloids and Surface B,2009,74:28-31.
[14]周谷珍,孙元喜,邓欢梅.聚结晶紫薄膜修饰电极的制备条件研究[J].湖南文理学院学报,2003,15(4):25-28.
[15]周谷珍,孙元喜.聚结晶紫薄膜修饰电极测定尿酸[J].分析测试学报,2004,23(6):18-21.
