应用生物电阻抗测量评估患者的容量状况
2014-03-21陈海燕综述龚德华审校
陈海燕 综述 龚德华 审校
无论是危重还是慢性疾病患者,准确地评估机体容量状态,控制液体负荷都极为重要。液体负荷增多是影响维持性透析患者生存预后的独立危险因素,长期液体负荷增多会加重心血管系统负担,导致左心室扩张,血压升高,甚至进展至充血性心力衰竭,增加患者心血管死亡率和全因死亡率[1]。
肾脏是调节机体容量平衡的最重要器官之一,肾功能正常时,机体通过内在调节保持容量平衡,当肾功能受损、尤其患者需行肾脏替代治疗(RRT)时,容量平衡则主要依靠临床医师治疗干预实现,此类患者的容量评估尤为重要。本文拟对近年来容量评估方法,特别是生物电阻抗法(BIA)在临床的应用作一简述。
容量评估的常用方法
容量评估包括三方面:总体水负荷(组织水化状态),有效循环血容量及心脏反应性。传统的方法包括病史询问,体格检查,监测血压、心率及体重变化,计算患者液体出入量[2],显然准确性及灵敏度都较差。精确用于总体水负荷判断的方法为核素标记稀释法,很显然临床无法常规应用。反映有效血容量的手段包括有创/无创血流动力学监测,多用于危重患者,临床使用亦并不广泛。一些生物学标志物如N末端脑利钠肽前体(NT-pro BNP)主要反映心脏的反应性。相较而言,BIA作为一种简便测量总体水负荷的方法,更具有临床使用前景。通常情况下,机体水负荷过多,会反映在组织细胞水平,出现水肿现象,也会反映在血循环部分,表现有效血容量增多,亦会引起心脏反应,表现为NT-pro BNP升高,即容量评估的三个方面具有较好的相关性。但在一些特殊情况下,特别是危重患者而言,容量评估的三个方面并不一致。如肾病综合征状态血管外水负荷增多而血容量并不增多甚至减少,此种情况只有BIA能反映而血流动力学指标及NT-pro BNP并不升高。类似情况还可见于肝硬化导致水负荷增多。而心脏泵功能衰竭患者则以NT-pro BNP升高为主,BIA及血流动力学监测指标并不一定升高。BIA虽然也只能反映容量状态的某一方面,但多数情况下,尤其是在判断长期容量负荷过多方面,与其他指标有很好相关性,且具有无创、实时、简便、廉价及重复性好的优点,值得在临床推广应用。
BIA技术原理及方法
BIA技术原理BIA通过测量及分析生物组织的电阻特性,包括阻抗特性及容抗特性来评估容量状态及机体组成。由于组织间隙及细胞内含导电性好的电解质溶液,在电路中起电阻作用,而细胞膜、组织界膜则导电性差,在交流电路中起类似电容作用。当通过体外发放某频率的电流通过机体时,可测得总抗值(Z),该指标与总体水(TBW)成反比,即机体含水量越多,组织导电能力越强,总抗值越小。而总抗值可分为阻抗(rR)和容抗(Xc),前者为电流在细胞内液(ICW)和细胞外液(ECW)中的阻力,代表组织水含量,后者代表细胞膜的容抗特性,与细胞膜或组织界膜的含量成正比,间接反映细胞数量,可作为机体成分组成指标。因为低频电流(<10 kHz)无法穿过细胞膜,只能流经细胞外,此时测量值主要反映ECW,而高频电流(>100 kHz)可穿过细胞膜,测量值可反映TBW,而不同频率情况下R及Xc的变化情况则反映ECW、ICW及细胞数。同时因肌肉组织(又称“瘦组织”)富含导电性好的电解质溶液,,而骨骼、脂肪及含气组织则导电性差,不同R及Xc亦可反映肌肉及脂肪的含量。由于电流频率过小或过大都会影响细胞膜的电容特性,一般使用中频(50kHz左右)电流测量以获得最大Xc。由于通过BIA测量得到的是R及Xc,一般通过R值与TBW的相关性以定性反映容量状态,或将不同测定值,与“金标准”测量得到的容量值通过数学模式建立对应公式,以通过测定值计算得到容量值。
BIA方法目前常用于容量评估的生物电阻抗分析方法主要有三种:多频生物电阻抗分析(MFBIA)、生物电阻抗频谱分析(BIS)和生物电阻抗矢量分析(BIVA),三种方法各具特色(表1)。
MFBIAMFBIA采用多种固定频率包括高频(100、200和500 kHz)和低频(0、1和5 kHz)电流测量的方法。低频电流主要用于计算ECW,高频电流计算TBW,而ICW由两者之差获得。临床发现低频测量数据准确性及重复性相对较好,测得的ECW值与“金标准”同位素稀释法吻合度好,而ICW测量准确性则相对较差[3]。
BISBIS亦属多频测量,通过从低频到高频的连续频率谱(5~1 000 kHz)电流测量ECW、ICW和TBW,对ECW的评估准确性不及MFBIA。正常人群通过MFBIA测量获得的TBW相对准确,而容量分布异常(如大量腹水的患者)或体脂含量较大的人群(如重度肥胖的患者),BIS测得的TBW更加准确[3,4]。
BIVABIVA属单频测量,测量频率通常为50 kHz。BIVA并不直接得出ICW、ECW或TBW值,而是将单次测量后得到的身高标化的阻抗、容抗值标点于以身高标化的阻抗、容抗为横、纵坐标的矢量分析图(图1),以其与正常参考范围50%、75%和95%三个容受区间进行对比来定性判断机体容量状态。
生物电阻抗分析还分为整体测量和节段测量,两种方法的电极片置放位置不同,前者应用“整体踝腕测量”的方法,电极片置于身体同侧上下肢末端,评估全身组织的水肿状态,但无法区分组织水肿的具体部位。而节段生物电阻抗分析则根据测量的具体部位调整电极片的位置,对评估局部组织水肿状态更有优势,如小腿电阻抗分析(Calf-BIA)。

表1 三种常用于容量评估的生物电阻抗技术的比较
MFBIA:多频生物电阻抗分析;BIS:生物电阻抗频谱分析;BIVA:生物电阻抗矢量分析;ECW:细胞外液;TBW:总体水;ICW:细胞内液
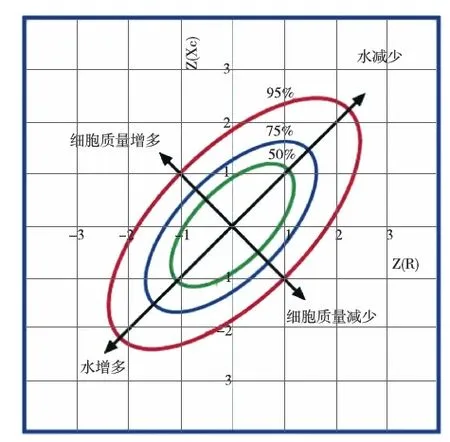
图1 生物电阻抗矢量分析图[5]
BIA容量评估的临床应用
长期透析患者的容量评估透析患者确定干体重至关重要。BIA方法根据测量数据及人群回归公式计算可得到TBW、ECW及ICW,但如何判断患者容量是否超出正常值还需其他参数。BIA判断容量状态包括定量及定性两种方法。定量是直接计算出患者干体重或计算出体内多余含水量,包括Chamney公式[5]及利用“金标准”方法得到的回归公式直接计算体内多余含水量[6];定性只判断容量状态正常与否,可采用ECW/TBW比值法及BIVA[7,8]。小腿部电阻抗比值法(高频电流200 kHz及低频电流5 kHz下阻抗的比值)也是近年来被认为是评估透析患者容量状态的有效指标[9]。选择小腿部主要因为该部位受重力影响大,更能代表全身组织含水状态,且类似于圆柱状,更符合电阻抗测量模型[9]。
BIA应用于透析患者容量评估的作用包括:(1)通过动态监测反映容量状态的变化,尤其用于研究性观察指标。有研究显示BIA测量的ECW变化与同位素测量的ECW变化相关性很好[6,10]。而关于艾考糊精的研究中发现,BIA测量ECW显著下降而BNP指标则无明显变化,显示出BIA反映容量变化的敏感性[11]。(2)BIA测量容量状态是判断患者预后的指标。很多队列研究显示,BIA测量的机体含水状态与腹膜透析(PD)患者预后密切相关,即使在校正了一些混杂因素如并发症,炎症状态及低白蛋白血症后亦是如此[12]。(3)作为确定透析患者“干体重”的工具。采用BIA评估透析患者患者容量及确定干体重,最终改善患者预后。Wabel等[13]研究证实,传统认为已达干体重的患者行BIA容量评估,血压升高的患者者中25%存在水过多,而在血压正常甚至低血压患者中,亦有相当比例患者存在水过多,由此说明临床评估的不准确性。目前认为,BIA指导的透析患者容量控制,与传统方法比较可改善血压控制情况,降低左室质量指数,改善患者长期存活率。最近的两项单中心随机对照研究比较BIA及传统临床方法评估干体重对患者预后的影响。Hur等纳入156例血液透析(HD)患者,随访观察1年,与传统组相比,BIA干预组容量超负荷状态控制更好,临床获益包括血压下降,使用降压药比例降低,更重要的是左室质量指数明显下降,除此之外,患者血浆白蛋白水平及血红蛋白水平轻度升高[14]。另一项研究纳入131例HD患者,随访观察2.5年,BIA干预组脉搏波传播速度明显降低,而传统组则上升,最重要的是两组患者生存率亦存在显著差异(传统组78%vsBIA组96%)[15]。这是一项首次以生存获益为研究终点的研究,结果证实两个问题:(1)证实透析患者容量控制的意义,即容量控制更好生存率更高;(2)与传统方法比较,BIA指导容量控制更准确。
与HD患者相比,PD患者似乎更需BIA来评估容量状态。PD患者易出现肌肉群减少及血浆低白蛋白血症。这样导致TBW分布上向ECW倾斜,即ECW/ICW比值增加,而ECW分布上则向血管外倾斜,即血管外容量增加更明显。此种特点导致水负荷状态的增多可能并不能从传统指标反映出来,如血压与容量的关系,只有在年轻及无明显并发症的患者中较明显,而在年老及有合并症患者中则不明显。同样,一些研究也显示,即使存在水负荷过多状态,血清BNP也不一定升高。因此PD患者更需BIA来替代传统方法以评估容量。很多队列研究显示BIA测量的机体含水状态与PD患者预后密切相关[12]。采用BIA评估容量需注意是否会导致容量控制过严后损害残余肾功能,这一点对PD患者尤为重要。而最近一项研究显示,采用BIA评估的ECW增加并不能保护残余肾功能[16]。
危重症患者的容量评估透析患者的一般状态相对稳定,BIA容量评估反映的是长期稳定状态的容量负荷。长期稳定状态的容量负荷与血流动力学状态之间有较好相关性。而危重症患者则需评估即时容量状态及变化,更重要的是血流动力学状态。在这种情况下,BIA评估的容量状态更多反映机体含水量多少,而与血流动力学状态之间的关联性则较差。因此,BIA定量判断容量多少的方法可能并不合适,而定性判断组织是否存在水肿则可能更准确。如BIVA是基于矢量分析的单频测量方法,通过正常对照或自身对照评估容量,不涉及众多其他参数,测量结果相对准确。Ronco等[17]建议心功能衰竭及心肾综合征的患者临床容量管理应遵循“5B”原则,即液体平衡(由体重变化衡量)(balance of fluids)、血压(blood pressure)、生物标志物(biomarkers)、BIVA及血容量(blood volume),其中BIVA作为重要的容量评估方法之一被列入其中。
目前应用BIA较多的是充血性心力衰竭患者的容量评估,以辅助液体治疗及容量管理。有研究通过阻抗心电图(一种胸部节段BIA)测量胸腔水含量(TFC),发现心衰患者的TFC显著高于其他ICU患者[18]。Khoury等[19]通过动物实验证实BIA测得的阻抗信号变化与心脏血流动力学参数密切相关,包括左心房压力、左室舒张末容积和心脏射血分数等,因而推断BIA有利于早期诊断充血性心力衰竭的失代偿期。然而尚缺乏脓毒症、多脏器衰竭、全身炎症反应综合征患者的BIA应用数据,仅少数研究探讨ICU患者术后容量管理,发现应用BIA测量患者TBW,可准确动态监测术后液体潴留情况,有利于患者术后容量控制,加快术后恢复[20]。
BIA与N末端脑利钠肽前体(NT-proBNP)
由于BIA主要反映组织水化状态,适合评估静态液体负荷量,而对于血管内容量评估敏感性较差。NT-proBNP主要反映心功能对当前容量状态的反应性,它与血管内容量状态及心脏功能状态密切相关。如前所述,BIA反映的机体水化状态与NT-proBNP反映的心脏反映性并不完全吻合,从而证据两者具有不同的价值。对于NT-proBNP的局限性人们已有认识。如对于冠心病或心肌梗死的患者,由于心功能较差,即使血管内容量无明显增加,血清NT-proBNP水平仍然居高不下。因此,有学者认为血清NT-proBNP水平升高从机制上需分为“干性”和“湿性”两种,“干性”指非容量原因导致的NT-proBNP水平升高,如冠心病、心肌梗死等存在心功能障碍的疾病,“湿性”指容量负荷增加导致NT-proBNP水平升高,如充血性心力衰竭[21]。这两种状态治疗上应有所区分,“湿性”NT-proBNP升高反映容量过多,可通过加强利尿或超滤来缓解,而“干性”NT-proBNP升高则反映容量并不多,进一步利尿或超滤可能加重机体脱水状态导致不利影响。同样,BIA反映的机体水化状态从机理上亦可分为两种状态,一种是伴血容量增多的组织水肿,一种是不伴血容量增多的组织水肿。这两种情况在进行治疗干预时也应有所区别。因此,只有将BIA及NT-proBNP结合使用,才能进一步更精确区分患者容量状态,以指导临床治疗及判断预后。目前还缺乏关于这类研究的数据,仅有一些关于慢性容量状态评估,如PD患者及慢性心功能不全患者中联合应用的报道,对于危重症患者,特别是接受肾脏替代治疗危重症患者的研究尚无报道。
BIA测量的局限性
BIA用于容量评估也有其局限性。电极片放置的位置及被测患者的体位均是影响测量结果的重要因素。皮肤出汗、结痂或者毛发增多也会导致电极片与皮肤贴合不良,部分患者在测量时配合欠佳,难以达到测量要求的标准体位(即平卧位且四肢外展远离躯干)等因素也影响测量结果。过度肥胖/消瘦、烧伤、义肢及装有心脏起搏器的患者中应用也受到一定限制。
小结:容量评估目前仍是临床需解决的重要问题之一。作为一种简便、无创、低成本且重复性好的手段,生物电阻抗分析应用于临床容量评估的准确性及价值得到越来越多的认识,其使用亦日益广泛。
1Paniagua R,Ventura MD,Avila-Díaz M,et al.NT-proBNP,fluid volume overload and dialysis modality are independent predictors of mortality in ESRD patients.Nephrol Dial Transplant,2010,25(2):551-557.
2Cocchi R,Degli Esposti E,Fabbri A,et al.Prevalence of hypertension in patients on peritoneal dialysis:results of an Italian multicentre study.Nephrol Dial Transplant,1999,14(6):1536-1540.
3Mager JR,Sibley SD,Beckman TR,et al.Multifrequency bioelectrical impedance analysis and bioimpedance spectroscopy for monitoring fluid and body cell mass changes after gastric bypass surgery.Clin Nutr,2008,27(6):832-441.
4Jaffrin MY,Morel H.Body fluid volumes measurements by impedance:A review of bioimpedance spectroscopy (BIS) and bioimpedance analysis (BIA) methods.Med Eng Phys,2008,30(10):1257-1269.
5Fisch BJ,Spiegel DM.Assessment of excess fluid distribution in chronic hemodialysis patients using bioimpedance spectroscopy.Kidney Int,1996,49(4):1105-1109.
6Chamney PW,Wabel P,Moissl UM,et al.A whole-body model to distinguish excess fluid from the hydration of major body tissues.Am J Clin Nutr,2007,85(1):80-89.
7Van Biesen W,Williams JD,Covic AC,et al.Fluid status in peritoneal dialysis patients:the European Body Composition Monitoring (EuroBCM) study cohort.PLoS One,2011,6(2):e17148.
8Cheng LT,Tian JP,Tang LJ,et al.Why is there significant overlap in volume status between hypertensive and normotensive patients on dialysis? Am J Nephrol,2008,28(3):508-516.
9Zhou YL,Liu J,Sun F,et al.Calf bioimpedance ratio improves dry weight assessment and blood pressure control in hemodialysis patients.Am J Nephrol,2010,32(2):109-116.
10 Raimann JG,Zhu F,Wang J,et al.Comparison of fluid volume estimates in chronic hemodialysis patients by bioimpedance,direct isotopic,and dilution methods.Kidney Int,2014,85(4):898-908.
11 Paniagua R,Orihuela O,Ventura MD,et al.Echocardiographic,electrocardiographic and blood pressure changes induced by icodextrin solution in diabetic patients on peritoneal dialysis.Kidney Int,2008,Suppl (108):S125-S130.
12 Davies SJ,Davenport A.The role of bioimpedance and biomarkers in helping to aid clinical decision-making of volume assessments in dialysis patients.Kidney Int,2014,Jun 11.
13 Wabel P,Moissl U,Chamney P,et al.Towards improved cardiovascular management:the necessity of combining blood pressure and fluid overload.Nephrol Dial Transplant,2008,23(9):2965-2971.
14 Hur E,Usta M,Toz H,et al.Effect of fluid management guided by bioimpedance spectroscopy on cardiovascular parameters in hemodialysis patients:a randomized controlled trial.Am J Kidney Dis,2013,61(6):957-965.
15 Onofriescu M,Hogas S,Voroneanu L,et al.Bioimpedance-guided fluid management in maintenance hemodialysis:a pilot randomized controlled trial.Am J Kidney Dis,2014,64(1):111-118.
16 McCafferty K,Fan S,Davenport A.Extracellular volume expansion,measured by multifrequency bioimpedance,does not help preserve residual renal function in peritoneal dialysis patients.Kidney Int,2014,85(1):151-157.
17 Ronco C,Kaushik M,Valle R,et al.Diagnosis and management of fluid overload in heart failure and cardio-renal syndrome:the "5B" approach.Semin Nephrol,2012,32(1):129-141.
18 Tuy T,Peacock WF 4th.Fluid overload assessment and management in heart failure patients.Semin Nephrol,2012,32(1):112-120.
19 Khoury DS,Naware M,Siou J,et al.Ambulatory monitoring of congestive heart failure by multiple bioelectric impedance vectors.J Am Coll Cardiol,2009,53(12):1075-1081..
20 Cagini L,Capozzi R,Tassi V,et al.Fluid and electrolyte balance after major thoracic surgery by bioimpedance and endocrine evaluation.Eur J Cardiothorac Surg,2011,40(2):e71-e76.
21 Valle R,Aspromonte N.Use of brain natriuretic Peptide and bioimpedance to guide therapy in heart failure patients.Contrib Nephrol,2010,164:209-216.
