5-(N-乙基-N-2-羟乙基胺)-2-戊胺的合成
2014-03-21刘小成邓嘉伦
余 丹,李 翔,刘小成,邓嘉伦,刘 昱,陈 刚
(华烁科技股份有限公司,湖北武汉430074)
外消旋羟基氯喹化学名称为7-氯-4-[5-(N-乙基-N-2-羟乙基)-2-戊基]氨基喹啉,结构式见图1。外消旋羟基氯喹硫酸盐由法国赛诺菲(Sanofi Winthrop Industries)公司以商品名Plaquenil RTM出售[1]。
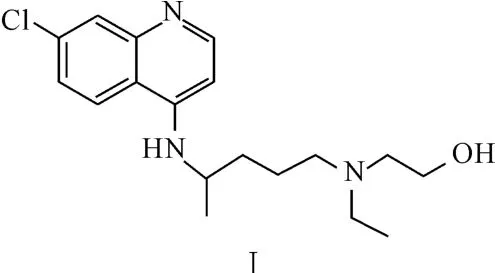
图1 羟基氯喹的结构式Fig.1 Structural formula of hydroxychloroquine
羟基氯喹是由4,7-二氯喹啉和5-(N-乙基-N-2-羟乙基胺)-2-戊胺(Ⅱ)经费歇尔合成反应制得[2-5],反应式见图2。

图2 羟基氯喹的合成反应Fig.2 Synthetic reaction of hydroxychloroquine
目前,临床上羟基氯喹是用来治疗结缔组织病红斑狼疮(盘状、亚急性皮肤型、系统性)的一线基础用药,也是治疗类风湿性关节炎的联合首选用药。随着羟基氯喹在国内临床使用的推广,中间体5-(N-乙基-N-2-羟乙基胺)-2-戊胺的需求量也越来越大。
5-(N-乙基-N-2-羟乙基胺)-2-戊胺(Ⅱ),俗称羟基氯喹侧链,是合成羟基氯喹的关键中间体。文献报道的羟基氯喹侧链的合成方法有两种:路线一是以5-氯-2-戊酮为原料与乙基乙醇胺直接反应,之后再氨化还原制得[1,6-8]。由于5-氯-2-戊酮不稳定,与乙基乙醇胺反应收率很低,中间产物也不稳定,致使目标产物的总收率和纯度不高;路线二是先将5-氯-2-戊酮转化成缩酮保护起来,与乙基乙醇胺反应,之后再脱保护,氨化氢化还原。该方法大大提高了中间体的稳定性,使得羟基氯喹侧链具备工业化生产可行性。但是缩酮与乙基乙醇胺反应收率很低,缩酮在反应条件下极易脱保护,形成三元环产物。
为此,作者经过对比研究,确定了一条以5-氯-2-戊酮为原料的经济可行的羟基氯喹侧链合成路线,见图3。
1 实验
1.1 2-(3′-chloropropyl)-2-methyl-1,3-dioxalane(Ⅲ)的合成
氮气保护下,在2 000mL四口烧瓶中加入5-氯-2-戊酮100g(0.83mol)、乙二醇62g(0.995mol)和环己烷800mL,搅拌均匀后加入无水氯化亚锡3g,装上油水分离器和冷凝管,反应液升温,回流,分水,反应至不再分出水,视为反应结束(约5h)。将反应液冷却至室温以下,加入200mL水,搅拌,静置,分出下层水相。水相加入环己烷(2×100mL)萃取,有机相合并,于旋转蒸发仪上80℃以下减压回收溶剂环己烷,得到浅黄色油状液体140g。减压蒸馏后,得到淡黄色透明液体即化合物Ⅲ115g,收率(以5-氯-2-戊酮计)84%,纯度98%(GC)。
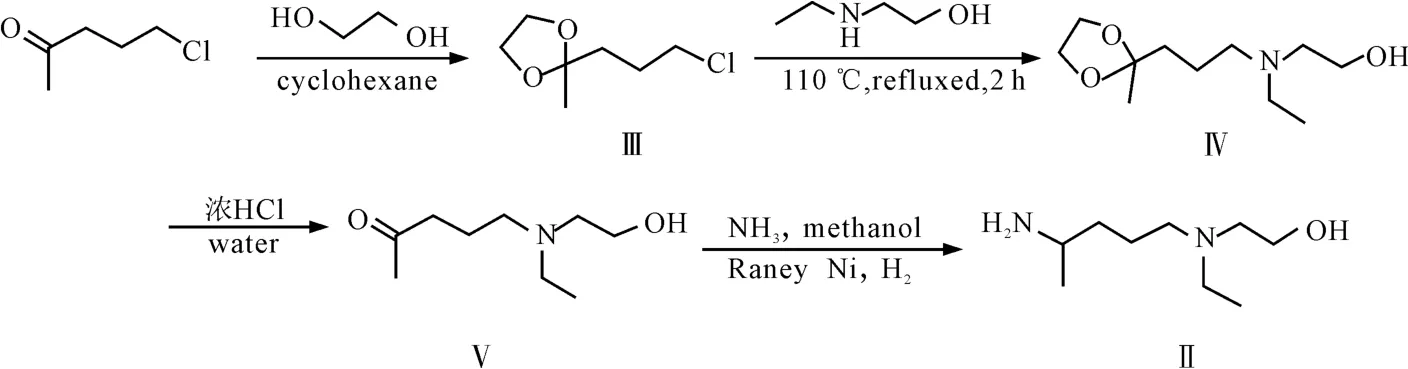
图3 5-(N-乙基-N-2-羟乙基胺)-2-戊胺的合成路线Fig.3 The synthetic route of 5-(N-ethyl-N-2-hydroxyethylamino)-2-pentylamine
1.2 2-(3′-N-ethyl-N-2-hydroxyethylaminopropyl)-2-methyl-1,3-dioxalane(Ⅳ)的制备
氮气保护下,在1 000mL三口烧瓶中加入化合物Ⅲ50g、乙基乙醇胺300g和水1g,搅拌升温至110℃回流2h,取样检测化合物Ⅲ转化率大于97%时,结束反应。将反应液于80℃以下减压蒸馏回收乙基乙醇胺[纯度98%(GC),含水量0.05%(卡尔费休法),回收率95%,可以直接用于反应],得到化合物Ⅳ粗品70 g(理论产量66g),直接进行下一步脱保护。
1.3 1-(N-ethyl-N-2-hydroxyethylamino)-4-pentanone(Ⅴ)的合成
氮气保护下,将化合物Ⅳ粗品70g加入到140 mL水中,再加10mL浓盐酸,搅拌,于50℃反应3h。反应完毕,将反应液在冰水浴下降温,边搅拌边加入40%的氢氧化钠溶液至pH值为13~14。加入二氯甲烷萃取(3×300mL),合并有机相,加入无水硫酸钠干燥,过滤。滤液于旋转蒸发仪上脱除溶剂,得到浅黄色油状液体。减压精馏后,得到无色透明液体即化合物Ⅴ34g(理论产量41.9g),收率81.1%,纯度97%(GC)。
1.4 5-(N-乙基-N-2-羟乙基胺)-2-戊胺(Ⅱ)的合成
取50g化合物Ⅴ置于1 000mL氢化瓶中,加入400mL氨甲醇(含NH3约15%)和10g Raney Ni,于50℃、15kg氢气压力下反应12h。反应结束后,用氮气置换体系中的氢气和氨气,反应液过滤,滤液经蒸馏回收甲醇。得到的残余液精馏,收集(101~104)℃/133Pa馏分,得无色透明液体即5-(N-乙基-N-2-羟乙基胺)-2-戊胺39.7g,收率79%,总收率53.8%,纯度99.0%(GC)。
2 结果与讨论
2.1 目标化合物表征
1HNMR(300MHz,CDCl3),δ:1.0~1.2(m,3H),1.2~1.3(m,2H),1.3~1.5(m,2H),1.9~2.0(m,3H),2.5~2.9(m,5H),3.0~3.2(m,2H),3.5~3.6(m,2H)。MS(Cl,Ammonia):175([M-H]+)。
2.2 讨论
(1)作者尝试采用路线一方法制备羟基氯喹侧链,结果发现,5-氯-2-戊酮和乙基乙醇胺反应,只有在乙基乙醇胺大幅过量的情况下才能有效转化为目标产物,特别是乙基乙醇胺过量5倍以上时,90%以上的5-氯-2-戊酮能转化为目标产物。但是在后处理过程中,产物极易变质,难以纯化,致使收率很低(<30%)。而且过量的乙基乙醇胺也难以回收,导致成本很高,不适合工业化生产。
(2)本研究采用乙基乙醇胺为溶剂。目前乙基乙醇胺市价500元·kg-1,尽管比较昂贵,但产品收率(以化合物Ⅲ计)高达90%,生成目标产物的转化率为99%,且未参加反应的乙基乙醇胺回收率达到95%。
(3)实验发现,化合物Ⅴ在室温下长期放置不稳定,颜色变黄,且纯度下降(室温敞口放置1d后纯度下降超过2%)。若充氮气低温(0℃)保存,可以保持其原有的纯度和颜色约3周。因此,化合物Ⅴ最好立即投入下一步反应。
3 结论
以5-氯-2-戊酮为原料,先进行羰基保护、与乙基乙醇胺反应之后脱保护,再进行羰基还原氨化,经4步反应合成羟基氯喹侧链5-(N-乙基-N-2-羟乙基胺)-2-戊胺,总收率53.8%,纯度99.0%(GC)。重要原料乙基乙醇胺回收率达95%。
[1] SURREY A R.7-Chloro-4-{5-[ethyl(2-hydroxyethyl)amino]-1-methylbutylamino}quinoline,its acid salts,and its preparation:US,2546658[P].1951-03-27.
[2] 卢家俐,赵铖.羟基氯喹在风湿性疾病中的应用进展[J].内科,2008,3(1):69-71.
[3] KUMAR A,VYAS K D,SINGH D,et al.An improved process for the preparation of 7-chloro-4-{5-[N-ethyl-N-(2-hydroxyethyl)amino]-2-pentyl}aminoquinoline and its intermediates via monoamination in the absence of phenol:WO,2005062723[P].2005-07-14.
[4] BLANEY P M,BYARD S J,CARR G,et al.A practical synthesis of the enantiomers of hydroxychloroquine[J].Tetrahedron:A-symmetry,1994,5(9):1815-1822.
[5] SURREY A R,HAMMER H F.Preparation of 7-chloro-4-[4-(N- ethyl-N-2-hydroxyethylamino)-1-methylbutylamino]quinoline and related compounds[J].Journal of the American Chemical Society,1950,72:1814-15.
[6] MOORE A M,ELSLAGER E F,SHORT F W.Benzacridine compounds:US,2915523A[P].1959-12-01.
[7] IULIAN M,BADEA V,COSTESCU R S,et al.N-Ethyl-N-hydroxyethyl-1,4-pentanediamine:RO,62684A[P].1978-02-15.
[8] STERLING DRUG INC.Process for the production of tertiary-amino alkylated primary amines:GB,1157637A[P].1969-07-09.
