纳米技术合成硅酸三钙及表征
2014-03-21豆贝贝刘志刚杨立荣姚少威白瑞英封孝信
豆贝贝,刘志刚,杨立荣,姚少威,白瑞英,封孝信
(河北联合大学材料科学与工程学院,河北唐山063009)
硅酸三钙(3CaO·SiO2,C3S)具有自固化性能,最早作为硅酸盐水泥熟料的主要矿物组成而常被用作建筑胶凝材料。C3S是一种难以制备的水泥熟料矿物,其传统制备方法是将SiO2与CaCO3(或CaO)粉磨,混合均匀并加压成型,然后在高于1 450℃的高温下多次煅烧[1,2]。要获得纯相C3S,需多次粉磨和煅烧。若要得到纳米C3S,还需用高能球磨机将块状煅烧产物长时间粉磨,耗时耗能。也有研究[3]利用溶胶-凝胶法制备C3S,不仅需要较长时间制备凝胶,还需高温煅烧,工艺较复杂。本文提出用燃烧法纳米合成技术制备纳米C3S。用燃烧法制备材料最早可追溯到十九世纪,迄今为止,燃烧法已在制备纳米氧化物及纳米复合氧化物等方面有着广泛地应用[4,5],成为了制备纳米材料的主要技术之一。该方法是将可溶性金属盐充当氧化剂,有机燃料充当还原剂,反应物体系在一定温度下点燃引发剧烈的氧化—还原反应,溢出大量气体,数分钟内即结束燃烧过程,获得质地疏松、不结块、易粉碎的超细粉体[6,7]。相比于传统的固相反应法,燃烧法具有工艺简单,产品纯度高、粒度小、活性高,节约时间和能源等优势,是一种制备纳米水泥矿物的有效方法[8]。本文以燃烧法合成纳米C3S,优化了合成工艺参数,并对产物的微观形貌、粒度分布和水化热等性能进行了表征。
1 实验
1.1 原料与试剂
本试验用硅溶胶、硝酸钙[Ca(NO3)3·4H2O]、尿素[CO(NH2)2]、无水乙醇[C2H5OH];乙二醇[C2H6O2]均为市售分析纯化学药品和试剂。硅溶胶粒度分布如图1所示。硅溶胶颗粒粒径主要集中在21.91~265.6 nm之间,在21.91~70.89 nm之间的颗粒体积百分数为40.9%,在70.89~265.6 nm之间的颗粒体积百分数为50.1%,颗粒的平均粒径为108.1 nm。

图1 硅溶胶的粒度分布
1.2 样品制备
固定Ca/Si摩尔比为3﹕1,称取相应质量的硝酸钙、硅溶胶和尿素,置于烧杯中,加入一定量的蒸馏水,搅拌溶解并于40 KHz超声振荡30 min,制得均匀的悬浮液。倒入坩埚,移至提前升至设定温度的马弗炉中,待燃烧结束,取出坩埚,空气中冷却至室温后,将样品在玛瑙研钵中磨细、密封保存。
1.3 样品测试
用乙二醇法[9]测定产物中f-CaO的含量。用D/MAX2500PC型X射线衍射仪(X-ray diffractometer,XRD)表征产物的物相种类,测试条件:采用Cu靶,电压为40 KV,电流为100 mA,扫描速度为10(°)/min。用S-4800型场发射扫描电镜(Field emission scanning electron microscope,FSEM)观察样品颗粒形貌、大小。用Zetasizer Nano ZS 90型Zeta电位及纳米粒度分析仪(Zeta potential/submicron size analyzer)测试样品的粒度分布。用C80型微量热仪(Digital display calorimeter)测试样品的水化热。
2 结果与分析
2.1 化学计量比Φ对产物中f-CaO含量的影响

图2 不同化学计量比Φ下合成样品中f-CaO的含量
配制不同化学计量比(参加反应的氧化剂原子价总和/还原剂原子价总和之比[7])的10组试样(见表1),在700℃下引燃,观察燃烧后冷却至室温的产物发现:Φ>0.38时,产物为坚硬团聚体,这是由于燃料过少,反应放出的气体量较少,不能有效抑制产物团聚所致;Φ≤0.38时,产物疏松多孔,稍加研磨后即成为细粉。用乙二醇法测试Φ≤0.38时所得样品中f-CaO的含量,结果如图2所示。
由图2可看出:随化学计量比Φ的增大,产物中f-CaO的含量逐渐降低,到Φ=0.24时,f-CaO含量达到最低值2.0%,继续增大化学计量比Φ,产物中f-CaO的含量逐渐升高,Φ达到0.33后,升高趋势变缓。由此可知,燃料较少或较多,都会引起合成产物中f-CaO含量的升高。燃料过少时,发热量不足,燃烧温度不高,不利于SiO2吸收CaO形成C3S;燃料过多时,反应放出大量气体,带走较多热量,导致燃烧温度降低[10],也不利于生成C3S。因此,确定Φ=0.24为该体系的最佳化学计量比。

表1 原料配比
2.2 引燃温度T对产物中f-CaO含量的影响
按化学计量比Φ=0.24配料,分别于500℃、600℃、700℃、800℃下引燃。用乙二醇法测得4个引燃温度下合成产物中f-CaO的含量,结果如图3所示。由图3可以看出:随引燃温度T的升高,产物中f-CaO含量逐渐降低,T=700℃时,f-CaO含量达到最低值2.0%,继续升高引燃温度,f-CaO含量逐渐升高。引燃温度低时,燃烧放热使反应体系达到的最高温度较低[10],不利于SiO2吸收CaO形成C3S;引燃温度过高时,可能是燃烧反应速度过快,不能为SiO2吸收CaO提供充分的反应时间,也不利于形成C3S。因此,引燃温度过低和过高都会使产物中f-CaO含量增加,T=700℃为该燃烧反应体系的最佳引燃温度。
2.3 纳米C3 S的表征
1)产物相组成分析
固定化学计量比Φ=0.24,引燃温度T=700℃条件下合成样品的XRD谱如图4所示。样品XRD谱中出现了较强的三斜型C3S衍射峰,同时出现β-C2S及CaO的杂质峰,说明用低温燃烧法可以合成难以合成的C3S晶相。但由于燃烧法温度低、速度快,反应难以充分进行,样品中仍有少量CaO未被C2S吸收形成C3S。
2)显微结构分析
图5为在 Φ=0.24,T=700℃条件下合成的 C3S的FSEM照片。由图5可看出:C3S矿物既有结晶良好的多面体颗粒,也有结晶较差的凝胶状颗粒,说明燃烧反应进行较快,晶粒来不及发育完全,难以生成形貌一致的产物。
3)颗粒组成分析
采用无水乙醇为分散剂,配制浓度为0.1 g/L的C3S样品,40 kHz下超声分散20 min,用Zeta电位及纳米粒度分析仪测其粒度分布,结果如图6所示。由图6可知:100%的C3S颗粒粒径在127.5~356.2 nm之间,颗粒的平均粒度为225.9 nm。
4)水化热分析
在化学计量比Φ=0.24,引燃温度T=700℃工艺条件下合成的纳米C3S早期水化放热速率曲线如图7所示。由图7可看出:纳米C3S在短时间内迅速水化放出热量,放热峰值出现的时间在69.2 s,所对应最大放热速率达到2.4368 mw/g,且实验只测出了一个水化放热峰。通过计算水化放热速率曲线积分面积,得出用燃烧法合成的纳米C3S在1 min内的累积水化热为611 mw·s/g。根据已有研究[11],在相同水灰比下,各种类型传统水泥及特殊水泥的第一峰值一般在10 min左右出现,峰值最大为1.2306 mw/g,且大部分水泥在30 min钟内的累积水化热才达到甚至低于800 mw·s/g。由此可以认为:燃烧法合成的纳米C3S因颗粒细小、比表面积大、活性高而表现出更为优良的水化特性。
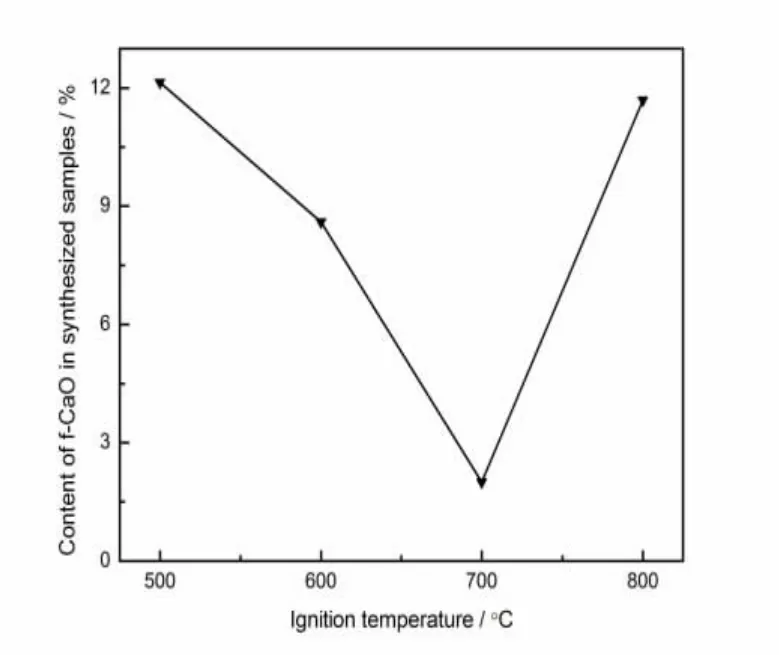
图3 不同引燃温度下合成样品中f-CaO的含量

图4 合成样品的XRD谱,(Φ=0.24,T=700℃)

图5 合成C3 S的FSEM照片,(Φ=0.24,T=700℃)

图6 合成C3 S的粒度分布

图7 纳米C3 S的早期水化放热速率曲线(水灰比,w/c=1)
3 结论
以尿素为燃料,硅溶胶、硝酸钙为原料,采用燃烧法合成纳米C3S,化学计量比为0.24,引燃温度为700℃时,产物中游离氧化钙含量达到最低值2.0%。合成的纳米C3S为不同结晶程度且呈现多种形貌的颗粒,平均粒径为225.9 nm。纳米C3S颗粒水化放热峰出现的时间仅为69.2 s,峰值达到2.4368 mw/g,比传统水泥表现出更高的水化活性。
[1] Stephan D,Maleki H,Knofel D,et al.Influence of Cr,Niand Zn on the properties of pure clinker phases partⅠC3S[J].Cemnet and Concrete Research,1999,29(4):545-552.
[2] LU Zhognyuan,XU Xun,XIAO Xiangqi.Effect of grain size CaCO3and SiO2on the formation of C3Sunder different conditions[J].Journal ofWuhan University of Technology-Mater.Sci.Ed.2007,22(3):533-536.
[3] 王捷,何真,张博,等.纳米技术合成水泥矿物工艺参数研究[J].新型建筑材料,2010,37(5):1-5.
[4] Patil K C.Aruna ST.Tanu Mimani.Combustion synthesis[J].Current Opinion in Solid State&Materials Science.1997.2:158-165.
[5] 黎大兵,胡建东,连建设,等.纳米粉体(CeO2)0.9-x(GdO1.5)x(Sm2O3)0.1的溶胶—凝胶低温燃烧合成[J].硅酸盐学报,2001,29(4):340-343.
[6] 卢利平,张希艳,柏朝辉,等.低温燃烧合成法研究进展[J].长春理工大学学报(自然科学版),2008,31(3):82-84.
[7] 张中太,张俊英.无机光致发光材料及应用[M].北京:化学工业出版社,2005.
[8] 纳米动力学公司.水泥以及制备水泥的方法[P].USPatent,101730668 A.2010-06-09.
[9] 毕文彦,管学茂,邢峰,等.水泥矿物游离氧化钙含量测定方法的评价及探讨[J].混凝土,2008,(12):21-23.
[10] Samir K G,Suijit K R.Synthesis of nano-sized hydroxyapatite powders through solution combustion route under different conditions[J].Materials Science and Engineering B.2011,176(1):14-21.
[11] 康宇.硅酸盐类水泥早期水化特性及其关系的探索[D].南宁:广西大学,2006.
