机械力化学作用下纳米淀粉的制备与性能
2014-03-13卢麒麟唐丽荣陈燕丹陈学榕
卢麒麟 黄 彪 唐丽荣 李 涛 陈燕丹 陈学榕
(福建农林大学材料工程学院1,福州 350002)
(福建农林大学金山学院2,福州 350002)
纳米淀粉(starch nanoparticles)是由天然淀粉中分离出的结晶度较高、粒径较小的淀粉纳米晶粒[1],具有天然淀粉的性质,且具备纳米粒子的特性,如较大的比表面积,较高的杨氏模量,良好的分散稳定性。纳米淀粉良好的分散性、吸附性、溶解性使其在聚合物材料、药物载体及其他领域具有广阔的应用前景,可用于化妆品扑粉、照相纸粉末、造纸施胶、糖果糖衣和药片赋形剂等[2-3]领域。
纳米淀粉的制备方法有反相乳液聚合法[4],交联沉淀法[5],微乳液法[6]和缓慢酸水解法[7],但采用机械力化学法(Mechanochemical Process)如研磨、超声波等制备纳米淀粉的研究很少。Ostwarldf[8]在20世纪初首次提出“机械力化学(mechanochemistry)”的概念,即认为在化学研究领域中存在着一个由机械能诱发化学变化和物理化学变化的反应。近年来,机械力化学法又被进一步用于制备超微及纳米材料等方面,在制备纳米材料与纳米复合材料方面,发挥了其独特的效应[9]。采用机械力的不同作用方式,如研磨、超声、剪切等,可促进能量累积,在物料界面产生瞬间的高温高压,同时,在热力的作用下,物料的理化性质和结构发生较快和较大变化,提高体系的反应活性,激发和加速化学反应。利用机械力化学法可以实现许多在热力学上无法发生的化学反应,合成一般物理、化学方法所不能得到的功能材料。
研磨过程中,物料受到强烈的剪切力、高频震荡力、摩擦力等机械力作用,导致物料的物理、化学及结构性质变化,即发生机械力化学效应。超声波处理过程中会产生空化作用,空化作用形成的瞬间产生较强的冲击波,形成瞬时高能环境,这些能量可促使化学键的断裂,使淀粉的大分子结构被破坏,有助于纳米颗粒的形成。本研究拟采用机械力化学法制备纳米淀粉,分析纳米淀粉的结构、微观形貌和谱学性能,以期为纳米淀粉的绿色、高效制备提供试验依据。
1 材料与方法
1.1 试验材料与仪器
玉米淀粉:河北华辰淀粉糖有限公司;溴化钾(AR):国药集团化学试剂有限公司;试验用水为去离子水。
SM-120型超细磨(研磨设备):无锡新光粉体加工工艺有限公司;KQ-250DB型超声波清洗器:昆山市超声仪器有限公司;GL-20G-Ⅱ型高速冷冻离心机:上海安亭科学仪器厂;TD-1B-50真空冷冻干燥机:北京博医康实验仪器厂;Hitachi-H7650透射电子显微镜:日本日立公司;Nicolet 380型傅里叶变换红外光谱仪:美国Thermo Electron公司;X’Pert Pro MPD X-射线粉末衍射仪:荷兰飞利浦公司;SZP-06型 Zeta电位测定仪:瑞典BTG公司;NETZSCH STA449F3热重分析仪:德国耐驰公司。
1.2 试验方法
1.2.1 纳米淀粉的制备
取10 g玉米淀粉,配制成质量分数为10%的淀粉溶液,加入到研磨设备中。增加压力至20 MPa,控制温度低于50℃,研磨反应一定时间。反应结束后,收集样品,静置12 h,高速离心去掉上层水溶液,下层样品,置于超声波反应器中,一定温度下超声处理(频率40 kHz,功率250W)。超声反应结束,混合液在转速9 000 r/min条件下进行多次离心,收集上层的乳白色悬浮液,直至上层不再出现乳白色悬浮液,停止收集。上层悬浮液和下层样品分别进行透射电子显微镜观察显示,乳白色悬浮液为纳米淀粉,下层样品粒径未达到纳米。
1.2.2 纳米淀粉得率的测定
测量纳米淀粉悬浮液的总体积,用移液管吸取20 mL于已称量过的称量瓶中,真空冷冻干燥48 h至恒重,然后在分析天平上称重。

式中:m1为冷冻干燥后样品与称量瓶的质量/g;m2为称量瓶的质量/g;m为原料的质量/g;v1为纳米淀粉悬浮液的总体积/mL;v2为移取纳米淀粉的体积/mL。
1.2.3 透射电镜分析(TEM)
采用透射电子显微镜对纳米淀粉的形貌进行观察。测试条件:0.2%的纳米淀粉悬浮液超声分散30 min,磷钨酸染色,滴到涂有碳膜的铜网上观察。
1.2.4 红外光谱分析(FTIR)
采用傅里叶变换红外光谱仪对样品的化学结构进行分析。测试条件:1 mg干燥后的样品与200 mg溴化钾混合,压膜制片,置于红外光谱仪上扫描,扫描范围4 000~400 cm-1。
1.2.5 X-射线衍射(XRD)分析
采用X-射线粉末衍射仪对样品的晶体结构进行研究。测试条件:特征射线Cu Ka,Ni片滤波,电压80 kV,测量范围2θ=6°~90°(θ为衍射角度)。
1.2.6 Zeta电位测试
采用Zeta电位测定仪测定样品的电位值,分析其电化学性质。测试条件:淀粉悬浮液以水作为介质,中性条件下超声分散60 min。
1.2.7 热失重分析(TGA)
采用热重分析仪测定样品的热稳定性。测试条件:试样质量5~10 mg,升温速率10℃/min,温度范围25~500℃,N2作为保护气。
2 结果与讨论
2.1 研磨时间对纳米淀粉得率的影响
固定超声温度为40℃,超声时间为5 h,考察研磨时间对纳米淀粉得率的影响。研磨时间对纳米淀粉得率的影响结果见图1。由图1可知,研磨时间在4~6 h内,随着研磨时间的延长,纳米淀粉得率明显增加,研磨时间为6 h时,基本达到最大值40%。原因可能是随着研磨时间的延长,淀粉在研磨过程中受到剪切力、摩擦力和高频震荡力等机械力的充分作用,产生机械力化学效应[10],淀粉颗粒的反应活性增加,淀粉的大分子结构变得松散,更容易在超声作用下形成纳米淀粉晶粒,而存在于上层悬浮液中,未达到纳米尺度的淀粉颗粒沉积在下层。当研磨时间超过6 h,随着研磨时间的增加,纳米淀粉得率呈下降趋势,原因可能是较长时间的研磨会使淀粉的结晶区受到破坏,淀粉发生水解。另外,较长时间的研磨也会导致已经形成的纳米淀粉颗粒发生团聚作用,使纳米淀粉的得率下降。因此确定最佳研磨时间为6 h。

图1 研磨时间对纳米淀粉得率的影响
2.2 超声时间对纳米淀粉得率的影响
固定研磨时间为6 h,超声温度为40℃,考察超声时间对纳米淀粉得率的影响。超声时间对纳米淀粉得率的影响结果见图2。由图2可知,随着超声时间的延长,纳米淀粉得率明显增加,超声时间为5 h时,基本达到最大值,此后再延长超声时间,纳米淀粉得率并没有明显增加。可能是由于超声时间的延长,淀粉颗粒受到超声波产生的强烈的空化作用,空化气泡在超声波的正负压相作用中积累能量,空化气泡破碎时产生暂时的强压力脉冲,形成高速微射流射向淀粉界面,使淀粉颗粒被破碎,形成纳米淀粉,超声时间5 h左右时,超声反应达到饱和,纳米淀粉得率基本趋于稳定[11]。

图2 超声时间对纳米淀粉得率的影响
2.3 超声温度对纳米淀粉得率的影响
固定研磨时间为6 h,超声时间为5 h,考察超声温度对纳米淀粉得率的影响。超声温度对纳米淀粉得率的影响结果见图3。由图3可知,超声温度在20~40℃范围内,随着超声温度的升高,纳米淀粉得率明显增加,温度为40℃时,基本达到最大值。主要是由于随着温度的升高,分子运动加剧,淀粉受到充分润胀,结构更为松散,在超声波的空化作用下更容易破碎成纳米淀粉。当温度超过40℃,随着温度的升高,纳米淀粉得率呈下降趋势,原因可能是淀粉的糊化温度较低,较高的温度会使淀粉糊化,导致纳米淀粉得率下降。因此确定最佳超声温度为40℃。
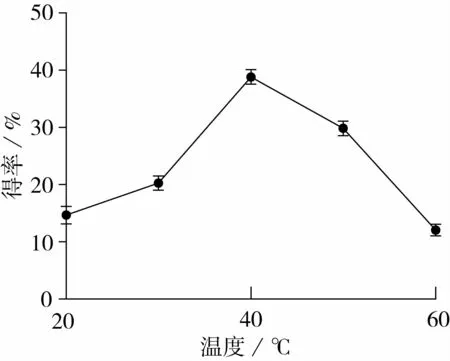
图3 超声温度对纳米淀粉得率的影响
综合分析研磨时间、超声时间、超声温度对纳米淀粉得率的影响可以得出,研磨时间为6 h,超声时间为5 h,超声温度为40℃,纳米淀粉得率较高,达到40.33%。
2.4 透射电镜分析
目前,淀粉颗粒粒径的测定方法主要有激光粒度分析法和聚焦光速发射分析法显微镜法。张本山等[12]对3种方法进行分析比较发现,不同方法测得的淀粉颗粒粒径不同,主要是由于仪器的原理不同引起的。激光粒度分析法测试速度快,测试范围大,通常测定粒径大小为微米及以上的颗粒。聚焦光速发射分析法需要在设定的淀粉浓度、介质及搅拌速率下进行,对粒径为纳米级以下的颗粒测试效果较好。显微镜法可直接观察颗粒的形貌,非常直观。透射电子显微镜分辨率达到0.1~0.2 nm,可用于观察纳米材料的超微结构,且操作环境不受限制[13]。因此,本研究采用透射电子显微镜分析纳米淀粉的微观形貌。图4为玉米淀粉的透射电镜图,图5为纳米淀粉的透射电镜图。由图4可观察到玉米淀粉呈球形,直径约为6~10μm,由图5可观察到,玉米淀粉在机械力化学作用下形成的纳米淀粉呈球形,直径约为50~70 nm,粒径较玉米淀粉减小,单个的纳米淀粉晶粒均匀分散。

图4 玉米淀粉的透射电镜图

图5 纳米淀粉透射电镜图
2.5 红外光谱分析
采用红外光谱法研究机械力化学作用下淀粉化学结构的变化。图6为玉米淀粉和纳米淀粉的红外光谱图。由图6可知,玉米淀粉经机械力化学作用后没有出现新的吸收峰,说明机械力化学作用下形成的纳米淀粉中没有新的基团产生,纳米淀粉的化学结构并未被破坏、改变,仍然保持着玉米淀粉的基本化学结构。573 cm-1为糖环内酯的C—O—C伸缩振动吸收峰,是淀粉的特征吸收峰,1 010 cm-1为淀粉醇的 C—O单键伸缩振动峰[14],1 170 cm-1为C—C骨架的伸缩振动吸收峰,1 640 cm-1为醛基的吸收峰。与玉米淀粉相比较,纳米淀粉在1 010 cm-1和1 170 cm-1处的吸收峰向低波数移动,1 640 cm-1处的吸收峰强度增强。原因可能是淀粉在机械力化学作用下,无定形区被破坏,结晶区中的淀粉链排列比较整齐,剩余的结晶区域含量的增加导致C—O—C键上连接的氢键比例增加,使得1 010 cm-1和1 170 cm-1处的吸收峰向低波数移动[15]。淀粉在机械力化学作用下,分子中的糖苷键发生断裂,产生更多的醛基,因此1 640 cm-1处的吸收峰强度增强。
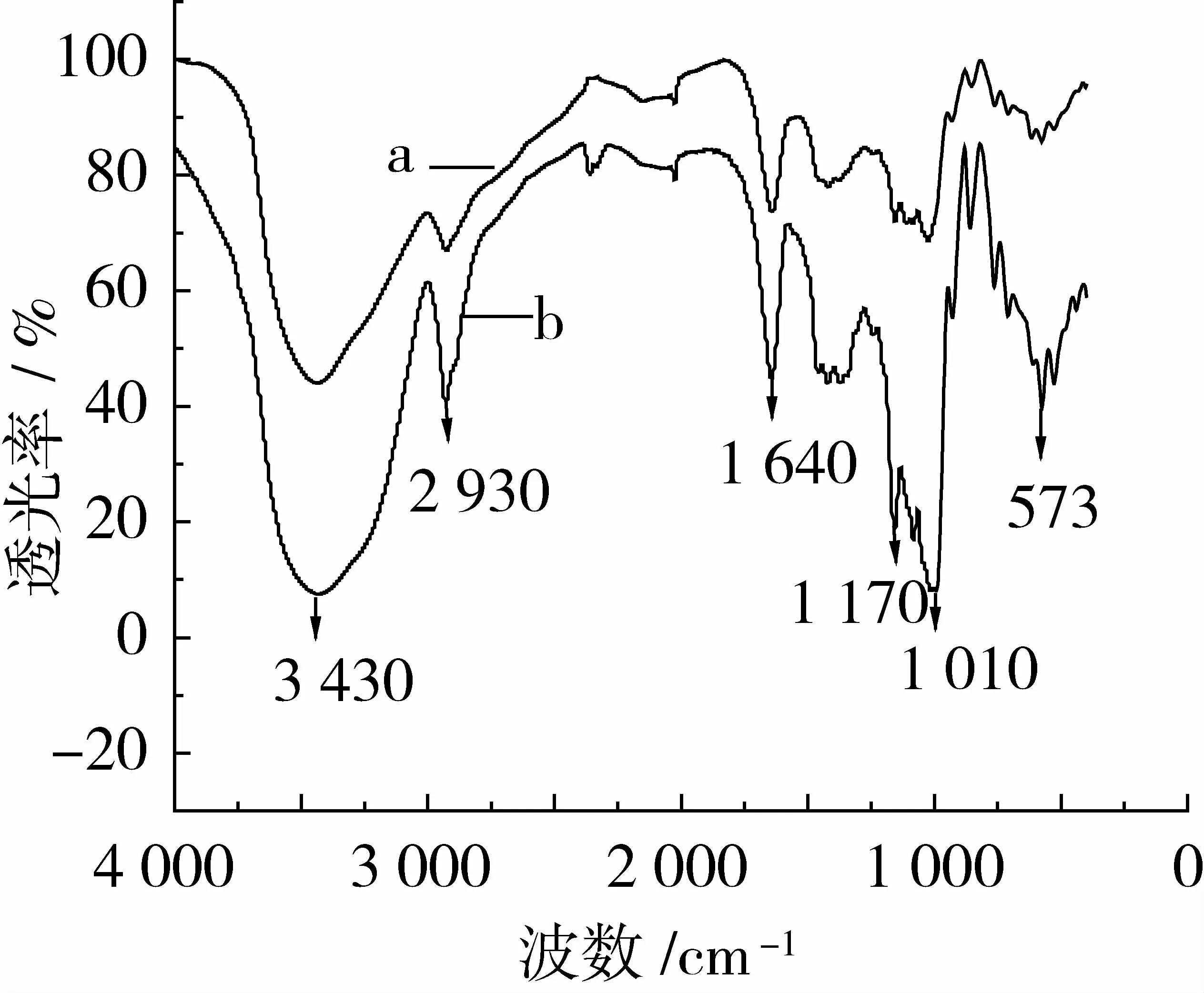
图6 不同淀粉的红外光谱
2.6 晶体结构分析
淀粉是复杂的多晶体系,其结晶度的测定方法还不完善,目前,X射线衍射法是测定淀粉颗粒结晶度最常用的方法。利用X射线衍射法测定其结晶度时,由于测定方案和数据处理方法的不同,其结果会有一定的差异。X射线衍射图谱如图7所示。由图7可知,2θ=17°,22°,26°有较强的衍射峰出现,因此认为制备的纳米淀粉属于B型[16]。结晶度的计算采用Nara和Komiya[17]等提出的计算公式:

式中:Xc为相对结晶度;Ac为晶区部分面积;Aa为非晶区部分面积。

图7 不同淀粉的XRD图谱
由式(1)可计算出纳米淀粉的结晶度为58%,玉米淀粉为38%,纳米淀粉的结晶度较玉米淀粉显著增大。这主要是由于在研磨、超声波等机械力作用下,淀粉大分子结构中的糖苷键断裂,结构较为松散的无定形区受到破坏,而结晶区由于其特有的晶体形态不易受到破坏而得以保留。杨成等[18]的研究报道中,以缓慢酸水解法制备纳米淀粉,结晶度达到了78.72%,本研究采用机械力化学法制备的纳米淀粉结晶度偏低,主要是因为缓慢酸水解过程中,淀粉中的无定形区水解较为充分,而且酸解的作用还逐渐破坏了结晶晶片之间的无定形区,使得纳米淀粉的结晶度较高。
2.7 Zeta电位测试
淀粉结构中含有糖醛酸基、极性羟基等基团,其表面总是带负电荷。采用Zeta电位测定仪测定淀粉的Zeta电位,结果如表1所示。由表1可知,制备的纳米淀粉的Zeta电位绝对值比玉米淀粉大。这可能是因为淀粉属于高分子聚合物,随着尺寸的减小其特性会发生很大变化,主要表现在体积效应和表面效应2个方面[19]。这2种效应使得纳米淀粉的表面积增加,官能团密度增大,选择性吸附能力增强,达到吸附平衡的时间缩短,导致其在水介质中的分散稳定性增强,因而其Zeta电位值增大。

表1 淀粉悬浮液的Zeta电位
2.8 热失重分析
淀粉的热稳定性受淀粉分子质量和其晶体结构的影响。热重分析,可以在程序控制温度下,测量物质的质量随温度变化的关系,分析物质的热稳定性[20]。因此可以采用热重分析法研究机械力化学作用下淀粉热性能的变化,由TG、DTG曲线的质量与温度变化关系表征样品的热稳定性。
玉米淀粉、纳米淀粉的TG曲线如图8所示,DTG曲线如图9所示。由图8可知,玉米淀粉和纳米淀粉在110℃之前有少量的失重,这主要是由于淀粉样品中结合水的蒸发[21]。表2中是TG和DTG曲线的热力学数据。采用SPSS 11.5数据处理软件进行显著性P值计算和分析。从表2可知,玉米淀粉的起始分解温度为300℃,纳米淀粉的起始热分解温度为290℃,略低于玉米淀粉,两者的起始分解温度具有显著性差异(P<0.05)。这是因为玉米淀粉的分子质量较大,分子链相互交叉、相互缠绕形成了稳定的凝胶状的网状结构,因此其起始分解温度较高。机械力化学作用下,淀粉的分子链变短,分子内的网状结构几乎消失,因而不能有效抵抗热分解作用,其起始分解温度降低[22]。从表2可知,315℃左右淀粉热失重速率达到最大,420℃左右淀粉热分解过程结束,玉米淀粉在315℃时的失重比例和420℃时的总分解比例均高于纳米淀粉,同时,SPSS 11.5数据处理软件分析显示,玉米淀粉和纳米淀粉在315和422℃时的分解比例分别具有显著性差异(P<0.05)。这是因为虽然纳米淀粉的分子质量减小,也没有了原淀粉中的网状结构,但其分子结构中的无定形区减少,结晶区所占比例增加,结晶区中分子链之间的结构紧凑,排列紧密,是淀粉颗粒中的最优结构排列,因此其热稳定性增强。

图8 不同淀粉的TG曲线

图9 不同淀粉的DTG曲线
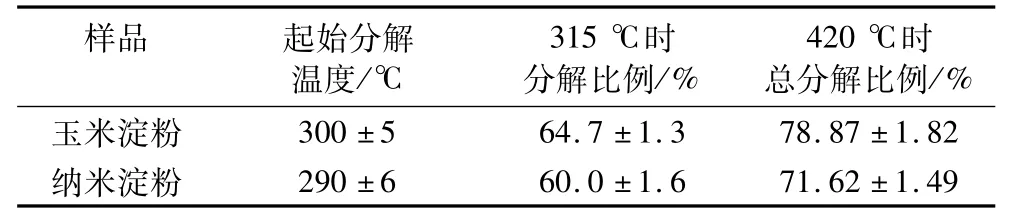
表2 样品的分解温度及失重比例
3 结论
3.1 淀粉在机械力化学作用下发生了机械力化学反应,使其粒径减小,形成纳米淀粉。
3.2 机械力化学法制备纳米淀粉的较佳工艺条件为:研磨时间6 h,超声温度40℃,超声时间5 h。在此条件下,纳米淀粉得率达到40.33%。
3.3 制备的纳米淀粉呈球形,直径约为50~70 nm,结晶度达到58%,热稳定性较玉米淀粉增强。
3.4 机械力化学法能够充分利用过程中产生的机械力、热力及化学力的协同效应,降低反应的活化能,提高反应速率,而且环境友好,可为纳米淀粉的绿色、高效制备提供理论依据。
[1]于泓鹏,高群玉,曾庆孝.大米淀粉制备及其综合利用研究进展[J].粮食与油脂,2004(4):14-16
[2]梁兰兰,吴军晖,幸芳,等.大米淀粉晶体特性对湿米粉质构的影响[J].中国粮油学报,2013,28(6):5-9
[3]陈忠敏,熊佳庆,廖大刚,等.丝胶/PVA/玉米淀粉共混凝胶膜的制备及其体外降解调控研究[J].功能材料,2012,43(4):457-461
[4]孙庆元,于英梅,倪长军,等.反相微乳法合成淀粉微球的研究[J].大连轻工业学院学报,2007,26(1):5-8
[5]Giezen FE,Jules R O,Feil H,etal.Biopolymer nanoparticles:US,6677386B1[P].2004-01-13
[6]谢彩锋,杨连生,高群玉.纳米淀粉微球的制备及其在生物医药中的应用[J].现代化工,2004,24(9):62-69
[7]Song SW,Wang C,Pan Z L,et al.Preparation and characterization of amphiphilic starch nanocrystals[J].Journal of Applied Polymer Science,2008,107(1):418-422
[8]Boldyrev V V,TkácˇováK.Mechanochemistry of solids:past,present,and prospects[J].Journal of Material Synthesis and Processing,2000,8(3-4):121-132
[9]Bálaz P.Mechanochemistry in nanoscience and minerals engineering[M].Berlin:Springer,2008
[10]高明炜,李长根,崔洪山.细磨和超细磨工艺的最新进展[J].国外金属矿选矿,2006,43(12):19-23
[11]胡爱军,张志华,郑捷,等.大米纳米淀粉的超声法制备及载药性研究[J].粮食与饲料工业,2011(8):32-35
[12]李芬芬,张本山.淀粉颗粒粒径不同测定方法的比较[J].食品与发酵工业,2010,36(4):171-174
[13]郭素枝.电子显微镜技术与应用[M].厦门:厦门大学出版社,2008
[14]Alemdar A,Sain M.Biocomposites from wheat straw nanofibers:morphology,thermal and mechanical properties[J].Composites Science and Technology,2008,68(2):557-565
[15]汪志芬,林华,黄洁,等.木薯淀粉纳米晶的结构研究[J].化学工程师,2010,24(11):1-3
[16]Buléon A,Colonna P,Planchot V,et al.Starch granules:structure and biosynthesis[J].International Journal of Biological Macromolecules,1998,23(2):85-112
[17]Nara S,Komiya T.Studies on the relationship between water-satured state and crystallinity by the diffraction method formoistened potato starch[J].Starch/Stärke,1983,35(12):407-410
[18]段彬,杨成.淀粉纳米晶粒的制备及其性质研究[J].材料导报,2008(S2):41-42
[19]Corre D L,Bras J,Dufresne A.Starch nanoparticles:a review[J].Biomacromolecules,2010,11(5):1139-1153
[20]张本山,王斌.淀粉多晶体系中的链链结晶与链水结晶结构研究[J].中国粮油学报,2008,23(1):48-50
[21]Yao F,Wu Q,Lei Y,et al.Thermal decomposition kinetics of natural fibers:activation energy with dynamic thermogravimetric analysis[J].Polymer Degradation and Stability,2008,93:90-98
[22]刘延奇,于九皋,孙秀萍.A型淀粉球晶的制备及表征[J].中国粮油学报,2004,19(1):31-34.
