龙木错与结则茶卡盐湖卤水兑卤及蒸发析盐规律研究*
2014-03-08崔玉虎袁建军杨美洁沙作良
崔玉虎 袁建军 杨美洁 沙作良
(天津科技大学天津市海洋资源与化学重点实验室 天津 300457)
中国盐湖众多,氯化物型、硫酸盐型、碳酸盐型等各类盐湖类型齐全,尤其是青海和西藏盐湖中钾、镁、锂、硼矿资源非常丰富,具有很高的开采价值和巨大的潜在经济效益。随着开发的力度加大,包括盐湖提锂提钾在内的盐湖资源综合利用已成为西部开发的热点(袁建军等,2003;宋彭生等,2011;程芳琴等,2011)。
西藏结则茶卡湖属碳酸盐型盐湖(伍倩等,2012),卤水中由于碳酸根含量较高,锂难以富集。在浓缩过程中,碳酸锂极易达到饱和,并与氯化钠、钾等盐混合析出。而龙木措湖属硫酸盐型盐湖(王云生等,2011),其卤水中镁的化学性质与锂非常相近,使得镁锂分离困难。特别是在高镁锂比盐湖沉淀法提锂工艺中,在蒸发浓缩及除镁过程时,由于析出盐类总量大,消耗沉淀剂量大,导致锂的收率低,生产成本高。
将上述两类盐湖卤水掺兑,可析出碳酸镁作为副产品,并改变混合卤水组成,从而解决两类盐湖单独提锂过程中的难题。如对结则茶卡卤水进行适当浓缩,则可用作碳酸锂沉淀剂,从而实现无需添加外加药剂提锂工艺。西藏龙木错及结则茶卡分属硫酸盐型及碳酸盐型盐湖,且相距不远,为实施上述兑卤工艺提供了有利条件。
本文对两个盐湖卤水兑卤及混合卤蒸发浓缩行为进行研究,获得了兑卤后卤水在蒸发过程中的化学组成变化和各种盐类的富集规律,并最终得到了富锂硼母液,用于后期分离提锂硼。为合理开发利用西藏盐湖卤水中的钾盐、硼砂、锂盐等资源提供了基础实验数据和技术基础(杨建元等,1996;郑绵平等,2007;高文远等,2012)。
1 实验及结果分析
本研究试验分为两部分,一是龙木错卤水与结则茶卡卤水兑卤实验;二是混合卤蒸发浓缩实验,研究其盐类的析出规律。
1.1 分析测定方法
1.1.1 离子测定方法 Cl–:硝酸银容量法;Ca2+,Mg2+:EDTA络合滴定法;:硫酸钡重量法;K+:四苯硼钾重量法;Li+:火焰原子吸收光度法;B2O3:甘露醇容量法;:甘露醇容量法;Na+:差减法计算。
1.1.2 密度、黏度及pH的测定 卤水密度采用比重瓶法测定,测定结果进行空气浮力校正。黏度用乌氏玻璃黏度计测定,计时秒表的精度为±0.02s。pH使用 PHB-8型笔式pH计测定(上海康仪仪器有限公司生产)
1.2 实验原料
实验原料取自西藏龙木错湖水及结则茶卡湖水。其主要化学组成见表1,2。

表1 龙木错湖水主要化学组成Tab.1 Chemical Composition of the Longmu Salt Lake brines

表2 结则茶卡湖水主要化学组成Tab.2 Chemical Composition of the Jieze Salt Lake brines
1.3 兑卤实验
由于 MgCO3溶解度很小(Ksp=3.5×10–8),由表1、表2卤水组成可知,当两湖卤水相兑,将产生沉淀反应:


图1 兑卤后混合卤水中离子的浓度与兑卤比的关系Fig.1 Relation of the ion concentration of the mixing brines and the mixing brine ratio

表3 不同兑卤比的卤水中离子含量Tab.3 Chemical composition of mixed brines
由实验结果可以看出:

(2)混合卤中的总碳浓度随兑卤比的增大而增大。由于混合卤pH的变化,兑卤比1:1之前,主要以形式存在,此后以形式存在;
(3)混合卤中Ca2+的浓度也随兑卤比的增大而明显减小,说明存在沉淀反应:
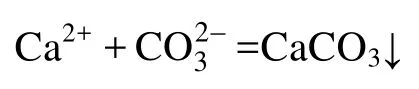
1.4 蒸发浓缩实验
实验中将定量体积比1:1兑卤后的混合卤水置于蒸发装置中,然后加热至沸腾蒸发。在蒸发装置中设有搅拌装置,以避免因在蒸发过程中固相析出而固结在蒸发装置底部,影响传热效果。当蒸发水量达到预定的蒸发量时,将试样转移至平衡槽内进行恒温平衡,并准确控制平衡槽温度为 15°C,平衡时间至少为 3天。平衡期间继续搅拌试样(特别是有大量固相生成的试样)。平衡结束后,再次进行称量,以确定准确的质量蒸发率,然后进行固液分离,并分别取固相和液相进行分析。在下文中 L1—L8分别表示特定质量蒸发率(19.66%、36.65%、49.92%、55.51%、65.16%、68.05%、77.48%、83.59%)液相节点,S1—S4分别表示特定质量蒸发率(65.16%、68.05%、77.48%、83.59%)固相节点。质量蒸发率定义为:

其中:ω—质量蒸发率(以下称蒸发率),%;
Wf—蒸发时所取混合卤质量,g;
WP—蒸发后所得卤水的质量,g。
蒸发实验结果见表4、表5及图2。

表4 兑卤蒸发过程中液相化学组成Tab.4 Chemical composition of the liquid phase in different evaporation ratio

表5 兑卤蒸发过程中固相化学组成Tab.5 Chemical composition of the solid phase in different evaporation rates
由实验结果可以看出:
(1)混合卤水在蒸发前对 NaCl是不饱和的,随着蒸发进行,NaCl逐渐浓缩,到质量蒸发率为65.16%(L5)时,NaCl达到饱和并析出。在质量蒸发率为68.05%之前(L6)为NaCl析出区,此时NaCl的析出率为41.33%。
(2)混合卤中仍存在少量碳酸根及碳酸氢根离子,随着蒸发进行,由于镁离子及总碳离子的富集,将导致少量碳酸镁析出。
(3)当蒸发到质量蒸发率达到 68.05%(L6)和77.48%(L7)之间时,软钾镁矾(Pic)达到饱和并析出,卤水中钾、镁、硫酸根的含量迅速减少。

图2 剩余母液中各离子总量与质量蒸发率的关系Fig.2 Relation between the total ion concentration of the residual mother liquor and the evaporation rate
(4)在试验范围内蒸发过程中混合卤水中的锂、硼浓度随着卤水的蒸发而不断增大,没有明显的析出现象。蒸发结束后的母液中锂的质量百分含量为0.24%(约 2.83g/L),硼的质量百分含量为 0.85%(约11.11g/L)。
2 相图分析
由图3可以看出,兑卤后的混合卤水原料处于Pic(软钾镁矾)结晶相区。蒸发初期原料混合卤水并未对 Pic饱和,故不会有析出。由于混合中存在 Mg2+及少量的,同时由于兑卤后混合卤水处于碱性状态,吸收空气中的CO2,会有MgCO3沉淀产生,体现在相图中表现为体系液相点向背离 Mg2+方向运动。同时,将混合卤水以及L6(质量蒸发率为68.05%)两点卤水的进行物料衡算,结果表明Ca2+、Mg2+的减少量与及 HCO3¯的减少总量基本相符,即从混合卤水点到 L6是卤水浓缩及MgCO3沉淀析出的过程。随着蒸发过程的进行,液相组成点达到 L4(质量蒸发率为 55.51%)以后,卤水中 NaCl开始饱和并析出。卤水继续蒸发,当蒸发到L6(质量蒸发率为68.05%)后Pic逐渐达到饱和并析出,即从 L6至 L8的过程是 Pic析出的过程。整个蒸发析盐路线与五元水盐体系15°C相图基本吻合。

图3 以 Na+、K+、Mg2+//Cl–、-H2O五元水盐体系15°C相图为参照的15°C蒸发结晶路线Fig.3 Phase diagram and crystallization path of the quinary system Na+,K+,Mg2+//Cl–、 —H2O at 15°C
在此兑卤蒸发过程中,盐类析出顺序为:碳酸镁、碳酸镁+氯化钠、氯化钠+软钾镁矾。
3 结论
通过结则茶卡卤水与龙木错卤水兑卤,分离碳酸镁盐后进行高温沸腾蒸发、15°C条件下平衡实验研究,可以得出:
(1)两盐湖卤水兑卤,可以使碳酸镁盐析出。控制不同的兑卤比例,可调节混合卤水的组成。通过采用适宜的兑卤比,可以解决提锂过程中碳酸盐湖卤水碳酸锂过早析出、难以富集、硫酸盐湖卤水镁锂比高、分离成本高的难题。在以提取锂、硼为主要目的的实验过程中,考虑到自然蒸发周期较长,弱碱性卤水不断吸收空气中的CO2,为避免蒸发过程中锂损失,以控制镁离子适当过量为宜。
(2)两盐湖卤水兑卤,析出固相仅为碳酸镁盐,钾、锂、硼等组分均未见析出。兑卤后生成的混合卤呈弱碱性。
(3)在本实验研究中,以 1:1兑卤比生产的混合卤为蒸发实验原料,其蒸发析盐阶段性明显,盐类析出顺序为:碳酸镁、碳酸镁+氯化钠、氯化钠+软钾镁矾。蒸发析盐规律基本与 15°C条件下的 Na+、K+、Mg2+//Cl–、五元水盐体系相符。
(4)在混合卤质量蒸发率约为55.51%时,NaCl达到饱和并开始析出;而软钾镁矾的饱和析出点在质量蒸发率为77.48%左右。
(5)由实验结果分析可以看出,在本实验研究范围内的蒸发浓缩过程中,锂及硼基本没有析出,但在析出固相中,由于母液夹带,会造成锂、硼的损失。所得富锂母液中 Li+的质量百分含量为 0.24%,B2O3为0.85%。
(6)兑卤及蒸发过程析盐阶段性明晰,可采用分段分离,分别生产碳酸镁、氯化钠、软钾镁矾等副产品。如对软钾镁矾母液继续蒸发,根据相图分析,析出的混合盐可能由钾盐镁矾、光卤石、硫酸镁等组成。蒸发过程中,锂、硼将进一步富集,在单独对龙木错卤水浓缩时,富锂卤水中锂(Li+)浓度可达0.8%—1%。
孙之南,郭绍珍,1985.海水蒸发浓缩析盐析盐规律研究.海湖盐与化工,14(4):1—8
李海民,王芝兰,李纪泽,1999.昆特依盐湖晶间卤水25°C等温蒸发实验研究.盐湖研究,17(3):15—21
杨建元,张 勇,程温霞等,1996.西藏扎布耶盐湖冬季卤水25°C等温蒸发研究.海湖盐与化工,25(5):21—24
郑绵平,邓月金,乜 贞等,2007.西藏扎布耶盐湖秋季卤水25°C等温蒸发研究.地质学报,81(12):1742—1749
伍倩,郑绵平,乜 贞等,2012.西藏当雄错碳酸盐型盐湖卤水自然蒸发析盐规律研究.无机化学学报,28(9):1895—1903
王云生,郑绵平,乜 贞等,2011.西藏扎北盐湖秋季卤水(硫酸钠亚型)5°C等温蒸发实验研究.地球学报,32(4):477—482
高文远,李昱昀,汤建良等,2012.西藏藏北某盐湖卤水 5°C等温蒸发实验研究.盐业与化工,41(9):7—10
袁建军,郭桂兰,陈丽芳,2003.盐湖卤水提锂过程中析盐规律的研究.中国井矿盐,11(6):10—13
宋彭生,李 武,孙 柏,乜 贞,卜令忠,王云生,2011.盐湖资源开发利用进展.无机化学学报,05:801—815
程芳琴,成怀刚,崔香梅,2011.中国盐湖资源的开发历程及现状.无机盐工业,07:1—4+12
薛自义,严亦彬,关 岳等,1994.制盐工业手册.北京:中国轻工业出版社,105—106
Baseggio G,1973.The composition of sea water and its concentrates.Fourth Symposium on Salt,2:351—358
