胃溶型银杏叶薄膜包衣片处方和质量研究
2014-03-08朱晓峰陈国喆
朱晓峰,陈国喆
(威海华洋药业有限公司,山东威海264400)
胃溶型银杏叶薄膜包衣片处方和质量研究
朱晓峰,陈国喆
(威海华洋药业有限公司,山东威海264400)
目的制备胃溶型银杏叶薄膜包衣片并考察处方与质量。方法以性状、重量差异、崩解时限、硬度、脆碎度、含量为指标因素,根据辅料相容性结果,采用正交设计试验,筛选最优处方,并进行质量考察。结果根据选定的优化处方和工艺制备的胃溶型银杏叶薄膜包衣片及片芯问题得到改善,质量符合药典规定要求。结论优选的胃溶型银杏叶薄膜包衣片处方工艺合理,成品质量符合要求。
银杏叶;处方;质量;正交设计
银杏叶为银杏科植物银杏Ginkgo biloba L.的干燥叶,秋季尚绿时采收,及时干燥。其活性成分主要为黄酮类和萜类,具有活血化瘀,通络止痛,敛肺平喘,化浊降脂的功能,用于瘀血阻络引起的胸痹心痛、中风偏瘫、半身不遂、舌强语謇,冠心病稳定型心绞痛、脑梗死,肺虚咳喘,高脂血症等临床症状。银杏叶薄膜衣片是采用银杏叶提取物浸膏干粉与辅料混合压制而成的中药片剂。因银杏叶提取物干粉吸湿性强,在放置过程中其片剂崩解时限变长,目前市场上剂型有胶囊、滴丸、片剂等。片剂中薄膜包衣较糖衣片在稳定性、耐温性等方面有很大优势[1]。其中,尤以胃溶型薄膜衣片的剂型最为普遍[2]。薄膜包衣技术现已广泛用于制药业,生产工艺成熟[3],但品种差异较大,因此,我们对本品处方进行筛选和质量研究,以得到符合要求的薄膜包衣片,从而保证产品的质量和用药的顺应性。
1 仪器与试药
1.1 仪器 GHL-250高效湿法混合制粒机(哈尔滨纳诺医药化工设备公司);LYK-160B摇摆式颗粒机(江苏瑰宝集团有限公司);GZP-28B1高速旋转式压片机(北京弘华制药机械分公司);BGB-150C高效包衣机(温州市制药设备厂);ZB-1D智能崩解仪(天长天发科技有限公司);U-300高效液相色谱仪(戴安(中国)有限公司);ELSD2000蒸发光散射检测仪(美国奥泰Alltech(中国)科技有限公司);FT-2000脆碎度检查仪(天大天发科技有限公司);YD-20KZ智能片剂硬度仪(天大天发科技有限公司);BS224S电子天平[赛多利斯科学仪器(北京)有限公司]。
1.2 试药 槲皮素(中国药品生物制品检定所,批号:100081-200907);山柰素(中国药品生物制品检定所,批号:110861-200304);异鼠李素(中国药品生物制品检定所,批号:110860-200608);白果内酯(中国药品生物制品检定所,批号:110865-200404);银杏内酯A(中国药品生物制品检定所,批号:110862-200608);银杏内酯B(中国药品生物制品检定所,批号:110863-200305);银杏内酯C(中国药品生物制品检定所,批号:110864-200505);银杏叶提取物(威海华洋药业有限公司);糊精(安徽山河药用辅料股份有限公司);乳糖(常州市朗生生物工程有限公司);蔗糖(嘉兴市白浪淀粉制品有限公司);淀粉(安徽山河药用辅料股份有限公司);硬脂酸镁(安徽山河药用辅料股份有限公司);药用酒精(德州又一村酿酒有限公司);欧巴代(上海卡乐康包衣技术有限公司)。
2 方法与结果
2.1 检验方法[2]
2.1.1 总黄酮醇苷含量测定 色谱柱:Agilent TC-C18柱(4.6 mm×250 mm,5μm);流动相:甲醇-0.4%磷酸溶液(50∶50);检测波长:360 nm;理论板数按槲皮素峰计算应不低于2 500。
分别精密称取槲皮素、山柰素、异鼠李素对照品适量,加甲醇制成每1 mL甲醇中分别含槲皮素、山柰素、异鼠李素0.03、0.03、0.02 mg的混合溶液,作为对照品溶液。
取本品10片,除去包衣,精密称定,按《中国药典》2010年版(一部)银杏叶片含量测定项下方法操作制备供试品溶液。
测定法:分别吸取对照品溶液与供试品溶液各10μL,注入高效液相色谱仪中,进行测定,分别计算出槲皮素、山柰素、异鼠李素的含量,并按下式换算成总黄酮醇苷的含量。
总黄酮醇苷含量=(槲皮素含量+山柰素含量+异鼠李素含量)×2.51,总黄酮醇苷含量应≥10 mg/片。
2.1.2 萜类内酯含量测定 色谱柱:Agilent TCC18柱(4.6 mm×250 mm,5μm);流动相:正丙醇-四氢呋喃-水(1∶15∶84);检测器:蒸发光散射检测器;理论塔板数按白果内酯峰计算应不低于2 500。
分别精密称取白果内酯、银杏内酯A、银杏内酯B和银杏内酯C对照品适量,加甲醇制成每1 mL含白果内酯、银杏内酯A、银杏内酯B和银杏内酯C分别为:1、1、1、0.5 mg的混合溶液,作为对照品溶液。
取本品20片,除去包衣,精密称定,按《中国药典》2010年版(一部)银杏叶片含量测定项下操作制备供试品溶液。
测定法:分别精密吸取对照品溶液5、20μL,供试品溶液20μL,注入高效液相色谱仪进行测定,用外标两点法对数方程分别计算出白果内酯、银杏内酯A、银杏内酯B和银杏内酯C的含量。
萜类内酯含量=白果内酯含量+银杏内酯A含量+银杏内酯B含量+银杏内酯C含量,以总内酯总量计,含量应≥2.6 mg/片。
2.1.3 重量差异 取本品,按重量差异测定法[《中国药典》2010年版(一部)附录ⅠD片剂]检测,应在平均片重的±6.5%之内,超出重量差异限度的不得多于2片,并不得有1片超出限度的1倍。
2.1.4 崩解时限 取本品,按崩解时限检查法[《中国药典》2010年版(一部)附录ⅫA]检测,应≤40 min。
2.2 胃溶型银杏叶薄膜包衣片的制备 本试验采用的银杏叶提取物干粉系采用挑拣、清洗、烘干后的洁净银杏叶为原料,经醇提、树脂吸附、洗脱、浓缩、喷雾干燥等工序而得的干燥细粉,以此为制剂产品原料。
2.2.1 制备过程 将银杏叶提取物、糊精、乳糖、蔗糖、淀粉按照比例混合均匀,加入适量的一定浓度乙醇制软材,挤压过16目筛网,60~70℃干燥控制水分不大于3.0%,16目筛整粒,加入适量硬脂酸镁,总混,φ9 mm冲头压片,包薄膜衣,包装,即得。图1为产品工艺流程图。
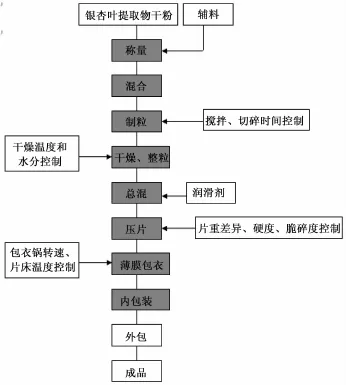
图1 产品工艺流程图
2.2.2 处方优化 胃溶型银杏叶薄膜包衣片剂型虽市场份额较大,但薄膜包衣技术对片芯的硬度要求较高。以干膏粉为半成品制备颗粒时,大多采用一定浓度的乙醇作为润湿剂,进行湿法制粒工艺路线制备[5],并应尽快完成制粒,否则制出的颗粒中细粉过多[6]。开始包衣时,片芯与包衣机内壁反复摩擦,若片芯硬度不够,片芯易被磨损,从而出现松片、麻面等现象[7],为降低此类问题出现的概率,对处方中辅料的配比,进行筛选和优化。
通过相容性试验,即将处方量的主药分别与各辅料混合均匀,于60℃放置10 d,测量其含量均无显著性变化。在辅料相容性试验的基础上,考虑到影响片剂质量的主要辅料为多组分填充剂(A)(乳糖:蔗糖:糊精=71.4∶19.1∶9.5,质量比)、崩解剂淀粉(B)、润湿剂乙醇浓度(C)、疏水性润滑剂硬脂酸镁(D)[8],以此4个因素、取3个水平(因素水平表1)进行正交试验。
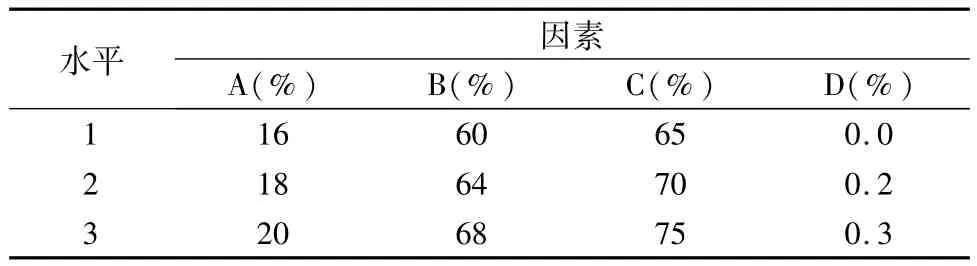
表1 因素水平表
本实验进一步采用正交设计法按L9(34)正交表设计4因素3水平的正交试验,固定压片力,以片剂外观、硬度、脆碎度、崩解时限为主要考察指标,优化处方。试验结果见表2。
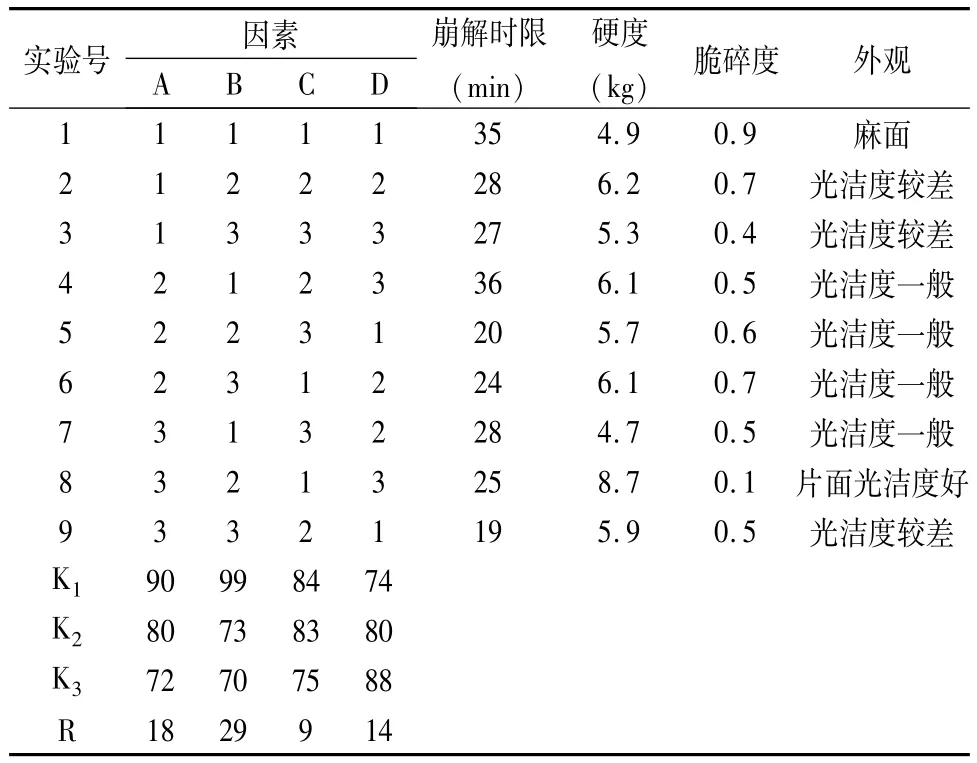
表2 正交试验结果与分析
由表2可见,各因素对崩解时间的主次关系为淀粉>多组分填充剂(乳糖:蔗糖:糊精)>硬脂酸镁>乙醇(浓度),综合其他指标因素,最终确定正交实验条件下优化水平组合为A3B2C1D3,多组分填充剂(乳糖:蔗糖:糊精)、淀粉、硬脂酸镁的用量及乙醇的浓度分别为20%、64%、65%、0.3%。
2.3 结果 根据选定的处方工艺进行压片、包衣,制备3批样品,并对片剂进行质量检验,结果:性状、崩解时限、重量差异及含量均符合规定,见表3。
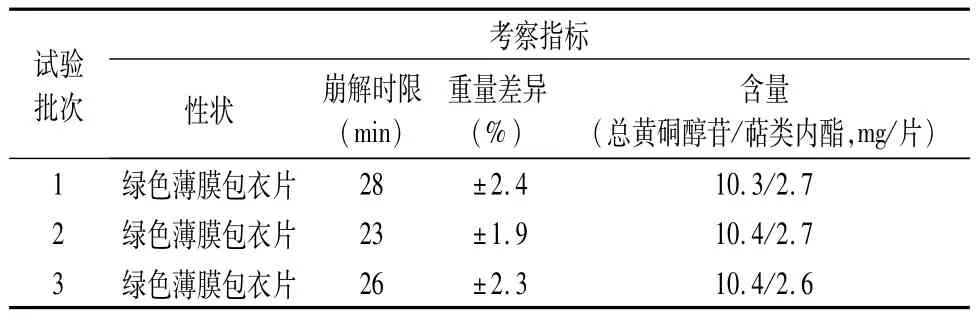
表3 试验3批样品质量检验表
3 讨论
通过对胃溶型银杏叶薄膜包衣片的处方筛选,得到硬度和脆碎度等指标符合包衣要求的最佳处方,经3批样品重现,包衣片质量符合要求,在包衣过程中未出现麻面和片芯磨碎等情况,通过本阶段的优化试验,验证了处方工艺的重现性及稳定性。
[1]刘涛,温利明,沙琦,等.银杏叶片薄膜包衣的生产工艺研究[J].中国药学杂志,2003,38(7):545-546.
[2]卢文胜,黄俊龙,候柏.银杏叶片的稳定性考察[J].中国药师,2008,11(10):1193-1194.
[3]庄越,曹宝成,萧瑞祥.实用药物制剂技术[M].北京:人民卫生出版社,1999:134-135.
[4]国家药典委员会.中华人民共和国药典2010年版(一部)[S].北京:中国医药科技出版社,2010:1079-1080.
[5]侯世祥.中药新制剂成型性研究思路与方法[J].中国中药杂志,2000,25(1):4-7.
[6]杨云.谈谈中药片剂中硬度和崩解的几个问题[J].基层中药杂志,1995,9(4):20-21.
[7]陈蔚,张学荣,胡征.银杏叶片全水型薄膜包衣工艺的研究[J].中草药,2007,38(Suppl):122-123.
[8]崔福德.药剂学[M].第5版.北京:人民卫生出版社,2004.
Investigation of formulation and quality of Gastric Soluble Ginkgo Leaf Film-coated Tablets
ZHU Xiao-feng,CHEN Guo-zhe
(Weihai Huayang Pharmaceuical Co.,Ltd.,Weihai264400,China)
ObjectiveTo prepare Gastric Soluble Ginkgo Leaf Film-coated Tablet and explore the formulation and quality.M ethodsThe formulation was optimized with traits,weight difference,disintegration time,hardness,friability,content as parameter by an excipient compatibility testing and orthogonal design,to optimize the formulation and improve quality study.ResultsAccording to the optimized formulation and preparation process,the Gastric Soluble Ginkgo Leaf Filmcoated Tablets and cores′problems had been improved,and met the requirement of Chinese Pharmacopoeia 2010 criteria.ConclusionThe preparation process was simple and reasonable,and the quality of the productsmet the requirements.
Ginkgo leaf;Formulation;Quality;formulation optimization formulation optimization Orthogonal design
R944.4
A
2095-5375(2014)10-0597-003
朱晓峰,男,研究方向:药品生产技术,E-mail:vip_smallboy@126.com
